Внесені зміни:
- Оновлене дозування налоксону
- Оновлені Стандартні операційні процедури (СОП) введення атропіну/скополаміну
- Оновлена послідовність дій при ураженні нервово-паралітичними речовинами
Вступ
У даних настановах описане надання медичної допомоги постраждалим, які зазнали впливу конкретних хімічних агентів, у рамках безперервного процесу - від місця отримання поранення/ураження до третього етапу медичної допомоги. Більш детальну інформацію ви можете знайти в “Посібнику з надання допомоги постраждалим від ураження хімічними і біологічними агентами в польових умовах” (“Field Management of Chemical and Biological Casualties Handbook”).1 Також для кожної категорії отруйних речовин додано картки-довідки для швидкого отримання інформації. Обговорення рекомендацій, що містяться в картках, знаходиться у тексті нижче. Крім того, можна використовувати наведену нижче схему для проведення швидкого сортування постраждалих від впливу хімічних бойових отруйних речовин на основі клінічної картини. Рішення щодо проведення діагностичних тестів та/або лікування будуть прийматися на основі наявності ресурсів і бойової ситуації на кожному етапі надання допомоги. Допомога при ураженні хімічними агентами повинна надаватися згідно з інтегрованим ХБРЯ-ТССС алгоритмом (MARCHE)2, як описано в Настановах з клінічної практики JTS “Хімічні, біологічні, радіологічні та ядерні (ХБРЯ) ураження. Частина I: Первинне реагування при ХБРЯ-ураженні”.2
Зображення 1. Швидка ідентифікація класу хімічних бойових отруйних речовин на основі токсидрому
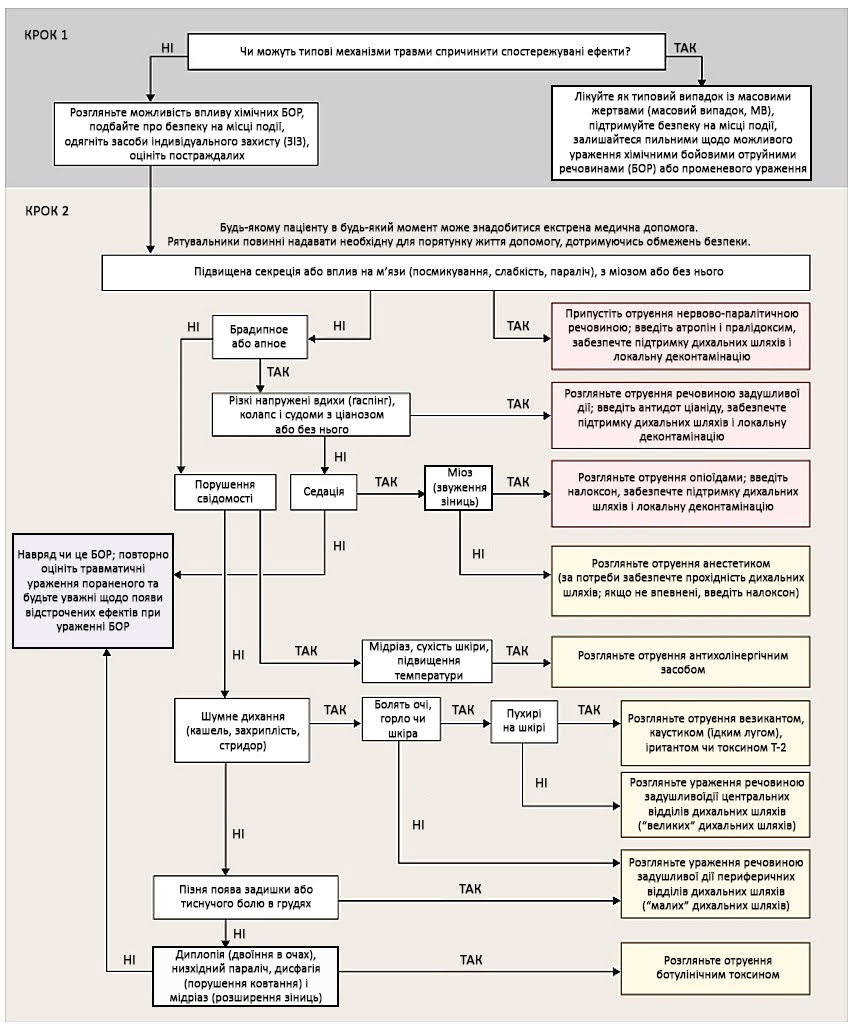
Джерело: Визначення токсидрому при атаках із використанням хімічних БОР. - Toxidrome Recognition in Chemical-Weapons Attacks, Ciottone GR. 26 квітня 2018 р. N Engl J Med 2018; 378:1611-1620
Отруєння ціанідами
Передумови
Історично, ціанід досить рідко використовувався як бойова отруйна речовина, однак летальність і доступність у всьому світі роблять його реальним потенційним агентом хімічного тероризму. Ціанід було знайдено в токійському метро після атак із застосуванням зарину і, як повідомляється, він, можливо, був у вибухівці під час теракту у Всесвітньому торговому центрі в 1993 році. Ціанід можна використовувати в летких, розчинних у воді та рідких формах ціанистого водню (ЦВ) і хлорціану (ХЦ). Реакційноздатні сольові форми ціаніду (ціаніди калію, натрію та кальцію) використовуються в промисловості, утворюючи ціанід водню (HCN) при змішуванні з кислотою. Ціанід дуже леткий і легко перетворюється з рідини в сильнодіючий газ (HCN). HCN виділяється під час піролізу синтетичних полімерів, наприклад, горіння пластмас, і може вивільнятися під час горіння будівель. Оскільки він легший за повітря, то швидко розсіюється у відкритому просторі. Однак слід зауважити, що хлорціан важчий за повітря, і тому є більш стійкою речовиною.
Ознаки та симптоми
Ціанід може викликати появу симптомів протягом декількох секунд або хвилин після вдихання. Хоча його класифікують як отруйну речовину, що вражає кров, ранніми симптомами є токсичний вплив на серцево-судинну та центральну нервову систему (ЦНС). Початкові симптоми можуть бути неспецифічними і тимчасовими. Можлива поява запаморочення, головного болю, слабкості, потовиділення та задишки, а тому диференційна діагностика може бути обширною. Патогномонічний запах гіркого мигдалю не є надійною ознакою, оскільки багато хто не може його розпізнати. Основним клінічним проявом, що вказує на діагноз, є тканинна гіпоксія без ціанозу (пульсоксиметрія може бути нормальною) з виявленням метаболічного ацидозу. Без вчасного лікування стан пацієнта може швидко прогресувати до коми, порушення гемодинаміки, аритмій, судом, вторинної зупинки серця та, зрештою, смерті.
Деконтамінація
Постраждалих, які зазнали впливу ціаніду, слід швидко вивести з місця, де відбулося отруєння, при цьому слід переконатися в безпеці рятувальника. У випадку впливу газу евакуація з місця події та зняття всього одягу є основними заходами деконтамінації. У подальшому можна провести деконтамінацію зрошувальними розчинами, але лікування антидотом є першочерговим, і його не слід відкладати.
Діагностика
Швидка діагностика для полегшення лікування є важливою. Однак слід зауважити, що у тактичному середовищі доступність допоміжних методів діагностики обмежена. Визначення рівня ціаніду не є швидко доступним, і його значення не є суттєвими у гострій фазі лікування. Клінічна картина в поєднанні з показниками газів артеріальної крові, які демонструють метаболічний ацидоз і дуже високий рівень лактату, повинні наштовхнути клініциста на думку про можливий вплив ціанідів. Цей діагноз іноді дуже складно встановити у випадку травми з масивною кровотечею та гіповолемічним шоком. Таким чином, високий рівень підозри та дані розвідки про ризик зараження є ключовими для ранньої діагностики.
Може бути корисним одночасний аналіз артеріальної та венозної крові та порівняння вмісту кисню. «Артеріалізація венозної крові» (подібний колір/PaO2 зразків) може доповнити клінічну картину. З практичної точки зору, малоймовірно, що медичний працівник матиме змогу проводити діагностичні обстеження в гарячій або теплій зоні, тому рішення про лікування буде виключно клінічним. На щастя, з наявністю гідроксокобаламіну (детально обговорюється нижче), побічні ефекти емпіричного введення антидота зведені до мінімуму порівняно з раніше використовуваним набором антидотів ціаніду.
Таблиця 1. Отруйні речовини, що уражають кров
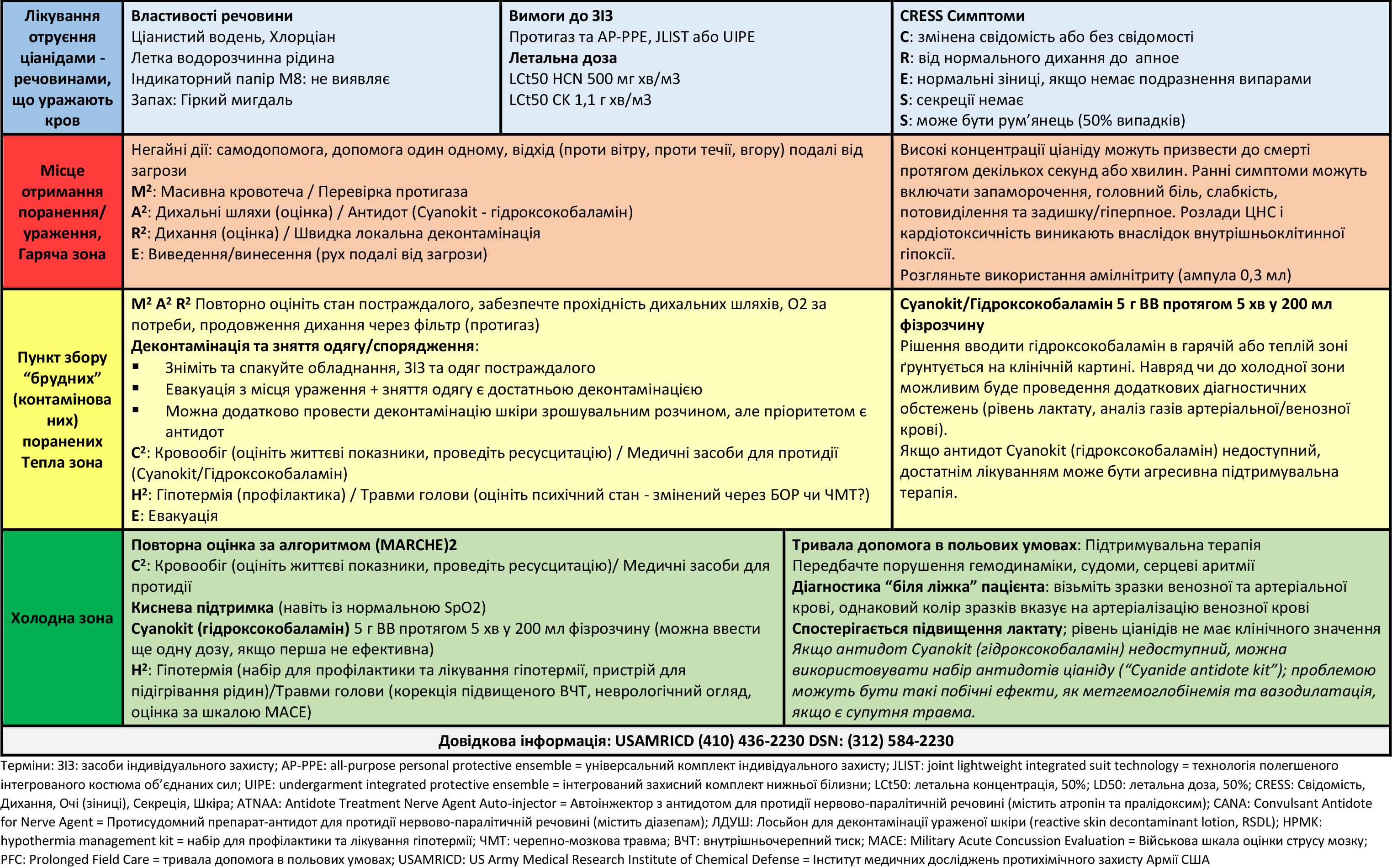
Лікування
Основою лікування є антидотна терапія гідроксокобаламіном. Підтримувальна терапія є важливою частиною ресусцитації. Забезпечення прохідності дихальних шляхів, внутрішньовенний доступ і моніторинг серцевої діяльності допомагають підтримувати стан пацієнта, який зазнав отруєння ціанідами. Корисним для постраждалого буде додатковий кисень, який підвищує ефективність антидота, сприяючи виведенню ціаніду під час дихання та покращуючи інші метаболічні процеси. Історично склалося так, що отруєння ціанідами лікували набором антидотів ціаніду, що складався з амілнітриту, нітриту натрію та тіосульфату натрію. Нітрити викликають метгемоглобінемію як побічний ефект, який може погіршити стан пацієнта з супутньою травмою. Зараз антидотом вибору є гідроксокобаламін (Cyanokit). Однак, якщо гідроксокобаламін недоступний, можна використовувати набір антидотів ціаніду. Інгаляція ампули амілнітриту може бути тимчасовим заходом, поки не буде встановлено ВВ/ВК доступ.
Гідроксокобаламін (вітамін B12a) діє як хелатуючий агент і зв’язується з ціанідом, утворюючи ціанокобаламін (вітамін B12). Доза гідроксокобаламіну, необхідна при отруєнні ціанідами, є набагато вищою, ніж доза, яка використовується при інших терапевтичних показах, тому для введення оптимальної дози без перевантаження рідиною необхідний комерційно виготовлений гідроксокобаламін у дозі 5 г внутрішньовенно (70 мг/кг у педіатричних пацієнтів) протягом 15 хвилин. Дозу можна повторити при важкому отруєнні або незначній реакції на початкову дозу. У випадку зупинки серця внаслідок ціанідної токсичності гідроксокобаламін настільки ж ефективний, як і адреналін. Він може спричинити червоне забарвлення шкіри та сечі, яке зберігається протягом кількох тижнів. Інші побічні ефекти мало виражені. Рішення вводити гідроксокобаламін у гарячій або теплій зоні має бути зваженим з тактичної точки зору, з огляду на ризики при зупинці для отримання ВВ/ВК доступу та початку інфузії.
Інші схеми лікування, а також профілактичні заходи добре висвітлені в літературі та підсумовані в таблиці нижче.
Таблиця 2. Інші схеми лікування
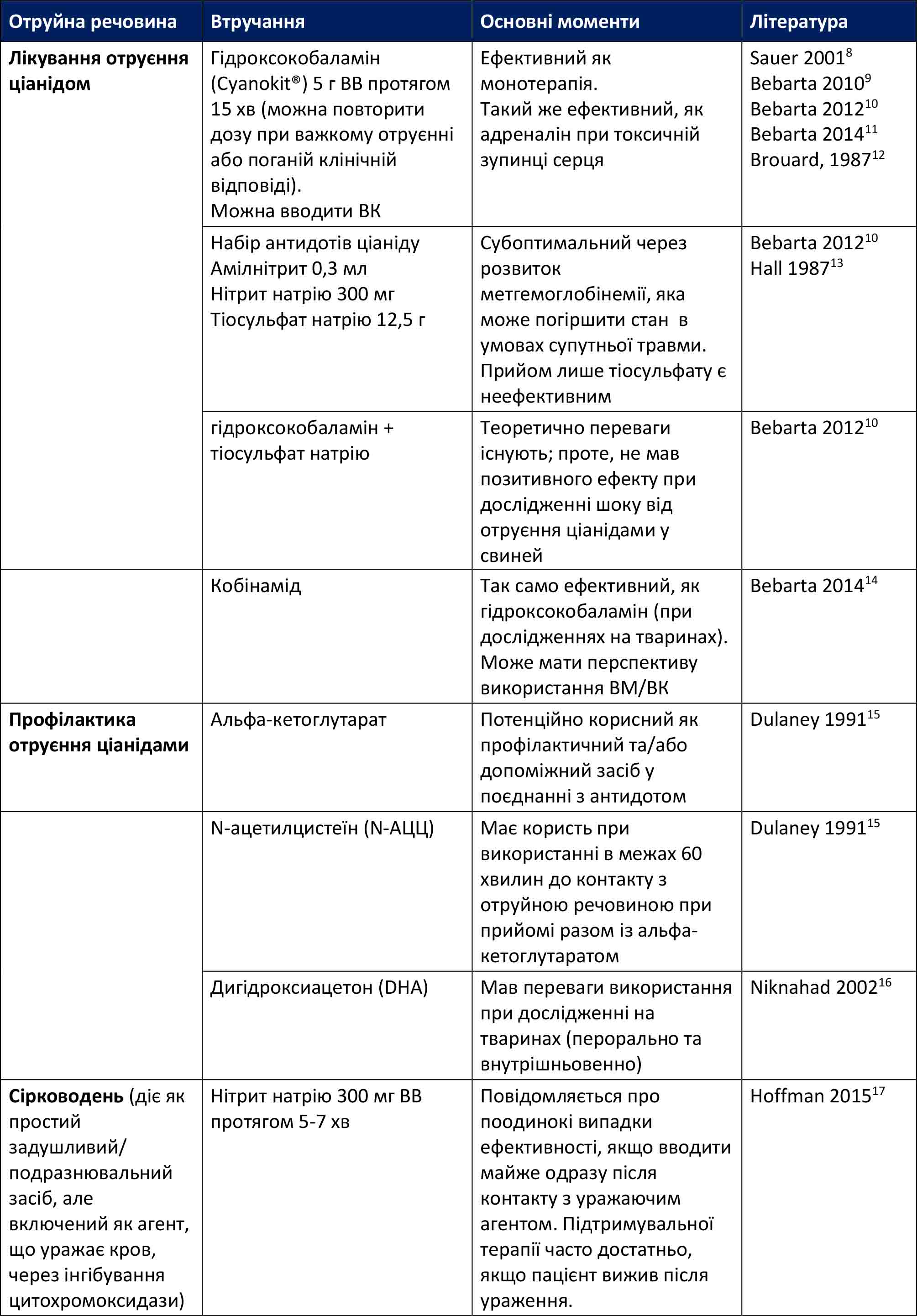
Отруєння нервово-паралітичними речовинами
Передумови
Нервово-паралітичні речовини, або інгібітори ацетилхолінестерази, є одними з найсильніших смертельних отрут, які коли-небудь використовувалися як зброя. Ці речовини існують у різних формах, від густих в’язких рідин до легкорозчинних газів. За хімічним складом вони подібні до фосфорорганічних речовин, що використовуються у сільському господарстві як пестициди, і синдроми, які вони викликають, частіше зустрічаються на фермерських полях, ніж на полі бою. Для найбільш смертоносних форм потрібно лише 0,03 грама речовини, щоб спричинити смерть у 50% ураженого населення (LD50).
Нервово-паралітичні агенти належать, в основному, до двох класів: V-агенти і G-агенти. V-агенти є в’язкими за своєю природою і можуть поширюватися різними способами. Вони надзвичайно небезпечні, якщо до них доторкнутися або проковтнути, але також можуть становити небезпеку, якщо знаходитись близько до їх отруйних випарів. G-агенти за кімнатної температури є рідинами. Вони надзвичайно ефективні як хімічна зброя завдяки здатності швидко спричиняти летальне інгаляційне ураження випарами у великої кількості людей.
В організмі дані речовини зв’язуються з ацетилхолінестеразою, пригнічуючи розпад ацетилхоліну. Двома основними типами холінергічних рецепторів, з якими взаємодіють нервово-паралітичні речовини, є мускаринові та нікотинові рецептори. Мускаринові рецептори розташовані на гладких м'язах і залозах. Симптоми, спричинені надмірною стимуляцією мускаринових рецепторів, можна запам’ятати за допомогою мнемонічного скорочення DUMBBELS (Diarrhea, Urination, Miosis, Bronchorrhea/Bronchoconstriction, Bradycardia, Emesis, Lacrimation, Salivation - діарея, сечовипускання, міоз, бронхорея/бронхоконстрикція, брадикардія, блювання, сльозотеча, слиновиділення). Ці симптоми можна усунути за допомогою введення атропіну (розглянутий нижче, в розділі лікування). Нікотинові рецептори, розташовані у скелетних м'язах і нервових гангліях, також піддаються впливу нервово-паралітичних речовин. Симптоми, спричинені надмірною стимуляцією нікотинових рецепторів, можна запам’ятати, використовуючи першу літеру днів тижня (Mydriasis, Tachycardia, Weakness, Hypertension, Fasciculations - Мідріаз, Тахікардія, Слабкість, Гіпертензія, Фасцикуляції). Введення пралідоксиму (2PAM) відновлює активність холінестерази, що зазвичай призводить до зменшення прояву “нікотинових” симптомів.
Ознаки та симптоми
Отруєння нервово-паралітичними речовинами може бути різного ступеня: від легкого до тяжкого; тяжке ураження може швидко призвести до смерті, якщо вчасно не надати допомогу. Швидка антидотна терапія надзвичайно важлива, оскільки деякі нервово-паралітичні речовини можуть необоротно зв’язуватися з ацетилхолінестеразою (наприклад, період піврозпаду необоротно зв’язаних сполук (так званий період піврозпаду при “старінні”) для зоману (GD) становить дві хвилини).
У людей з легким ступенем ураження, які не мали засобів захисту очей, зазвичай спостерігається міоз. Інші видимі мускаринові ефекти включають сильну сльозотечу та рясне потовиділення, що супроводжується нудотою та блюванням, а також задишкою та утрудненим диханням через бронхорею та бронхоконстрикцію. Найбільш серйозно уражені пацієнти матимуть усі ці ознаки та симптоми, а також виражену слабкість, фасцикуляції, судоми, втрату свідомості, апное та смерть.
Швидкість появи симптомів залежить від шляху ураження та дози отруйної речовини. Інгаляційне ураження, як правило, призводить до швидшої появи симптомів і може спричинити негайну смерть через стрімке системне поширення. Ураження шкіри (наприклад вплив V-агентів), може зумовити відстрочений початок симптомів.
Таблиця 3. Нервово-паралітичні речовини
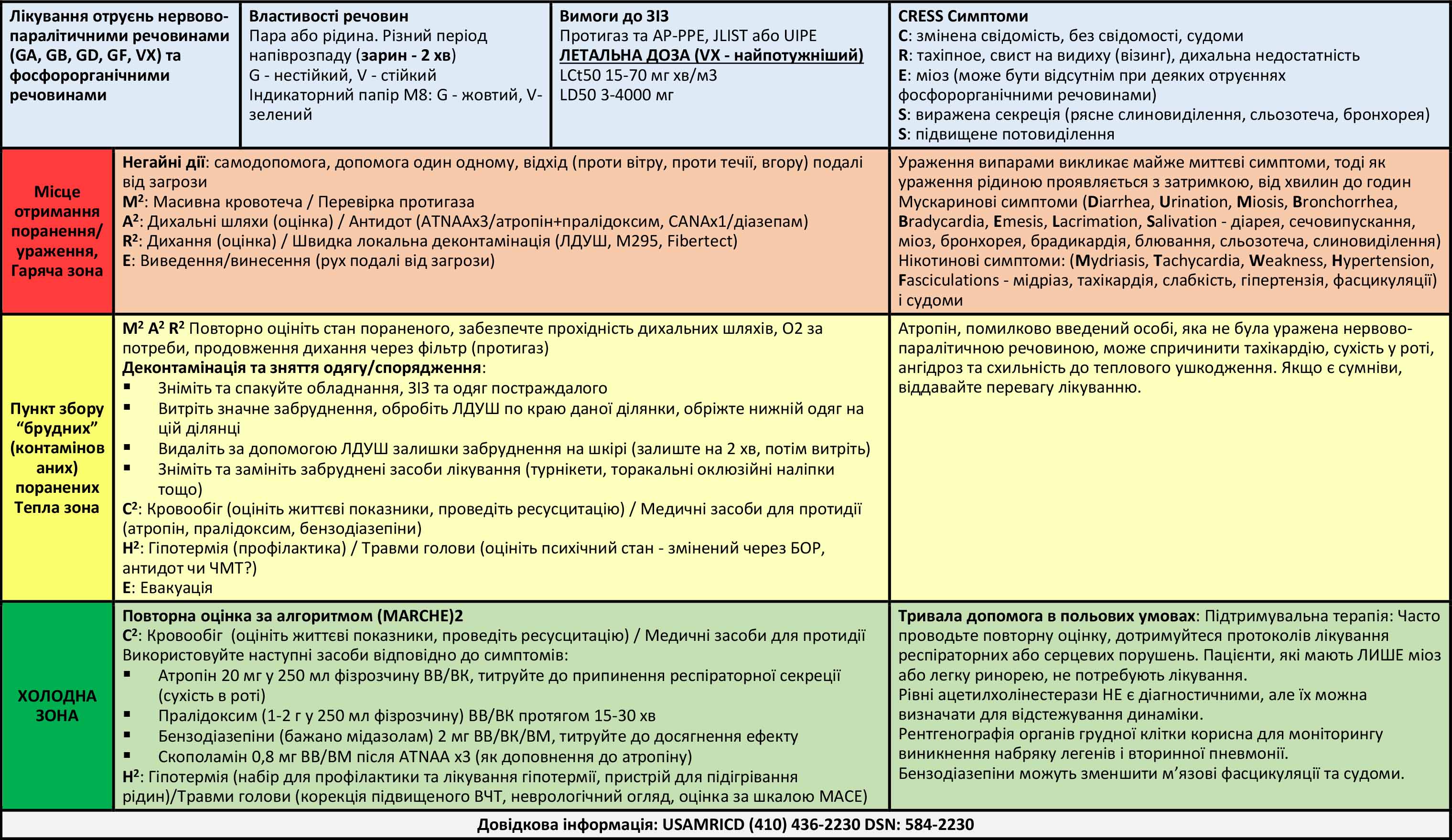
Деконтамінація
Як і з більшістю хімічних речовин, найважливішим кроком є виведення пацієнта із забрудненої зони, щоб запобігти подальшому ураженню. Якщо є ураження отруйними випарами, слід вивести пораненого із зони і швидко зняти одяг або обладнання, яке потенційно є забрудненим отруйною речовиною.
Лосьйон для деконтамінації ураженої шкіри (ЛДУШ, RSDL) широко визнаний як найефективніший засіб для деконтамінації шкірних покривів при ураженні нервово-паралітичними речовинами. Нанесення ЛДУШ на всі відкриті ділянки шкіри якнайшвидше після ураження може врятувати життя. Якщо ЛДУШ недоступний, альтернативою є 0,5% розчин гіпохлориту або вода з милом. Деконтамінацію не слід відкладати, якщо ЛДУШ недоступний. Постраждалим із симптомами середнього та тяжкого ступеня (дихальна недостатність, судоми, порушення свідомості) слід негайно ввести антидоти одночасно із початком проведення деконтамінації.
Діагностика отруєнь нервово-паралітичними речовинами
Діагностика ураження нервово-паралітичними речовинами базується на швидкому виявленні клінічних симптомів та ідентифікації речовини за допомогою діагностичних методів. Лабораторне вимірювання рівня ацетилхолінестерази (АХЕ) в сироватці крові не є корисним, оскільки воно не корелює з ознаками та симптомами чи прогнозом. Через індивідуальну варіабельність визначення базового рівня АХЕ не має користі.
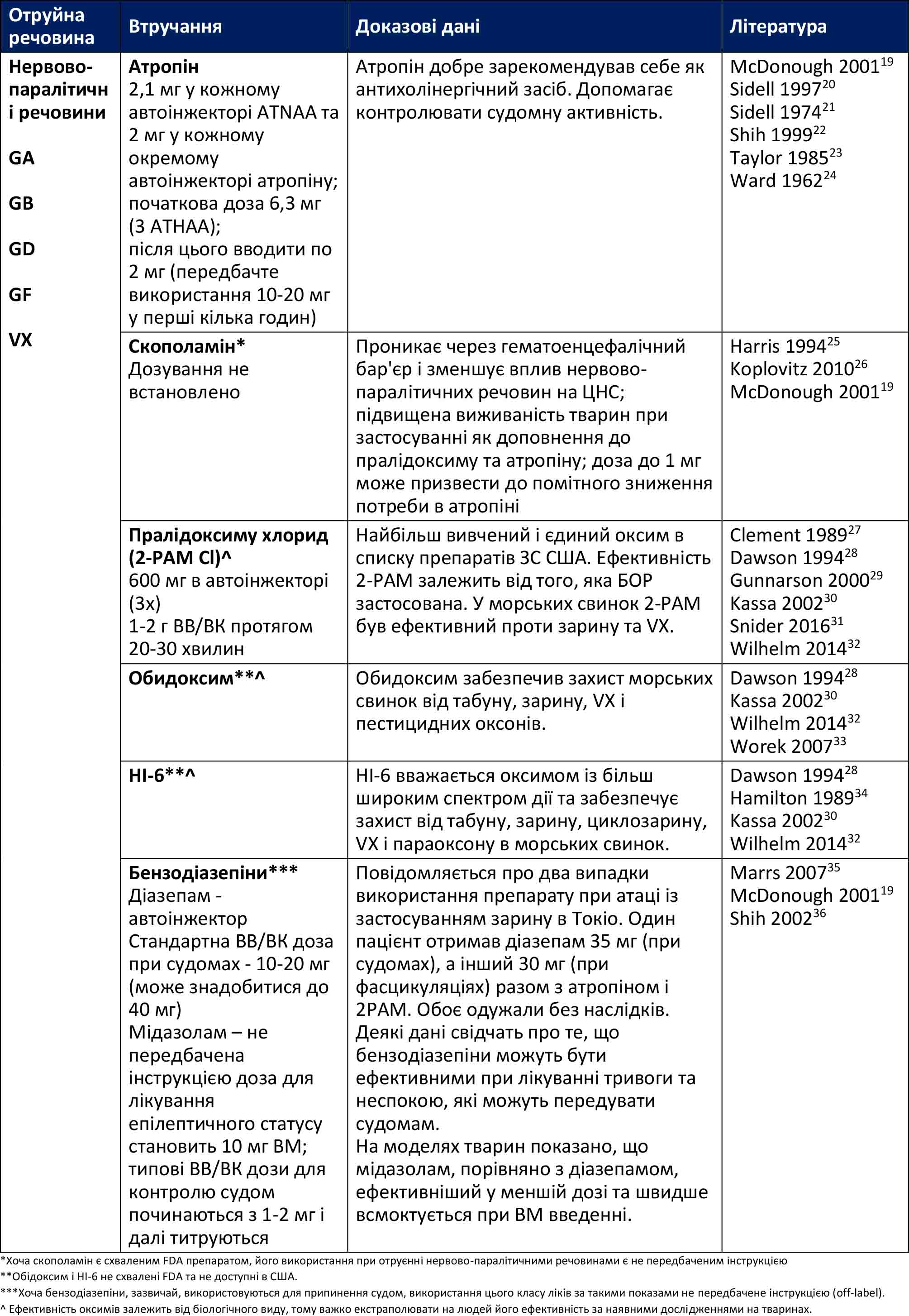
Лікування отруєнь нервово-паралітичними речовинами
Антидотами до нервово-паралітичних отрут є пралідоксим (2PAM), атропін і бензодіазепіни. Автоінжектор (шприц-ручка) для лікування нервово-паралітичних отруєнь доступний у вигляді Autoinjector Nerve Agent Antidote (ATNAA), який містить атропін і 2PAM, а також Convulsant Antidote Nerve Agent (CANA), який містить бензодіазепін діазепам.
2PAM (пралідоксим)
2-піридин альдоксим метилхлорид, або пралідоксим, (вводиться за допомогою автоінжектора ATNAA або ВВ/ВК) реактивує ацетилхолінестеразу, запобігаючи незворотному зв’язуванню нервово-паралітичної речовини з ацетилхолінестеразою, яке називається “старінням”. 2PAM доступний як у формі автоінжектора, так і у вигляді форми для ВВ введення. 2PAM діє синергічно з атропіном (приблизно в 30 разів сильніше). Існують інші оксими з різним ступенем ефекту залежно від діючої речовини, але доступним засобом, який є у списку Міністерства оборони США, є пралідоксим.
Атропін
Атропін (вводиться за допомогою автоінжектора ATNAA або ВВ/ВК) використовується для усунення мускаринових ефектів. Атропін “висушує” надмірну секрецію (бронхорею) і зменшує бронхоконстрикцію, спричинену нервово-паралітичним агентом. Кількість нервово-паралітичної речовини та важкість симптомів у пацієнта визначатимуть кількість атропіну, необхідного для контролю цих симптомів. Для усунення дії деяких нервово-паралітичних речовин, зокрема фосфорорганічних кислот, можуть знадобитися великі дози атропіну. Тахікардія НЕ є протипоказанням для введення атропіну, оскільки тахікардія може бути вторинною щодо дихальної недостатності. Тому атропін слід продовжувати вводити для усунення загрозливої для життя бронхореї та бронхоконстрикції навіть за наявності тахікардії.
Бензодіазепіни
Бензодіазепіни, такі як діазепам (CANA) або мідазолам, є основними при лікуванні судом. Бензодіазепіни також можуть допомогти усунути ефекти подразнення нікотинових рецепторів, зокрема м’язові фасцикуляції. Сучасна література визначає мідазолам як найефективніший засіб для припинення судом (на основі досліджень на тваринах). Мідазолам має найвищу біодоступність при внутрішньом’язовому введенні. Діазепам міститься в автоінжекторі і є ефективним, але цілком доцільно використовувати інший бензодіазепін, якщо є ВВ доступ або коли автоінжектори закінчились.
Антидоти нервово-паралітичних речовин можуть бути дозовані залежно від тяжкості симптомів. Однак у польових умовах, коли кількість і тип впливу нервово-паралітичної речовини невідомі, введіть 3 ATNAA та 1 CANA будь-якому пацієнту з симптомами (окрім ізольованого міозу), які могли бути спричинені нервово-паралітичною речовиною. Якщо, незважаючи на введені антидоти, симптоми зберігаються, розгляньте крапельне введення атропіну (див. протокол застосування атропіну/скополаміну в Додатку А). При тяжкому отруєнні можна ввести додатково 2PAM після введення 3 ATNAA. Існує недостатня кількість даних стосовно дозування, але поточний консенсус експертів рекомендує додатково вводити 500 мг ВВ/ВК протягом 5 хвилин, а потім продовжити введення краплинно, 10 мг/кг/год, до стабільного клінічного покращення, що може вимагати інфузії більше 24 годин. (Див. Додаток B.)
Профілактика
Особливості планування та аналіз співвідношення ризик/користь у прийнятті рішення щодо профілактики піридостигміну бромідом (ПБ) виходять за межі даних настанов. Однак, медикам важливо розуміти клінічні ефекти при профілактиці піридостигміном, і те, як таке профілактичне введення може вплинути на клінічні прояви ураження та відповідь на лікування. Піридостигмін (таблетки по 30 мг) схвалено FDA для використання в якості профілактичного засобу при очікуваному ураженні зоманом на основі ефективності зниження летальної дії зоману при застосуванні разом із 2PAM та атропіном у тварин. (Див. листок-вкладку FDA щодо використання піридостигміну броміду) Досліджень на людях не проводилося.
Піридостигмін діє шляхом пригнічення 20-40% периферичної ацетилхолінестерази. Він не проникає через гематоенцефалічний бар’єр, тому не викликає центрального гальмування. Таким чином, побічними ефектами профілактики піридостигміном є, як правило, легкі холінергічні або нікотинові симптоми (діарея, біль у животі та дисменорея були найпоширенішими побічними ефектами у добровольців). Піридостигмін і мефлохін (для профілактики малярії), прийняті разом, можуть мати адитивний ефект на шлунково-кишковий тракт із посиленням діареї. Якщо поєднати піридостигмін з опіоїдами, то може посилитися опіоїд-асоційована брадикардія. Піридостигмін може підвищити ефект деполяризуючих міорелаксантів (сукцинілхоліну), але може спричинити потребу в вищих дозах недеполяризуючих міорелаксантів. Лікування при ураженні нервово-паралітичними речовинами для тих, хто прийняв профілактично піридостигмін, нічим не відрізняється.
Таблиця 4. Лікування отруєнь нервово-паралітичними речовинами
Отруєння речовинами задушливої дії
Передумови
Отруйні речовини задушливої дії (їх також називають токсичними промисловими хімікатами та задушливими речовинами) мають історичне значення як попередники сучасної хімічної війни та все ще залишаються актуальними сьогодні як ймовірні хімічні використовувані агенти, враховуючи їх доступність. Хлор і фосген виробляються і зберігаються у великих кількостях по всьому світу, і можуть мати руйнівні наслідки при випаровуванні. Існують інші речовини, які можуть спричинити хімічне пошкодження легенів, наприклад аміак, сірководень, оксид цинку, фосфорний дим та перфторізобутилен (побічний продукт синтезу тефлону). Ці агенти подразнюють легені, але, менш імовірно, що вони будуть використані під час хімічної атаки.
Хлор стає газоподібним при -34 °C і тому зберігається у вигляді стисненої рідини. Фосген стає токсичним газом при 8,33 °C. Ступінь ураження будь-яким газом залежить від тривалості впливу та концентрації речовини. Інші чинники, які впливають на токсичність, включають частоту та глибину дихання (хвилинний об’єм дихання) і, можливо, положення тіла.
Вплив 30 ppm (0,03 г/л) хлору викликає кашель; більш серйозне пошкодження легень відбувається при рівнях вище 40-60 ppm (0,04-0,06 г/л) при впливі більше 30 хвилин. Фосген важче виявити, а його токсичність при тривалому впливі виникає при рівні нижче порога запаху (0,4 ppm - 0,004 г/л). Крім того, може виникнути “нюхова втома”, тому людина може лише тимчасово відчувати небезпечний запах. IDHL (Immediately Dangerous to Life or Health - доза, яка становить негайну небезпеку для життя або здоров’я) для фосгену становить 2 ppm (0,002 г/л), тоді як IDHL для хлору становить 100 ppm (0,1 г/л).
Обидва гази реагують з вологою в дихальній системі та піддаються гідролізу. Хлор спричиняє пошкодження легень через реакції з утворенням соляної та гіпохлоритної кислот, які, у свою чергу, реагують із сульфгідрильними групами цистеїну та викликають інгібування ферментів. На додаток до цієї реакції, гідроліз хлору веде до утворення вільних радикалів, які можуть призвести до прямого пошкодження клітини та її смерті. Фосген також реагує з водою з утворенням вуглекислого газу та хлористого водню. Однак, вважається, що основна токсичність фосгену виникає внаслідок ацилювання, під час якого фосген взаємодіє з сульфгідрильними, амінними та гідроксильними групами, спричиняючи денатурацію білків та ліпідів, руйнуючи структуру мембрани та перешкоджаючи функціонуванню ферментів. Фосген також пошкоджує легеневий сурфактант.
Ознаки та симптоми
Обидва гази мають здатність викликати асфіксію через витіснення кисню, якщо вони вивільняються в замкнутому просторі. Найчастіше гази діють як подразники та спричиняють пошкодження дихальних шляхів через описані вище механізми. Нарешті, гази можуть викликати системну запальну реакцію.
Хлор має неприємний запах і сильну подразнювальну дію. Оскільки хлор піддається більш швидкому гідролізу при контакті зі слизовими оболонками, він швидше викликає симптоми на зволожених ділянках очей, рота та верхніх дихальних шляхів. Частими є біль в очах, блефароспазм і сльозотеча. Інші симптоми можуть включати головний біль, слиновиділення, задишку, кашель, кровохаркання, печіння в грудях і блювоту.
Фізикальне обстеження може виявити тахікардію, тахіпное та, можливо, ціаноз. Якщо є подразнення очей, слід оглянути постраждалого на предмет опіків/пошкодження рогівки за допомогою фарбування ока флюоресцеїном. За наявності орофарингеальної еритеми можливе бути більш значне дистальне пошкодження, що вимагає ретельної оцінки дихальних шляхів. Стридор, захриплість або афонія можуть свідчити про набряк гортані або ларингоспазм. Може бути рясна секреція з ротоглотки.
Фосген пахне свіжоскошеним сіном. Він діє більш непомітно, тому в ранньому періоді симптоми можуть бути невираженими або зовсім відсутніми. Типовий початок симптомів, викликаних фосгеном, настає через 2-6 годин після впливу, а відстрочені симптоми були описані до 15 годин після впливу. Основний вплив фосгену відбувається на периферичні дихальні шляхи, тому типовими симптомами є задишка, стиснення в грудях (або біль) і кашель. Розвиток гіпоксії та набряку легенів може відбуватися через кілька годин після появи симптомів. Переміщення рідини внаслідок набряку легень може призвести до гіповолемії. Рання поява набряку легенів свідчить про поганий прогноз.
Деконтамінація при ураженні речовинами задушливої дії
При токсичному впливі хлору або фосгену пріоритетом є безпечне виведення з зони ураження. Захист органів дихання рятувальників і медиків у зоні потенційного ураження має вирішальне значення. Після того, як пораненого виведено із зони впливу отруйної речовини, слід продовжити деконтамінацію, знявши весь одяг. При впливі токсичного газу це усуває більшість ризиків, пов’язаних із газами. Для повної деконтамінації достатньо використовувати воду та мило.
Діагностика отруєнь речовинами задушливої дії
Немає доступних діагностичних тестів для підтвердження або кількісної оцінки токсичності речовин задушливої дії. Стандартні тести, такі як гази артеріальної крові та рентгенографія органів грудної клітки, повинні використовуватися для визначення підтримувальної терапії, якщо це необхідно. Гази артеріальної крові можуть бути корисними для моніторингу оксигенації, але їх показники можуть бути нормальними на ранньому етапі ураження фосгеном. PCO2 може бути підвищеним у пацієнтів з бронхообструкцією та вказувати на потребу в бронходилятаторах або кортикостероїдах.
Подібно до газів артеріальної крові, рентгенографія органів грудної клітки, виконана невдовзі після ураження, може бути нормальною, але є ймовірність розвитку набряку легень протягом кількох годин після ураження. На щастя, рентгенографія може виявити набряк легенів до появи фізикальних ознак. Вихідний рентгенографічний знімок органів грудної клітки може бути корисним для порівняння при спробі виявити незначні ранні ознаки набряку легень. Якщо результати рентгенографії нормальні через 8 годин, малоймовірно, що у пацієнта розвинеться набряк легень.
Таблиця 5. Отруйні речовини задушливої дії
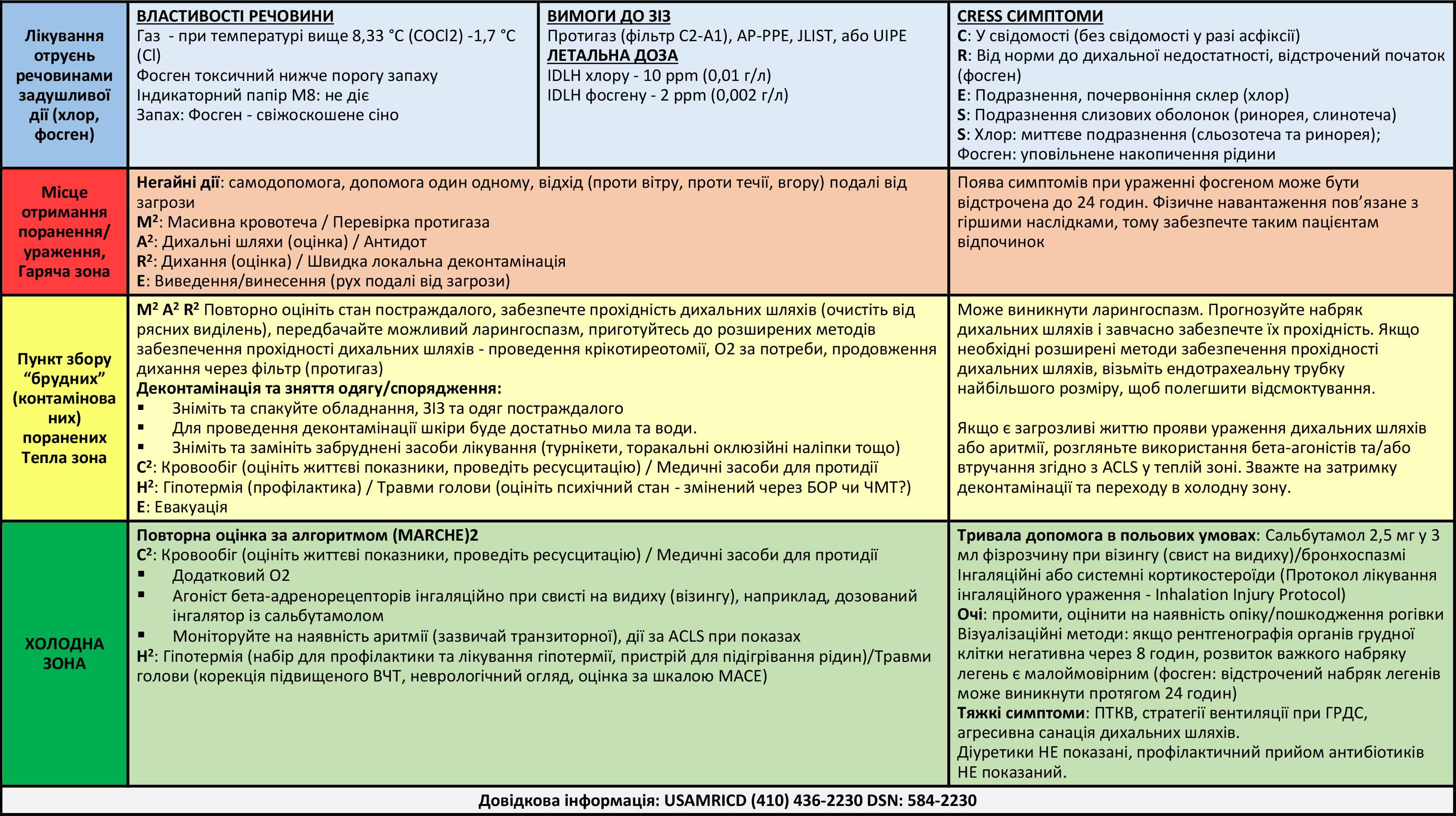
Лікування отруєнь речовинами задушливої дії
Ураження хлором може призвести до рясних виділень і ларингоспазму незабаром після контакту, тому медики повинні бути готові до забезпечення прохідності дихальних шляхів і, можливо, невідкладного хірургічного втручання (крікотиреотомії). Важливо пам’ятати, що пацієнтів, які зазнали впливу фосгену, незважаючи на відсутність симптомів, потрібно лікувати як постраждалих. Вони повинні залишатися в спокої, оскільки фізичне навантаження пов’язане з розвитком набряку легень та в загальному з гіршими наслідками для таких пацієнтів. Якщо застосовані розширені методи забезпечення прохідності дихальних шляхів, встановлена ендотрахеальна трубка великого діаметра полегшить санацію дихальних шляхів, оскільки вплив токсичних газів може спричинити відшарування слизової оболонки з обструкцією дихальних шляхів.
Внутрішньовенне введення рідини може бути необхідним у разі дефіциту об’єму циркулюючої крові, але його не слід проводити емпірично. Перевантаження рідиною може сприяти розвитку набряку легенів, тому його слід уникати. Може знадобитися проведення ларингоскопії та/або бронхоскопії, а на випадок вираженого порушення прохідності дихальних шляхів слід приготувати розширені методи забезпечення їх прохідності. Використання портативних апаратів штучної вентиляції легень зі спрощеним автоматичним налаштуванням параметрів (наприклад, апарати ШВЛ SAVe) може бути недостатнім для забезпечення адекватної вентиляції у цих пацієнтів. Через асоційований набряк легенів, бронхоспазм і ризик ГРДС вміння відповідно налаштовувати апарат ШВЛ має вирішальне значення. Крім того, відсмоктування є ключовим компонентом підтримки прохідності дихальних шляхів. Проведення санації грушею (спринцівкою) навряд чи буде ефективним, тому перевага надається механічній аспірації з можливістю використання закритої аспіраційної системи.
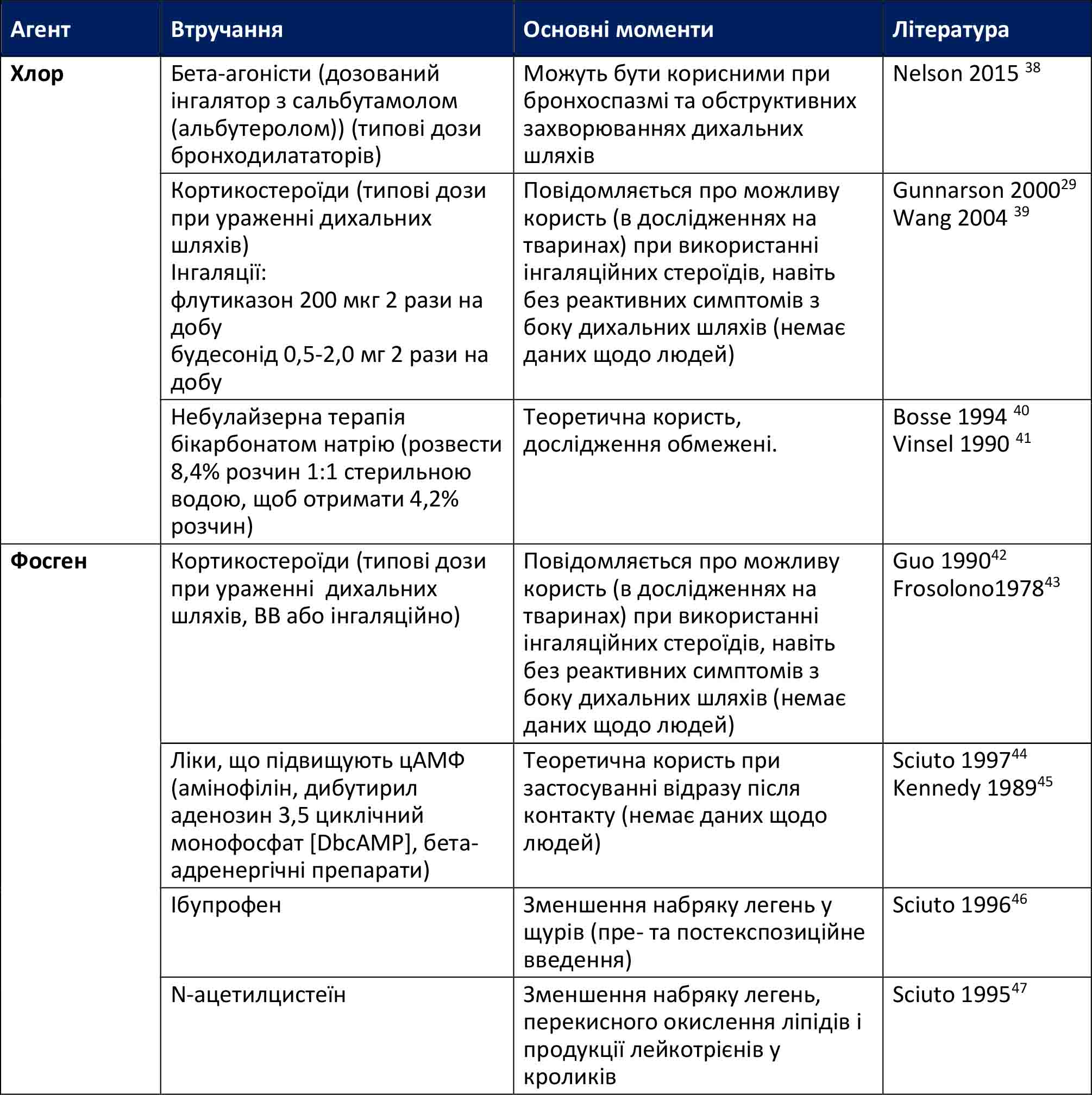
Розширені втручання та докази на їх підтримку описані в таблиці нижче. Значна частина доказів базується на дослідженнях у тварин. Дані щодо людей обмежені.
Таблиця 6. Лікування отруєнь речовинами задушливої дії
Отруйні речовини шкірно-наривної дії (везиканти)
Передумови
Отруйні речовини шкірно-наривної дії були розроблені та використовувалися під час Першої світової війни як хімічні бойові отруйні речовини48, 49. Ці речовини можуть використовуватися в різних формах, включаючи тверду, рідку чи газоподібну. Існують такі види отруйних речовин шкірно-наривної дії: сірчаний іприт, азотний іприт і люїзит. Сірчаний іприт використовується в різних концентраціях та формах; у даний час він є найпоширенішою речовиною шкірно-наривної дії, яка використовується на полі бою.
Сірчаний іприт має три основні форми: HD, який є дистильованим продуктом і має близьку до 100% чистоту; Н, що є недистильованим сірчаним іпритом; і HT, який є сумішшю HD і T (загущувач, який можна додавати до сірчаного іприту). HD, або чистий іприт, прозорий і пахне часником. Сірчаний іприт Н може бути прозорим, жовтим, червоно-коричневим або чорним залежно від хімічної суміші. Під час останніх конфліктів, включаючи конфлікт з ІДІЛ, саме сірчаний іприт Н був хімічною речовиною, яку використовували на полі бою. Ця речовина, виготовлена в саморобних хімічних лабораторіях, є густою мастилоподібною чорною речовиною, яка швидко розкладається, маючи термін придатності всього 2-3 тижні.
Азотний іприт набагато рідше використовується як бойова хімічна речовина. Існує 3 форми азотного іприту: N1, N2 і N3. Азотний іприт може мати різні запахи: N1 більше нагадує рибу, N2 – фрукти, а N3 – гіркий мигдаль. Азотні іприти — це олійні речовини, від прозорих до жовтого кольору, які повільно випаровуються і можуть спричинити ураження рятувальників через безпосередній контакт або виділення газу від постраждалих контамінованих осіб. Використовувані в медичних цілях, таких як хіміотерапія або видалення бородавок, ці речовини досі ніколи не використовувалися на полі бою.
Люїзит є останньою отруйною речовиною шкірно-наривної дії у цій групі хімічних речовин. Споріднений з миш’яком, люїзит в чистому вигляді - прозора рідина, бурштиновий або чорний - у сумішах. Як і інші везиканти, він дуже подразнює шкіру, очі та дихальні шляхи. Люїзит можна змішувати з HD для отримання більш потужної хімічної бойової речовини з властивостями обох речовин. На відміну від інших везикантів, люїзит - єдина речовина, яка має антидот для протидії системним ефектам.
Ознаки та симптоми ураження везикантами
Найпоширеніший шлях впливу всіх отруйних речовин шкірно-наривної дії – через шкіру. Сірчані іприти викликають хімічні опіки з пухирями протягом кількох годин після контакту зі шкірою або слизовими оболонками. Одразу при контакті ефект не виникає, сірчаний іприт всмоктується протягом декількох хвилин після контакту зі шкірою або оболонками очей. Опіки другого та третього ступеня розвиваються протягом 2-10 годин на очах і шкірі, викликаючи інтенсивний біль, перфорації рогівки, ерозії слизової оболонки очей та утворення пухирів на всій відкритій шкірі. Рівень смертності від HD під час Першої світової війни становив 2-3%, але опіки понад 25% поверхні тіла можуть бути смертельними. Азотний іприт має подібну до сірчаного іприту дію на шкіру та очі. Щодо люїзиту, то він миттєво впливає на шкіру та очі, викликаючи негайний біль та подразнення, а також утворення пухирів набагато раніше, ніж HD або азотистий іприт.
Вдихання або проковтування везикантів веде до подібних пошкоджень слизової оболонки дихальної і травної систем, спричиняючи виникнення сильних опіків. Рідкі агенти, які є концентрованішими, завдають більшої шкоди, ніж випари, які можна вдихнути. Так само, як вплив на шкіру та очі, вдихання HD має відстрочену дію на дихальні шляхи, призводячи до виникнення свиту на видиху (візингу) та набряку бронхіол через кілька годин після впливу. Як і у випадку шкірних симптомів, люїзит викликає респіраторні симптоми набагато швидше, як правило, протягом декількох секунд або хвилин, після чого стан швидко прогресує до набряку легенів.
Залежно від дози та шляху впливу, всі види БОP шкірно-наривної дії можуть спричиняти деякі пізні ефекти. Може виникнути пригнічення функцій кісткового мозку, що призведе до підвищеної схильності до розвитку інфекцій. Азотистий іприт може спричинити анемію. Високі дози сірчаного іприту можуть викликати судоми і підвищену збудливість. Високі дози люїзиту можуть призвести до некрозу печінки, гострої ниркової недостатності та шоку через підвищену проникність капілярів - так званий «люїзитний шок». Є багато ймовірних віддалених наслідків, таких як злоякісні пухлини, рубцювання рогівки, хронічні респіраторні захворювання та рубці на шкірі.
Деконтамінація при ураженні везикантами
Безпека рятувальників і медичних працівників є найважливішим початковим кроком при наданні допомоги постраждалим від ураження іпритом. Рятувальники повинні одягнути засоби захисту органів дихання та шкіри. Бутилкаучук - рекомендований рівень захисту для рук, однак дві пари нітрилових рукавичок також захищають від шкідливого впливу. Пам’ятайте, що контаміновані пацієнти можуть не виглядати такими, що несуть небезпеку зараження оточуючих, через відстрочену появу симптомів, однак медики все одно можуть зазнати значних ушкоджень легень, очей і шкіри, якщо їх не захистити належним чином. Постраждалому необхідно провести деконтамінацію, зняти весь одяг та обладнання; везиканти потрапляють в організм протягом декількох хвилин, але також можуть залишатися на обладнанні чи одязі протягом кількох днів після контакту.
Очищення від отруйної речовини повинно відбуватися протягом трьох-п'яти хвилин, щоб зменшити всмоктування. Очищення сухою тканиною є першим кроком при деконтамінації шкіри, після чого слід застосувати ЛДУШ. До везикантів не існує антидота, як до нервово-паралітичних речовин, тому початкове лікування зосереджується на швидкій деконтамінації. Потрапляння в очі спричиняє швидше всмоктування, ніж на шкірі, тому очі слід негайно промити водою, щоб зменшити наслідки. Набори для промивання очей з іригаційними лінзами Моргана можуть полегшити деконтамінацію очей. Важливо не викликати блювоту, якщо є підозра щодо проковтування; ефективність активованого вугілля в таких ситуаціях не доведена. Після деконтамінації рекомендується стандартне лікування, як при опіках шкіри. Інфузійна терапія може не відповідати розрахункам, рекомендованим при термічних опіках; однак, виділення сечі залишається хорошим маркером адекватної ресусцитації, тому кількість рідини слід титрувати, щоб досягти цільового рівня діурезу 30-50 мл/год.
Хімічно контаміновані рани слід ретельно промити та обробити за принципом обробки дуже забруднених ран. Іприт потрапляє в організм та розповсюджується системно практично відразу після контакту з відкритими ранами або слизовими оболонками. Після первинної деконтамінації пацієнта слід транспортувати до лікарні та спостерігати за системними та місцевими ефектами контамінованої рани. Для таких ран майже завжди буде потрібне проведення хірургічної обробки (як при відкритих ранах).
Діагностика отруєння речовинами шкірно-наривної дії
Немає швидкого і доступного тесту для підтвердження контакту з везикантами. У перший день виникає лейкоцитоз і наростає відносно до ступеня ураження. Згодом відбувається пригнічення функцій кісткового мозку, кількість лейкоцитів починає знижуватись орієнтовно на третій-п’ятий день, з найнижчим рівнем приблизно на 9-й день. Показники менше 500 означають поганий прогноз. Рентгенографію органів грудної клітки можна використовувати для моніторингу пневмоніту, який зазвичай з’являється в перші 2-3 дні.
Лікування отруєнь речовинами шкірно-наривної дії
Для безсимптомних пацієнтів, які зазнали впливу сірчаного іприту та азотного іприту, ефекти з боку шкіри, очей і легенів можуть бути відстроченими, тому рекомендується спостерігати за ними 6-10 годин.
Пацієнтам із ураженням очей може бути корисним регулярне застосування антихолінергічної офтальмологічної мазі для запобігання утворенню синехій. Мазь із антибіотиком/стероїдами слід наносити кожні 1-2 години зі швидким скеруванням до офтальмолога. Нанесення мазі на повіки запобігає їх злипанню і може допомогти запобігти утворенню спайок, забезпечуючи дренування патологічних виділень. При блефароспазмі можна призначити місцевий анестетик, щоб полегшити огляд очей. При постійному болю в очах слід призначити системні анальгетики.
Таблиця 7. Лікування отруєнь речовинами шкірно-наривної дії (везикантами)
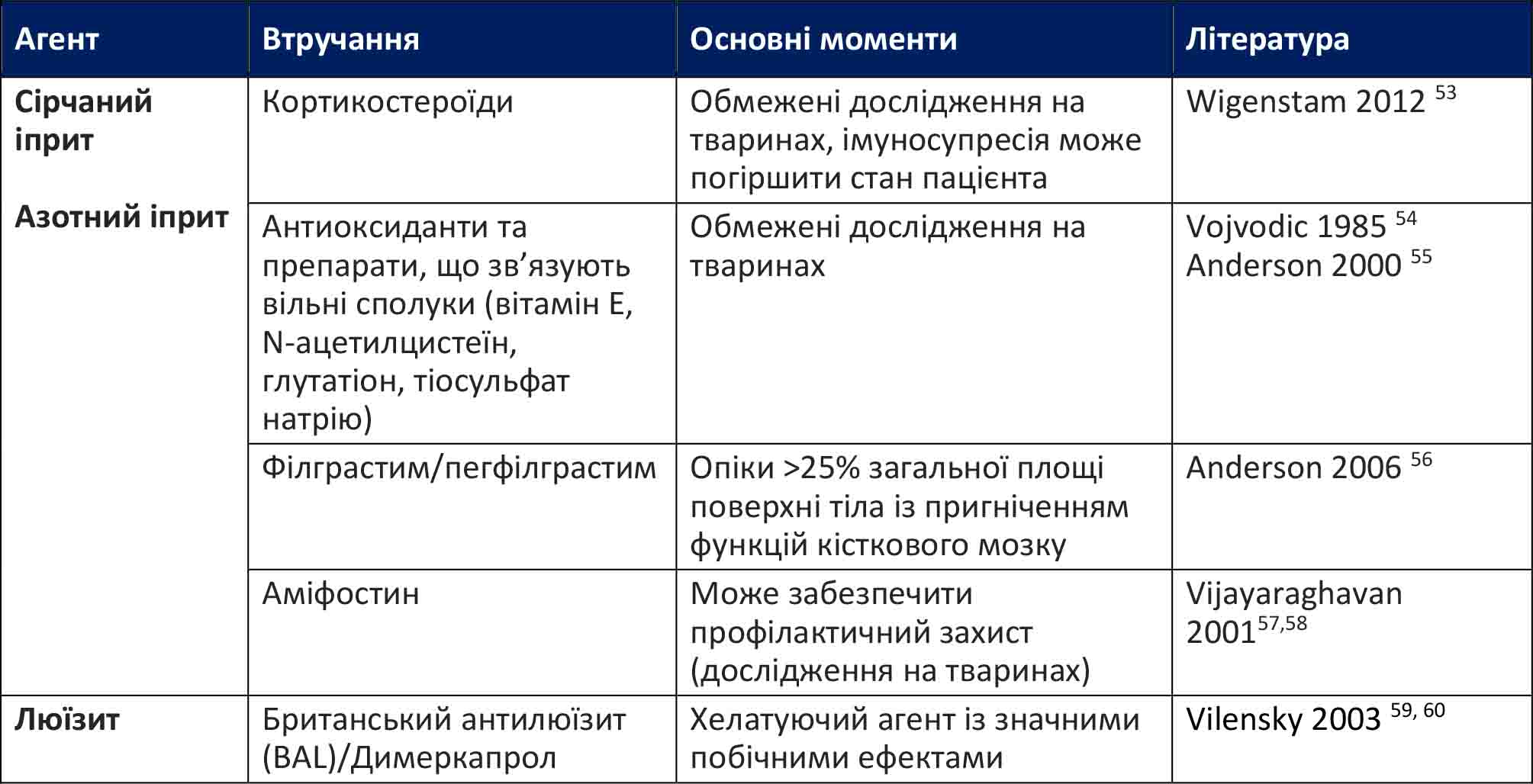
Якщо у пацієнтів виникають респіраторні симптоми через кілька годин після впливу агента, їх слід лікувати як хімічний пневмоніт; необхідно агресивно призначати альбутерол (сальбутамол) і при відсутності належної реакції розглядати інвазивне лікування дихальних шляхів на ранніх стадіях лікування. Використання системних стероїдів рекомендується у разі неефективності альбутеролу, але подальше пригнічення імунітету може бути недоцільним. Застосування бікарбонату натрію інгаляційно також було запропоновано як можливе лікування, але немає надійних доказів на підтримку його використання. Інші антиоксиданти та препарати, що зв’язують вільні сполуки, такі як тіосульфат натрію, продемонстрували певну користь у дослідженнях на тваринах, але немає даних, які б підтверджували користь від їх використання у людей. Цю терапію слід розглядати лише у пацієнтів, які не мають ефекту від підтримувальної терапії, коли користь від недоказового лікування переважає потенційні ризики.
Пригнічення кісткового мозку зазвичай досягає піку приблизно на 9-10 день. Можна вводити аналоги гранулоцитарного колонієстимулюючого фактора. Важке пригнічення функцій кісткового мозку може бути показанням до трансплантації кісткового мозку.
Антидотом до люїзиту є британський антилюїзит (BAL), також відомий як димеркапрол. BAL слід застосовувати лише в умовах стаціонару у вигляді внутрішньом’язової ін’єкції. BAL є хелатуючим агентом, але через можливість важкої гострої ниркової недостатності та інших побічних ефектів BAL рекомендується використовувати лише у пацієнтів, які мають важкі респіраторні симптоми або люїзитний шок.
Таблиця 8. Отруйні речовини шкірно-наривної дії (везиканти)
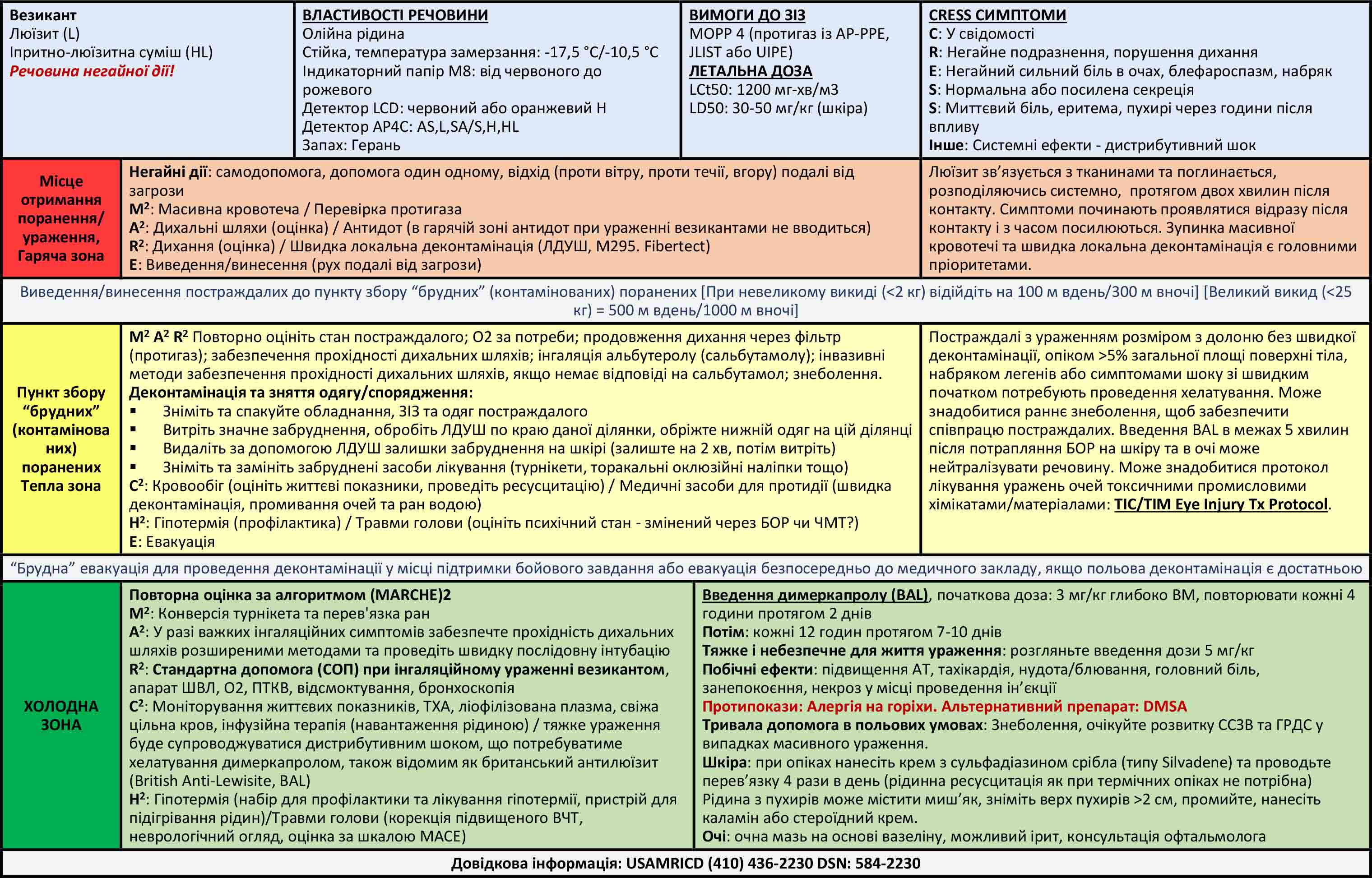
Інкапаситанти (психохімічні речовини)
Передумови
Інкапаситанти (психохімічні речовини) спричиняють тимчасові фізичні та/або психічні ефекти, які призводять до нездатності постраждалої особи продовжувати виконувати свої обов’язки чи звичайну діяльність. Часто їх описують як нелетальні агенти, але якщо вводити їх у достатньо високих дозах, інкапаситанти можуть призвести до смерті або тяжких захворювань. Існує три категорії отруйних речовин, що призводять до тимчасової втрати працездатності.
1. Антихолінергічні засоби
BZ (3-хінуклідинілбензилат) є типовим антихолінергічним засобом, але для бойових дій можуть виготовлятися й інші антихолінергічні речовини. Повідомляється, що британці мають подібний засіб, відомий як Агент 15. BZ — це антихолінергічний засіб центральної дії, який спочатку був розроблений як шлунково-кишковий спазмолітик, але через виражені ефекти з боку центральної нервової системи від нього відмовились як від фармацевтичного засобу. Як інкапаситант, він має дуже високий профіль безпеки завдяки відносно слабким периферичним антимускариновим ефектам порівняно з атропіном. Ефективна доза, що призводить до втрати працездатності, становить 0,5 мг. BZ, зазвичай, розсіюється у вигляді аерозолю або в димових боєприпасах.
2. Седативні засоби
Опіоїди та леткі анестетики є потенційними седативними або заспокійливими засобами. Фентаніл є синтетичним опіоїдом, у 100 разів сильнішим за морфін. Постійно розробляються нові похідні фентанілу. Одним із таких прикладів є карфентаніл з дією, яка в 100 разів перевищує фентаніл. Незважаючи на те, що ці речовини є дуже ефективними, розпилення їх як інкапаситантів може бути проблематичним. Досліжено, що поглинання в натовпі буде різним.
3. Іританти (засоби контролю натовпу)
Засоби контролю натовпу, також відомі як отруйні речовини для боротьби з масовими заворушеннями, викликають подразнення та дискомфорт, часто у вигляді сльозотечі, подразнення слизових оболонок, сильного кашлю або блювоти. Типові агенти включають хлорацетофенон (CN), широко відомий як Mace, хлорбензиліден малононітрил (CS), олеорезин капсікум (OC) - перцевий спрей, та дифеніламінохлорарсин (DM), або адамсит. CN є більш токсичним, ніж інші агенти з нижчою LCt50. DM має тенденцію викликати блювоту.
Таблиця 9. Інкапаситанти (психохімічні речовини)
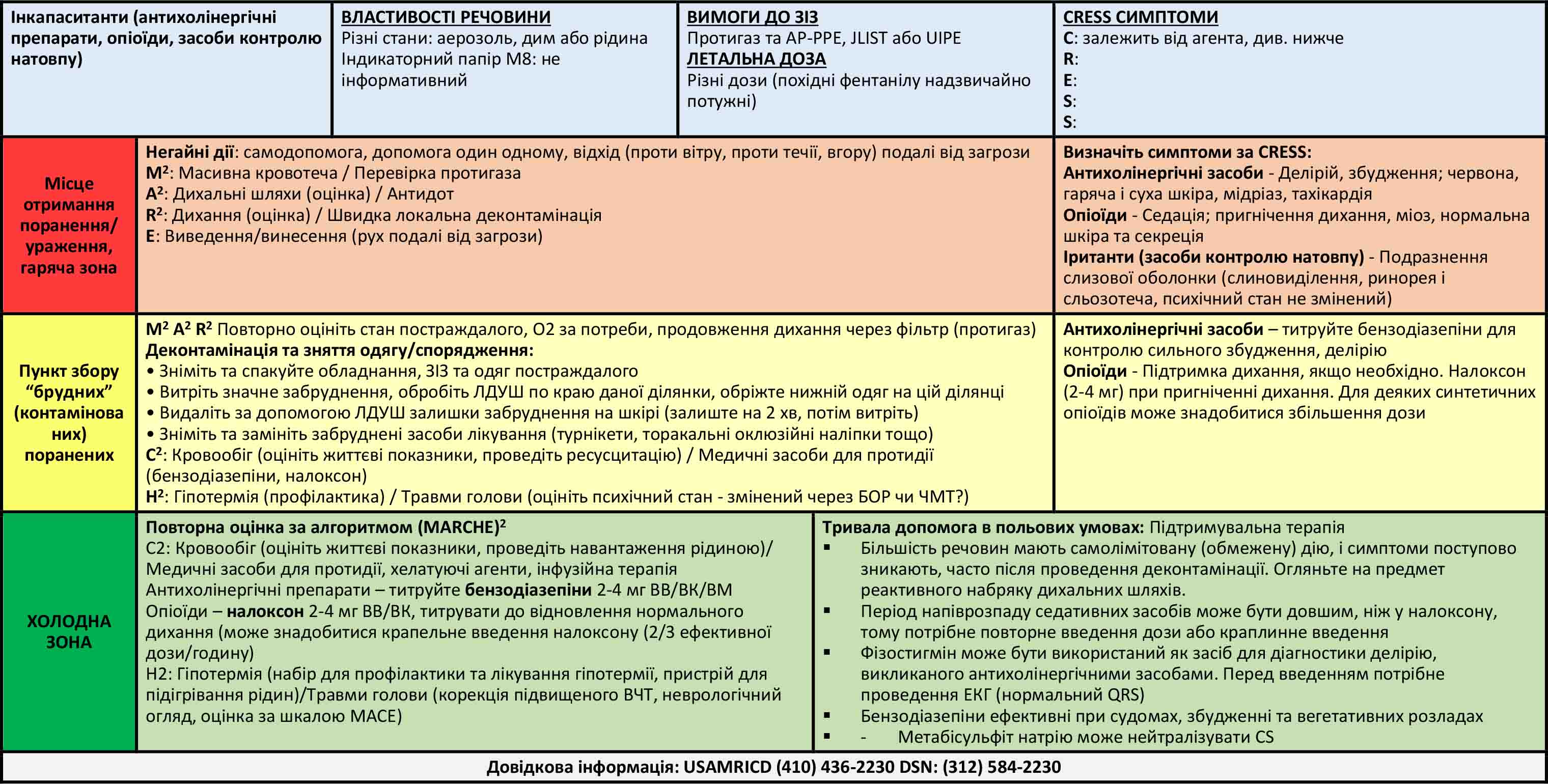
Ознаки та симптоми отруєння інкапаситантами
Антихолінергічні засоби
BZ призначений уражати ЦНС, тому основним симптомом буде антихолінергічний делірій, а периферичні ефекти будуть менш вираженими. Часто пацієнт не може надати чіткий анамнез через деліріозний стан. Делірій може бути лабільним і варіюватися від легкого порушення до коми. Можуть виникнути галюцинації, сильне збудження і навіть судоми. Класичні периферичні прояви, які часто описують як «сухий, як кістка, гарячий, як заєць, червоний, як буряк, і сліпий, як кажан», можуть бути різної інтенсивності або виникати пізніше.
Седативні засоби
Седативні засоби, які є похідними опіоїдів, можуть викликати класичний опіоїдний токсидром з міозом, пригніченням ЦНС і дихання. Брадикардія, артеріальна гіпотензія та гіпотермія можуть виникати як вторинні наслідки в результаті дозозалежного прогресування до опіоїдної коми.
Іританти
Іританти (засоби контролю натовпу) уражають шкіру, дихальну систему та очі. Офтальмологічні симптоми включають біль, сльозотечу та блефароспазм. Ступінь ураження дихальних шляхів може бути різним: симптоми варіюють від легкого подразнення слизової оболонки до сильної задишки, кашлю та відчуття стискання в грудях. Бронхоспазм є поширеним явищем і може бути важким у тих, хто має супутні захворювання дихальних шляхів. Можуть виникнути рясна ринорея та слиновиділення, тому необхідне клінічне обстеження, щоб виключити можливість впливу нервово- паралітичних речовин. Дерматологічні ефекти зазвичай включають біль та печіння, крім того, при більш високих дозах може бути утворення пухирів.
Загальні принципи надання допомоги
Безпечне виведення/винесення постраждалого з зони впливу агента є пріоритетом. Захист органів дихання для медиків у зоні потенційного впливу має вирішальне значення. Після того, як постраждалого виведено із зони ураження, можна продовжити проведення деконтамінації, знявши весь одяг та особисті речі. Для повної деконтамінації достатньо простого мила та великої кількості води. Пам’ятайте, що покращення симптомів, викликаних інкапаситантами, після деконтамінації може бути тимчасовим.
Лікування при ураженні інкапаситантами є переважно підтримувальним і залежить від симптомів та загального стану пацієнта.
Антихолінергічні засоби
Пацієнти з ураженням антихолінергічними речовинами можуть мати сухість у роті і тахікардію, що наведе медика на думку про дегідратацію, у той час, як насправді у пацієнта еуволемія. Однак, поширеними також є і психомоторне збудження та гіпертермія, тому важливий ретельний моніторинг внутрішньої температури, рідинного статусу та діурезу. При наявності гіпертермії слід негайно провести заходи з охолодження.
Фармакологічне лікування включає усунення делірію та збудження. Збудження можна безпечно контролювати за допомогою бензодіазепінів, титруючи до досягнення ефекту. Часто при зменшенні збудження знижується тахікардія та гіпертермія. Фізостигмін також є варіантом лікування делірію. Це третинний амін, який проникає через гематоенцефалічний бар'єр. Перед застосуванням фізостигміну важливо виключити прийом інших блокаторів натрієвих каналів, таких як трициклічні антидепресанти. Перед застосуванням фізостигміну слід зробити ЕКГ, щоб переконатися у нормальній тривалості комплексу QRS (<100 мс). Таким чином, відсутність негайної можливості зробити ЕКГ обмежує застосування фізостигміну. Крім того, слід приготувати атропін на випадок побічної холінергічної реакції, яка негативно впливає на прохідність дихальних шляхів. У більшості випадків бензодіазепіни вважаються основним варіантом лікування, оскільки їх можна безпечно призначати майже всім пацієнтам.
Седативні засоби
Підтримка дихання є основним напрямком лікування опіоїдної токсичності, пов’язаної із седативними засобами. Налоксон є антидотом вибору, його слід титрувати, щоб усунути пригнічення дихання. Назальний налоксон можна швидко ввести без забезпечення внутрішньовенного доступу. Дозу налоксону слід титрувати до отримання ефекту. Доцільно починати з 2-4 мг, але, щоб усунути ефект синтетичних опіоїдів, можуть знадобитися значно вищі дози. Період напіввиведення налоксону може бути коротшим, ніж період напіввиведення отруйної речовини, а тому може знадобитися повторне введення дози або крапельна інфузія налоксону.
Іританти
Більшість засобів контролю натовпу мають коротку дію, і підтримувальної терапії зазвичай достатньо (проводиться до зникнення симптомів).
Діагностика при отруєнні інкапаситантами
Лабораторні показники мають низьку діагностичну цінність. Опіоїди можуть бути виявлені під час рутинного токсикологічного скринінгу.
Лікування при отруєнні інкапаситантами
Розширені втручання та доказові дані наведені в таблиці нижче.
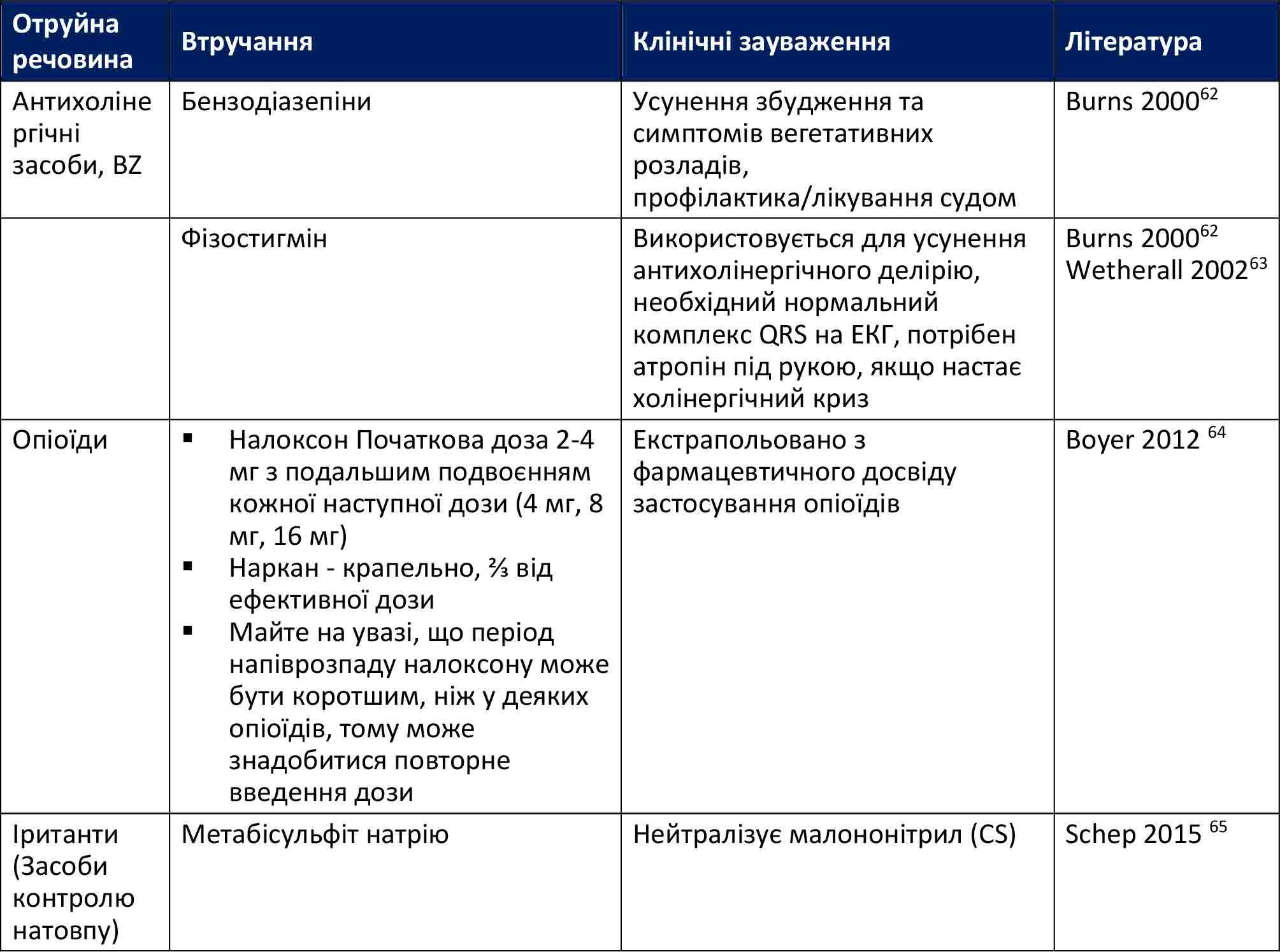
Таблиця 10. Лікування при ураженні інкапаситантами (психохімічними речовинами)
Скорочення
ACLS: Advanced Cardiac Life Support (Розширена серцево-судинна підтримка життя)
AP4C: Ручний пристрій-детектор для хімічної деконтамінації
AP-PPE: All-purpose Personal Protective Ensemble (Універсальний індивідуальний захисний комплект)
ARDS: Acute Respiratory Distress Syndrome (Гострий респіраторний дистрес-синдром)
CANA: Convulsant Antidote for Nerve Agent (Протисудомний препарат-антидот для протидії нервово-паралітичній речовині (містить діазепам))
CCP: Casualty Collection Point (Пункт збору поранених)
Cl: Хлор
COCL2: Фосген
CRESS: Consciousness, Respirations, Eyes, Secretions, Skin (Свідомість, Дихання, Очі (зіниці), Секреція, Шкіра)
CWA: Chemical Warfare Agents (Хімічні БОP - бойові отруйні речовини)
DMSA: Dimercaptosuccinic Acid (Димеркаптобурштинова кислота)
FDP: Freeze-dried Plasma (Ліофілізована плазма)
FWB: Fresh Whole Blood (Свіжа цільна кров)
HPMK: Hypothermia Management Kit (Набір для лікування гіпотермії)
ICP: Intracerebral Pressure (ВЧТ - Внутрішньочерепний тиск)
IDLH: Immediately Dangerous to Life or Health (Негайна небезпека для життя або здоров'я)
JLIST: Joint lightweight integrated suit technology (технологія полегшеного інтегрованого костюма об’єднаних сил);
LCD: Lightweight Chemical Detector (Полегшений хімічний детектор)
LCt50: Летальна концентрація, 50%;
LD50: Летальна доза, 50%
MDI: Metered Dose Inhaler (Дозований інгалятор)
MACE: Military Acute Concussion Evaluation (Військова шкала оцінки струсу мозку)
MOPP: Mission Oriented Protective Posture (Захисне спорядження, орієнтоване на бойове завдання)
MSS: Mission Support Site (Місце підтримки бойового завдання)
NS: Normal Saline (Фізіологічний розчин, 0,9% NaCl)
PEEP: Positive End Expiratory Pressure (ПТКВ, Позитивний тиск наприкінці видиху)
PFC: Prolonged Field Care (Тривала допомога в польових умовах)
PPE: Personal Protective Equipment (ЗІЗ, Засоби індивідуального захисту)
RSDL: Reactive Skin Decontaminant Lotion (ЛДУШ, Лосьйон для деконтамінації ураженої шкіри)
SIRS: Systemic Inflammatory Response Syndrome (ССЗВ, Синдром системної запальної відповіді)
ЧМТ: черепно-мозкова травма
TIC: Toxic Industrial Chemical (Токсичний промисловий хімікат)
TIM: Toxic Industrial Material (Токсичний промисловий матеріал)
TXA: Tranexamic Acid (Транексамова кислота)
UIPE: Undergarment Integrated Protective Ensemble (Інтегрований захисний комплект нижньої білизни)
USAMRICD: US Army Medical Research Institute of Chemical Defense (Інститут медичних досліджень протихімічного захисту Армії США)
-
- Field Management of Chemical and Biological Casualties Handbook. Garr JH, ed. 2016, Borden Instutute, Office of the Surgeon General, Falls Church, VA. Available at:
- Joint Trauma System, Chemical, Biological, Radiological and Nuclear Injury Response Part I: Initial Response Clinical Practice Guideline, 01 May 2018. https://jts.health.mil/index.cfm/PI_CPGs/cpgs. Accessed Jan 2019.
- Suzuki T, Morita H, Ono K,.et al. Sarin poisoning in Tokyo subway. The Lancet. 1995;345(8962) 1446-1447
- Okumura T, Taskasu N, Ishimatsu S, et al. Report on 640 victims of the Tokyo subway sarin attack. Annals of Emergency Medicine. 1996;28(2): 129-35.
- Baskin SL, Kelly JB, Maliner BL, et al. Cyanide poisoning. In: Medical aspects of chemical and biological warfare. Washington D.C.: Office of the Surgeon General; 2008: 371-410.
- Parachini JV. The World Trade Center bombers (1993). In: Tucker JB, ed. Toxic Terror: Assessing Terrorist Use of Chemical and Biological Weapons. Cambridge, MA: MIT Press; 2000: 185-206.
- Baud FJ, Borron SW, Mégarbane B, et al. Value of lactic acidosis in the assessment of the severity of acute cyanide poisoning. Crit Care Med. 2002 Sep;30(9):2044-50.
- Sauer SW, Keim ME. Hydroxocobalamin: improved public health readiness for cyanide disasters. Annals of Emergency Medicine. 2001;37(6): 155-68.
- Bebarta VS, Tanen DA, Lairet J, et al. Hydroxocobalamin and sodium thiosulfate versus sodium nitrite and sodium thiosulfate in the treatment of acute cyanide toxicity in a swine (Sus scrofa) model. Annals of Emergency Medicine. 2010;55: 345–51.
- Bebarta VS, Pitotti RL, Dixon P, et al. Hydroxocobalamin and epinephrine both improve survival in a swine model of cyanide-induced cardiac arrest. Annals of Emergency Medicine. 2012;60(4): 415-22.
- Bebarta VS, Pitotti RL, Boudreau S, et al. Intraosseous versus intravenous infusion of hydroxocobalamin for the treatment of acute severe cyanide toxicity in the swine model. Academic Emergency Medicine. 2014;21:1203-1211.
- Brouard A, Blaisot B, Bismuth. Hydroxocobalamin in cyanide poisoning. Journal de Toxicologie Clinique et Experimentale. 1987;7(3): 155-68.
- Hall AH, Rumack BH. Hydroxycobalamin/sodium thiosulfate as a cyanide antidote. Journal of Emergency Medicine. 1987;5(2): 115-21
- Bebarta VS, Tanen DA, Boudreau S, et al. Intravenous cobinamide versus hydroxocobalamin for acute treatment of severe cyanide poisoning in a swine (Sus scrofa) model. Annals of emergency medicine. 2014;64(6): 612-19.
- Dulaney Jr MD, Brumley M, Willis JT, Hume AS. Protection against cyanide toxicity by oral alphaketoglutaric acid. Veterinary and Human Toxicology. 1991;33:571-5.
- Niknahad H1, Ghelichkhani E. Antagonism of cyanide poisoning by dihydroxyacetone. Toxicol Lett. 2002 Jun 14;132(2):95-100.
- Hoffman RS, Howland MA, Lewin NA, et al. Toxicologic Emergencies. 10th Ed. New York, NY: McGraw-Hill Education; 2015.
- Food and Drug Administration. Pyrodistigmine bromide package insert. https://www.fda.gov/downloads/drugs/emergencypreparedness/bioterrorismanddrugpreparednes s/ucm133154.pdf. Accessed Jan 2019.
- McDonough JH. Midazolam: An improved anticonvulsant treatment for nerve agent-induced seizures. Paper presented at: ADA409494 Proceedings of the 2001 Edgewood Chemical Biological Center Scientific Conference on Chemical and Biological Defense Research; Mar 2001; Hunt Valley, MD.
- Sidell FR. Nerve Agents. In Medical Aspects of Chemical and Biological Warfare, Textbook of Military Medicine, Part I Warfare, Weaponry and the Casualty (Sidell FR, Takafuji ET, and Franz DR eds). The Office of the Surgeon General. Washington DC. 1997: 129-179.
- Sidell FR. Soman and Sarin: clinical manifestations and treatment of accidental poisoning by organophosphates. Clinical Toxicology. 1974;7(1): 1-17.
- Shih T, McDonough JH. Organophosphorus nerve agents-induced seizures and efficacy of atropine sulfate as anticonvulsant treatment. Pharmacology, biochemistry and behavior. 1999;64:147-153.
- Taylor P. Anticholinesterase agents (Chapter 10) in The pharmacological basis of therapeutics (6th Ed), Gilman AG, Goodman LS, Rall TW, Murad F. Macmillan, New York.1985: 110-129.
- Ward JR. Case report: exposure to nerve gas. In: Whittenberger JL, ed. Artificial respiration: theory and application. New York, NY: Harper and Row; 1962: 258-65.
- Harris LW, Gennings C, Carter WH, et al. Efficacy comparison of scopolamine (SCP) and diazepam (DZ) against soman-induced lethality in guinea pigs. Drug and Chemical Toxicology. 1994;17(1): 35-50.
- Koplovitz I, Schulz S. Perspectives on the use of scopolamine as an adjunct treatment to enhance survival following organophosphorus nerve agent poisoning. Military Medicine. 2010;175(11): 878-82.
- Clement JG. Survivors of soman poisoning: recovery of the soman LD50 to control value in the presence of extensive acetylcholinesterase inhibition. Archives of Toxicology. 1989;63(2): 150-54.
- Dawson, R. M. Review of oximes available for treatment of nerve agent poisoning. J. Appl. Toxicol. 1994;14: 317–331. doi:10.1002/jat.2550140502
- Gunnarson M WS, Seidal T, Lennquist S. Effects of inhalation of corticosteroids immediately after experimental chlorine injury. Journal of Trauma and Acute Care Surgery. 2000;48(1): 101.
- Kassa J. Review of Oximes in the Antidotal Treatment of Poisoning by Organophosphorus Nerve Agents. Journal of Toxicology. 2002;40(6): 803-16.
- Snider TH, Yeung DT, Jett, DA, Babin M. Toxicity and median effective doses of oxime therapies against percutaneous organophosphorus pesticide and nerve agent challenges in the Hartley guinea pig. J Toxicol Sci, Jul 2016. ;41(4):511-21.
- Wilhelm CM, Snider TH, Babin MC, et al. A comprehensive evaluation of the efficacy of leading oxime therapies in guinea pigs exposed to organophosphorus chemical warfare agents or pesticides. Toxicology and Applied Pharmacy. 2014;281(3):254-65.
- Worek F, Aurbek N, Thiermann H. Reactivation of organophosphate-inhibited human AchE by combinations of obidoxime and HI 6 in vitro. Journal of Apllied Toxicology. 2007;27(6):582-588.
- Hamilton MG, Lundy PM. HI-6 therapy of soman and tabun poisoning in primates and rodents. Archives of Toxicology. 1989;63(2): 144-49.
- Marrs TC, Maynard RL, Sidell FR. The use of benzodiazepines in organophosphorus nerve agent intoxication. In: Chichester, UK: John Wiley & Sons, Ltd; 2007:331-342
- Shih TM, Duniho SM, and McDonough JH. Control of Nerve Agent-Induced Seizures is Critical for Neuroprotection and Survival. U.S. Army Medical Research Institute of Chemical Defense Report. Jan 2002.
- Diller WF. Early diagnosis of phosgene overexposure. Toxicology and Industrial Health. 1985;1(2): 73-80.
- Nelson LS, Odujebe OA. Simple Asphyxiants and Pulmonary Irritants. In Goldfrank’s Toxicologic Emergencies 10th ed. McGraw Hill. 2015.
- Wang J, Zhang L, Walther SM. Administration of aerosolized terbutaline and budesonide reduces chlorine gas-induced acute lung injury. J Trauma. Apr 2004;56(4):850-862.
- Bosse GM. Nebulized sodium bicarbonate in the treatment of chlorine gas inhalation. Journal of Toxicology – Clinical Toxicology. 1994;32:233-241.
- Vinsel PJ. Treatment of acute chlorine gas inhalation with nebulized sodium bicarbonate. J Emerg Med. 1990 May-Jun 1990;8(3):327-329.
- Guo YL, Kennedy TP, Michael R, et al. Mechanism of phosgene induced lung injury: role of arachidonate mediators. Journal of Applied Physiology. 1990;69(5): 1615-22
- Frosolono MF, Scarpelli EM, Holzman BH, et al. Effect of aminophylline, hydrocortisone, and prostaglandin E1 on survival time and percent lung water in rabbits after exposure to phosgene. American Review of Respiratory Disease. 1978;117(suppl): 233-34.
- Sciuto AM, Strickland PT, Kennedy TP, Gurtner GH. Postexposure treatment with aminophylline protects against phosgene induced acute lung injury. Experimental Lung Research. 1997;23(4): 31732.
- Kennedy TP, Michael JR, Hoidal JR, et al. Dibutyryl cAMP, aminophylline, and beta-adrenergic agonists protect against pulmonary edema caused by phosgene. Journal of Applied Physiology. 1989;67(6): 2542-52.
- Sciuto AM, Stotts RR, Hurt HH. Efficacy of ibuprofen and pentoxifylline in the treatment of phosgene-induced acute lung injury. Journal of Applied Toxicology. 1996;16(5): 381-84.
- Sciuto AM, Strickland PT, Kennedy TP, Gurtner GH. Protective effects of N-acetylcysteine treatment after phosgene exposure in rabbits. American Journal of Respiratory and Critical Care Medicine. 1995;151(3 Pt 1): 68-72
- Fitzgerald GJ. Chemical warfare and medical response during World War I. American Journal of Public Health. 2008;98(4): 611-25
- Le HQ, Knudsen SJ. Exposure to a First World War blistering agent, Emergency Medicine Journal. 2006;23: 296–99.
- Medical management guidelines for blister agents: sulfur mustard agent H/HD, sulfur mustard agent HT. US Centers for Disease Control and Prevention, Agency for Toxic Substances and Disease Registry Web site.
- Medical management guidelines for blister agents: HN-1HN-2HN-3 nitrogen mustards. US Centers for Disease Control and Prevention, Agency for Toxic Substances and Disease Registry Web site.
- Johns Hopkins Center for Health Security, Sulfur mustard (blister agent) Fact Sheet, 25 Mar 2013.
- Wigenstam E, Jonasson S, Koch B, Bucht A. Corticosteroids treatment inhibits airway hyperresponsiveness and lung injury in a murine model of chemical-induced airway inflammation. Toxicology. 2012;301(103):66-71.
- Vojvodić V, Milosavljević Z, Bosković B, Bojanić N. The protective effect of different drugs in rats poisoned by sulfur and nitrogen mustards. Fundamental and Applied Toxicology. 1985;5(6 Pt 2): S160-8.
- Anderson DR, Byers SL, Vesely KR. Treatment of sulfur mustard (HD)-induced lung injury. Journal of Applied Toxicology. 2000;20(supp 1): S129-32.
- Anderson DR, Holmes WW, Lee RB, et al. Sulfur mustard-induced neutropenia: treatment with granulocyte colony-stimulating factor. Military Medicine. 2006;171: 448-53.
- Vijayaraghavan R, Kumar P, Joshi U, et al. Prophylactic wfficacy of amifostine and its analogues against sulfur musturd toxicity. Toxicology. 2001;163(2-3):83-91.
- Bhattacharya IR, Rao PVL, Pant SC, et al. Effects of Amifostine and Its Analogues on Sulfur Mustard Toxicity in Vitro and in Vivo. Toxicology and Applied Pharmacology. 2001;176(1): 24-33.
- Vilensky JA, Redman K. British anti-Lewisite (dimercaprol): an amazing history. Annals of Emergency Medicine. 2003;41(3): 378-83.
- Medical management guidelines for blister agents: lewisite (L), mustard-lewisite mixture (HL). US Centers for Disease Control and Prevention, Agency for Toxic Substances and Disease Registry Web site.
- Ketchum JS, Sidell, FR. Incapacitating Agents. In: Borden Institute. Textbook of Military Medicine: Medical Aspects of Chemical Warfare. United States Department of Defense. 2009. https://ke.army.mil/bordeninstitute/published_volumes/chemwarfare/ch12_pgs411-440.pdf Accessed Jan 2019.
- Burns MJ, Linden CH, Graduins A, et al. A comparison of physostigmine and benzodiazepines for the treatment of anticholinergic poisoning. Annals of Emergency Medicine. 2000;35(4):374-381.
- Wetherall J, Hall T, Passingham S. Physostigmine and hyoscine improves protection against the lethal and incapacitating effects of nerve agent poisoning in the guinea pig. Neurotoxicology. 2002;23:341-349.
- Boyer E. Management of opioid analgesic overdose. The New England Journal of Medicine. 2012;367(2): 146-55.
- Schep LJ, Slaughter RJ, McBride DI. Riot control agents: the tear gases CN, CS and OC-a medical review. Journal of the Royal Army Medical Corps. 2015;161(2): 94-9.
Додаток А: Протокол введення атропіну/скополаміну
Предмети, необхідні для одного пораненого
- (2) Скополамін 0,4 мг/мл, ампули
- (1) Шприц 3 мл
- (1) Жорстка голка 18G
- (1) Пакет із 250 мл фізіологічного розчину.
- (3) Атропін 8 мг/20 мл, ампули
- (1) Система для проведення мікрокраплинної інфузії з регулятором потоку барабанного типу
- (1) Інфузійний пристрій для введення рідини під тиском
- (1) Пристрій для ВК-доступу “FAST 1“/Шприц з набраним фізрозчином для промивання або набір для забезпечення ВВ доступу
Підготовка
Якщо очікуються постраждалі, уражені нервово-паралітичними речовинами/фосфорорганічними речовинами/карбаматами:
Приготуйте скополамін наступним чином:
- Наберіть 0,8 мг (2 мл) скополаміну з ампул по 0,4 мг в один трьохмілілітровий шприц.
- Відкладіть шприц разом зі закритою голкою 18G, щоб він був готовий до швидкого введення.
- Напишіть на шприці «СКОП 0,8 мг/2 мл»
Приготуйте пакет для крапельної інфузії атропіну наступним чином:
- Додайте 50 мл 8 мг/20 мл атропіну в пакет з 250 мл фізіологічного розчину.
- Пакет тепер має 20 мг/300 мл атропіну. Переконайтеся, що в пакеті немає повітря, оскільки зайві 50 мл ледве вмістяться.
- Підпишіть пакет добре помітним написом “АТРОПІН 20 мг/300 мл, прибл. 1 мг/3 хв”
Введення
Після введення 3 ATNAA та 1 CANA ВМ оцініть стан пацієнта та, якщо покращення не відбулося, введіть скополамін (бажано) АБО атропін відповідно до таких протоколів:
- Якщо адекватної відповіді на 3 ATNAA та 1 CANA немає, введіть 0,8 мг скополаміну гідроброміду ВВ або ВК та промийте. ВМ є вторинним методом введення.
АБО
- Введіть болюсну дозу атропіну, за потреби збільшуйте вдвічі наступні дози, вводячи їх кожні 3-5 хвилин. Почніть з 2 мг, потім 4 мг, 8 мг, 16 мг.
- Після досягнення контролю над симптомами розпочніть крапельне введення атропіну, приготованого, як описано вище, зі швидкістю введення - 10 % сумарної болюсної дози (включаючи 6 мг атропіну в 3 початкових ATNAA) на годину.
- Якщо необхідне повторне болюсне введення для контролю рецидивуючих симптомів, тоді збільшіть краплинне введення до 20% від початкової ефективної дози.
- 0,8 мг скополаміну приблизно відповідають 10 мг атропіну (при розрахунку початкової ефективної дози).
- Швидкість краплинного введення 300 мл/год забезпечить введення приблизно 1 мг атропіну кожні 3 хв.
Примітка: Цей протокол призначений як стартовий для медичних працівників, які не вводять рутинно дані ліки. Протокол мають переглянути лікарі, які консультуватимуть некваліфікованих щодо такого введення медиків. Цей протокол не замінює клінічне судження відповідального медичного професіонала.
Послідовність дій при ураженні нервово-паралітичними речовинами повинна бути наступною:
- 3xATNAA
- 1xCANA
- ВК доступ
- 2 г TXA (якщо є супутня травма)
- 500 мг пралідоксиму ВК/ВВ струминно (покращення стану на 15-20 хв)
- 0,8 мг скополаміну ВК/ВВ
- Атропін 2 мг ВК/ВВ з подальшим подвоєнням кожної наступної дози, кожні 3-5 хв (якщо немає змін у психічному стані, навіть якщо сухий/атропінізований)
- Мідазолам 10 мг при субклінічних судомах
- Пралідоксим ВВ краплинно
Налоксон:
- Початкова доза 2-4 мг з подальшим подвоєнням кожної наступної дози (4 мг, 8 мг, 16 мг)
- Наркан краплинно зі швидкістю введення ⅔ від ефективної дози (дози, на яку настала клінічна відповідь)
Додаток B: Протокол краплинного введення пралідоксиму (2-PAM)

Додаток C: Протокол лікування отруєнь, викликаних впливом речовин задушливої дії

Додаток D: Протокол лікування уражень очей

Додаток E: Протокол лікування при тяжкому інгаляційному ураженні везикантами

Додаток F: Інформація щодо не передбаченого інструкцією застосування лікарських засобів у Настановах з клінічної практики
Мета
Мета цього Додатка — надати роз’яснення політики та практики Міністерства оборони США щодо включення в Настанови з клінічної практики «незатверджених» показів для продуктів, які були схвалені Управлінням з контролю якості продуктів харчування і лікарських засобів США (FDA). Це стосується використання препаратів не за призначенням для пацієнтів, які належать до Збройних сил США.
Вихідна інформація
Незатверджене (тобто «не за призначенням» - “off-label”) використання продуктів, схвалених FDA, надзвичайно поширене в медицині США і зазвичай не регулюється окремими нормативними актами. Проте, згідно з Федеральним законодавством, за деяких обставин застосування схвалених лікарських засобів за незатвердженими показами регулюється положеннями FDA про «досліджувані нові ліки». До цих обставин належить використання в рамках клінічних досліджень, а також, у військовому контексті, використання за незатвердженими показами згідно з вимогами командування. Деякі види використання за незатвердженими показами також можуть підлягати окремим нормативним актам.
Додаткова інформація щодо застосування за незатвердженими показами у Настановах з клінічної практики
Включення до Настанов з клінічної практики використання медикаментів за незатвердженими показами не належить до клінічних випробувань і не є вимогою командування. Більше того, таке включення не передбачає, що Військова система охорони здоров’я вимагає від медичних працівників, які працюють в структурах Міноборони США, застосовувати відповідні продукти за незатвердженими показами або вважає це «стандартом медичної допомоги». Швидше, включення до CPGs використання засобів «не за призначенням» має поглиблювати клінічне судження відповідального медичного працівника шляхом надання інформації щодо потенційних ризиків та переваг альтернативного лікування. Рішення приймається на основі клінічного судження відповідальним медичним працівником у контексті відносин між лікарем і пацієнтом.
Додаткові процедури
Виважений розгляд
Відповідно до цієї мети, в обговореннях використання медикаментів «не за призначенням» в CPG конкретно зазначено, що це використання, яке не схвалено FDA. Крім того, такі обговорення є збалансованими у представленні даних клінічних досліджень, включаючи будь-які дані, які свідчать про обережність у використанні продукту, і, зокрема, включаючи усі попередження, видані FDA.
Моніторинг забезпечення якості
Що стосується використання «не за призначенням», діяльність Міністерства оборони США полягає у підтримці регулярної системи моніторингу забезпечення якості результатів і відомих потенційних побічних ефектів. З цієї причини підкреслюється важливість ведення точних клінічних записів.
Інформація для пацієнтів
Належна клінічна практика передбачає надання відповідної інформації пацієнтам. У кожних Настановах з клінічної практики, де йдеться про використання засобу «не за призначенням», розглядається питання інформування пацієнтів. За умови практичної доцільності, слід розглянути можливість включення додатка з інформаційним листком для пацієнтів, що видаватиметься до або після застосування продукту. Інформаційний листок має в доступній для пацієнтів формі повідомляти наступне: a) що дане застосування не схвалене FDA; b) причини, чому медичний працівник Міністерства оборони США може прийняти рішення використати продукт з цією метою; c) потенційні ризики, пов’язані з таким застосуванням.




































