Клінічний сценарій

Вступ
Цей документ є третьою частиною настанов з клінічної практики щодо ХБРЯ-уражень. У ньому містяться рекомендації щодо розпізнавання, деконтамінації, лікування та сортування підозрюваних або підтверджених випадків опромінення та/або контамінації пацієнтів.
Оскільки не існує доказів 1 рівня щодо ведення таких постраждалих, галузеві експерти, які розробили ці настанови, використовували довідкові матеріали, найкращі медичні практики та історичні прецеденти. Дані настанови з клінічної практики можна використовувати в поєднанні з Посібником з медичної допомоги постраждалим від радіаційних уражень (Medical Management of Radiological Casualties Handbook). Звернутися до Інституту радіобіологічних досліджень збройних сил США (англ., Armed Forces Radiobiology Research Institute, AFRRI) та отримати консультацію можна в режимі 24/7/365 за номером 301-295-0530; звертатись слід до Консультативної групи з медичної радіобіології (англ., Medical Radiobiology Advisory Team).
Якщо ви підозрюєте радіаційне опромінення, або ядерне ураження під час війни, або ядерний інцидент, що може вплинути на навколишнє середовище:1
- Негайно повідомте своє командування.
- Створіть окремі зони для сортування та лікування таких поранених.
- Запишіть якомога більше клінічних даних у медичну карту:
- Час, коли було отримане ураження
- Тривалість експозиції
- % від загальної площі поверхні тіла, якщо є опік
- ЗІЗ, які були на постраждалому
- Перші симптоми та час, коли вони почалися
- Зателефонуйте в AFRRI (301-295-0530) і попросіть допомоги у веденні постраждалих у Консультативної групи з медичної радіобіології або Консультативно-тренувального центру з допомоги при надзвичайних радіологічних ситуаціях (англ., Radiation Emergency Assistance Center/Training Site, REAC/TS), 865-576-1005.
- Надішліть усі клінічні записи до Об’єднаної системи лікування травм (англ., Joint Trauma System, JTS) з метою оперативного покращення ефективності (ПЕ) надання допомоги та розробки настанов з клінічної практики на основі доказів.
Приклад історичного випадку: контекст



Основи радіології

Радіація і радіаційне ураження є складними; зрозуміти їх допоможуть два важливі поняття - радіоізотопи та іонізація.
По-перше, радіоізотопи (також звані ізотопами, або радіонуклідами — це фізичні речовини, які виділяють енергію у вигляді іонізуючого випромінювання під час свого розпаду. Такі радіоізотопи можуть бути токсичними самі по собі, незалежно від їхньої радіоактивності (тобто здатності виділяти іонізуюче випромінювання). Радіоізотопи можуть знаходитись у будь-якому фізичному стані (твердий стан, порошок, рідина, пара, газ, солі або інші сполуки).
Друге поняття - іонізуюче випромінювання. Це «променева» частина радіоізотопів. Іонізуюче випромінювання - невидима доза енергії, яка спричиняє пошкодження на біологічному рівні. Таке пошкодження виникає лише під час впливу радіоізотопу.2
Чотири потенційних джерела радіаційного ураження:
- Опромінення (без контамінації, подібно до впливу рентген-променів).
- Зовнішня контамінація (радіоізотоп фізично присутній на пацієнті і може його опромінювати).
- Внутрішня контамінація (пацієнт вдихнув або проковтнув радіоізотоп, або його ввели у вигляді ін’єкції: цей радіоізотоп також може опромінювати пацієнта зсередини).
- Інкорпорація (поглинання радіоізотопів клітинами або тканинами: окрім потенційного отруєння важкими металами, радіоізотопи опромінюють пацієнта зсередини).
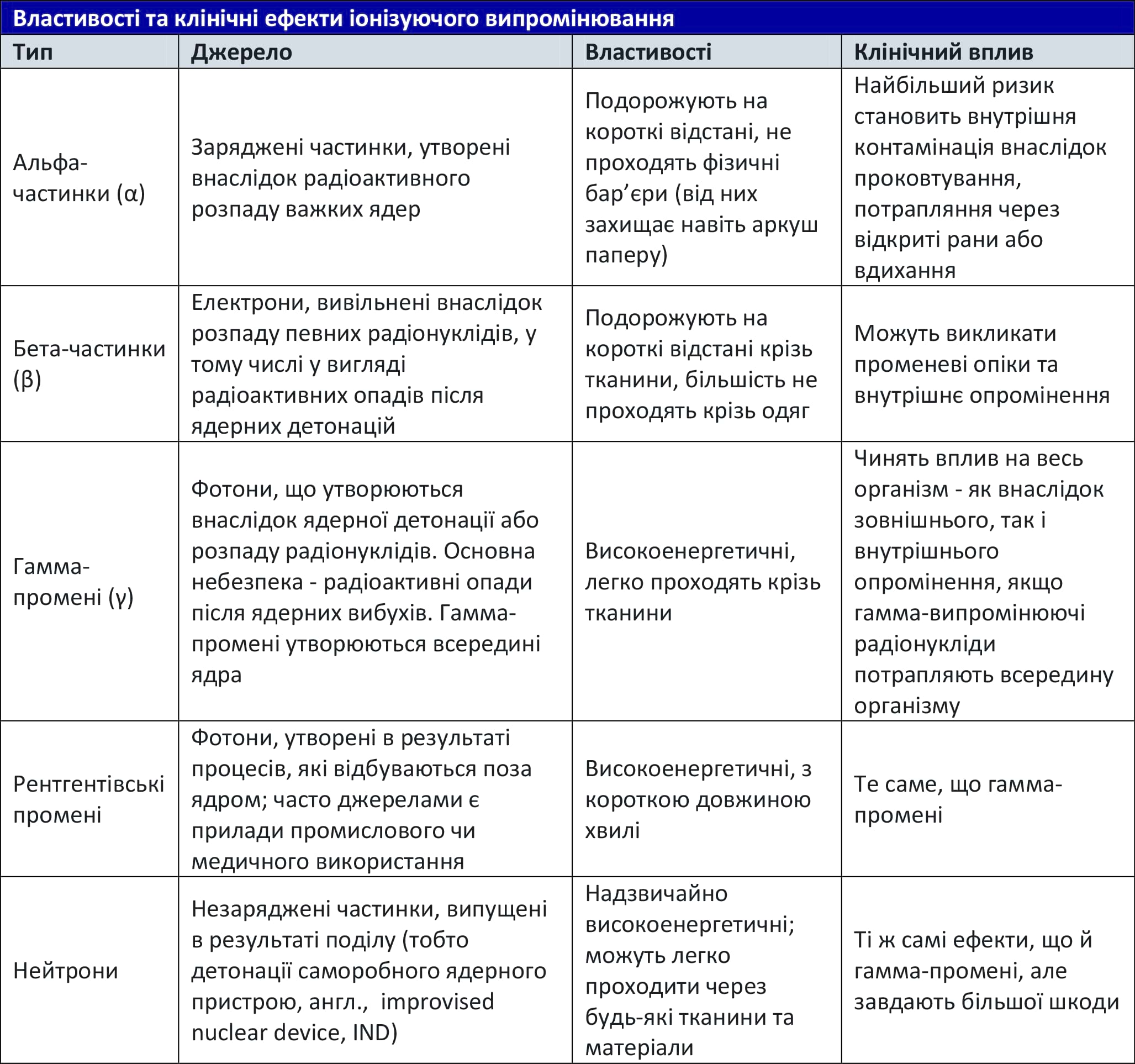
Іонізуюче випромінювання - це випромінювання, яке має достатню енергію, щоб «відривати» електрони від атомів, створюючи іони. Іони - це атоми, які мають позитивний або негативний заряд. Існує п’ять типів іонізуючого випромінювання (ІВ): альфа-, бета-, гамма-, нейтронне та рентгенівське.3,4 Детальну інформацію про джерела та властивості ІВ можна знайти в Таблиці 1. Усі ці типи випромінювання можуть спричинити клінічно значущий вплив на постраждалого. Клінічні ефекти визначаються видом ізотопів, шляхом впливу, тривалістю та інтенсивністю опромінення, а також відстанню до джерела радіації.5
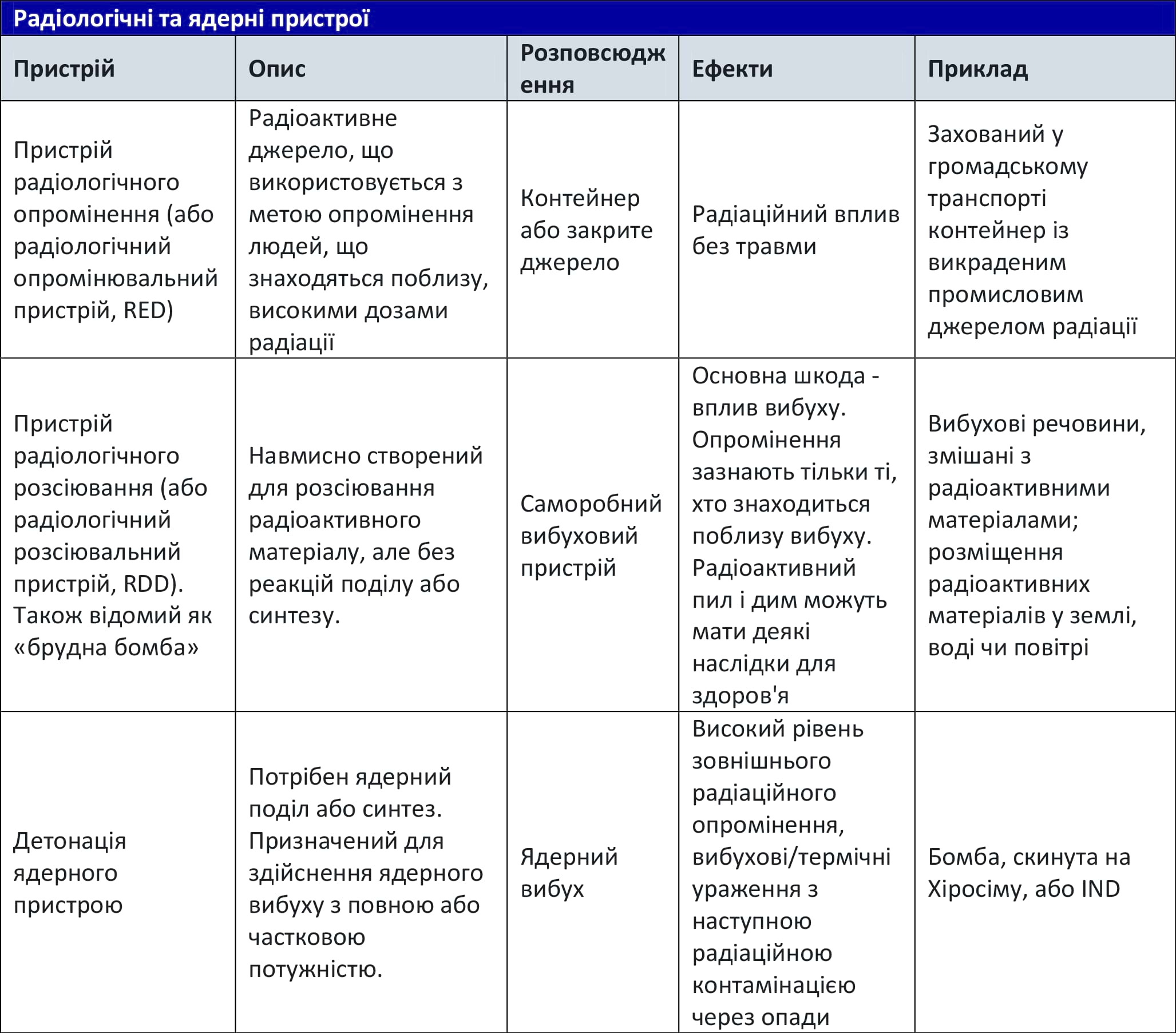
Зазнавати впливу іонізуючого випромінювання можна внаслідок контакту з природними і штучними джерелами. Найбільше занепокоєння медичних працівників викликає ІВ від штучних джерел. До них належать промислові радіологічні пристрої, діагностичні та терапевтичні клінічні джерела, а також незаконне використання радіоактивних речовин як частин пристрою радіологічного опромінення (ПРО, англ., radiological exposure device, RED) чи радіологічного розсіювання (ПРР, англ., radiological dispersal device, RDD) або під час детонації ядерної зброї. У Таблиці 2 наведена потенційна радіологічна та ядерна зброя, яка може бути використана для ураження населення іонізуючим випромінюванням.6,7
Ізотопи — це дві або більше форм одного елемента, які містять різну кількість нейтронів. Широко використовувані ізотопи поділяють на чотири категорії, що викликають занепокоєння:
- «Університетська п'ятірка» (C14, P32, I125, I131 і Cf252) - використовуються в лабораторіях і для медичного обслуговування.
- «Промислова трійка» (Ir192, Cs137 і Co60) - зустрічається в промислових радіологічних джерелах; ці речовини найчастіше використовуються в терористичних цілях через легкий доступ і високу випромінювану енергію.
- «Військова п’ятірка» (H3, U235, U238, Pu239 і Am241) - використовуються для створення ядерної зброї.
- Продукти поділу - це продукти радіоактивного розпаду, що виділяються після ядерної детонації або аварії на атомній електростанції.
Таблиця 1. Властивості та клінічні ефекти іонізуючого випромінювання8
Таблиця 2. Радіологічні та ядерні пристрої
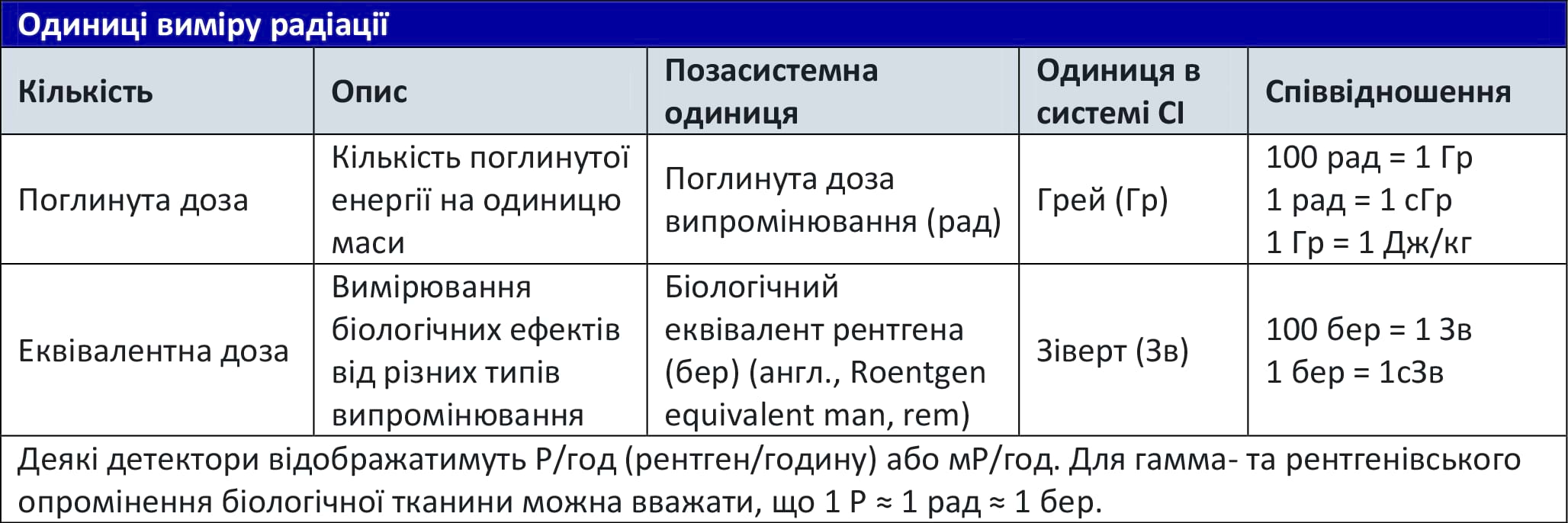
Радіологічні одиниці вимірювання
Експозиційна доза випромінювання, кількість енергії, яка накопичується в тканинах внаслідок опромінення, і біологічні ефекти від опромінення описуються трьома різними одиницями вимірювання. Широко використовуються як позасистемні, так і одиниці вимірювання за системою СІ. Експозиційна доза вимірюється в Рентгенах (Р) або Кулонах на кілограм (Кл/кг). Детерміновані клінічні ефекти від поглинутої дози вимірюються в Радах (рад) або Греях (Гр). Еквівалентна, або біологічна, доза внаслідок різних типів випромінювання вимірюється в Берах (бер) або Зівертах (Зв).9,10 Визначення еквівалентної дози стосується стохастичних ефектів і залежить від типу іонізуючого випромінювання.
Відразу після інциденту медики зможуть оцінити експозиційну дозу в Рентгенах (Р) за допомогою детектора та говоритимуть про гострий радіаційний синдром (ГРС) і шкірний радіаційний синдром (ШРС) на основі дози, отриманої в Радах (рад) і Греях (Гр). Ця інформація підсумована в Таблиці 3. Надзвичайно важливо уточнити одиниці вимірювання, які використовує детектор, особливо їх префікси, оскільки мілі (м, m) і мікро (мк, µ) часто плутають або навіть пропускають під час оцінки дози та/або її потужності.
Таблиця 3. Одиниці виміру радіації
Клінічний індекс підозри
Хоча у Реєстрі травм Міністерства оборони США (DoDTR) відсутні випадки радіаційного ураження, військові повинні мати клінічний індекс підозри щодо використання радіологічної зброї на полі бою в майбутньому. Першим кроком допомоги буде визначення та розпізнавання ризику застосування радіологічної зброї та радіаційного ураження в зоні проведення операцій. У деяких постраждалих, якщо вони перебували поблизу джерела радіації, одразу з’явиться опік, який не був спричинений полум’ям чи очевидним ушкодженням. Основними факторами, які призводять до клінічних проявів, є час опромінення, відстань від джерела та будь-яке екранування (наявність бар’єрів). Інші симптоми є відносно неспецифічними. Тяжкість і початок симптомів залежить від отриманої дози. Клінічні синдроми детальніше описані далі в цих настановах, але клініцисти можуть бути першими, хто визначить факт застосування радіологічної зброї вже на основі неспецифічних ознак, виявлених у постраждалих.

Особливості деконтамінації

У разі надання допомоги постраждалим у відомій радіаційно гарячій зоні: немає жодного задокументованого випадку отримання медичним персоналом клінічно значущої дози під час проведення рятувальних втручань контамінованому постраждалому. Надзвичайно малоймовірно, що медичний персонал отримає значущу з медичної точки зору гостру дозу опромінення під час надання допомоги постраждалим із радіоактивними уламками в ранах від RDD (радіологічного розсіювального пристрою).4,11 З огляду на це, постачальники повинні захищати себе та носити відповідні ЗІЗ.
Фізичний стан радіоізотопу визначить найкращий метод деконтамінації. Якщо пацієнт лише піддався впливу іонізуючого випромінювання, ДЕКОНТАМІНАЦІЯ НЕ ПОТРІБНА.
Засоби індивідуального захисту (ЗІЗ) слід вибирати таким чином, щоб були закриті очі, ніс, рот, волосся та вся відкрита шкіра.
Захист органів дихання повинен складатися з маски N95 або P100. Подвійні рукавички та одноразовий фартух або верхній одяг з довгими рукавами є достатнім покриттям шкіри для персоналу, який виконує деконтамінацію.5,12 Під час роботи в тактичних або польових умовах орієнтоване на бойове завдання захисне спорядження 4 рівня (англ., Mission Oriented Protective Posture, MOPP), може бути обмежене до маски та рукавичок, щоб забезпечити захист органів дихання та шкіри (див. Додаток А для опису рівнів ЗІЗ). Хоча повна заміна ЗІЗ може бути неможливою під час переходу від пораненого до пораненого, рекомендується принаймні часта зміна рукавичок. Під час деконтамінації поранений повинен носити маску N95 або P100 (або залишатися в тактичному респіраторі), щоб звести до мінімуму вдихання будь-яких аерозольних радіоактивних частинок. Відкриті рани слід вважати контамінованими та промити чистою або стерильною водою, а потім накрити, щоб запобігти повторній контамінації. Якщо потрібне хірургічне видалення радіоактивних осколків, розгляньте використання рентгенівських (свинцевих) фартухів як ЗІЗ для хірургічної команди або накривайте пацієнта в періодах між активними оперативними втручаннями. Це зменшить дозу, отриману медиками.
Суха деконтамінація полягає у знятті з пораненого всього одягу, обладнання та особистих речей, і лише цей крок усуває близько 90% зовнішнього забруднення внаслідок впливу твердих радіоактивних речовин або рідин. Подальша суха деконтамінація передбачає очищення шкіри щіткою з метою видалення поверхневих клітин епітелію та/або використання валиків для ворсу чи малярської стрічки.6,13 Використання дитячих або вологих серветок, що не містять етанолу, буде достатнім для видалення забруднень зі шкіри; їх слід використовувати змітаючими рухами, щоб витерти частинки з обличчя та відкритих ран.
При вологій деконтамінації для видалення забруднення зі шкіри пацієнта використовують воду та м’яке мило. За умови великої кількості постраждалих ті з них, які можуть ходити, можуть самостійно прийняти душ. Уникайте подразнення шкіри через занадто активне тертя та уникайте потрапляння контамінованої рідини в рот/ніс або рани. При температурі навколишнього середовища нижче 18 градусів, якщо є можливість, для проведення вологої деконтамінації використовуйте приміщення всередині будівлі. Якщо вони недоступні, рекомендовано проводити суху деконтамінацію, щоб запобігти гіпотермії.
Деконтамінація повинна бути підтверджена навченим персоналом за допомогою відповідного обладнання для радіологічного моніторингу (див. Додаток B). Мета деконтамінації полягає в тому, щоб зменшити зовнішнє забруднення вдвічі від початково виміряного рівня, однак рівень контамінації може залишатися вищим від бажаного значення (яке є вдвічі менше базового рівня) без значного ризику для здоров’я інших.
Радіаційні детектори та дозиметри дають показники в різних одиницях вимірювання. Під час деконтамінації пацієнта детектор має відображати одиниці вимірювання за хвилину (англ., counts per minute, cpm) або за секунду (англ., counts per second, cps). Це дає інформацію про кількість присутнього радіоактивного матеріалу, але не дає інформації про поглинуту дозу, що накопичується в тканинах. Записані cpm до та після деконтамінації вказують на ефективність методу та визначають, чи потрібно ще раз провести деконтамінацію.
Малюнок 1. Принципи деконтамінації при радіаційному та ядерному ураженні

Сортування
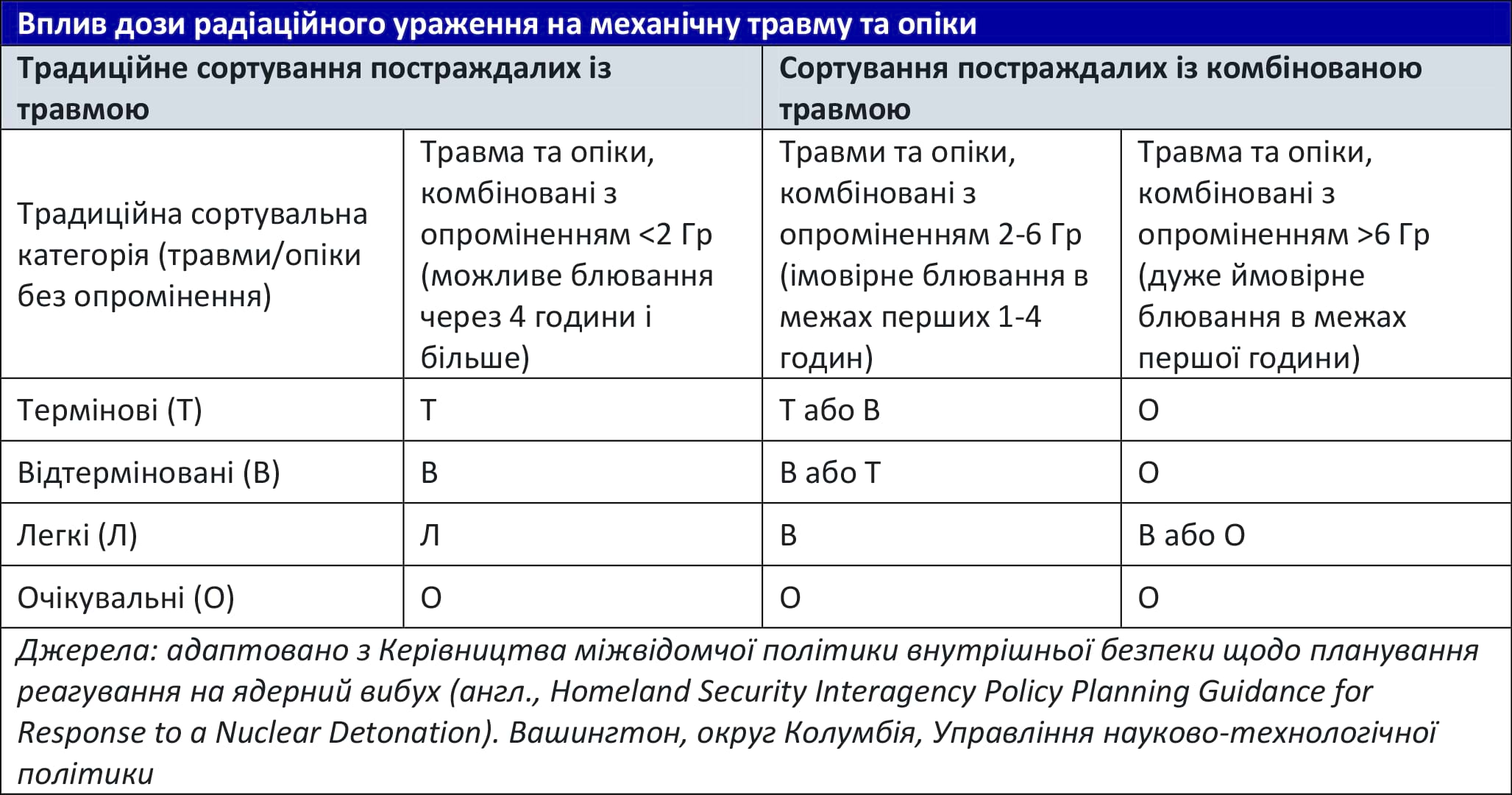
У масовому випадку сортуйте постраждалих за категоріями на основі «стандартних» травм. Після стабілізації травматичних ушкоджень, і якщо будуть доступні ресурси для оцінки дози, необхідно провести вторинне сортування постраждалих з урахування радіаційного ураження. Додаткові відомості щодо початкової оцінки дози (біодозиметрія) наведені в Додатку C. Ті, у кого є підозра на комбіноване ураження, мають бути переміщені до наступної вищої категорії сортування. Якщо є пацієнт з підозрою на отримання дози понад 6 Гр, його сортують до категорії «очікувальних», доки не буде доступно більше ресурсів. 14 Таблиця 4 коротко описує, як оновити категорії сортування постраждалих з променевим ураженням. Більш комплексні інструменти сортування можна знайти на вебсторінці https://remm.hhs.gov/triagetool5.htm.
У міру розвитку подій та появи додаткових ресурсів має відбуватися повторне сортування всіх постраждалих у всіх категоріях сортування, включаючи очікувальних.
При ізольованому опроміненні найбільш надійними ранніми клінічними показниками променевого ураження всього тіла є час до виникнення блювання та/або підвищення температури тіла, які можна побачити в перші години після опромінення. На 2 або 3 етапах медичної допомоги (де буде з’являтися можливість лабораторних досліджень) найнадійнішим раннім лабораторним індикатором є швидкість зниження лімфоцитів; таке дослідження може бути недоступним в межах перших 24-48 годин залежно від масштабів масового випадку та ступеня пошкодження інфраструктури. Хоча час до виникнення блювання є швидким і незатратним методом для оцінки дози опромінення, його слід використовувати з обережністю, оскільки він є неточним і може призвести до дуже високої частоти хибнопозитивних результатів.15
Таблиця 4. Вплив дози радіаційного ураження на механічну травму та опіки
TCCC у випадках радіологічних/ядерних уражень (MARCHE)2
Допомога постраждалим внаслідок радіологічної/ядерної події має надаватися відповідно до основних принципів, викладених у вигляді алгоритму (MARCHE)2, як описано в 1 частині CPG JTS «ХБРЯ-ураження». Однак існують деякі нюанси щодо застосування (MARCHE)2 у випадку радіологічної/ядерної події; вони зазначені у кожній фазі надання допомоги пораненим та наведені у наступних розділах (виділені синім). Важливо відзначити, що опромінення або контамінація плюс травма, що також описується як комбіноване ушкодження, ускладнює надання допомоги пораненим. Послідовність (MARCHE)2 об’єднує оцінку та відповідну дію як у випадку травмованого постраждалого, так і постраждалого внаслідок радіологічної/ядерної події.
Допомога під вогнем/надзвичайно гаряча зона
Важливо шукати укриття при перших ознаках радіологічної або ядерної події. Навіть шар тканини може захистити від великих частинок, тому слід докладати всіх зусиль, щоб повністю закрити відкриті ділянки, включаючи очі та рот. Постраждалий не потребує специфічного протирадіологічного лікування на місці отримання ураження; всі зусилля повинні бути спрямовані на лікування кровотечі, що загрожує життю, і переміщення в безпечну зону. Медики повинні пам’ятати про важливість мінімізації часу особистого опромінення та максимізації відстані від джерела під час допомоги постраждалим. Якщо тактична ситуація вимагає надання певної допомоги пораненим у Надзвичайно гарячій зоні або Гарячій зоні, використання екранування знизить потужність дози, але збільшить час опромінення. Перетягування пораненого на кілька метрів від джерела випромінювання може принести користь, одночасно зменшивши ризик для рятувальників.

Таблиця 5. Радіологічна загроза в зонах надання допомоги
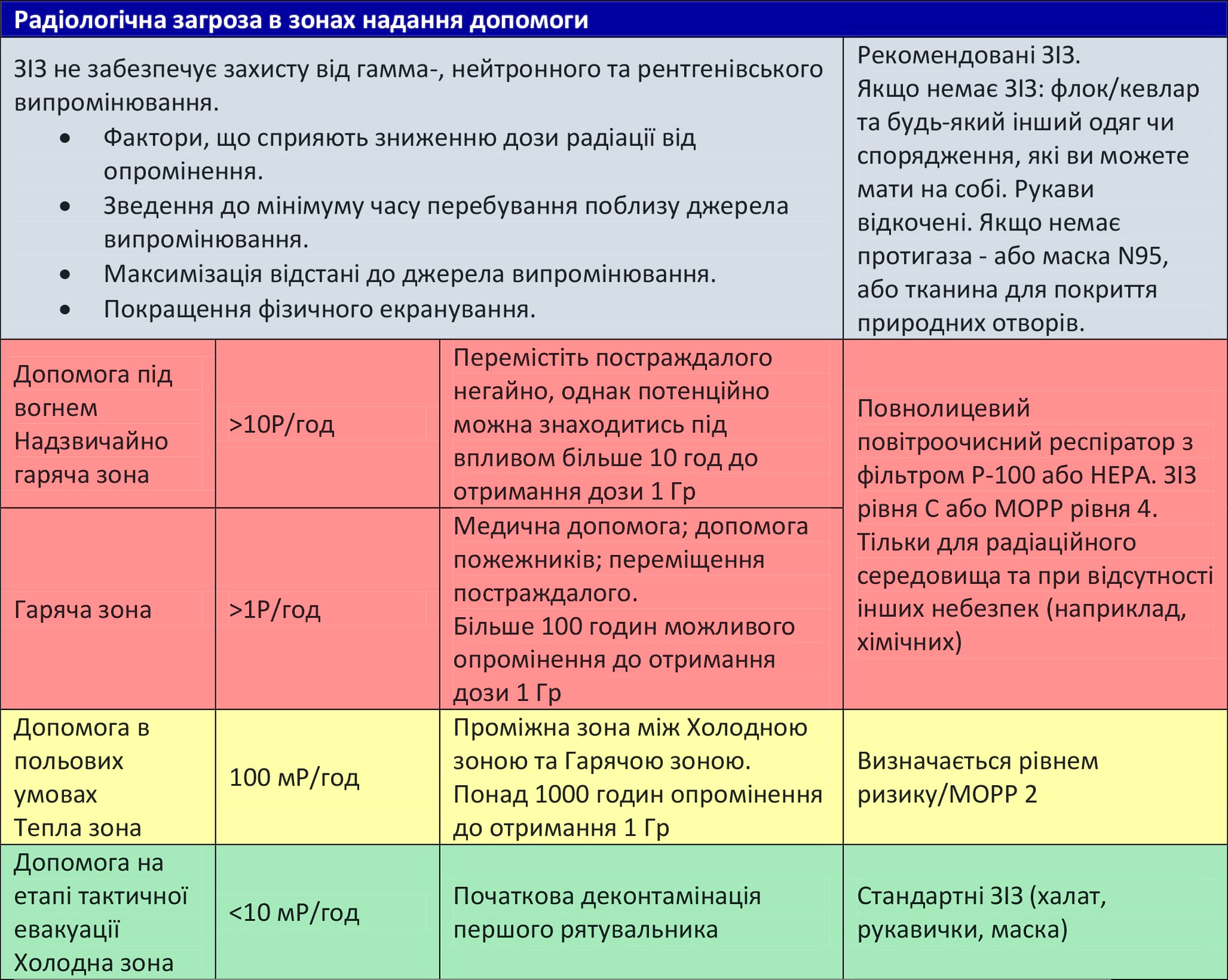
Ці дози - модифіковані величини з 3-го видання Настанов із планування щодо реагування на саморобний ядерний пристрій (IND) Федерального агентства з управління надзвичайними ситуаціями (FEMA) . Командири можуть адаптовувати дози відповідно до вимог бойового завдання.
Таблиця 6. Місце отримання ураження (Надзвичайно гаряча зона / Допомога в Гарячій зоні - (MAR)2
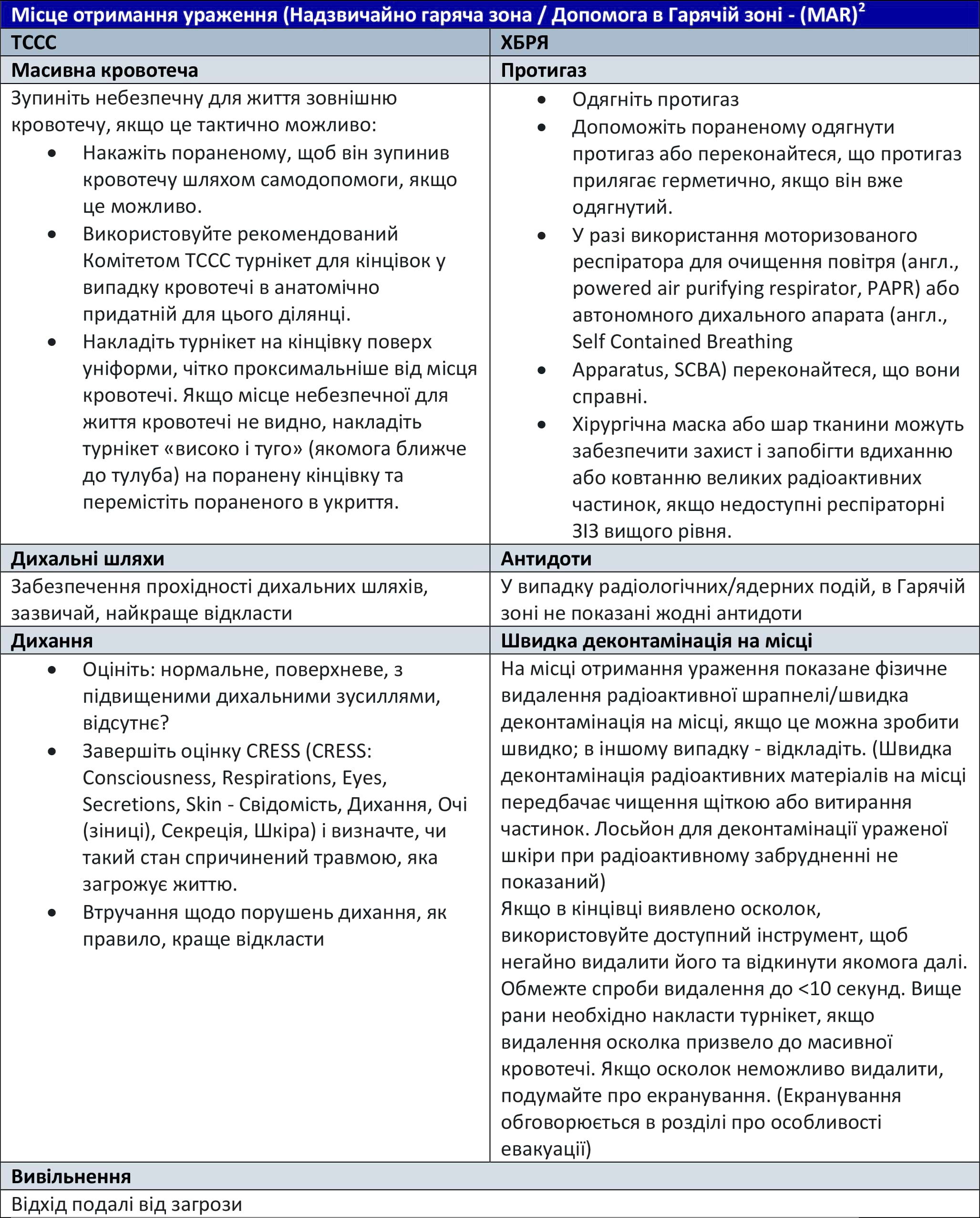
Джерело: JTS CPG «ХБРЯ-ураження. Частина 1: Первинне реагування при ХБРЯ-ураженні»
Допомога в польових умовах/тепла зона

Допомога в цій фазі повинна надаватися з обережністю, враховуючи принцип «настільки низько, наскільки це розумно і можливо», щоб мінімізувати подальший вплив або контамінацію після виведення з Гарячої зони. Ідеальним прикладом буде переміщення у підвал будівлі. Переконайтеся, що медичне обладнання та матеріали накриті. В ідеалі, всі втручання, крім тих, що рятують життя, потрібно відкласти, доки пацієнт не досягне Холодної зони, де ризик подальшої контамінації мінімальний. У випадку, якщо радіаційне поле настільки велике або евакуація обмежена, ці обставини можуть вимагати переходу до надання тривалої допомоги в польових умовах, все ще знаходячись в Теплій зоні.
Початкова оцінка
- Оцінити наявність КОМБІНОВАНИХ пошкоджень, що призведуть до негайної втрати життя (наприклад, знекровлення)
- Деконтамінація ПІСЛЯ стабілізації
- Травматичні пошкодження несуть більшу загрозу життю, ніж радіаційні
- Ефективність зняття одягу та миття пацієнта становлять >90%.
- Вимоги до роботи деяких медичних працівників у «радіаційному середовищі»
- Ризик для медиків дуже низький
***Не відкладайте ресусцитацію для проведення деконтамінації***
Таблиця 7. Оцінювання в пункті збору «брудних» (контамінованих) поранених (Тепла зона)– (M A R C H E)2
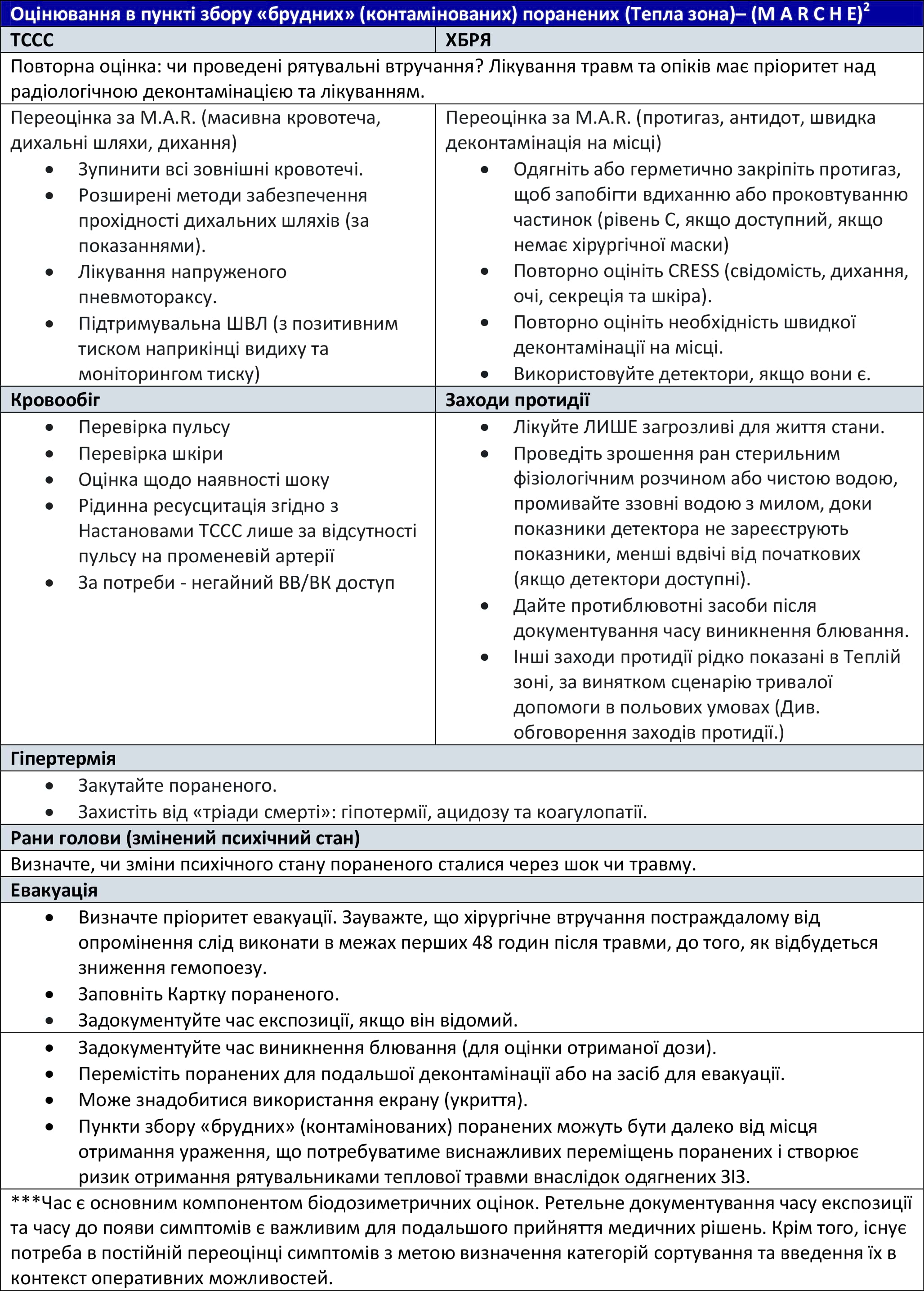
Джерело: JTS CPG «ХБРЯ-ураження. Частина 1: Первинне реагування при ХБРЯ-ураженні»
Допомога на етапі тактичної евакуації
У цих Настановах ми ще раз наголошуємо на важливості належного сортування з метою ефективного використання ресурсів CASEVAC і MEDEVAC. Пріоритет евакуації поранених із комбінованими пошкодженнями з 1 етапу медичної допомоги на 3 етап має ґрунтуватися на присутніх травмах. Повторне сортування з метою визначення пріоритетності евакуації має вирішальне значення. Якщо у постраждалого з’являються ознаки та симптоми значного променевого ураження, медик може змінити категорію сортування залежно від можливостей евакуації, часу до отримання хірургічної допомоги та інших «неклінічних» ризиків. Евакуацію з поля бою тих, хто скоріше за все отримав опромінення, яке спричинить гострий радіаційний синдром, описано нижче. Додаткові вказівки щодо операцій з евакуації в контамінованих середовищах можна знайти в Публікації JP3-11. Рішення про використання наземних і повітряних транспортних засобів для перевезення контамінованих постраждалих приймається командирами після розрахунку прийнятного ризику та інформування медичним персоналом, який має досвід у цій галузі. Ризики включають, але не обмежуються наступним:
- контамінований постраждалий або залишений радіоактивний матеріал.
- кумулятивний вплив на транспорт і медичний персонал під час транзиту через контаміноване середовище.
- перехресне забруднення транспортного засобу.
Незважаючи на те, що літаки можуть безпечно літати під час радіоактивних опадів (Публікація ATP 3-05.11), а ризик проковтування та вдихання є невеликим при наявності ЗІЗ, промивання роторів вертольотів може збурити/поширити осілі частинки радіоактивного пилу, рідини та тверді речовини, що може збільшити ризик. Наземний персонал і екіпажі літаків, які виконують операції CASEVAC/MEDEVAC, повинні використовувати вказівки щодо ЗІЗ, подані в цих настановах з клінічної практики, якщо літак забирає пацієнтів у Теплій зоні. Використання захисних протигазів (військових або рівня C) може спочатку забезпечити певний захист, але слід пам’ятати, що каністра або фільтр протигаза може накопичувати радіоактивні частинки за умови тривалого використання.
Готуючись до проведення CASEVAC/MEDEVAC для постраждалого від опромінення, медичні працівники повинні врахувати проведення деконтамінації, ізоляцію пацієнтів з ослабленим імунітетом та доступ до відповідного медичного закладу. Тим, хто все ще має в тілі осколки, може знадобитися захист екраном/бар’єром. Портативні екрануючі пристрої, такі як свинцеві рулони, наразі не випускаються як поширене обладнання та й навряд чи знадобляться. Екранування потребують не всі пацієнти, а лише ті, що мають радіоактивні осколки, що буває рідко. Екрануючий пристрій має бути такого розміру, щоб покрити радіоактивно небезпечну ділянку, а не всього пацієнта.
Тривала допомога в польових умовах/допомога на етапах 1-3/холодна зона
Лікування пацієнтів у цій фазі має впливати як на контамінацію, так і на експозиційний вплив. Пацієнти з внутрішнім забрудненням потребують спеціальних заходів протидії залежно від типу радіонукліда, що обговорюється нижче та наведено в Таблиці 10. Пацієнти з опроміненням потребують оцінки дози (див. Додаток C для детальної інформації про біодозиметрію), щоб визначити належний рівень моніторингу та лікування. Оцінювання дози або використання якісних факторів для класифікації пацієнтів відповідно до ризику є необхідним процесом вторинного сортування для належного визначення та розподілу ресурсів.
Клінічні впливи поділяються на детерміновані та стохастичні. Детерміновані ефекти залежать від дози і складаються з субсиндромів гострого радіаційного синдрому (ГРС) і синдрому вивільнення цитокінів (СВЦ). Ці два синдроми обговорюються нижче. Стохастичні ефекти залежать від ймовірностей та найбільше зосереджені на довгостроковому ризику розвитку раку.
Гострий радіаційний синдром
Гострий променевий синдром – це поєднання клінічних ознак і симптомів, що виникають поетапно протягом періоду від годин до тижнів через значне опромінення частини (70%) або всього тіла дозою понад 1 Гр (100 сГр іонізуючого випромінювання) у вигляді пошкодження різних тканин і органів. ГРС спричинений іонізуючим опроміненням всього тіла дозами >1 Гр/100 рад. ГРС має передбачуваний клінічний перебіг, який включає чотири періоди: 1) продромальний, 2) латентний, 3) явне захворювання, 4) одужання або смерть. Час переходу між фазами залежить від поглинутої дози. Чим вища доза для всього тіла, тим коротша кожна з фаз. У Таблиці 8 нижче показано час до появи продромальних симптомів залежно від дози.16
Малюнок 2. Час до виникнення блювання
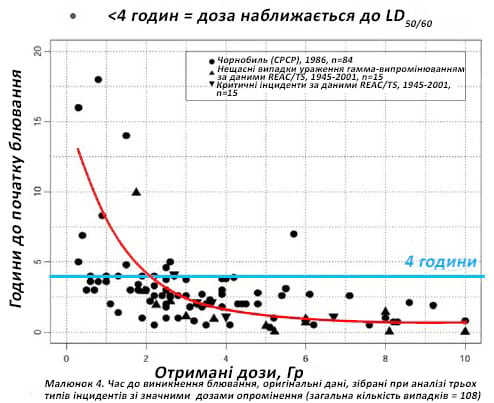
Нудота, блювання, діарея, гарячка та транзиторна еритема шкіри характеризують продромальний період, який може тривати від хвилин до днів. Потім пацієнт може виглядати добре протягом кількох годин або навіть кількох тижнів під час латентного періоду, який характеризується тихим руйнуванням клітин і тканин. Пізніше ця деструкція проявляється клінічно як один або більше з трьох синдромів: 1) гемопоетичний (Г-ГРС), 2) шлунково-кишковий (ШКТ-ГРС), 3) цереброваскулярний (Ц-ГРС). Смерть може настати протягом кількох днів у випадку шлунково-кишкових і цереброваскулярних синдромів, але може бути відстрочена на тижні у випадку гемопоетичного синдрому.14,17-18
Без втручань летальна доза (LD50/60) у випадку іонізуючого випромінювання становить близько 4 Гр. При належному втручанні та лікуванні доза зростає приблизно до 6 Гр. Досвід тих, хто отримав навіть вищі дози, показує, що за умови агресивної ресусцитації та інтенсивної терапії виживання можна продовжити до місяців. Цей фактор може привести до кінцевої необхідності евакуації цих постраждалих.14
Таблиця 8. Гострі радіаційні синдроми

Джерело: Створено COL (Ret.) Melissa Givens, USA
До початку прояву наслідків від отриманої дози менше 1-2 Гр може минути більше двох тижнів. У масових випадках, тих, хто отримав легкі дози (1-2 Гр) без травми, можна спостерігати амбулаторно та евакуювати за допомогою немедичних транспортних засобів. За цими постраждалими необхідно постійно спостерігати та регулярно переоцінювати їх стан здоров’я на предмет погіршення. Постраждалих, які зазнали опромінення у помірних та великих дозах (>2 Гр), слід госпіталізувати та визначити пріоритет для евакуації, щоб отримати спеціалізовану допомогу до початку явного періоду захворювання. Основою лікування пацієнтів у продромальному періоді ГРС є підтримувальна терапія. Її можна забезпечити на 1-3 етапах медичної допомоги або на етапі тривалої допомоги в польових умовах під час очікування евакуації.
Лікування, яке може бути потрібне в очікуванні транспортування до місця остаточного лікування, описана в Таблиці 9. Подумайте про ранню консультацію з гематологом/онкологом та/або використання консультативної лінії ADVISOR щодо лікування симптомів та гострого радіаційного синдрому.
Малюнок 3. Дія радіації на систему крові
- Лімфоцити мають високу радіочутливість
- Підрахунок лімфоцитів можна використовувати для ранньої діагностики ГРС
- Зниження рівня лімфоцитів на 50% через 48 годин властиве для дози >/+3 Гр
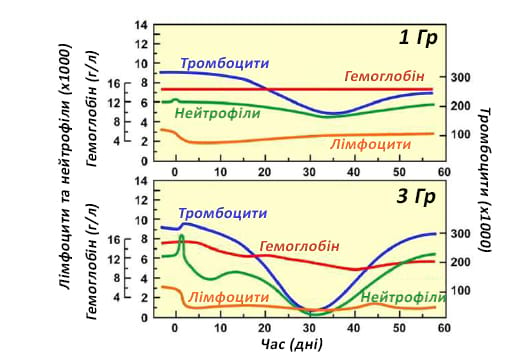
Джерело: Курс «Медичні ефекти іонізуючого випромінювання» (англ., Medical Effects of Ionizing Radiation (MEIR) Course)
Малюнок 4. Оцінка дози з використанням динаміки рівня лімфоцитів крові
- Реакція лімфоцитів залежить від дози – значне зниження вказує на більші дози.
- Можна використовувати для оцінки доз від 3 до 7 Гр – якісна відповідь
- Зниження рівня лімфоцитів на 50% в межах 48 годин вказує на поганий прогноз (> 4 Гр).
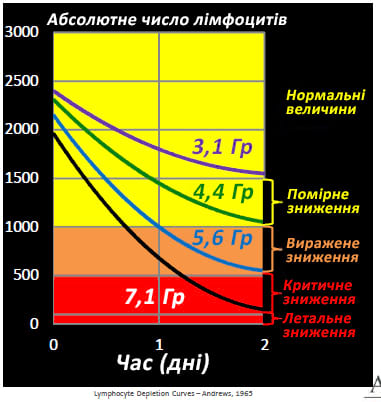
Джерело: Криві зниження рівня лімфоцитів - Andrews, 1965, Курс «Медичні ефекти іонізуючого випромінювання» (англ., Medical Effects of Ionizing Radiation (MEIR) Course)
Малюнок 5. Ядерна детонація в умовах бойових дій
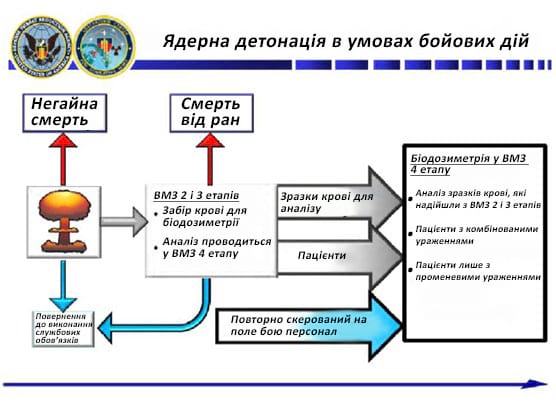
Джерело: Курс «Медичні ефекти іонізуючого випромінювання» (англ., Medical Effects of Ionizing Radiation (MEIR) Course)
Таблиця 9. Терапія гострого радіаційного синдрому
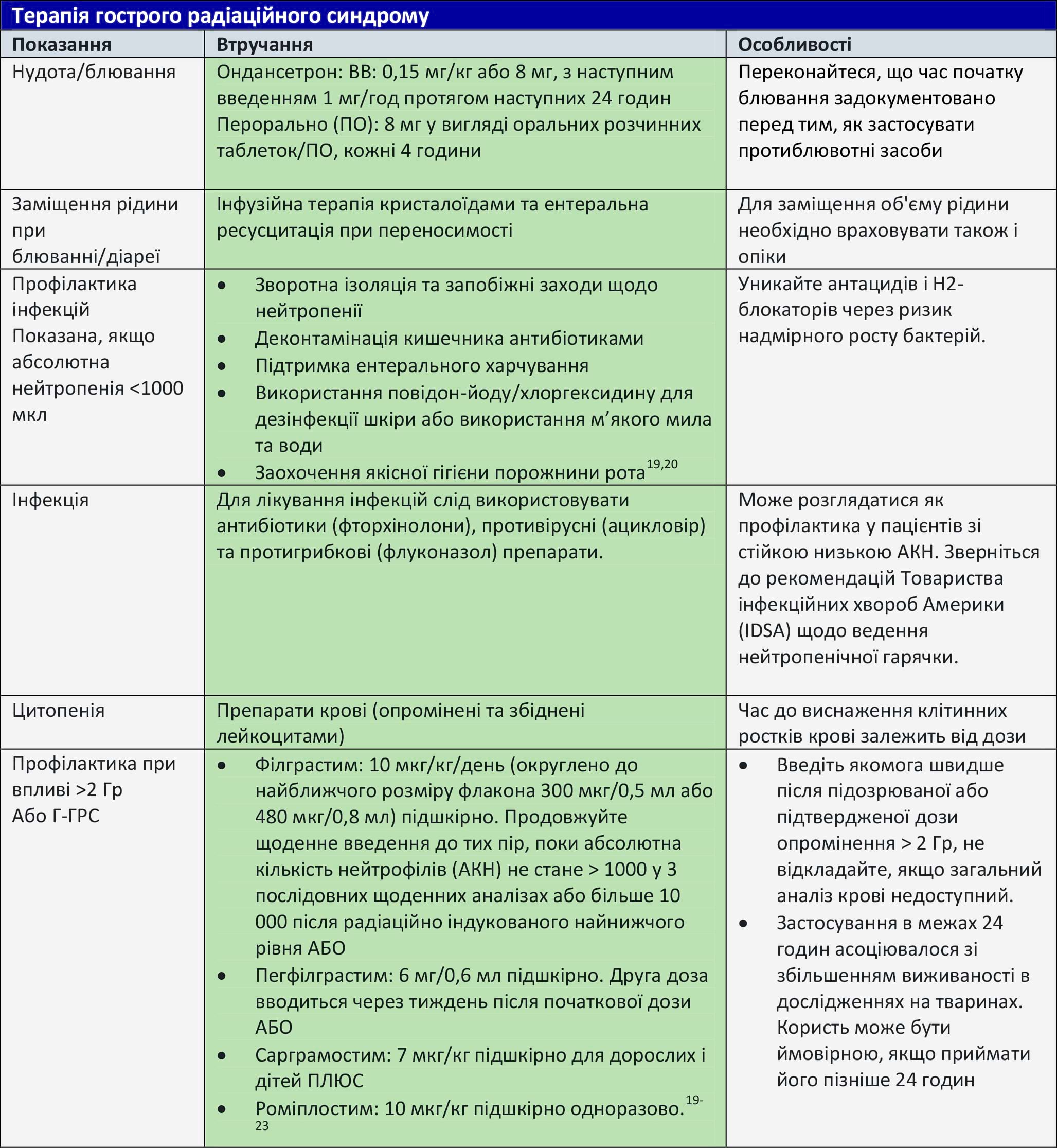
Комбіноване ураження
Детонація ядерної зброї та RDD може призвести до радіаційного ураження, зовнішньої та внутрішньої контамінації та супутньої травми. Комбіновані ураження мають синергічний ефект, що призводить до погіршення прогнозу.24,25
Пацієнти з гемопоетичним субсиндромом ГРС матимуть підвищений ризик інфікування та кровотечі. Терапію мієлоїдними цитокінами та роміплостимом слід розпочати якомога швидше.24,26,27 Хірургічні процедури слід завершити якомога швидше до появи лімфопенії та тромбоцитопенії. Використання цитокінів може подовжити хірургічне «вікно» до настання виснаження формених елементів. Переливання крові слід здійснювати, використовуючи опромінені продукти крові, коли це можливо.
Таблиця 10. Комбіновані ефекти опромінення всього тіла та опіків на різних моделях тварин
- Підвищений ризик смертності
- Гірший прогноз
- Множник смертності
- Синергічний ефект
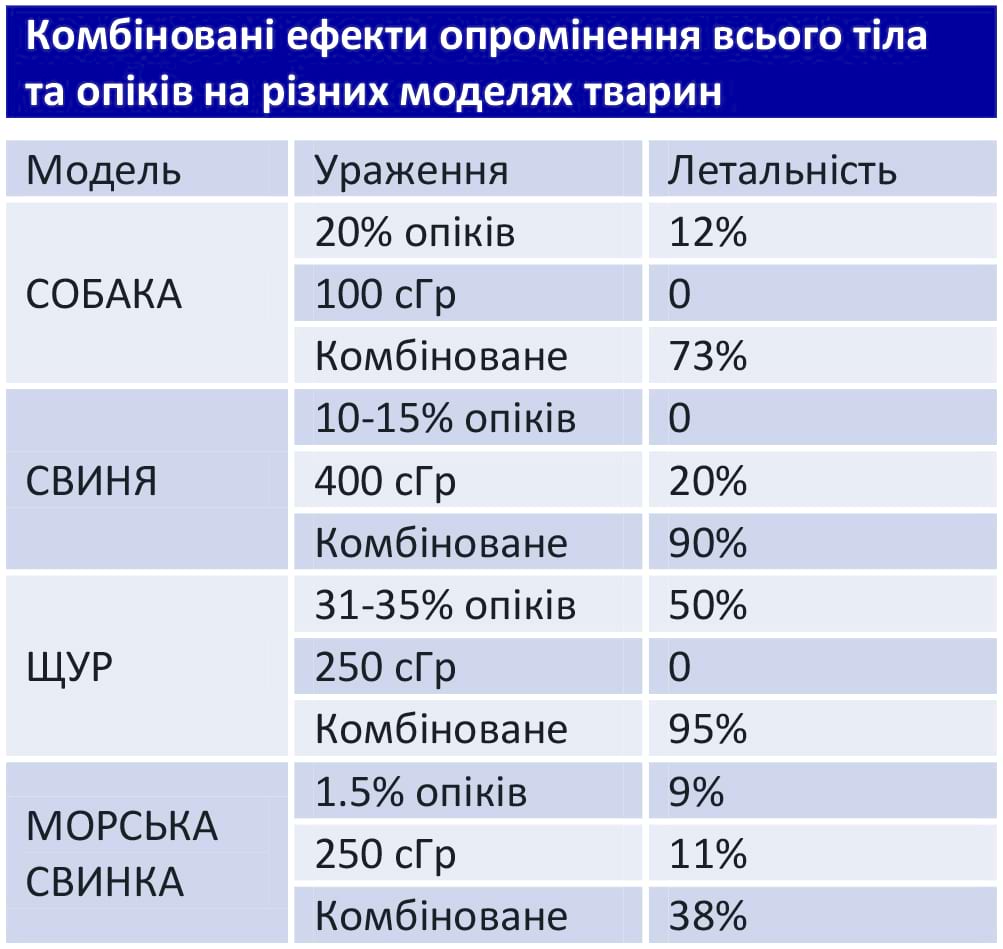
Джерело: Курс «Медичні ефекти іонізуючого випромінювання» (англ., Medical Effects of Ionizing Radiation (MEIR) Course)
Первинна медична допомога
- Стандартні рятувальні втручання при комбінованих ураженнях.
- Дії за алгоритмом XABC (англ., (Exsanguination risks, Airway, Breathing, Circulation - ризики знекровлення, дихальні шляхи, дихання, кровообіг).
- Оцінка ризиків розвитку гострого радіаційного синдрому ПІСЛЯ проведення рятувальних втручань.
- Блювання, що виникло в межах перших 4 годин → Можна припустити, що пацієнт отримав променеве ураження.
- Початок серійних розгорнутих аналізів крові кожні 6-8 годин, щоб оцінити гемопоетичний субсиндром у всіх пацієнтів групи ризику.
- Динаміка рівня лімфоцитів: зниження рівня лімфоцитів на 50% через 48 годин корелює з дозою 3-4 Грей.
- Розгляд спеціалізованих методів біодозиметрії, такі як дицентричні хромосомні аналізи (ДХА, англ., Dicentric Chromosome Assays, DCA).
Вагітність
- Плід дуже чутливий до радіації.
- Плід, зазвичай, отримує дозу меншу, ніж мати, за винятком наступного:
- Є внутрішня контамінація – близькість сечового міхура до матки
- При опроміненні радіоактивним йодом – щитоподібна залоза плода дуже активно поглинає йод після 12 тижнів гестації
- Потрібна окрема оцінка дози для даної категорії пацієнток.
- Препарати категорії С (спостерігались побічні ефекти на тваринах, але не було досліджень на людях)
- Усі колонієстимулюючі фактори
- Більшість протимікробних засобів
- Багато протиблювотних засобів
- Вода є чудовим засобом захисту від радіації.
Раннє хірургічне втручання
- Не відноситься до втручань для порятунку життя (які слід виконувати негайно), а до процедур, які слід виконати в межах 1-2 тижнів для «нормального» пацієнта, який не зазнавав опромінення (наприклад, пацієнт з переломами кісток обличчя).
- Хірургічне втручання слід проводити до того, як почне знижуватись рівень нейтрофілів і тромбоцитів
- У межах перших 36–48 годин
- Використання цитокінів гранулоцитарного колонієстимулюючого фактора може розширити це часове «вікно»
Малюнок 6. Часові рамки виконання хірургічних втручань в межах 36-48 годин
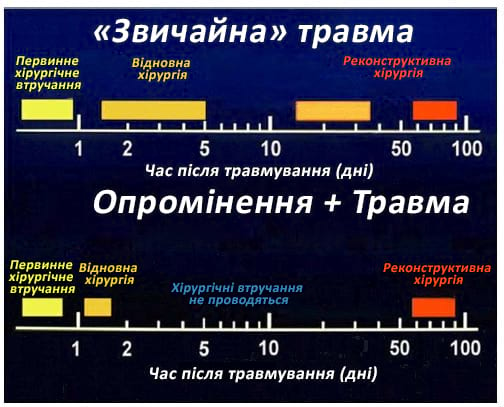
Внутрішня контамінація
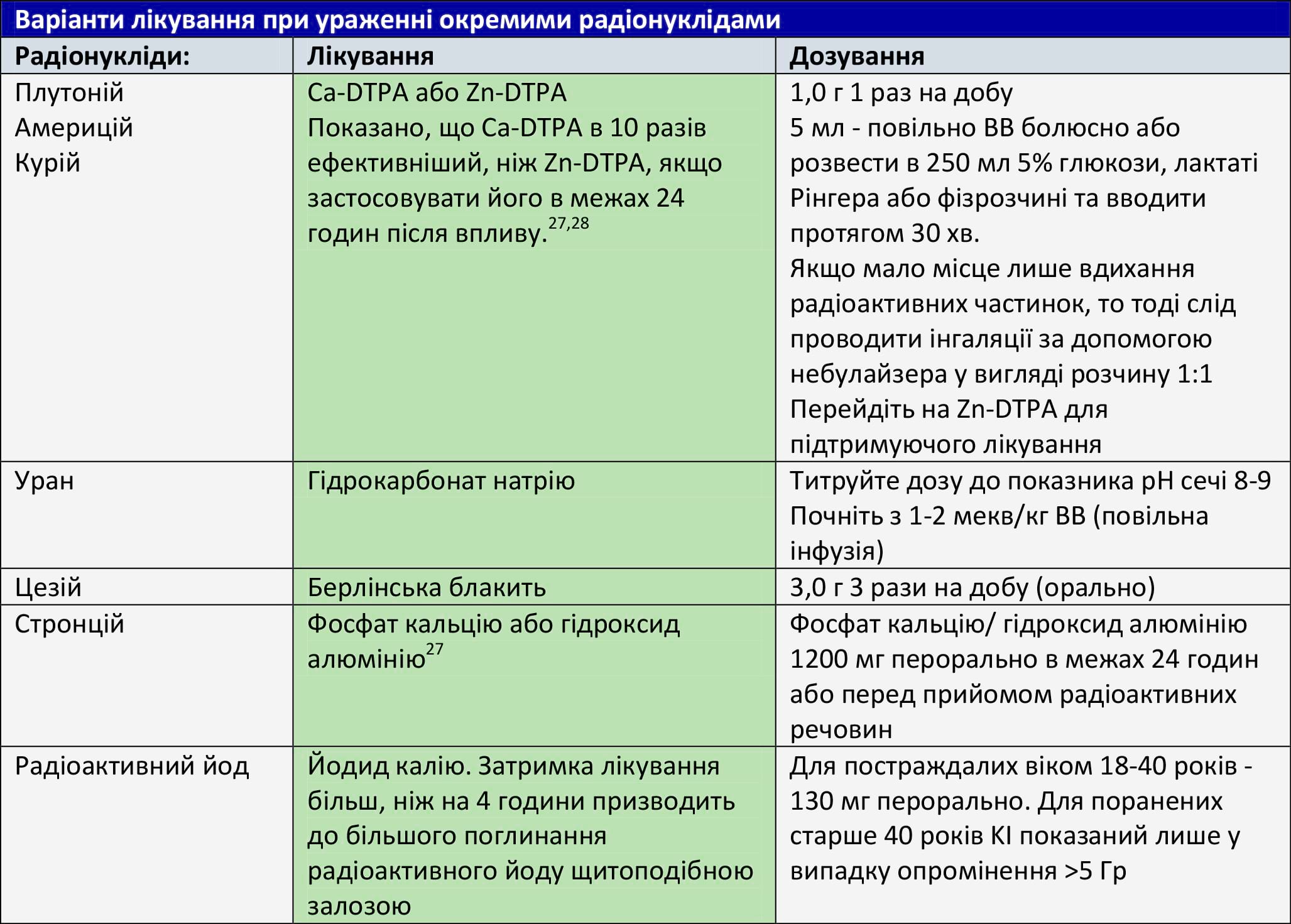
Внутрішня контамінація є результатом проковтування, вдихання або забруднення відкритих ран радіоактивним матеріалом. Ведіть таких пацієнтів як тих, що мають інтоксикацію невідомою речовиною з виконанням повного об’єму токсикологічних досліджень. Ідентифікація ізотопів, яка визначається згідно з анамнезом опромінення або використовуючи спеціальні детектори, має вирішальне значення для визначення медичного лікування. До догляду за цими пацієнтами застосовуються деякі загальні принципи, які базуються на зниженні триваючого впливу та інкорпорації. Доступні методи зменшення внутрішнього забруднення включають блокування, розведення, хелатування та зміну хімічного складу для інтенсифікації виведення ізотопу з організму. Промивання або використання проносних засобів може зменшити всмоктування в шлунково-кишковому тракті; контамінацію в легенях можна зменшити за допомогою бронхоальвеолярного лаважу; контаміновані тканини в ранах можна висікти або ретельно промити. Подальше лікування скеровують на декорпорацію ізотопів.
Існує обмежена кількість засобів протидії, які схвалені для використання у випадках, пов’язаних із радіоактивним цезієм, стронцієм, йодом і плутонієм. Медична розвідка, моделювання та використання радіонуклідних детекторів допомагають створити повну картину для діагностики та лікування внутрішнього забруднення. Лікування пацієнта із внутрішньою контамінацією, як описано в Таблиці 10, починається в межах 24 годин після події. Якщо цього не було розпочато в початкове 24-годинне вікно, лікування має спиратися на вказівки та рекомендації експертів. Йодид калію має обмежене застосування за межами аварій на атомних електростанціях, а також у вагітних/годуючих жінок і дітей. Вплив на деякі найбільш поширені ізотопи наведена в Таблиці 11.
Захист від радіоактивного йоду
- Використовуйте йодид калію для захисту щитоподібної залози
- Призначайте цей препарат рано
- В ідеалі - в межах 24 годин перед експозицією
- Бажано - в межах 4 годин після впливу
- Захист діє 24 години
- Препарат слід приймати щодня, поки існує ризик
- Пріоритет для укриття має бути в тих, хто не переносить KI, а також вагітних і годуючих жінок (FDA.gov)
Таблиця 11. Варіанти лікування при ураженні окремими радіонуклідами28
Малюнок 7. Актуальні протирадіаційні засоби USFDA та препарати у процесі розробки
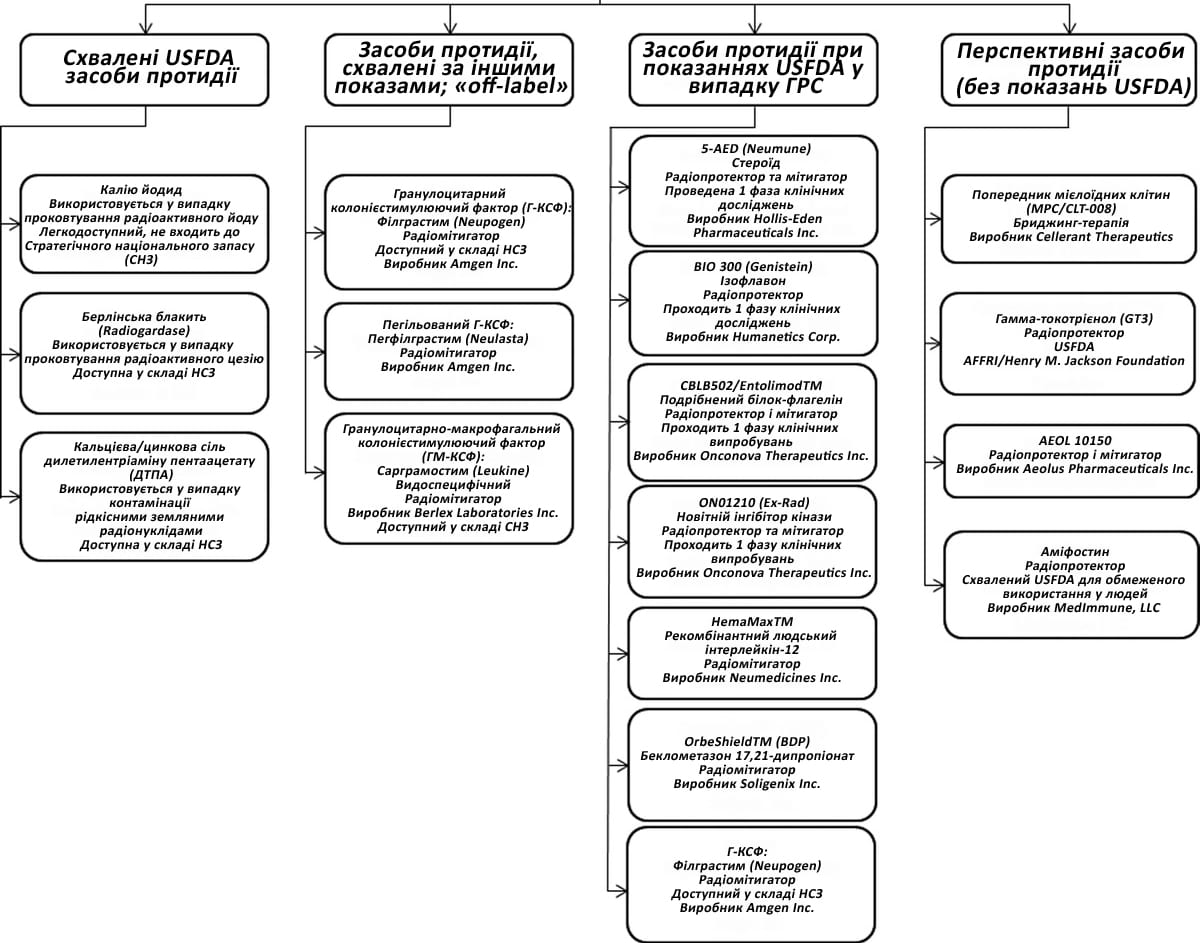
Джерело: Singh VK; Romaine PLP, Seed TM.Medical countermeasures for radiation exposure and related injuries: characterization of Medicines, FDA-approval status and inclusion into the strategic national stockpile. Health Physics 108(6):p 607-630, June 2015 (Медичні засоби проти радіаційного опромінення та пов'язаних з ним уражень: характеристика ліків, статус схвалення FDA та включення до стратегічного національного запасу)
Променеве ураження шкіри
Променеве ураження шкіри (ПУШ, англ., cutaneous radiation injury, CRI), також відоме як місцеве променеве ураження, є наслідком опромінення шкіри великими дозами радіації. Порогова доза, що викликає ПУШ, сильно варіюється через індивідуальні фактори пацієнта та властивості випромінювання (доза, потужність дози та якість випромінювання). ПУШ може виникати за відсутності ГРС. Коли це відбувається разом з ГРС, це відомо як шкірний радіаційний синдром (ШРС, англ., cutaneous radiation syndrome, CRS). Ступінь пошкодження шкіри є важливим фактором, що визначає виживання. Негайна поява еритеми зазвичай свідчить про термічний або хімічний опік. Еритема, яка виникає протягом 2 годин після гамма-випромінювання, свідчить про дуже сильне місцеве опромінення. Більшість змін шкіри відбуваються більше, ніж через тиждень після опромінення.29,30
Якщо є підозра на гостре опромінення шкіри, прохолодна вода може зменшити запалення. Можуть бути корисними консервативні методи лікування, адаптовані з протоколів для непроменевих ушкоджень шкіри, такі як місцеві стероїди, антигістамінні препарати та антибіотики.20,31 Системна антибіотикотерапія не рекомендована. Знеболення та відновлення водного балансу є важливою частиною терапії. Потреба у відновленні рідини є меншою, ніж при термічних опіках, але інфузійна терапія повинна бути адаптована до клінічного стану пацієнта.30
Для пацієнтів, які зазнали сильного опромінення, може бути необхідним спеціалізоване лікування, таке як, наприклад, пересадка шкіри або навіть ампутація для зупинки некротизування тканин.30,31 Інші методи лікування (імовірно, доступні лише на вищих рівнях надання медичної допомоги), такі як пентоксифілін, α-токоферол, трансформуючий фактор росту-β, фактор росту фібробластів, інтерферон-γ та естрадіол можуть бути розглянуті після консультації з радіологом, комбустіологом чи дерматологом.32-35
Малюнок 8. Часові рамки при променевому ураженні шкіри
- 3 Гр: Епіляція зазвичай починається через 2-4 тижні після інциденту
- 6 Гр: Еритема може виникнути протягом годин після інциденту, а потім зникнути, з наступною появою вторинної еритеми через 2-4 тижні після інциденту
- 10-15 Гр: Суха десквамація з’являється через 2-4 тижні після інциденту
- 15-25 Гр: Волога десквамація спостерігається через 2-4 тижні після інциденту
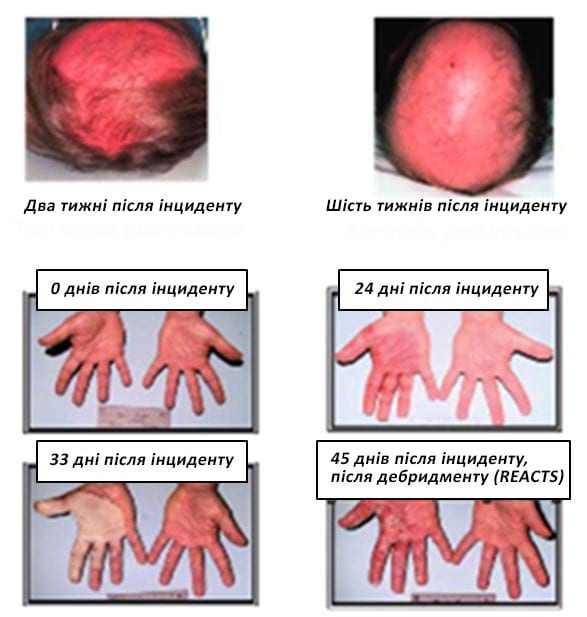
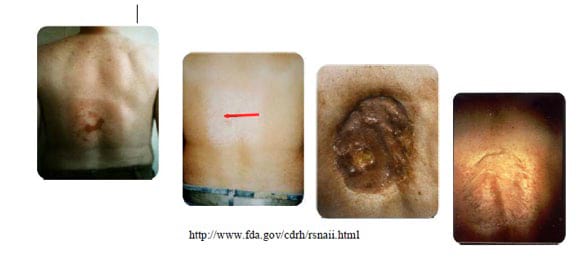
Малюнок 9. Пошкодження шкіри при рентгеноскопії
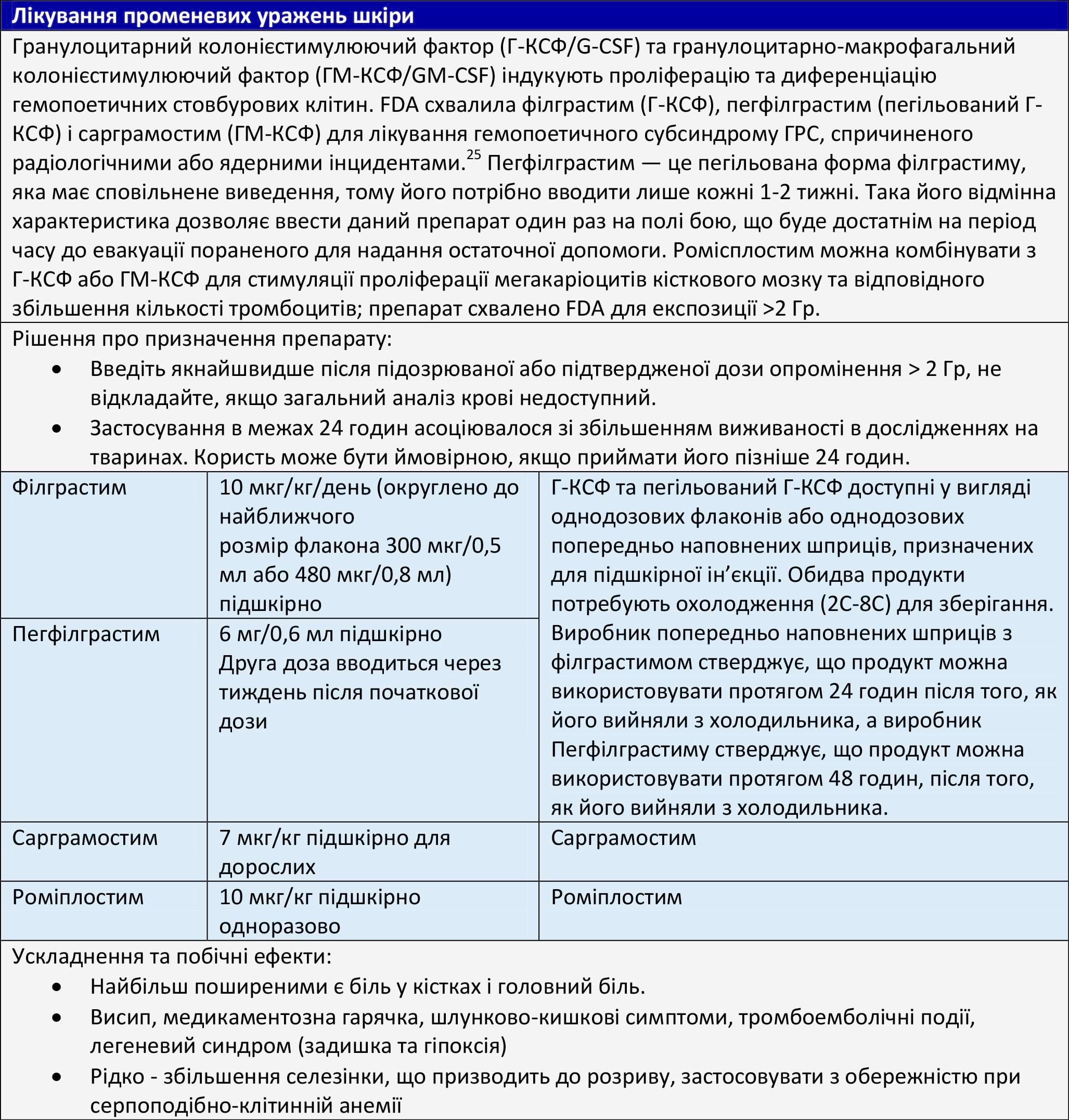
Таблиця 12. Лікування променевих уражень шкіри (ПУШ)37-39
Моніторинг покращення ефективності (ПЕ)
Досліджувані групи
- Усі пацієнти, які зазнали впливу опромінення
- Усі пацієнти, які зазнали впливу опромінення та мають супутні травми (тяжкість за шкалою ISS >16 і >2 ділянок тіла з оцінкою за AIS >= 2, САТ <100, ЧСС > 100 в межах 3 годин після травми
- Усі пацієнти, які зазнали впливу опромінення, мають задокументовані оцінки отриманої дози на основі прямої дозиметрії або клінічних критеріїв.
Мета (очікувані результати)
- Біодозиметрія оцінюється у всіх пацієнтів із використанням часу експозиції, часу до початку блювання, +/- АКН.
- Радіонукліди ідентифікуються якомога раніше, а засоби протидії призначаються згідно з Таблицею 10.
- Розгорнутий аналіз крові проводиться якомога раніше і повторюється кожні 8 годин для пацієнтів із експозицією >1 Гр.
- Пацієнти з експозицією >1 Гр, які потребують хірургічного втручання, скеровуються на операцію якнайшвидше.
- Пацієнти з експозицією >2 Гр отримують засоби протидії згідно з Таблицею 11.
- Пацієнтам з АКН <1000 проводиться деконтамінація ШКТ.
- Пацієнти з >1 Гр, які потребують препаратів крові, отримують опромінену кров зі зниженим вмістом лейкоцитів.
Показники результативності/дотримання рекомендацій
- Кількість і відсоток пацієнтів, які зазнали впливу опромінення та мають задокументовані оцінки отриманого опромінення.
- Кількість і відсоток пацієнтів із комбінованими ураженнями (опромінення плюс травма/опік).
- Якщо є опік – задокументуйте % обпеченої ділянки від ЗППТ
- Задокументуйте початок та тривалість експозиції
- Задокументуйте використовувані ЗІЗ
- Задокументуйте джерело та тип випромінювання, якщо це відомо
- Задокументуйте час до початку блювання
- Документуйте температуру щогодини протягом перших 4 годин, а потім - кожні 2 години протягом перших 24 годин
Джерела даних
- Медична картка пацієнта
- Реєстр травм Міністерства оборони США
- TMDS
Системна звітність та її частота
Згідно з даними настановами, вказане вище становить мінімальні критерії моніторингу ПЕ. Системна звітність проводитиметься щороку; додатковий моніторинг ПЕ та системну звітність можна проводити залежно від потреб.
Системний огляд та аналіз даних виконуватиме керівник JTS та відділ ПЕ JTS.
Обов'язки
Керівник команди з надання допомоги при травмах відповідає за ознайомлення з даними Настановами з клінічної практики, належне дотримання вказаних у ній вимог та моніторинг ПЕ на місцевому рівні.
-
- Chairman Joint Chiefs of Staff. JP 3-11, Operations in Chemical, Biological, Radiological, and Nuclear (CBRN) Environments, 29 Oct 2018. Validated: 28 Oct 2020
- National Council on Radiation Protection and Measurements. NCRP Report No. 161, Management of persons contaminated with radionuclides, 2009.
- Christensen DM, Jenkins MS, Sugarman SL, Glassman ES. Management of ionizing radiation injuries and illnesses, part 1: physics, radiation protection, and radiation instrumentation. J Am Osteopath Assoc. 2014 Mar;114(3):189-99.
- Christensen DM, Iddins CJ, Parrillo SJ, Glassman ES, Goans RE. Management of ionizing radiation injuries and illnesses, part 4: acute radiation syndrome. J Am Osteopath Assoc. 2014 Sep;114(9):702-11.
- Gusev I, Guskova A, Mettler F, eds. Medical management of radiation accidents, 2nd ed. Boca Raton, FL: CRC Press; 2001.
- Mettler F, Upton A. Medical effects of ionizing radiation, 3rd ed. Philadelphia: Saunders; 2008.
- Mickelson AB. Medical consequences of radiological and nuclear weapons. Falls Church, VA: Office of the Surgeon General United States Army and Fort Detrick, MD: Borden Institute; 2012.
- Canadian Nuclear Safety Commission. Types and sources of radiation. https://nuclearsafety.gc.ca/eng/resources/radiation/introduction-to-radiation/types-and-sources-of-radiation.cfm
- Mettler FA, Voelz GL. Major radiation exposures—what to expect and how to respond. N Engl J Med 346:1554–1561; 2002.
- Environmental Protection Agency. Radiation Basics. Sources and Doses.
- Medical Aspects of Radiation Incidents, 4th Edition p.13, July 2017
- Hick JL, Hanfling D, Burstein JL, Markham J, Macintyre AG, Barbera JA. Protective equipment for health care facility decontamination personnel: regulations, risks, and recommendations. Ann Emerg Med. 2003 Sep;42(3):370-80.
- Thomas RG. Evaluating and caring for contaminated patients. In advanced hazmat life support for radiologic incidents and terrorism 4th Edition. Ed. Kazzi Z, Nemhauser JB, and Walter FG. University of Arizona. 2016.
- Flynn DF ,Goans RE. Triage and treatment of radiation and combined-injury mass casualties. medical consequences of radiological and nuclear weapons, US Army Office of the Surgeon General, Borden Institute, 2012.
- Demidenko E, Williams BB, Swartz HM. Radiation dose prediction using data on time to emesis in the case of nuclear terrorism. Radiat Res. 2009 Mar;171(3):310-9.
- U.S. Department of Health and Human Services. Radiation Emergency Medical Management. Diagnosis and Treatment.
- Kiang JG, Olabisi AO. Radiation: a poly-traumatic hit leading to multi-organ injury. Cell Biosci 2019; 9:25.
- Waselenko JK, MacVittie TJ, Blakely WF, et al. Strategic National Stockpile Radiation Working Group. Medical management of the acute radiation syndrome: recommendations of the Strategic National Stockpile Radiation Working Group. Ann Intern Med. 2004;140(12):1037–1051.
- Dainiak N, Gent RN, Carr Z, et al. First global consensus for evidence-based management of the hematopoietic syndrome resulting from exposure to ionizing radiation. Disaster Med Public Health Prep. 2011;5(3):202-12.
- Dainiak N. Medical management of acute radiation syndrome and associated infections in a high-casualty incident. J Radiat Res. 2018 Apr 1;59(suppl_2):ii54-ii64.
- Singh VK, Romaine PL, Newman VL, Seed TM. Medical countermeasures for unwanted CBRN exposures: part II radiological and nuclear threats with review of recent countermeasure patents. Expert Opin Ther Pat. 2016 Dec;26(12):1399-1408
- Singh VK, Seed TM. Radiation countermeasures for hematopoietic acute radiation syndrome: growth factors, cytokines and beyond. Int J Radiat Biol. 2021;97(11):1526-1547.
- Bunin DI, Javitz HS, Gahagen J, et al. Survival and Hematologic Benefits of Romiplostim After Acute Radiation Exposure Supported FDA Approval Under the Animal Rule. Int J Radiat Oncol Biol Phys. 2023 Nov 1;117(3):705-717.
- DiCarlo AL, Hatchett RJ, Kaminski JM, et al. Medical countermeasures for radiation combined injury: radiation with burn, blast, trauma and/or sepsis. report of an NIAID Workshop, March 26–27 2007. Radiat Res. 2008;169(6):712–721.
- Kiang JG, Garrison BR, Burns TM, Zhai M, Dews IC, Ney PH, Cary LH, Fukumoto R, Elliott TB, Ledney GD. Wound trauma alters ionizing radiation dose assessment. Cell Biosci 2012; 2:20
- Assistant Secretary of Defense. Policy for Department of Defense stockpile of pentetate calcium trisodium injection and pentetate zinc trisodium injection. February 2009.
- Kazzi ZN, Heyl A, Ruprecht J. Calcium and Zinc DTPA Administration for internal contamination with plutonium-238 and americium-241. Curr Pharm Biotechnol. 2012;13(10):1957-63.
- National Council on Radiation Protection and Measurements. Management of persons contaminated with radionuclides: scientific and technical bases report no. 161, Vol. II, 2008.
- Iddins CJ, Christensen DM, Parrillo SJ, Glassman ES, Goans RE. Management of ionizing radiation injuries and illnesses, part 5: local radiation injury. J Am Osteopath Assoc. 2014 Nov;114(11):840-8.
- Müller K, Meineke V. Advances in the management of localized radiation injuries. Health Phys. 2010;98(6):843-850.
- Ashcroft GS, Greenwell-Wild T, Horan MA, Wahl SM, Ferguson MW. Topical estrogen accelerates cutaneous wound healing in aged humans associated with an altered inflammatory response. Am J Pathol. 1999;155(4):1137–1146.
- Benderitter M, Gourmelon P, Bey E, Chapel A, Clairand I, Prat M, Lataillade JJ. New emerging concepts in the medical management of local radiation injury. Health Phys. 2010 Jun;98(6):851-7.
- Kagan RJ, Peck MD, Ahrenholz DH et al. Surgical management of the burn wound and use of skin substitutes: an expert panel white paper. J Burn Care Res 2013;34(2):60-79.
- Peter RU, Gottlober P. Management of cutaneous radiation injuries: diagnostic and therapeutic principles of the cutaneous radiation syndrome. Mil Med. 2002;167(2) Suppl:110–112.
- Tattini C, Manchio J, Zaporojan V, et al. Role of TGF-beta and FGF in the treatment of radiation-impaired wounds using a novel drug delivery system. Plast Reconstr Surg. 2008;122(4):1036–1045.
- Neupogen (filgrastim) Healthcare Provider Site by Amgen.
- Nuelasta (pegfilgrastim) Official Patient Website.
- Nplate (romisplatin) Official Patient Website.
Додаток A: Засоби індивідуального захисту
Рівень ризику для персоналу, який реагує на подію, базується на потенційному впливі іонізуючого випромінювання та контамінації. У той час як ЗІЗ легко забезпечують захист від альфа- та бета-частинок, вони не можуть захистити від зовнішнього впливу іонізуючого випромінювання високої енергії та високої проникаючої здатності, наприклад гамма-променів (див. Малюнок 1). Особливості щодо різних ЗІЗ можуть включати широкий спектр варіантів для цивільних, військових, урядових чи польових умов. Такі ЗІЗ можуть або не можуть бути доступними під час початкового реагування. У Таблиці 1 описано рівні ЗІЗ, а в Таблиці 2 наведено рекомендовані рівні ЗІЗ у разі надзвичайної радіологічної ситуації. Детальніше військові ЗІЗ (орієнтоване на бойове завдання захисне спорядження, англ., Mission Oriented Protective Posture,MOPP) і цивільні ЗІЗ описані в Таблицях 3 і 4.
Малюнок 1. Види іонізуючого випромінювання
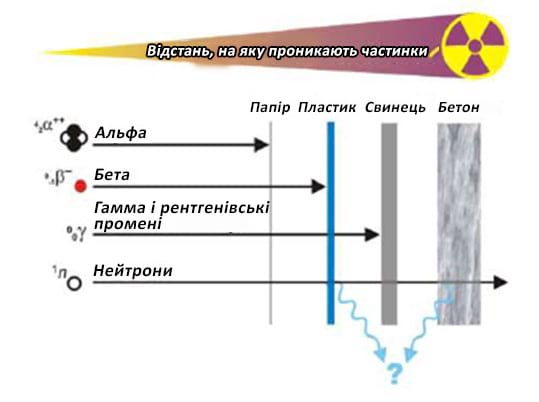
Джерело: Курс MEIR
Таблиця 1. Рівні ЗІЗ
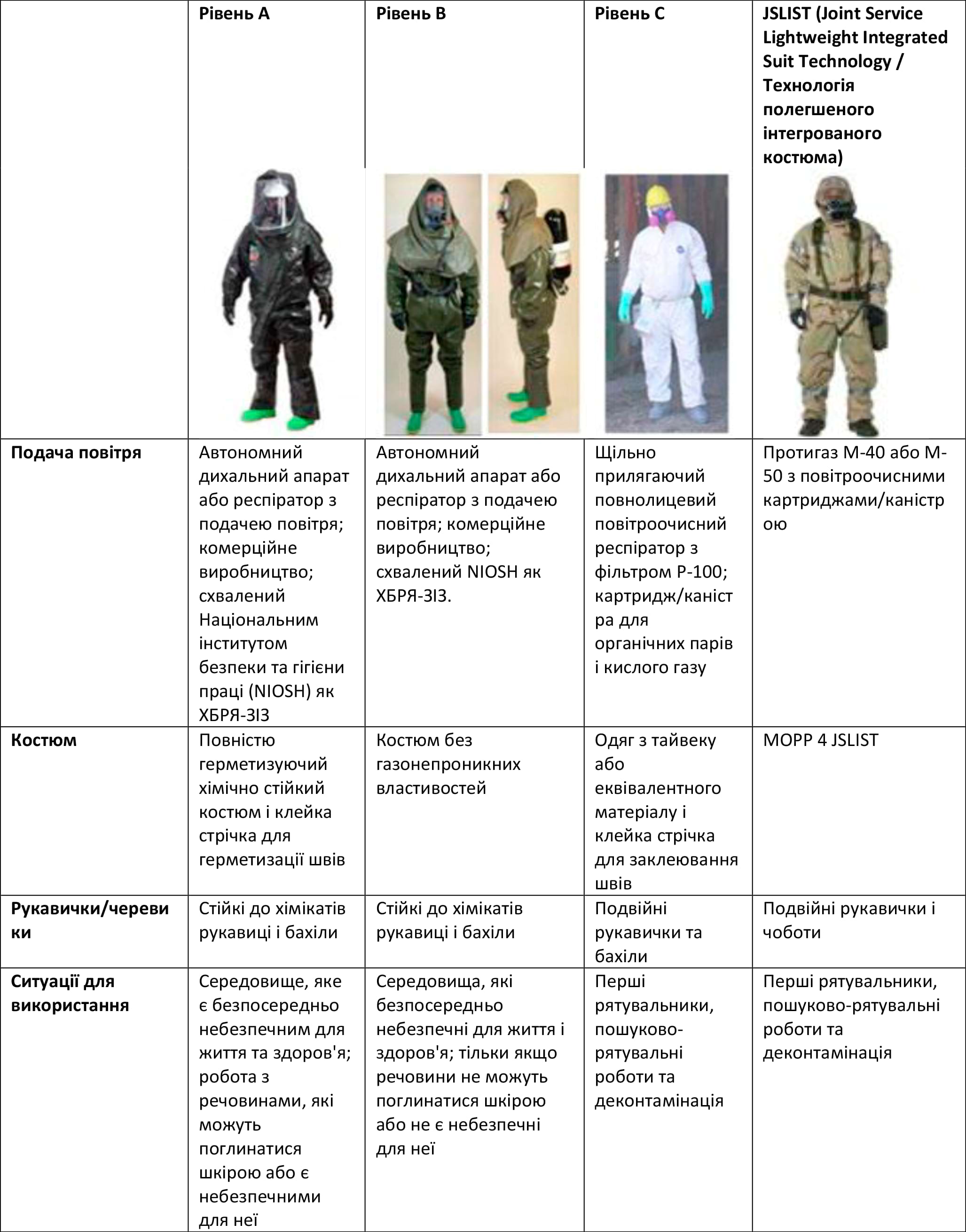
Таблиця 2. ЗІЗ при надзвичайній радіологічній ситуації

Джерело: Медичний менеджмент надзвичайної радіологічної ситуації (hhs.gov)
Таблиця 3. Військові ЗІЗ – Спорядження MOPP
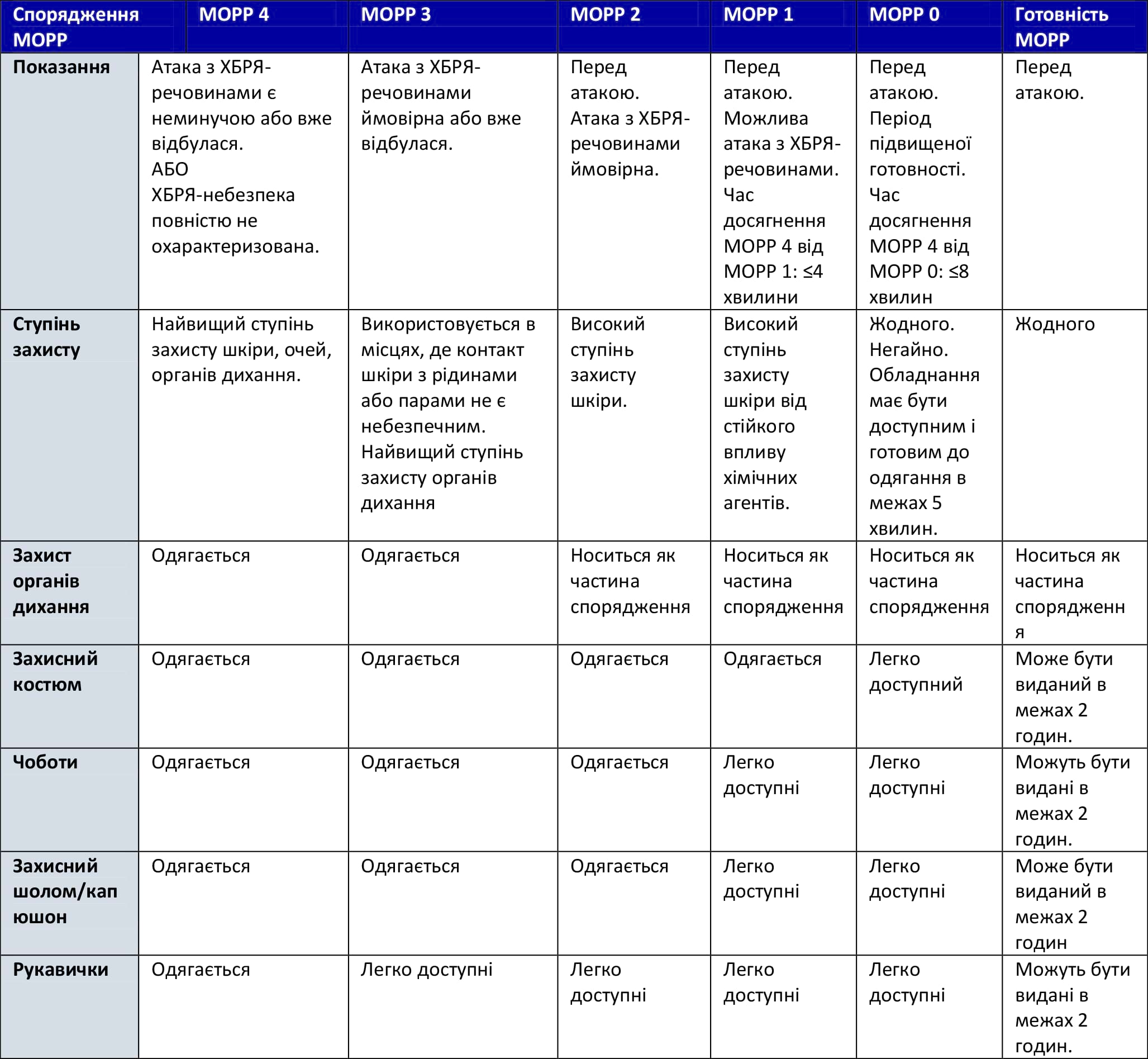
Джерело: ЗІЗ в умовах надзвичайної радіологічної ситуації - Медичний менеджмент надзвичайної радіологічної ситуації (hhs.gov)
Таблиця 4: Цивільні ЗІЗ в умовах надзвичайної радіологічної ситуації - Медичний менеджмент надзвичайної радіологічної ситуації
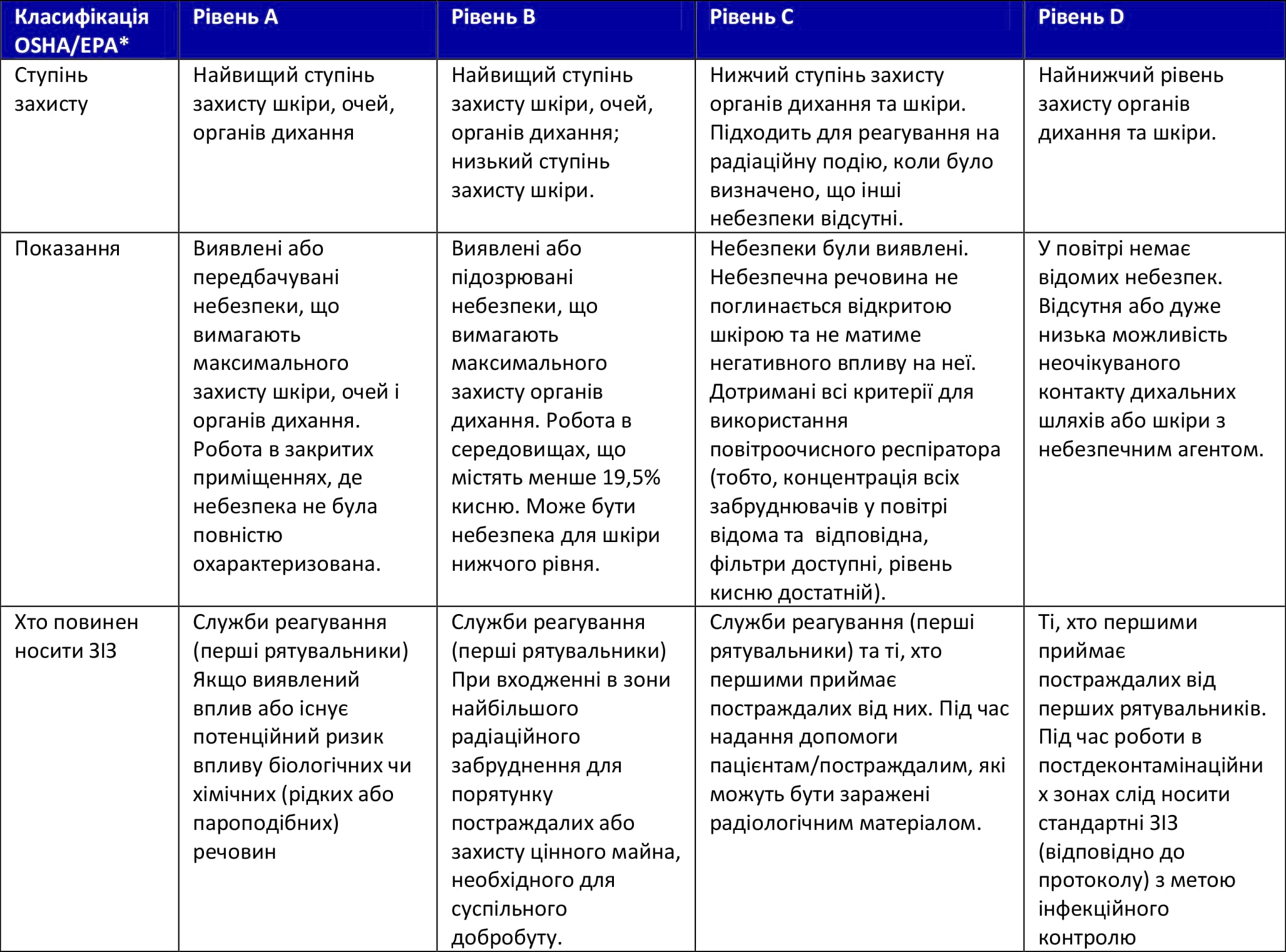
*Occupational Safety and Health Administration (OSHA) - Управління з охорони праці / Environmental Protection Agency (EPA) - Агентство з охорони навколишнього середовища
- Інформація EPA щодо ЗІЗ
- Інформація OSHA щодо ЗІЗ
- Стандартні ЗІЗ та процедури, що використовуються для запобігання передачі інфекцій у медичних закладах, забезпечують належний захист проти низьких рівнів радіологічного забруднення, які можуть бути виявлені в постдеконтамінаційних зонах лікарні (наприклад, відділення екстреної/ невідкладної допомоги та операційні). Під час надання допомоги особам із високими дозами радіаційного опромінення не вимагається одягання стандартних ЗІЗ, хоча необхідно буде дотримуватися процедур зворотної ізоляції у процесі розвитку нейтропенії.
Додаток B: Стандарти та особливості виявлення радіації
У додатку міститься інформація про різні технології, які можуть виявляти радіацію та підтверджувати наявність забруднення персоналу чи навколишнього середовища. Більше інформації можна знайти на сайті https://jacks.jpeocbd.army.mil/ Жоден окремий пристрій не може виявити всі форми радіації, і жоден пристрій не може бути корисним у всіх ситуаціях. Прилади виявлення радіації виявляють і вимірюють наступне: 1) конкретні типи випромінювання (наприклад, альфа, бета, гамма, нейтрони), 2) конкретні рівні (або діапазони) енергії випромінювання (у кеВ, МеВ) 3) «Підрахунок» за одиницю часу (хвилина або секунда) 4) рентгени (Р) за одиницю часу (наприклад, мілірентген за годину [мР/год]) 5) кумулятивну дозу (в Грей або рад) 6) потужність дози (в Грей або рад за одиницю часу).


Додаток C: Біодозиметрія
Клінічні ознаки та симптоми залежать від дози. Тому знання ранніх маркерів для оцінки дози радіації у пацієнтів, які зазнали радіологічного опромінення, може бути дуже корисним. Дозу радіації можна оцінити, використовуючи час до виникнення блювання, анамнез хвороби та серійні аналізи крові з підрахунком формули. Анамнез хвороби повинен включати обставини підозрюваного опромінення, місцезнаходження відносно до інциденту, укриття та інші цінні деталі щодо опромінення, такі як запах або смак пилу/диму та наявність пилу/сміття на шкірі, на додаток до клінічних симптомів.
Якщо доступна лабораторна підтримка, серійні розгорнуті аналізи крові є одним із найбільш доступних і корисних методів для характеристики отриманої дози. Початковий загальний аналіз крові з формулою, а потім серійні вимірювання тричі на день протягом 2-3 днів полегшать визначення швидкості виснаження лімфоцитів. Зменшення кількості лімфоцитів більш, ніж на 50% протягом перших 48 годин вказує на потенційно летальний вплив. Якщо мав місце лише вплив іонізуючого випромінювання, за відсутності лабораторної підтримки або як доповнення до підрахунку лімфоцитів можна використовувати час до виникнення блювання. Блювання протягом 1-2 годин після контакту має поганий прогноз.
Ознаки та симптоми ранньої фази
Оцінка дози за допомогою цитогенетичної біодозиметрії лімфоцитів крові
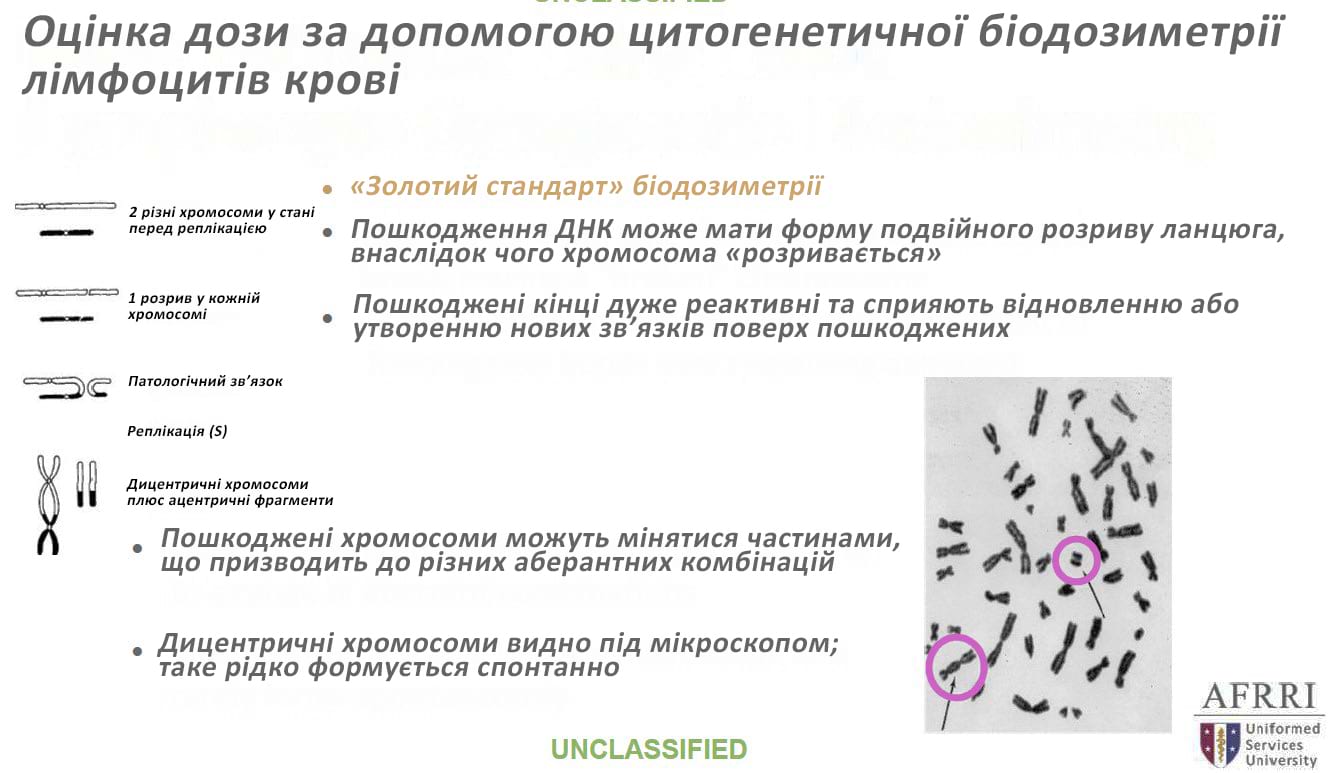
Цитогенетичний біоаналіз хромосомних аберацій (зокрема дицентрики лімфоцитів) вважається «золотим стандартом» оцінки отриманої дози. Однак зразки повинні бути отримані через 24 години після впливу, а результати можуть бути недоступними протягом 2-3 днів, тому час до появи блювання та кількість лімфоцитів залишаються найкориснішими інструментами в період початкової оцінки. Корисно пам’ятати, що якщо людина не блювала протягом 8–10 годин після опромінення, малоймовірно, що він чи вона зазнали впливу дози, що перевищує 1 Гр. Інструмент біодозиметричної оцінки Інституту радіобіологічних досліджень збройних сил США (англ., Armed Forces Radiobiology Research Institute Biodosimetry Assessment Tool) — це програмний пакет, який може допомогти постачальникам оцінити опромінення та вибрати лікування. Інструмент має безкоштовний пакет для перших реагувальників під назвою «Сортування відповідно до радіологічної оцінки для перших рятувальників» (англ., First Responders Radiological Assessment Triage). Ці корисні інструменти можуть сприяти оптимізації стандартизованої системи реагування на ядерний або радіологічний інцидент. На веб-сторінці Департаменту охорони здоров’я та соціального захисту населення від надзвичайних радіологічних ситуацій США розміщені інтерактивні інструменти для допомоги в біодозиметрії. Ці інструменти можна знайти за адресою: https://remm.hhs.gov/ars_wbd.htm
Додаток D: Алгоритми надання допомоги постраждалому від радіаційного ураження
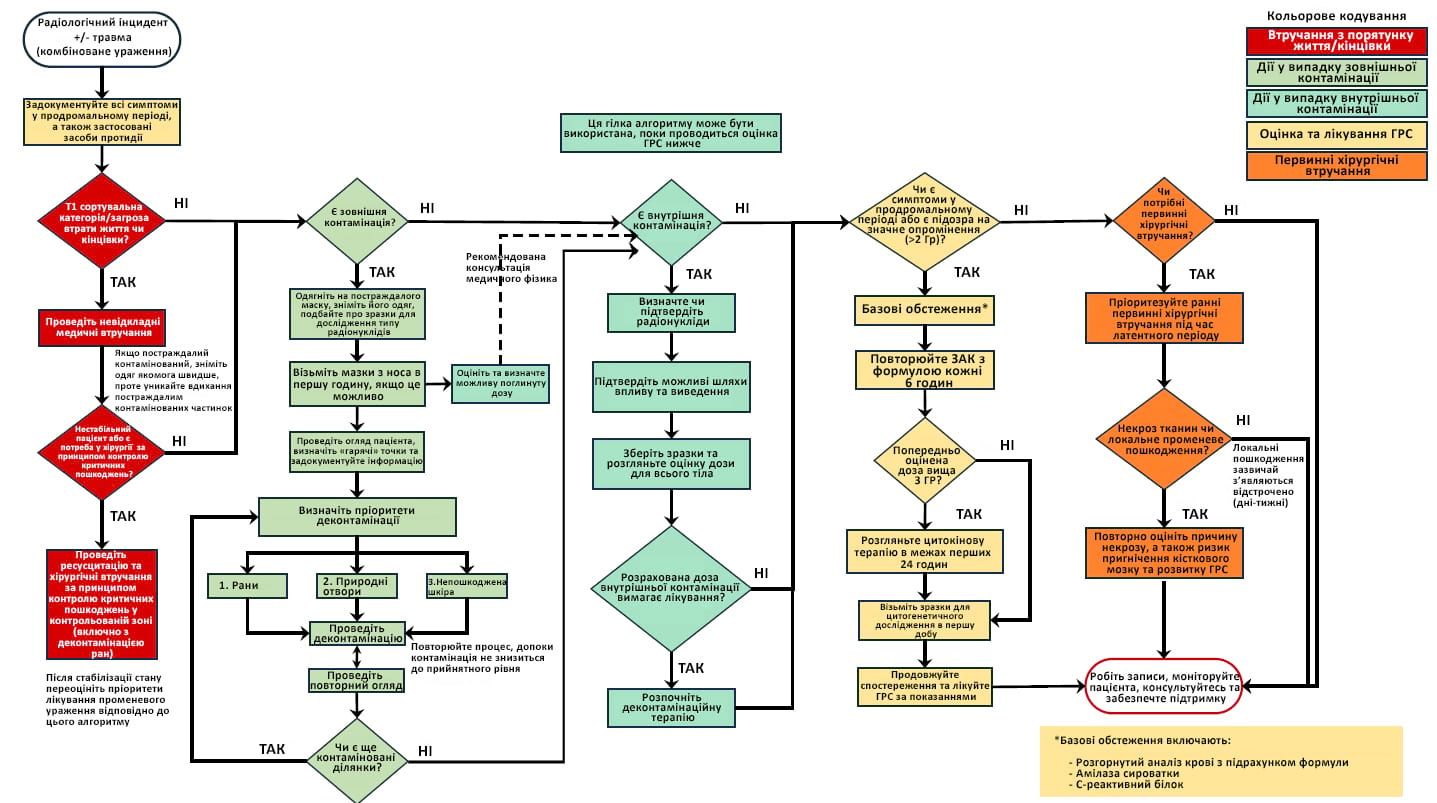
Адаптовано з Алгоритму лікування REACT/TS
Додаток E: Форма для допоміжної інформації при ХБРЯ-ураженні

Додаток F: Телемедична консультація
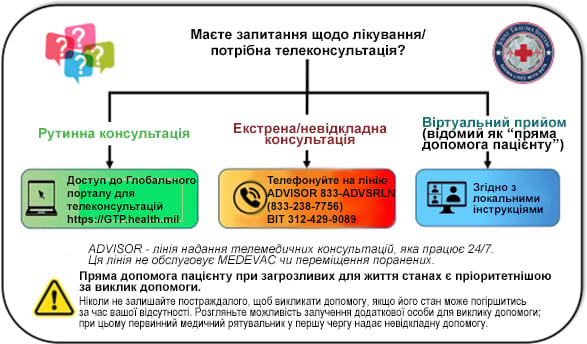
Ілюстрація Raymond Samonte
Глобальний портал для телеконсультацій: https://GTP.health.mil
Додаток G: Інформація щодо не передбаченого інструкцією застосування лікарських засобів у настановах з клінічної практики
Мета
Мета цього Додатка — надати роз’яснення політики та практики Міністерства оборони США щодо включення в Настанови з клінічної практики «незатверджених» показань для продуктів, які були схвалені Управлінням з контролю якості продуктів харчування і лікарських засобів США (FDA). Це стосується використання препаратів не за призначенням для пацієнтів, які належать до Збройних сил США.
Вихідна інформація
Незатверджене (тобто «не за призначенням» - “off-label”) використання продуктів, схвалених FDA, надзвичайно поширене в медицині США і зазвичай не регулюється окремими нормативними актами. Проте, згідно з Федеральним законодавством, за деяких обставин застосування схвалених лікарських засобів за незатвердженими показаннями регулюється положеннями FDA про «досліджувані нові ліки». До цих обставин належить використання в рамках клінічних досліджень, а також, у військовому контексті, використання за незатвердженими показаннями згідно з вимогами командування. Деякі види використання за незатвердженими показаннями також можуть підлягати окремим нормативним актам.
Включення до Настанов з клінічної практики використання медикаментів за незатвердженими показаннями не належить до клінічних випробувань і не є вимогою командування. Більше того, таке включення не передбачає, що Військова система охорони здоров’я вимагає від медичних працівників, які працюють в структурах Міноборони США, застосовувати відповідні продукти за незатвердженими показаннями або вважає це «стандартом медичної допомоги». Швидше, включення до CPGs використання засобів «не за призначенням» має поглиблювати клінічне судження відповідального медичного працівника шляхом надання інформації щодо потенційних ризиків та переваг альтернативного лікування. Рішення приймається на основі клінічного судження відповідальним медичним працівником у контексті відносин між лікарем і пацієнтом.
Додаткові процедури
Виважений розгляд
Відповідно до цієї мети, в обговореннях використання медикаментів «не за призначенням» в CPG конкретно зазначено, що це використання, яке не схвалено FDA. Крім того, такі обговорення є збалансованими у представленні даних клінічних досліджень, включаючи будь-які дані, які свідчать про обережність у використанні продукту, і, зокрема, включаючи усі попередження, видані FDA.
Моніторинг забезпечення якості
Що стосується використання «не за призначенням», діяльність Міністерства оборони США полягає у підтримці регулярної системи моніторингу забезпечення якості результатів і відомих потенційних побічних ефектів. З цієї причини підкреслюється важливість ведення точних клінічних записів.
Інформація для пацієнтів
Належна клінічна практика передбачає надання відповідної інформації пацієнтам. У кожних Настановах з клінічної практики, де йдеться про використання засобу «не за призначенням», розглядається питання інформування пацієнтів. За умови практичної доцільності, слід розглянути можливість включення додатка з інформаційним листком для пацієнтів, що видаватиметься до або після застосування продукту. Інформаційний листок має в доступній для пацієнтів формі повідомляти наступне: a) що дане застосування не схвалене FDA; b) причини, чому медичний працівник Міністерства оборони США може прийняти рішення використати продукт з цією метою; c) потенційні ризики, пов’язані з таким застосуванням.
































































