ПЕРЕДМОВА
Повномасштабна війна в Україні поставила безпрецедентні виклики перед національною системою охорони здоров’я, зокрема – у сфері безпечного та своєчасного транспортування пацієнтів у критичному стані. У відповідь на ці виклики було започатковано важливу ініціативу, спрямовану на посилення спроможності системи екстреної медичної допомоги шляхом розроблення комплексного набору посібників із транспортування пацієнтів у критичному стані (CCT).
Ці матеріали були створені у співпраці національних і міжнародних експертів – на запит Всесвітньої організації охорони здоров’я та Державного закладу « Український науково практичний центр екстреної медичної допомоги та медицини катастроф МОЗ України» – за фінансової підтримки Європейського Союзу. Посібники ґрунтуються на найкращих міжнародних практиках і водночас ретельно адаптовані до українських умов, що забезпечує їхню актуальність і практичне застосування в реальній системі охорони здоров’я.
П’ять розділів цього видання покликані уніфікувати й удосконалити процеси, інфраструктуру та структуру управління, які необхідні для надання якісної медичної допомоги під час транспортування пацієнтів у критичному стані.
- Розділ 1 визначає стратегічні та організаційні засади функціонування системи транспортування пацієнтів у критичному стані ( далі CCTS).
- Розділ 2 містить клінічні настанови для забезпечення безпечного та ефективного надання допомоги під час транспортування пацієнтів у критичному стані.
- Розділ 3 охоплює стандартизовані операційні процедури.
- Розділи 4 і 5 є навчальними посібниками для фахівців та інструкторів, сприяючи як поширенню знань, так і сталому професійну розвитку у межах CCTS.
Ці посібники – не лише технічні документи. Вони є свідченням стійкості, солідарності та непохитної відданості справі збереження життя. Вони уособлюють спільне бачення системи охорони здоров’я, здатної діяти швидко, скоординовано й ефективно навіть за найскладніших умов.
Закликаємо всіх медичних працівників, представників органів влади, освітян і партнерів активно впроваджувати ці інструменти, використовувати їх у повсякденній практиці та сприяти їх поширенню по всій території України. Це дозволить забезпечити надання допомоги кожному пацієнту саме тоді, коли вона найбільш необхідна, а також зробить систему сильнішою, більш скоординованою та стійкою до майбутніх викликів.
ВСТУП
Транспортування пацієнтів у критичному стані між закладами охорони здоров’я належить до найбільш складних і високоризикових процесів сучасної медицини. В умовах України, де система охорони здоров’я функціонує в умовах обмежених ресурсів та постійного операційного навантаження, виникає нагальна потреба у впровадженні уніфікованих протоколів, заснованих на доказових даних. Саме з цією метою розроблено Клінічні настанови з транспортування пацієнтів у критичному стані (CCT Clinical Guidance), які визначають комплексну рамкову структуру для забезпечення безпечного, ефективного та орієнтованого на пацієнта міжлікарняного транспортування.
Документ підготовлений у результаті співпраці фахівців екстреної медичної допомоги та адміністративного персоналу закладів охорони здоров’я. Настанови адаптовано до клінічних і логістичних умов функціонування системи охорони здоров’я України, при цьому вони залишаються придатними до застосування в інших країнах і контекстах. У документі визначено чіткий розподіл ролей і відповідальності між направляючими та приймаючими закладами охорони здоров’я, бригадами транспортування пацієнтів у критичному стані (CCT) та центрами координації. Особливий акцент зроблено на забезпеченні безперервної комунікації, належної підготовки та безперервного удосконалення якості.
Від первинної оцінки стану пацієнта до забезпечення прохідності дихальних шляхів, підтримки дихання, кровообігу та контролю неврологічного стану під час транспортування — кожен розділ настанов містить практичні рекомендації та стандартизовані операційні процедури, спрямовані на підвищення безпеки пацієнта і покращення результатів лікування. Метою є забезпечення медичних працівників знаннями та інструментами, необхідними для належного виконання завдань, пов’язаних із транспортуванням пацієнтів у критичному стані.
Використання стандартизованих процесів — чек - листів, клінічних протоколів та структурованих інструментів комунікації — сприяє мінімізації ризиків, удосконалює міжпрофесійну координацію та підтримує безперервність надання медичної допомоги на всіх етапах транспортування. Крім того, підкреслюється необхідність проведення післятранспортних дебрифінгів та моніторингу ефективності із застосуванням ключових показників, що сприяє формуванню культури навчання та постійному вдосконаленню системи.
Висловлюється вдячність усім фахівцям, які здійснюють транспортування пацієнтів у критичному стані. Їхня відданість безпеці пацієнтів та високим стандартам клінічної практики стала основою для створення цього документа. Клінічні настанови CCT призначені для лікарів, парамедиків, середнього медичного персоналу та медичних координаторів, які працюють у складних умовах для забезпечення кожному пацієнтові належної медичної допомоги у належний час і в належному місці.
ПОДЯКИ

Повномасштабне вторгнення Російської Федерації в Україну у 2022 році та пов’язана з ним війна призвели до різкого збільшення кількості пацієнтів у критичному стані як поблизу лінії фронту, так і в інших регіонах країни. Окремі заклади охорони здоров’я (далі ЗОЗ) зазнали перевантаження та потребували допомоги. Це зумовило необхідність створення системи розподілу та транспортування пацієнтів у критичному стані по території України та за її межі.
З огляду на закритий повітряний простір і значні відстані, перевезення пацієнтів у критичному стані автомобільним транспортом поступово виокремилося в окрему спеціалізовану сферу медицини., що на той час залишалася практично не врегульованою належними клінічними рекомендаціями. Ці матеріали покликані заповнити цю прогалину.
Від імені ДЗ „УНПЦ ЕМД та МК МОЗ України» щиро дякую всім фахівцям і організаціям, чий професійний досвід і плідна співпраця стали вирішальними у створенні цього ресурсу. Завдяки їхнім спільним зусиллям вдалося зробити вагомий крок у реалізації нашої спільної мети — удосконалення системи екстреної медичної допомоги в Україні, передусім для пацієнтів у критичному стані, які потребують допомоги саме тоді, коли вона є життєво необхідною.
Неможливо подякувати кожному окремо, оскільки багато фахівців долучилися до рецензування, надали зворотний зв’язок та внесли змістовні пропозиції під час розробки матеріалів, що склали пакет ресурсів з транспортування пацієнтів у критичному стані (Critical Care Transfer Package). Нижче зазначено основних партнерів:
- Artesans-ResQ Німеччина: Джонатан Бен Вінке
- Artesans-ResQ Україна: Ілля Білоконов, Максим Дорманн
- Міністерство охорони здоров’я України: Арман Качарян
- Український науково-практичний центр екстреної медичної допомоги та медицини катастроф МОЗ України: Ольга Білощицька
- Екстрена медична допомога (ЕМД): Едуард Горзов (ЕМД Закарпаття), Богдан Фостяк (ЕМД Рівне)
- Регіональне бюро ВООЗ у Європі: Джонатан Бен Вінке (технічний консультант), Рейчел Джейн Флетчер (технічний консультант), Гуннар Фарстад (технічний консультант), Тімоті Дас (технічний консультант), Ігор Перегінець (регіональний директор з питань надзвичайних ситуацій)
- Окрема подяка Європейському товариству екстреної медицини (EUSEM) за їхній фаховий перегляд і коментарі: Вільгельм Берінгер, Роберт Ліч, Крістоф Тесторі, Абдо Хурі, Ерік Ревю, Александр Нюрнбергер, Рут Браун, Йованка Блунк, Карен Пітерс, Атул Бансал
Особлива вдячність — усім українським фахівцям екстреної медичної допомоги, які взяли участь у тренінгах та поділилися своїми ідеям. Ваші відгуки допомогли значно покращити цей матеріал.
Окремо висловлюємо щиру вдячність пану Джонатану Вінке, який вклав надзвичайно багато зусиль, часу та енергії у розробку цього пакету ресурсів — від концепції до фінального втілення. Його робота охопила регіони України, до яких рідко дістаються іноземні фахівці. Працюючи пліч-о-пліч із українськими колегами зі служби екстреної медичної допомоги, він надавав підтримку під час складних транспортувань пацієнтів у критичному стані, ділився практичними знаннями й досвідом.Глибоке розуміння контексту і щире ставлення до українських колег стали важливою основою для співпраці.
Без його особистої участі створення цього комплексу матеріалів було б неможливим.
Візуальне оформлення та макет публікації стали можливими завдяки креативній роботі бригади 4PLUS4, за що висловлюємо особливу подяку Акселю Карлссону та Беатріс Ґраф-Перейра.
Переклад здійснено командою бюро перекладів AplusLS у складі: Ольги Рожнятовської, Богдана Висоцького, Юлії Конаш та директора бюро Наталії Зачинської.
Окрема подяка висловлюється Галині Юріївні Цимбалюк за редакторську роботу над перекладом, зокрема за перевірку точності й коректності медичної термінології та її узгодження з офіційними стандартами й протоколами.
Підготовка та публікація цих матеріалів стала можливою завдяки фінансовій підтримці Служби інструментів зовнішньої політики Європейської Комісії (FPI).
З повагою,
д-р Віталій Крилюк
Директор
Державного закладу
Український науково-практичний центр екстреної медичної допомоги та медицини катастроф
Міністерства охорони здоров’я України

СКОРОЧЕННЯ
| AKI | Acute Kidney Injury - гостра ниркова недостатність |
| ГРДС | Acute Respiratory Distress Syndrome - гострий респіраторний дистрес-синдром (ГРДС) |
| BP | Blood Pressure - артеріальний тиск |
| bpm | Beats Per Minute - частота серцевих скорочень |
| BPS | Behavioral Pain Scale - поведінкова шкала болю |
| CCTT | Critical Care Transfer Team - бригада транспортування пацієнтів у критичному стані |
| см | Centimeter - см |
| CO | Cardiac Output - хвилинний об'єм кровообігу (ХОК), або серцевий викид |
| CRM | Crew Resource Management - управління ресурсами бригади |
| CT | Computed Tomography - комп'ютерна томографія |
| CVVH | Continuous Veno-Venous Hemofiltration - подовжена вено-венозна гемофільтрація (ПВВГФ) |
| ECG | Electrocardiogram - ЕКГ |
| EHR | Electronic Health Record - електронна медична картка |
| EMR | Electronic Medical Record - електронна медична історія пацієнта |
| EtCO₂ | End-Tidal Carbon Dioxide - концентрація CO₂ в кінці видиху |
| FiO₂ | Fraction of Inspired Oxygen - частка кисню в дихальній суміші |
| GABA | Gamma-Aminobutyric Acid - гамма-аміномасляна кислота (ГАМК) |
| GCS | Glasgow Coma Scale - шкала ком Глазго (ШКГ) |
| hr. | Hour - година |
| HR | Heart Rate - частота серцевих скорочень |
| I:E | Inspiratory: Expiratory (Ratio) - співвідношення вдих/видиху |
| ICP | Intracranial Pressure - внутрішньочерепний тиск |
| ICU | Intensive Care Unit - відділення інтенсивної терапії (ВІТ) |
| ISBAR | Ідентифікація, Ситуація, Передумови, Оцінка, Рекомендації |
| IV | в/в доступ |
| JVP | Jugular Vein Pressure - центральний венозний тиск (ЦВТ) |
| KDIGO | Глобальна ініціатива з удосконалення лікування захворювань нирок |
| kg | Kilogram - кг |
| KPI | Key Performance Indicator - ключові показники ефективності (КПІ) |
| L | Liter - л |
| CAT | Mean Arterial Pressure - Середній артеріальний тиск (САТ) |
| mg | Milligram - міліграм - мг |
| min | Minute - хв |
| mL | Milliliter - мл |
| mmHg | Millimeters of Mercury - мм рт. ст. |
| mmol/L | Millimoles per Liter - ммоль/л |
| NEWS2 | National Early Warning Score 2 - національна шкала раннього реагування, версія 2 |
| NMDA | N-Methyl-D-Aspartate - N-метил-D-аспарагінова кислота (NMDA) |
| NRS | Numeric Rating Scale - числова шкала болю |
| O₂ | Oxygen - кисень |
| PCV | Pressure Controlled Ventilation - вентиляція з керованим тиском |
| pCO₂ | Partial Pressure of Carbon Dioxide - парціальний тиск вуглекислого газу |
| PDE-3 | Phosphodiesterase-3 - фосфодіестераза-3 |
| PEEP | Positive End-Expiratory Pressure - позитивний тиск у кінці видиху (ПТКВ) |
| PO | Per Oral (by mouth) - пероральний |
| POCUS | Point-of-Care Ultrasound - ультразвукову діагностику безпосередньо біля ліжка пацієнта |
| PPE | Personal Protective Equipment - засоби індивідуального захисту (ЗІЗ) |
| RAAS | Renin-Angiotensin-Aldosterone System - Ренін-ангіотензинова система |
| RASS | Richmond Agitation-Sedation Scale - шкала збудження-седації Річмонда |
| RHF | Receiving Healthcare Facility - приймаючий ЗОЗ |
| RRT | Renal Replacement Therapy - замісна ниркова терапія |
| SBAR | Situation, Background, Assessment, Recommendation - Ситуація, Передумови, Оцінка, Рекомендації |
| SHF | Sending Healthcare Facility - направляючий ЗОЗ |
| SpO₂ | Peripheral Oxygen Saturation - сатурація кисню в крові |
| SV | Stroke Volume - ударний об'єм (УО) |
| SVR | Systemic Vascular Resistance - системний судинний опір |
| TBI | Traumatic Brain Injury - черепно-мозкова травма (ЧМТ) |
| VCV | Volume Controlled Ventilation - вентиляція з керованим об'ємом |
| Vₜ | Tidal Volume - дихальний об'єм (ДО) |
РОЗДІЛ 1. ПИТАННЯ, ЩО ПІДЛЯГАЮТЬ УРАХУВАННЮ ПЕРЕД ТРАНСПОРТУВАННЯМ
ВСТУП
Транспортування пацієнтів у критичному стані між медичними закладами є складним і надзвичайно відповідальним процесом, який вимагає ретельного планування, чіткої комунікації та стандартизованих протоколів. Настанова «Процес транспортування» покликана забезпечити чітку й комплексну структуру дій для безпечного та ефективного перевезення пацієнтів, які потребують інтенсивної терапії — від первинної оцінки та ухвалення рішення про транспортування до аналізу результатів після його завершення. Цей документ розроблено для підтримки медичних працівників, координаційних центрів і бригад CCT у розумінні та впровадженні найкращих практик транспортування пацієнтів у критичному стані з метою покращення результатів лікування пацієнтів та забезпечення безперервності медичної допомоги.
Настанова починається з визначення ключових ролей і обов’язків, деталізуючи взаємодію між медичними закладами, що направляють і приймають пацієнтів, центрами координації та бригадами CCT. У ній надаються докладні рекомендації щодо первинної оцінки стану пацієнта, критеріїв для прийняття рішення про транспортування та способів ініціювання запиту на транспортування, із застосуванням стандартизованих процедур, які забезпечують точну передачу важливої інформації. Центральним елементом цієї настанови є роль центру координації, який управляє всім процесом транспортування — комунікуючи з обома закладами (що направляє та приймає пацієнта), знаходячи ресурси для лікування та забезпечуючи повну поінформованість і підготовленість бригади транспортування.
«Процедура транспортування» підкреслює критичну необхідність безперервного обміну інформацією на всіх етапах — від підготовки закладу, що направляє пацієнта, та бригади транспортування до підтвердження наявності місць у медичному закладі, який приймає пацієнта. У документі викладено протоколи активаціі бригади CCT, зосереджено увагу на готовності бригади, обладнанні, стандартах безпеки та планах транспортування. У ньому також описано весь процес транспортування пацієнта — від початкової передачі до догляду під час транспортування і формального приймаючий ЗОЗ. Кожен етап підтримується стандартними операційними процедурами та контрольними списками, щоб жодна деталь не була упущена.
Щоб сприяти постійному вдосконаленню, настанова включає потужні заходи забезпечення якості та заохочує впровадження КПЕ для моніторингу результативності й безпеки процесу транспортування. Запропоновано стратегії проведення дебрифінгу після транспортування та аналізу якості з метою формування культури навчання й вдосконалення. Крім того, надано детальні протоколи з підготовки до надзвичайних ситуацій і планування дій на випадок непередбачуваних обставин для пом’якшення можливих викликів під час транспортування.
Настанова наголошує на важливості міждисциплінарної співпраці, навчання та стандартів компетентності, щоб гарантувати належну підготовку всього персоналу, задіяного в процесі транспортування. Інтеграція концепції «Справедлива культура» та принципів управління командними ресурсами (Crew Resource Management, CRM) підсилює орієнтованість настанови на відкриту комунікацію, ефективну командну взаємодію та відсутність карального підходу до помилок, що, у свою чергу, сприяє підвищенню безпеки й якості медичної допомоги під час транспортування пацієнтів у критичних станах.
Цей комплексний документ слугує ресурсом для медичних систем, допомагаючи стандартизувати протоколи транспортування, покращити комунікацію між усіма сторонами та забезпечити своєчасне й належне надання допомоги під час міжлікарняних перевезень. Його доповнюють додатки з практичними інструментами — шаблонами, чек-листами та чіткими визначеннями — для полегшення впровадження. «Процес транспортування» пропонує шлях до постійного покращення якості, гарантуючи, що транспортування пацієнтів у критичному стані відбувається з найвищим рівнем безпеки, ефективності та орієнтованості на пацієнта.
ЧАСТИНА 1: ПРОЄКТУВАННЯ СИСТЕМИ ССТ ТА ІНФРАСТРУКТУРА
Ролі та обов’язки
Процедура транспортування залучає різні організаційні структури та процеси. Для створення безпечної, ефективної та стійкої системи транспортування необхідно чітко окреслити ролі, обов’язки та взаємодію між зацікавленими сторонами. У межах системи CCT кілька сторін мають чітко визначені ролі та обов’язки, що є критично важливими для забезпечення ефективної та скоординованої допомоги під час транспортування пацієнтів у критичному стані або з травмами.
НАПРАВЛЯЮЧИЙ ЗОЗ (SHF)
Направляючий ЗОЗ, є відправною точкою будь-якого транспортування пацієнтів у критичному стані та несе ключову відповідальність за те, щоб такого пацієнта було безпечно та ефективно переведено на відповідний рівень медичної допомоги. Ця роль охоплює низку узгоджених дій, які мають бути виконані точно та швидко з метою оптимізації результатів лікування пацієнта при дотриманні високих стандартів медичної допомоги протягом усього процесу транспортування. Розглянемо детальніше основні аспекти ролей і обов’язків направляючого ЗОЗ, а також системні рекомендації, необхідні для ефективного забезпечення цих дій.
| КЛЮЧОВІ РЕКОМЕНДАЦІЇ: SHF |
| 1 | Впровадити стандартизовані протоколи оцінювання. |
| 2 | Проводити підготовку клінічного персоналу з питань прийняття обґрунтованих рішень |
| 3 | Застосовувати інструменти підтримки прийняття клінічних рішень для оцінювання показань до транспортування пацієнтів. |
| 4 | Розробити «контрольні списки перед транспортуванням» для стабілізації пацієнта. |
| 5 | Забезпечити наявність необхідного обладнання та медикаментів. |
| 6 | Встановити протоколи комунікації для запитів на транспортування. |
| 7 | Використовувати стандартизовану документацію з транспортування. |
| 8 | Призначити окремого координатора транспортування. |
| 9 | Використовувати стандартизовані шаблони документації. |
| 10 | Підтримувати контрольний список інформації для передачі ССТ. |
| 11 | Впровадити структуровані протоколи передачі (наприклад, SBAR). |
| 12 | Забезпечити контрольовані зони для безпечної передачі. |
| 13 | Створити канали комунікації для постійного оновлення інформації. |
| 14 | Підтвердити наявність місць та ресурсів у приймаючому ЗОЗ. |
| 15 | Поділитися повним планом лікування з приймаючим ЗОЗ. |
| 16 | Створити «протоколи організації транспортування» з деталізацією маршруту та виду транспорту. |
| 17 | Розробити план дій на випадок непередбачуваних ситуацій. |
Оцінка стану пацієнта та рішення про транспортування
Першим і найважливішим обов’язком направляючого ЗОЗ, є ретельна оцінка стану пацієнта. Комплексна оцінка необхідна для визначення, чи виходять потреби пацієнта у лікуванні за межі можливостей наявного закладу охорони здоров’я. Якщо так, це слугуватиме підставою для його транспортування до закладу вищого рівня. Цей процес потребує використання стандартизованих інструментів оцінювання, що гарантують уніфікованість та належну ретельність оцінки у різних медичних працівників і за різних клінічних обставин.
Медичний персонал повинен бути добре підготовленим до розпізнавання випадків, коли пацієнту потрібна спеціалізована або високоспеціалізована допомога, враховуючи такі фактори, як важкість захворювання (поранення, травми), необхідні втручання та прогноз. Інструменти підтримки прийняття рішень можуть бути надзвичайно цінними для того, щоб допомогти клініцистам ухвалювати об’єктивні рішення на основі конкретних критеріїв і клінічних показників, забезпечуючи врахування всіх аспектів стану пацієнта в процесі ухвалення рішень.
Стабілізація та підготовка пацієнта до транспортування
Стабілізація пацієнта є критично важливим обов’язком до початку будь-якого транспортування. Метою направляючого ЗОЗ є забезпечити максимально стабільний стан пацієнта для мінімізації ризиків під час транспортування. Цей процес включає забезпечення прохідності дихальних шляхів, надання необхідних медикаментів та забезпечення заходів підтримки життєдіяльності. З метою надання безпечного транспортування, необхідно ретельно підготувати пацієнта, враховуючи оцінку потреб у медичному обладнанні, встановлення внутрішньовенних ліній та, за потреби, забезпечення підтримки дихальної функції. На цьому етапі стандартизований «чек лист перед транспортуванням» має ключове значення, оскільки допомагає переконатися, що всі аспекти стабілізації враховано, та запобігти будь-яким пропущеним деталям, які можуть вплинути на безпеку пацієнта. Направляючий ЗОЗ також повинен мати оперативний доступ до необхідних медичних матеріалів, лікарських засобів і спеціалізованого обладнання, щоб забезпечити стабілізацію пацієнта в максимально можливому обсязі перед транспортуванням.
Комунікація з центром координації
Комунікація з центром координації Ефективна комунікація між направляючим ЗОЗ і центром координації є основою успішного транспортування. Після ухвалення рішення про транспортування направляючий ЗОЗ має подати офіційний запит на транспортування, надаючи чітку та вичерпну інформацію про медичну історію пацієнта, його поточний стан і потреби в лікуванні.
Щоб цей процес був ефективним і без помилок, направляючий ЗОЗ повинен мати структуровані комунікаційні протоколи та стандартизовану документацію для запитів на транспортування. Електронні форми для транспортування, якщо можливо, забезпечують покриття всіх необхідних деталей та швидку й точну передачу інформації. Крім того, призначений координатор транспортування або контактна особа в направляючому ЗОЗ можуть оптимізувати цей процес, щоб запобігти затримкам або перервам у комунікації.
Обмін інформацією та документація
Належне ведення медичної документації є обов’язковою умовою безпечного транспортування пацієнтів. Направляючий ЗОЗ несе відповідальність за збирання та передачу всієї відповідної інформації про пацієнта до центру координації, бригади транспортування та приймаючого ЗОЗ. Цей обмін включає детальні медичні записи, анамнез, призначені медикаменти, проведені втручання та будь-які спеціальні інструкції з догляду. Якість цієї інформації має критичне значення, оскільки вона дозволяє персоналу приймаючого ЗОЗ підготуватися до прибуття пацієнта, а бригаді транспортування — мати всю необхідну інформацію для ведення пацієнта під час транспортування.
Стандартизовані шаблони та форми для транспортування гарантують, що нічого не буде упущено, тоді як електронні медичні записи (EMR) можуть пришвидшити обмін інформацією. Чітка передача інформації зменшує кількість непорозумінь і запобігає можливим затримкам чи ускладненням під час транспортування.
Передача пацієнта бригаді CCT
Структурований і детальний процес передачі має вирішальне значення для безпеки та безперервності надання медичної допомоги під час транспортування. Направляючий ЗОЗ повинен ефективно передати нагляд за пацієнтом бригаді CCT, яка супроводжуватиме пацієнта під час транспортування. Передача містить актуальну інформацію про стан пацієнта, його життєві показники та останні зміни у плані надання медичної допомоги.
Формалізований протокол передачі, наприклад SBAR має бути впроваджений, щоб гарантувати чітку та послідовну передачу всієї необхідної інформації. Крім того, у відправляючому закладі слід створити спеціально відведену зону для передачі, яка дозволить бригаді CCT переконатися, що вони отримали всю необхідну інформацію, обладнання та медикаменти.
Координація з приймаючим ЗОЗ
Протягом усього процесу транспортування направляючий ЗОЗ, має працювати у співпраці з центром координації, щоб приймаючий ЗОЗ був поінформованим і підготовленим до прибуття пацієнта. Це включає підтвердження того, щоб приймаючий ЗОЗ мав можливість прийняти пацієнта і забезпечити належний догляд та персонал на момент прибуття пацієнта.
Безперервна комунікація між направляючим ЗОЗ, центром координації та приймаючим ЗОЗ є необхідною для обміну інформацією в режимі реального часу, очікуваним часом прибуття та будь-якими критичними змінами в стані пацієнта. Своєчасна та ефективна комунікація забезпечує безперервність передачі пацієнта після його прибуття до закладу охорони здоров’я (RHF) та дає змогу бригаді завчасно підготуватися до проведення необхідних медичних втручань.
Підготовка логістичного забезпечення транспортування
Логістика транспортування вимагає ретельного планування. (SHF) Направляючий ЗОЗ у співпраці з центром координації і бригадою CCT повинні точно визначити спосіб транспортування (наземне або повітряне), час транспортування та будь-які особливі потреби в обладнанні чи персоналі. Усі деталі, зокрема планування маршруту, готовність транспорту та заходи безпеки, мають бути ретельно сплановані, щоб забезпечити безпечне та своєчасне транспортування.
Слід розробити протоколи логістики транспортування, які деталізують кожен етап процесу, включаючи надзвичайні ситуації та плани дій на випадок непередбачених обставин, таких як зміни в стані пацієнта, затримки транспорту або відмова обладнання.
Впровадження цих рекомендацій дає змогу забезпечити виконання кожного етапу транспортування на високому рівні, дбаючи про ефективність, безпеку та якість, що в підсумку підвищує шанси на успішний результат для критично хворих пацієнтів, які потребують спеціалізованої допомоги
ПРИЙМАЮЧИЙ ЗОЗ (RHF)
Приймаючий ЗОЗ відіграє важливу роль у забезпеченні ефективного переведення та безперервності надання допомоги тяжкохворим пацієнтам. Після того як направляючий ЗОЗ ухвалює рішення про переведення пацієнта, приймаючий ЗОЗ має оперативно підготуватись і скоординувати дії для надання необхідного рівня спеціалізованої допомоги після прибуття пацієнта. Нижче наведено розподіл ключових ролей і обов’язків приймаючого ЗОЗ, а також рекомендації щодо системного підходу для забезпечення безперебійного та ефективного процесу переведення.
| КЛЮЧОВІ РЕКОМЕНДАЦІЇ: RHF |
| 18 | Розробити систему відстеження ліжко-місць у режимі реального часу. |
| 19 | Виділити зону тріажу або відділення ЕМД для переведених пацієнтів. |
| 20 | Встановити чіткі протоколи комунікації. |
| 21 | Призначити відповідальну особу, яка координуватиме всю комунікацію щодо переведення. |
| 22 | Використовувати захищені та зашифровані системи зв'язку для обміну даними пацієнтів. |
| 23 | Використовувати стандартизовану структуру передачі (наприклад, ISBAR). |
| 24 | Забезпечити надання медичної допомоги одразу після прибуття пацієнта. |
| 25 | Створити спеціально визначену зону для передачі з належним моніторинговим обладнанням. |
| 26 | Запровадити «протокол прибуття» для швидкої оцінки та втручання. |
| 27 | Забезпечити наявність фахівців для надання невідкладної медичної допомоги. |
| 28 | Надати ресурси для безперервного моніторингу та підтримки. |
| 29 | Стандартизувати шаблони документації для швидкого й точного внесення інформації. |
| 30 | Створити процес дебрифінгу після прибуття пацієнта. |
| 31 | Встановити протоколи забезпечення якості для відстеження результатів і проблем у процесі. |
| 32 | Використовувати зворотний зв’язок для вдосконалення процесу транспортування та навчання. |
Підготовка до прибуття пацієнта та його прийому
Як тільки запит на переведення підтверджено, приймаючий ЗОЗ має переконатися, що зроблено всі необхідні приготування для прийому пацієнта. Це означає підтвердження наявності відповідного ліжка, готовність спеціального обладнання або медикаментів, необхідних для пацієнта, а також підготовку умов, у яких пацієнта можна буде ефективно прийняти. Мета — мінімізувати будь-які затримки після прибуття пацієнта та забезпечити негайне й належне лікування.
Для цього критично важливо мати систему відстеження місць у режимі реального часу, яка дозволить швидко виявляти та підтверджувати наявність вільних місць. Приймаючий ЗОЗ також має визначити спеціальну зону, куди можуть надходити пацієнти після транспортування для тріажу та прийому, з наявним персоналом і обладнанням, готовими до роботи в критичній ситуації.
Здійснення комунікації та отримання підтвердження від центру координації та направляючого ЗОЗ
Одним із ключових завдань приймаючого ЗОЗ є підтримання відкритих і чітких каналів комунікації з центром координації і направляючого ЗОЗ. Це забезпечує надходження актуальної інформації щодо стану пацієнта, статусу транспортування та будь-яких змін, які можуть виникнути в процесі транспортування. Комунікація має бути чіткою та оперативною, щоб приймаючий заклад міг ефективно підготуватися до прибуття пацієнта.
Запровадження стандартизованих протоколів комунікації важко переоцінити. RHF має визначити відповідальну особу, яка здійснюватиме управління комунікацією на всіх етапах транспортування, щоб забезпечити безперебійний обмін інформацією між усіма сторонами. Крім того, використання захищених електронних медичних записів або інших зашифрованих інструментів зв’язку гарантує, що конфіденційна інформація про пацієнта передається безпечно й ефективно.
Активація персоналу RHF
Після підтвердження транспортування RHF має активувати мультидисциплінарну бригаду здатну прийняти пацієнта після прибуття. До цієї бригади зазвичай входять лікарі та середній медперсонал, готові надати необхідні втручання після прибуття пацієнта. Кожен член бригади має чітко розуміти свою роль — чи то первинний тріаж, стабілізація, чи надання спеціалізованої допомоги відповідно до потреб пацієнта.
Запровадження протоколів за функціями допомагає гарантувати, що кожен учасник бригади знає свої обов’язки — від прийому пацієнта до надання розширеної допомоги при загрозливих станах, якщо це потрібно. Для підтримки готовності персонал має регулярно проходити навчання щодо протоколів транспортування - це дозволить їм ефективно реагувати на будь-які критичні ситуації, пов’язані з транспортуванням.
Процедура передачі пацієнта від бригади CCT
Процес передачі між бригадою CCT і RHF є критичним моментом, який потребує чіткого та структурованого підходу, щоб ніяка інформація не була втрачена під час передачі пацієнта. Як тільки пацієнт прибуває, бригада CCT повинна передати всю відповідну медичну інформацію, включно з поточним станом пацієнта, маніпуляціями, проведеними під час транспортування, та будь-якими іншими важливими клінічними даними.
Щоб досягти цього, рекомендується використовувати стандартизовану структуру передачі інформації, таку як ISBAR). Така структурована комунікація забезпечує передачу всієї важливої інформації без будь- яких втрат. Спеціально відведене місце для передачі пацієнта, обладнане необхідною моніторинговою апаратурою, сприяє безпечній та організованій передачі, дозволяючи бригаді RHF негайно розпочати надання необхідної допомоги.
Забезпечення безперервного надання допомоги та стабілізація стану пацієнта
RHF має бути готовим вчасно надати спеціалізовану допомогу для стабілізації стану пацієнта відразу після його прибуття. Бригада RHF повинна оперативно оцінити стан пацієнта й застосувати відповідні втручання, щоб забезпечити його стабільність. З огляду на терміновість і складність таких ситуацій, RHF повинен мати чіткий «протокол прибуття», який допомагає здійснювати швидку оцінку, прийняття рішень і лікування.
Для ефективного та безперервного надання допомоги, RHF має мати у своєму розпорядженні спеціалістів, доступних постійно або на виклик, які здатні провести критично необхідні втручання. Присутність відповідних ресурсів для постійного моніторингу та підтримки в перші години після транспортування є надзвичайно важливою для стабілізації стану пацієнта та швидкого реагування на ускладнення, що можуть виникнути.
Документація та управління інформацією
Коректне оформлення документації є наріжним каменем процесу переведення, і RHF несе відповідальність за належну фіксацію всієї інформації, отриманої від бригади CCT. Це включає документування поточного стану пацієнта, процедур, проведених під час транспортування, а також будь-якої додаткової допомоги, наданої після прибуття. Належна документація не лише підтримує прийняття клінічних рішень, а й забезпечує чіткий запис усіх етапів транспортування пацієнта.
Рекомендується використовувати електронні медичні історії пацієнтів (EHRs) для оптимізації цього процесу, адже це дозволяє швидко та точно вносити дані. Стандартизовані шаблони для фіксації інформації про переведення пацієнта допомагають уніфіковано відобразити всі важливі деталі та забезпечують чіткість дій усіх членів команди, залучених до надання допомоги.
Зворотний зв’язок з центром координації та підвищення якості
Після завершення транспортування RHF відіграє важливу роль у наданні зворотного зв’язку центру координації щодо процесу транспортування. Це передбачає оцінку ефективності транспортування, клінічних результатів для пацієнта та труднощів, що виникли під час процесу транспортування чи передачі пацієнта. Такий зворотний зв’язок є ключовим для безперервного вдосконалення системи, дозволяючи своєчасно усувати недоліки та коригувати протоколи для наступних трансферів.
Регулярний дебрифінг повинен проводитися після кожного транспортування для аналізу того, що пройшло добре, і виявлення сфер, які потребують покращення. Протоколи забезпечення якості, наприклад, відстеження результатів пацієнтів і ефективності процесу, допомагають виявити сфери, де потрібно покращити навчання, ресурси або системи. Мета — створити середовище постійного навчання та вдосконалення, що дозволить RHF адаптуватися до нових викликів і забезпечувати найвищий рівень допомоги пацієнтам у критичному стані.
БРИГАДА ТРАНСПОРТУВАННЯ ПАЦІЄНТІВ У КРИТИЧНОМУ СТАНІ (CCTT)
Бригада CCT відіграє ключову роль у безпечному та ефективному транспортування і пацієнтів у критичному стані або постраждалих пацієнтів між медичними закладами. Основна мета бригади — забезпечення безперервного, високоякісного догляду під час транспортування, підтримання стабільного стану пацієнта та реагування на будь-які невідкладні стани. Для цього бригада CCT має бути добре підготовленою, висококваліфікованою та здатною оперативно реагувати на різноманітні сценарії. Нижче наведено детальний огляд ключових обов’язків бригади CCT і рекомендованих механізмів для покращення процесу переведення.
| КЛЮЧОВІ РЕКОМЕНДАЦІЇ: БРИГАДА ССТ |
| 33 | Визначити склад бригади відповідно до потреб пацієнта. |
| 34 | Забезпечити регулярне навчання з клінічних навичок і протоколів надання екстреної допомоги. |
| 35 | Використовувати стандартизований чек-лист перед транспортуванням для обладнання, медикаментів і логістики. |
| 36 | Перевіряти плани переведення та резервні варіанти разом з бригадою. |
| 37 | Підтримувати зв’язок із SHF та RHF для отримання оновлень. |
| 38 | Використовувати чек-листи обладнання відповідно до потреб пацієнта. |
| 39 | Переконатися, що все обладнання справне та придатне до транспортування. |
| 40 | Розробити клінічні протоколи для надання екстреної допомоги. |
| 41 | Підтримувати комунікацію в бригаді для швидкого реагування. |
| 42 | Використовувати структуровані протоколи передачі (наприклад, ISBAR). |
| 43 | Проводити передачу пацієнта в контрольованому середовищі. |
| 44 | Призначити відповідального за комунікацію для забезпечення чіткості та узгодженості інформації для забезпечення чіткості. |
| 45 | Забезпечити безпеку пацієнта та обладнання під час транспортування. |
| 46 | Дотримуватися процедур щодо ЗІЗ (засобів індивідуального захисту) та інфекційного контролю. |
| 47 | Розробити плани дій у разі відмови обладнання або погіршення стану пацієнта. |
| 48 | Надавати регулярне оновлення інформації для RHF під час переведення. |
| 49 | Підготувати стислий звіт для передачі інформації. |
| 50 | Забезпечити безперервне функціонування обладнання для моніторингу та підтримки життєвих функцій пацієнта |
| 51 | Проводити дебрифінги після кожного транспортування. |
| 52 | Документувати відгуки та проблеми для покращення якості. |
| 53 | Використовувати зібрану інформацію для вдосконалення протоколів і навчання. |
Склад бригади та готовність
Успішне транспортування починається з правильного складу бригади. Бригада CCT є спеціалізованою міждисциплінарною групою, яка зазвичай складається з лікаря, що має досвід інтенсивної терапії (наприклад, анестезіолога - інтенсивіста або лікаря з МНС, парамедика, та іншого персоналу, залучення якого зумовлене станом пацієнта. Враховуючи різноманітність потреб пацієнтів, склад бригади має бути досить гнучким, щоб включати спеціалістів залежно від тяжкості та характеру стану пацієнта.
Щоб забезпечити це, бригада CCT повинна мати чітко визначені протоколи, які регулюють склад бригади для різних типів транспортуванняів. Безперервне навчання має вирішальне значення, щоб гарантувати, що кожен член бригади володіє необхідними навичками як для планових, так і для екстрених випадків під час транспортування. Крім того, підтримка добре організованого реєстру персоналу дозволяє швидко сформувати бригаду та забезпечувати її готовність у разі потреби у транспортуванні.
Підготовка та планування до транспортування
Перш ніж бригада CCT розпочне транспортування, необхідна ретельна підготовка. Це передбачає перегляд медичної документації пацієнта, оцінку його клінічного стану та прогнозування можливих ускладнень під час транспортування. Базові етапи включають детальне планування маршруту, вибір виду транспорту (наземна чи повітряна швидка допомога) та підготовку необхідного обладнання й медикаментів, упакованих і готових до використання.
Уніфікований чек-лист для підготовки до транспортування може полегшити цю підготовку, адже він враховує усі аспекти потреб пацієнта, справність обладнання та логістичні заходи. Бригада CCT також повинна тісно співпрацювати як із SHF, так і з RHF для збору всієї необхідної інформації, гарантуючи, що бригада повністю поінформована про стан пацієнта та будь-які спеціальні вимоги.
Підготовка обладнання та медикаментів
Критично важливою відповідальністю бригади CCT є забезпечення того, щоб усе обладнання та медикаменти, необхідні для транспортування, були підготовлені та справні. З огляду на високий ризик таких перевезень, усі пристрої мають бути портативними, надійними й здатними підтримувати життєві функції пацієнта навіть за складних умов, таких як обмежений простір або турбулентність під час авіаперевезень.
Стандартизовані чек-листи обладнання є незамінними адже такі дозволяють впевнитися, що монітори, апарати штучної вентиляції легень, джерела кисню, інфузійні насоси та медикаменти для надання невідкладної медичної допомоги медикаменти готові до використання. Перевірка обладнання має проводитись проводитися до відправлення — з підтвердженням, що всі пристрої справні, батареї заряджені, а резервні засоби наявні при потребі. Під час кожного трансферу має бути доступний набір медикаментів, що включає засоби для седації, знеболення, підтримки серцево-судинної системи та надання невідкладної медичної допомоги.
Моніторинг і медична допомога під час транспортування
Під час транспортування бригада CCT зобов’язана забезпечувати безперервний моніторинг і оцінку стану пацієнта. Бригада повинна контролювати життєво важливі показники, гемодинамічну стабільність, вентиляцію та інші клінічно важливі параметри, що відображають стан здоров’я пацієнта. Під час транспортування бригада CCT зобов’язана забезпечувати безперервний моніторинг пацієнта та бути готовою до своєчасного втручання для стабілізації його клінічного стану у разі погіршення або виникнення непередбачених подій.
Портативні системи моніторингу є критично важливими, оскільки забезпечують безперервне отримання ключових показників клінічного стану пацієнта. Бригада CCT повинна діяти за чітко визначеними клінічними протоколами для реагування на невідкладні стани, зокрема порушення прохідності дихальних шляхів та функції дихання, критичні порушення ритму чи гемодинамічну нестабільність, а також підтримувати ефективну комунікацію між членами команди для оперативного ухвалення рішень і своєчасного втручання протягом усього транспортування.
Комунікація та передача інформації в закладах, що направляють і приймають
Чітка комунікація — основа успішного транспортування. Бригада ССТ повинна здійснити детальну передачу інформації від SHF, до RHF після завершення транспортування. Ця передача має охоплювати всі важливі аспекти стану пацієнта: надане лікування до та під час транспортування, зміни в клінічному статусі та будь-які потреби в інтенсивній терапії.
Структуровані схеми передачі інформації, такі як ISBAR, допомагають забезпечити чітку та стислу передачу всієї необхідної інформації. Процес має відбуватися у контрольованому середовищі, що забезпечує належну комунікацію та безперервну, узгоджену передачу клінічної відповідальності й опіки над пацієнтом. Призначення у складі бригади CCT відповідального за комунікацію сприяє чіткості та послідовності під час передачі.
Безпека пацієнта та управління ризиками під час транспортування
Безпека пацієнта є найвищим пріоритетом для бригади ССТ і вимагає уважного ставлення як до клінічних, так і до логістичних ризиків. Необхідно надійно зафіксувати пацієнта та обладнання під час транспортування, запобігти зміщенню або падінню, а також забезпечити фізичну безпеку членів бригади. Крім того, бригада ССТ повинна дотримуватися суворих протоколів інфекційного контролю, використовуючи ЗІЗ, щоб захистити як пацієнта, так і медичну бригаду.
Бригада ССТ також повинна бути готова до непередбачуваних ситуацій, таких як несправності обладнання, зміни маршруту або раптове погіршення клінічного стану пацієнта. Для таких сценаріїв мають бути розроблені додаткові СОП, що забезпечить готовність бригади до реагування на будь-яку ситуацію без шкоди для безпеки пацієнта.
Координація з RHF з метою своєчасного та безперервного транспортування пацієнта
Однією з ключових функцій бригади ССТ є ефективна координація з RHF, щоб забезпечити готовність бригади RHF до надання допомоги одразу після прибуття пацієнта. Ця координація включає регулярне оновлення інформації про стан пацієнта під час транспортування, орієнтовний час прибуття та проведені втручання.
Для забезпечення безперервної передачі бригада CCT повинна підготувати стислий клінічний звіт про транспортування та поточний стан пацієнта, забезпечивши узгоджену передачу клінічної відповідальності персоналу RHF. Обладнання для моніторингу та підтримки життєвих функцій, використане під час транспортування, має бути оперативно підключене до систем RHF для безперервного спостереження та надання допомоги.
Аналіз після транспортування та заходи з покращення якості
Після завершення транспортування бригада ССТ має взяти участь у дебрифінгу для оцінки процесу, виявлення того, що пройшло успішно, та усунення виявлених проблем. Такий огляд дозволяє навчатися з кожного досвіду й підвищувати якість наступних транспортувань.
Структуроване обговорення за участю всіх членів бригади ССТ, а за можливості — представників SHF та RHF, може допомогти виявити шляхи покращення. Документування всіх відгуків і результатів дозволяє бригаді ССТ вдосконалювати свої протоколи, покращувати програми підготовки йсприяти безперервному вдосконаленню якості транспортувань пацієнтів у критичному стані.
Центр координації (СС)
Центр координації є оперативним ядром процесу транспортування пацієнтів у критичному стані. Він виконує роль диригента, який координує складний процес переміщення пацієнта з одного медичного закладу до іншого. Цей центральний вузол відповідає за безперервне управління всіма етапами транспортування — від оцінки потреб до визначення необхідних ресурсів і координації дій бригади ССТ на кожному етапі маршруту. Характер роботи центру координації змінюється залежно від того, чи здійснюється транспортування в межах одного регіону, між регіонами або за межі країни. Кожен тип транспортування має свої виклики, і центр координації має бути готовим ефективно їх долати.
| КЛЮЧОВІ РЕКОМЕНДАЦІЇ: ЦЕНТР КООРДИНАЦІЇ І ЙОГО ОСНОВНІ ФУНКЦІЇ |
| 54 | Створити систему підтримки прийняття рішень для оцінки терміновості, клінічних потреб і логістики транспортування. |
| 55 | Призначити спеціалізовані бригади для внутрішньо регіональних і міжрегіональних транспортувань. |
| 56 | Впровадити критерії пріоритетності на основі клінічної терміновості, відстані та наявності ресурсів. |
| 57 | Використовувати централізовану платформу зв'язку для оновлень у реальному часі та координації. |
| 58 | Призначити офіцера зв'язку для контролю всіх оновлень і координації взаємодії між SHF, RHF та бригадою ССТ. |
| 59 | Створити спеціальні протоколи комунікації для внутрішньо регіональних і міжрегіональних перевезень. |
| 60 | Розробити та підтримувати базу даних у реальному часі щодо місць в ВІТ, спеціалізованих відділень і доступних ресурсів у закладах. |
| 61 | Установити угоди про швидке реагування між SHf та RHF, для оптимального розподілу місць. |
| 62 | Уніфікувати протоколи підтвердження наявності місць, забезпечивши готовність RHF, перед передачею пацієнта.. |
| 63 | Запровадити структурований брифінг перед транспортуванням для бригади ССТ, що охоплює всі клінічні та логістичні аспекти. |
| 64 | Забезпечити, щоб вибір способу транспортування враховував терміновість, стабільність пацієнта та відстань. |
| 65 | Розробити плани дій на випадок надзвичайних ситуацій під час транспортування та довести їх до відома бригади ССТ. |
| 66 | Використовувати засоби моніторингу в реальному часі для відстеження місцеперебування та стану бригади ССТ і пацієнта. |
| 67 | Налагодити регулярний зв’язок між центром координації і бригадою ССТ під час транспортування. |
| 68 | Впровадити протоколи ескалації для надзвичайних ситуацій, забезпечивши оперативну підтримку для бригади ССТ. |
| 69 | Проводити структуровані сесії обговорення з усіма сторонами після кожного транспортування для отримання зворотного зв’язку. |
| 70 | Відстежувати ключові показники ефективності, такі як час транспортування, клінічні результати та ефективність комунікації. |
| 71 | Використовувати дані після транспортувального аналізу для оновлення програм навчання, протоколів і покращення майбутніх перевезень. |
Обробка запитів на транспортування та ухвалення рішень
Подорож починається з моменту надходження запиту на транспортування. Центр координації є першим пунктом контакту, який отримує виклик від SHF, щодо критично хворого пацієнта, якого необхідно перевезти до закладу, краще обладнаного для надання медичної допомоги. У такі моменти важливими є швидке та чітке ухвалення рішень. бригада центру координації повинна негайно оцінити терміновість ситуації, медичні потреби пацієнта та ресурси, необхідні для здійснення транспортування.
У випадку внутрішньорегіональних перевезень процес зазвичай проходить швидко. Центр координації, який має повну картину місцевих ресурсів лікарень і варіантів транспортування, може оперативно визначити відповідний RHF. Такі транспортування зазвичай відбуваються на короткі відстані, тому основна увага приділяється швидкій мобілізації — визначенню вільного ліжка, направленню бригади ССТ та якнайшвидшому транспортування і пацієнта.
Однак у разі міжрегіональних перевезень складність зростає. Більші відстані, можливі регіональні передавання відповідальності та потреба у спеціалізованому транспорті (наприклад, санітарна авіація) вимагають додаткової координації. Центр координації повинен враховувати такі чинники, як час у дорозі, рівень спеціалізованої допомоги, необхідної в RHF, а також можливості бригади транспортування забезпечувати безперервну допомогу під час потенційно тривалої подорожі. У цій ситуації роль центру координації подібна до ролі диспетчера й стратегічного планувальника, який гарантує ретельне планування кожного аспекту транспортування.
Налагодження комунікаційних циклів для ефективної координації
Основою роботи центру комунікації є комунікація. Надійні комунікаційні цикли є критично важливими для безперебійного обміну інформацією між SHF, RHF та бригадою ССТ. Уся інформація — від оновлень щодо стану пацієнта, змін у наявності місць до логістичних викликів у дорозі — має передаватися оперативно, щоб усі учасники процесу залишалися на одній хвилі.
Для внутрішньорегіональних перевезень комунікаційної петлі зазвичай є простішим. Оскільки ці транспортування відбуваються в межах меншої географічної зони, оновлення в реальному часі є критично важливими для оперативних і ефективних дій. Координаційний центр підтримує прямий зв’язок як із закладом охорони здоровʼя, який відправляє пацієнта (SHF), так і з закладом охорони здоровʼя, який отримує пацієнта, а також із бригадою ССТ після її виїзду. Така постійна двостороння комунікація дає Координаційному центру змогу швидко реагувати на зміни та забезпечувати готовність RHF прийняти пацієнта без затримок.
У випадку міжрегіональних перевезень складність комунікаційного циклу суттєво зростає. Такі транспортування можуть включати декілька координаційних центрів у різних регіонах, різні види транспортування та потребу в детальному плануванні. У цьому разі Координаційний центр відіграє роль ключового посередника, забезпечуючи безперервність і чіткість комунікації попри масштаб координації. Центр забезпечує регулярне інформування бригади ССТ, своєчасне повідомлення RHF про зміни у стані пацієнта, а також організовує всі логістичні процеси для безпечної та злагодженої передачі пацієнта від бригади ССТ до закладу охорони здоров’я.
Визначення доступних ресурсів і розподіл ліжкового фонду
Одним із критичних завдань для центру координації є пошук відповідного RHF, що має достатні потужності для надання необхідної медичної допомоги. Пошук необхідних ресурсів часто відбувається в умовах обмеженого часу, адже пацієнтам у критичному стані потрібен швидкий доступ до медичної допомоги належного рівня. Завдання центру — визначити заклад (RHF), який має вільне ліжко, відповідне обладнання та спроможність забезпечити потреби конкретного пацієнта.
Для внутрішньорегіональних перевезень центр координації зазвичай добре орієнтується в локальній системі охорони здоров’я. Він може оперативно звернутися до місцевих лікарень, перевірити наявність місць у відділеннях інтенсивної терапії та визначити, який заклад найкраще підходить для прийому пацієнта. Це знання місцевих можливостей дозволяє центру координації прискорити пошук і забезпечити місце без значних затримок.
У випадку міжрегіональних перевезень цей процес стає складнішим. Центр координації має розширити зону пошуку за межі безпосереднього регіону, враховуючи лікарні, які можуть бути розташовані далі, але мають необхідні потужності та можливості для надання медичної допомоги. Центр також має зважати на потенційні переваги переміщення пацієнта на більшу відстань і ризики, пов’язані з тривалим транспортуванням. Цей процес вимагає не лише логістичної майстерності, а й клінічного розуміння, щоб забезпечити доставку пацієнта в належний заклад у потрібний час.
Мобілізація бригади ССТ
Після того як місце зарезервоване і транспортування підтверджене, наступним кроком є активація бригади ССТ. Ця бригада, що спеціалізується на транспортуванні пацієнтів у критичному стані, має бути проінформована про стан пацієнта, його потреби та можливі ускладнення під час транспортування. Центр координації відіграє ключову роль у забезпеченні належної підготовки бригади ССТ: надає всю необхідну інформацію, забезпечує її обладнанням і матеріалами, необхідними для транспортування.
Під час внутрішньорегіональних перевезень мобілізація зазвичай відбувається швидко. Бригаду ССТ направляють оперативно, оскільки відстані зазвичай короткі, і існує нагальна потреба швидко перевезти пацієнта. Центр координації має забезпечити, щоб бригада ССТ володіла найактуальнішою інформацією про стан пацієнта і була готова реагувати на будь-які зміни під час короткого транспортування.
У разі міжрегіональних перевезень роль центру координації стає ще ширшою. З огляду на більші відстані та можливі складніші маршрути, бригаді ССТ може знадобитися бути готовою до триваліших поїздок і мати наявні додаткові медичні засоби. Центр має координувати не лише бригаду ССТ, а й усіх регіональних партнерів, які можуть знадобитися для допомоги під час транспортування. Підготовка до непередбачених ситуацій є ключовою, оскільки несподівані події — такі як несправність обладнання, затримки в дорозі або зміни у стані пацієнта — можуть вимагати негайного коригування планів.
Моніторинг транспортування та підтримка під час транспортування
Протягом усього транспортування центр координації виступає як опора, забезпечуючи постійну підтримку та моніторинг. Він підтримує постійний зв’язок із бригадою ССТ, щоб відстежувати хід транспортування та стан пацієнта в режимі реального часу. Центр також підтримує зв’язок із закладом охорони здоровʼя, який отримує пацієнта (RHF), надаючи оновлення про розрахунковий час прибуття та будь-які події під час транспортування.
У разі внутрішньорегіонального транспортування ця функція моніторингу зазвичай є простою. Центр координації бригаду ССТ, вирішуючи будь-які логістичні труднощі, які можуть виникнути, і тримає RHF в курсі, щоб заклад був готовий прийняти пацієнта одразу після прибуття.
Однак у випадку міжрегіонального транспортування підтримка стає більш складною. Центр координації повинен активно вирішувати будь-які проблеми, які виникають під час тривалішого транспортування, надаючи інструкції бригаді ССТ та координуючи дії з RHF, щоб гарантувати готовність до будь-якої ситуації. Центр повинен мати плани дій у надзвичайних ситуаціях і бути здатним швидко реагувати на надзвичайні ситуації під час транспортування, і забезпечувати надання медичної допомоги пацієнтові, що є найвищим пріоритетом.
Аналіз після транспортування та забезпечення якості
Обов’язки центру координації не закінчуються після завершення транспортування. Після того як пацієнт прибув до RHF, центр проводить аналіз після транспортування, щоб оцінити, як пройшов процес, що можна було зробити краще і які уроки винесено. Ця рефлексивна фаза є важливою для постійного вдосконалення, дозволяючи центру координації уточнювати свої протоколи, стратегії комунікації та плани реагування на майбутні транспортування.
Центр взаємодіє з SHF, RHF та бригадою ССТ, щоб зібрати зворотний зв’язок, відстежити результати та виявити прогалини в процесі. Цей механізм зворотного зв’язку допомагає покращити загальну якість і безпеку наступних транспортуванняів, і забезпечує можливість для всіх сторін ефективніше реагувати в майбутньому.
ЧАСТИНА 2: ОЦІНКА ТА РІШЕННЯ ЩОДО ТРАНСПОРТУВАННЯ
Початкова оцінка та рішення щодо транспортування
Під час надання допомоги пацієнтам у критичному стані необхідність їх транспортування з одного закладу охорони здоров’я до іншого вимагає ретельного врахування кількох чинників, включно з клінічною терміновістю, потребою у спеціалізованій допомозі, наявністю ресурсів та логістичними обмеженнями. Рішення про транспортування пацієнта в критичному стані не слід приймати легковажно; воно має збалансувати ризики та переваги для досягнення найкращих результатів для пацієнта. Нижче наведено структурований опис того, коли варто розглядати транспортування, які є типи перевезень і як ефективно реалізувати рішення про транспортування.
| Основні рекомендації: центр координації (оцінка та прийняття рішення) |
| 72 | Провести негайну оцінку, щоб визначити, чи є стан пацієнта загрозливим для життя або швидко погіршується. |
| 73 | Визначити, чи може SHF забезпечити проведення розширених або спеціалізованих втручань. |
| 74 | Вчасно здійснити транспортування, якщо заклад охорони здоров'я, який відправляє пацієнта не може забезпечити необхідні, життєво важливі втручання. |
| 75 | Провести ретельну оцінку ресурсів закладу охорони здоров'я, який відправляє пацієнта, включаючи ліжка в реанімації, апарати ШВЛ та життєво необхідні лікарські засоби для стабілізації. |
| 76 | Забезпечити наявність кваліфікованого персоналу, такого як анестезіологи-реаніматологи, анестезисти та хірурги-травматологи, забезпечення необхідного обсягу медичної допомоги. |
| 77 | Оцінити, чи може SHF, і надалі забезпечувати безпечний догляд за пацієнтом, з урахуванням наявних місць, обладнання та можливих надзвичайних ситуацій. |
| 78 | Оцінити логістичні процеси транспортування, включаючи стабільність стану пацієнта та відстань до RHF, щоб визначити, який транспорт - наземний чи повітряний - є найбільш доречним. |
| 79 | Переконатися, що транспортні ресурси (транспортні засоби, персонал) готові до початку транспортування, щоб уникнути непотрібних затримок. |
| 80 | Класифікувати терміновість транспортування відповідно до клінічної потреби: негайне (загроза життю), термінове (чутливе до часу, протягом 1-2 годин), спеціалізоване (протягом 4 годин) або нетермінове (реабілітація, поетапна допомога). |
| 81 | Призначити відповідний вид транспортування на основі терміновості та стану пацієнта: наземний транспорт — для стабільних пацієнтів на короткі відстані; повітряний транспорт — для критичних випадків на далекі відстані. |
| 82 | Класифікувати терміновість транспортування відповідно до клінічної потреби: негайне (загроза життю), термінове (чутливе до часу, протягом 1–2 годин), спеціалізоване (протягом 4 годин) або нетермінове (реабілітація, поетапна допомога). |
| 83 | Призначити відповідний вид транспортування на основі терміновості та стану пацієнта: наземна швидка допомога — для стабільних пацієнтів на короткі відстані; повітряна швидка допомога — для критичних випадків на далекі відстані. |
| 84 | Перевірити здатність закладу охорони здоров'я, який отримує пацієнта, надавати спеціалізовані послуги, як-от нейрохірургія, високоспеціалізована кардіологічна допомога або інтенсивна неонатальна підтримка відповідно до стану пацієнта. |
| 85 | Підтвердити наявність місць у ВІТ або спеціалізованих підрозділів у RHF, перед початком транспортування. |
| 86 | Забезпечити координацію RHF, передати дані анамнезу, перебігу захворювання та проведених втручань потреби в лікуванні та очікуваний час прибуття. |
| 87 | Залучити бригаду ССТ і забезпечити участь підготовленого персоналу невідкладної допомоги, зокрема парамедиків, медичних сестер і лікарів, які мають навички надання екстреної медичної допомоги. |
| 88 | Підготувати необхідне медичне обладнання для транспортування, зокрема апарати ШВЛ, інфузійні насоси та лікарські засоби, визначені відповідно до клінічного стану пацієнта. |
| 89 | Встановити чітку комунікацію між SHF, бригадою ССТ і RHF, щоб забезпечити постійне оновлення інформації щодо стану пацієнта та логістики. |
| 90 | Забезпечити безперервний моніторинг стану пацієнта під час транспортування: контроль життєвих показників, рівня кисню та інших критичних параметрів протягом усього маршруту. |
| 91 | Підтримувати регулярну комунікацію між SHF, бригадою ССТ та RHF, щоб оновлювати інформацію про стан пацієнта під час транспортування та підготувати RHF до його прибуття. |
Коли варто розглядати транспортування: розпізнавання потреби
Першим кроком у процесі прийняття рішення є визначення потреби у транспортуванні пацієнта у критичному стані. Зазвичай рішення ґрунтується на трьох основних чинниках: клінічному стані пацієнта, можливостях SHF, і логістичних міркуваннях.
КЛІНІЧНІ ПІДСТАВИ ДЛЯ ТРАНСПОРТУВАННЯ
| Клінічні чинники для транспортування | Опис |
| 1 | Стан пацієнта загрожує життю або є нестабільним | Якщо стан пацієнта стрімко погіршується або існує безпосередня загроза життю, яку неможливо ефективно усунути в SHF, необхідне транспортування. Прикладами є дихальна недостатність, що потребує проведення розширеної штучної вентиляції легень, тяжка травма або зупинка серця за відсутності можливості проведення розширених кардіальних втручань. |
| 2 | Наростання потреби у наданні медичної допомоги | Коли стан пацієнта погіршується або виникають нові ускладнення, які потребують вищого рівня медичної допомоги, ніж той, що може надати SHF, може виникнути необхідність у переведенні до спеціалізованого закладу. Наприклад, стабільний пацієнт на апараті штучної вентиляції легень, якому потрібен інтенсивний респіраторний моніторинг, або пацієнт, стан якого погіршується до потреби в мультиорганній підтримці, може потребувати переведення до відділення інтенсивної терапії з вищим рівнем надання допомоги. |
| 3 | Необхідність у спеціалізованих послугах | Пацієнту може знадобитися доступ до спеціалізованих медичних послуг, які SHF не може надати, таких як нейрохірургія, тромбектомія при інсульті, педіатрична або неонатальна інтенсивна терапія, або трансплантація органів. Якщо в SHF немає відповідного персоналу, обладнання або ресурсів для здійснення певного втручання чи моніторингу, найкращим рішенням є переведення пацієнта. |
ТРИГЕРИ ТРАНСПОРТУВАННЯ, ПОВ’ЯЗАНІ З РЕСУРСАМИ
Навіть якщо стан пацієнта стабільний, переведення все одно може бути необхідним через обмежені ресурси закладу охорони здоровʼя, який відправляє пацієнта.
| Тригери транспортування, пов’язані з ресурсами | Опис |
| 1 | Обмежена спроможність або перевантажені ресурси | Якщо SHF зіштовхується з нестачею місць у ВІТ, нестачею персоналу або проблемами з обладнанням, переведення пацієнта до закладу з наявними ресурсами може бути критично важливим для забезпечення своєчасної та належної медичної допомоги. |
| 2 | Катастрофи або події з масовим ураженням | У ситуаціях, коли місцеві ресурси перевантажені внаслідок катастрофи або подій з масовим ураженням, переведення пацієнтів може бути необхідним для раціонального розподілу навантаження та забезпечення своєчасної медичної допомоги постраждалим. |
Неклінічні тригери для переведення
Немедичні чинники також можуть зумовити необхідність транспортування.
| Немедичні тригери | Опис |
| 1 | Переведення до закладу з нижчим рівнем інтенсивності допомоги або реабілітації | Після стабілізації стану пацієнт може бути переведений з відділення інтенсивної терапії з високим рівнем інтенсивності до профільного відділення, закладу відновного лікування або реабілітаційного центру для подальшого лікування. |
| 2 | Побажання пацієнта або родини | Переведення ближче до місця проживання пацієнта або до його родини може бути необхідним для отримання тривалого догляду або паліативної допомоги |
Типи транспортування: відповідність між потребою та терміновістю
Після того як потребу в переведенні виявлено, важливо класифікувати транспортування залежно від клінічних потреб пацієнта та рівня терміновості. Зазвичай транспортування поділяються на такі категорії:
| Категорія транспортування | Опис |
| Негайне транспортування (Категорія 1) | Застосовується у ситуаціях, що загрожують життю, і потребує негайного транспортування протягом кількох хвилин. Таке переведення здійснюється за нагальної потреби у втручаннях, які SHF не може забезпечити (наприклад, невідкладна хірургія, надання невідкладної розширеної допомоги при загрозі життю). Логістику транспортування пришвидшують для уникнення затримок. |
| Термінове транспортування (Категорія 2) | Застосовується для пацієнтів, яким необхідно надати часозалежну медичну допомогу в межах 1–2 годин. Прикладами є пацієнти, які потребують нейрохірургічного втручання через внутрішньочерепну кровотечу, або пацієнти з інсультом, які потребують тромбектомії. Хоча ситуація є критичною, все ж є трохи більше часу для організації спеціалізованої бригади транспортування та забезпечення готовності RHF. |
| Транспортування для спеціалізованої допомоги (Категорія 3) | Пацієнти, які є клінічно стабільними, але потребують доступу до спеціалізованих послуг або моніторингу протягом кількох годин (зазвичай до 4 годин). До цієї категорії належать пацієнти, які потребують складної візуалізації, допомоги у відділенні інтенсивної терапії (якщо вона недоступна в SHF), або спеціалізованих хірургічних втручань. Такі транспортування передбачають більше часу на планування, хоча ефективність залишається критично важливою. |
| Нетермінове транспортування (Категорія 4) | Ці транспортування здійснюються з неклінічних причин або для зниження рівня медичної допомоги. Вони можуть плануватись відповідно до наявності транспорту та місць і організовуватись з урахуванням побажань пацієнта чи його родини щодо тривалого догляду, реабілітації або паліативної допомоги. |
Оцінка спроможностей направляючого закладу охорони здоров’я (SHF)
Фундаментальним етапом у прийнятті рішення щодо транспортування критично хворого пацієнта є всебічна оцінка спроможностей закладу, що направляє (SHF), щодо ефективного забезпечення потреб пацієнта. Транспортування не завжди є обов’язковим лише через тяжкий стан пацієнта. Якщо SHF має необхідні ресурси та відповідну клінічну експертизу для надання потрібної допомоги, лікування на місці може бути більш безпечнішим і ефективнішим варіантом.
Щоб ухвалити це рішення, медична бригада має поставити собі низку ключових запитань. Насамперед: чи має заклад, що направляє (SHF), необхідне обладнання та умови для ефективної стабілізації та лікування пацієнта? Це передбачає оцінку наявності місць у відділенні інтенсивної терапії, апаратів ШВЛ, моніторингових пристроїв і медикаментів відповідно до клінічних потреб пацієнта. Важливу роль у процесі прийняття рішення може відігравати також здатність надавати спеціалізовані втручання.
Не менш важливим є наявність компетентного, підготовленого персоналу. Чи має заклад, що направляє (SHF), у своєму розпорядженні необхідних фахівців, таких як реаніматологи, хірурги-травматологи, анестезіологи та медичні сестри інтенсивної терапії, які мають досвід у веденні складних клінічних випадків? Їхня здатність надавати невідкладну й кваліфіковану медичну допомогу часто визначає, чи можна стабілізувати пацієнта на місці, чи виникає потреба в його транспортуванні до закладу вищого рівня.
Якщо відповідь на будь-яке з цих запитань — «ні» (SHF, не має відповідного обладнання, спеціалізованого персоналу чи достатньої спроможності), рішення про транспортування слід ухвалити швидко, з урахуванням терміновості стану пацієнта та потенційних переваг більш оснащеного закладу, який отримує пацієнта.
Вибір відповідного медичного закладу для прийому (RHF) та підготовка до транспортування
Якщо необхідність у переведенні пацієнта підтверджено, наступним кроком є визначення RHF, найбільш придатного для надання необхідного рівня медичної допомоги. Вибір такого закладу є критично важливим і має ґрунтуватися на кількох ключових чинниках. По-перше, клінічні потреби пацієнта мають відповідати можливостям RHF. Обраний заклад повинен надавати спеціалізовані послуги, мати відповідне обладнання та експертні ресурси для для забезпечення належної медичної допомоги пацієнту. Наприклад, якщо пацієнту потрібна нейрохірургія, RHF, має мати високоспеціалізоване нейрохірургічне відділення, здатне провести необхідні втручання. Відповідність між станом пацієнта та спеціалізацією RHF, є визначальною для успішного транспортування. Ще одним важливим чинником є наявність місць і спроможність прийняти пацієнта: має бути вільне місце у ВІТ або іншому спеціалізованому підрозділі, готовому прийняти пацієнта. Необхідно забезпечити добре скоординовану комунікацію із RHF, щоб підтвердити готовність усіх необхідних ресурсів і можливість безперебійної передачі пацієнта. Нарешті, потрібно врахувати відстань і логістичні аспекти транспортування. Близькість закладу є важливою логістичною перевагою, оскільки коротша відстань знижує ризики для пацієнта і забезпечує швидший доступ до спеціалізованої допомоги. Терміновість потреб пацієнта також впливає на те, наскільки далеко можна перевезти пацієнта і з якою швидкістю має бути виконане транспортування.
Організація логістики транспортування
Після вибору відповідного RHF, організація логістичних аспектів транспортування є ретельним процесом, що потребує точності та координації задля забезпечення безпеки та своєчасності. Необхідно завчасно спланувати кілька ключових елементів. Одним із перших чинників є вибір способу транспортування. Залежно від терміновості та стабільності стану пацієнта можуть бути доцільні різні методи. Для стабільних пацієнтів і на коротких дистанціях зазвичай достатньо наземного транспорту ( автомобіля ЕМД). Однак, якщо йдеться про велику відстань або критичний стан пацієнта, може знадобитися повітряне транспортування — гелікоптером або літаком — для забезпечення швидкого переміщення. Активація бригади ССТ є ще одним критичним етапом. Цю бригаду слід оперативно мобілізувати; вона має складатися з підготовленого персоналу, який володіє навичками надання розширеної невідкладної допомоги під час транспортування. Такі бригади зазвичай включають парамедиків, медичних сестер і лікарів інтенсивної терапії, здатних реагувати на будь-які надзвичайні ситуації під час транспортування. Необхідною умовою є чітка комунікація та повноцінна передача інформації між SHF, бригадою ССТ та RHF. Уся актуальна медична інформація, поточне лікування, очікуваний час прибуття, а також усі клінічні застереження мають бути передані заздалегідь, щоб RHF був повністю готовим до його прийому та подальшого надання допомоги без затримок.
На основі уніфікованої СОП щодо запиту на переведення, наведеної у даному документі, далі подано структурований опис розділу «Запит на транспортування». У ньому дотримано стандартного порядку, визначеного СОП, та пояснено необхідні етапи, порядок комунікації та ведення документації в процесі транспортування.
СОП PRE 2: “Чи потребує даний пацієнт транспортування?”
СОП PRE 2: “Чи потребує даний пацієнт транспортування?” передбачає структурований підхід до оцінки доцільності переведення критично хворого пацієнта до іншого закладу. Ця стандартна операційна процедура (СОП) уніфікує процес ухвалення рішення, забезпечуючи систематичну оцінку всіх чинників — клінічного стану пацієнта, наявності ресурсів та логістичних аспектів — перед тим, як визначити необхідність транспортування.
Клінічна оцінка та прийняття рішень
СОП підкреслює важливість початкової клінічної оцінки стану пацієнта, яка включає:
Оцінка стану пацієнта: оцінювання тяжкості захворювання пацієнта за клінічними ознаками, результатами лабораторних досліджень та діагностикою. Основна мета — визначити, чи може стан пацієнта бути ефективно стабілізований у поточному закладі.
Визначення наявних компетенцій і можливостей: SHF повинен оцінити, чи має він необхідні клінічні компетенції для лікування пацієнта. Це включає врахування наявності фахівців, таких як інтенсивісти, травматологи або підготовлений середній медперсонал, залежно від потреб пацієнта.
На цьому етапі необхідно відповісти на кілька запитань:
- Чи може бути надане ефективне лікування?
- Чи доступний необхідний професійний потенціал (спеціалісти)?
- Чи діагноз підтверджений (верифікований), чи потрібні додаткові обстеження?
Відповідь “НІ” на будь-яке з цих запитань свідчить про те, що пацієнт може потребувати транспортування.
Стратегічне прийняття рішень
Після прийняття рішення щодо ведення пацієнта СОП переходить до етапу стратегічного прийняття рішень, що зосереджений на наявності ресурсів і спроможності закладу надавати допомогу пацієнту:
Наявність ресурсів: заклад має оцінити, чи є в нього необхідні ресурси для лікування, такі як місце у відділенні інтенсивної терапії, апарати штучної вентиляції легень та обладнання для моніторингу пацієнта. У разі нестачі ресурсів, особливо в періоди підвищеного навантаження, може бути рекомендовано ранній розподіл пацієнтів у критичному стані до інших закладів задля збереження спроможність надавати медичну допомогу.
- Чи доступні необхідні ресурси для лікування пацієнта?
- Чи може заклад впоратися з очікуваним напливом пацієнтів і водночас надавати належну допомогу?
- Якщо ресурси недоступні, рішення про транспортування має бути прийнято без зволікань.
- Категоризація транспортування та терміновість
СОП описує чотири категорії транспортувань залежно від терміновості стану пацієнта. Після ухвалення рішення про необхідність транспортування слід визначити його спосіб і терміновість:
| Категорія 1: Негайне (Життєво небезпечний стан) | Пацієнти, які потребують термінового втручання, яке SHF не може надати, мають бути транспортувані негайно. Приклади включають пацієнтів, які потребують екстреної операції або розширеного забезпечення прохідності дихальних шляхів. |
| Категорія 2: Термінове (1–2 години) | Потрібна допомога, чутлива до часу, і пацієнт має бути транспортований протягом 1–2 годин. Ця категорія охоплює, наприклад, пацієнтів з інсультом, які потребують механічної тромбектомії або нейрохірургічного втручання через крововилив у мозок. |
| Категорія 3: Спеціалізована допомога (4–8 годин) | Клінічно стабільні пацієнти, які потребують спеціалізованої допомоги, недоступної в SHF (наприклад, поглибленої діагностики, моніторингу в ВІТ або хірургічного втручання). Транспортування має бути виконане впродовж 4–8 годин. |
| Категорія 4: Нетермінове (<24 годин) | Такі транспортування здійснюються з планових причин, зокрема для продовження лікування на наступному етапі: проведення реабілітаційних заходів або надання паліативної допомоги. Транспортування в цій категорії менш термінові, однак мають бути завершені протягом 24 годин. |
ОЦІНЮВАННЯ РИЗИКІВ ТРАНСПОРТУВАННЯ
СОП також враховує ризики, пов’язані з транспортуванням пацієнта, зокрема:
- Погіршення стану пацієнта: можливе ускладнення стану пацієнта під час транспортування.
- Відтермінування надання медичної допомоги внаслідок логістичних труднощів, пов’язаних з організацією транспортування пацієнта.
- Безпека пацієнта: необхідність забезпечити стабільний стан пацієнта перед транспортуванням і вжити відповідних запобіжних заходів.
- Інфекційний контроль: запобігання інфікуванню під час транспортування, особливо у пацієнтів групи високого ризику.
Процес транспортування та координація
Після ухвалення рішення про транспортування, фінальний етап включає:
- Вибір способу транспортування: наземне чи повітряне транспортування обирається залежно від терміновості транспортування та відстані до медичного закладу, що приймає пацієнта (RHF).
- Комунікація та координація: медичний заклад, що направляє пацієнта (SHF), повинен координувати дії з медичним закладом, що приймає пацієнта (RHF), щоб забезпечити готовність приймаючої сторони до госпіталізації та наявність необхідних ресурсів (наприклад, ліжка у відділенні інтенсивної терапії, спеціалізований персонал). Чітка передача клінічної інформації між SHF, бригадою транспортування пацієнтів у критичному стані (CCT) та RHF є критично важливою для уникнення затримок або ускладнень під час транспортування.
Дотримання СОП PRE-TR 1 дозволяє медичним працівникам здійснювати транспортування пацієнтів у критичному стані на основі системного оцінювання, ефективно, відповідно до індивідуальних потреб пацієнта, мінімізуючи ризики та покращуючи результати лікування.
ЗАПИТ НА ТРАНСПОРТУВАННЯ (див. Додаток 3)
Процедура подання запиту на транспортування є критично важливим етапом для забезпечення безпечного та ефективного транспортування пацієнтів у критичному стані між медичними закладами. Стандартизований процес подання запиту на транспортування (Додаток ІІ: PRE-TR 2) ґрунтується на чіткій комунікації, детальному документуванні та дотриманні протоколів, які визначають ступінь терміновості транспортування.
| Основні рекомендації: запит на транспортування в процесі прийняття рішень |
| 92 | Налагодити чітку комунікацію між медичним закладом, що направляє пацієнта (SHF), та Координаційним центром з метою формування запиту на транспортування. |
| 93 | Надати детальну інформацію про стан пацієнта та ступінь терміновості транспортування. |
| 94 | Підтвердити наявність вільного ліжка в медичному закладі, що приймає пацієнта (RHF), і забезпечити готовність бригади транспортування пацієнтів у критичному стані (ССТ) до виїзду. |
| 95 | Використовувати стандартизовану форму для документування всіх необхідних відомостей про пацієнта, включно з медичним анамнезом та станом пацієнта. |
| 96 | Забезпечити внесення до форми основних параметрів життєдіяльності пацієнта, зокрема рівня свідомості, стану дихання та стану гемодинаміки. |
| 97 | Класифікувати терміновість транспортування за категоріями: негайне, термінове, спеціалізоване або не термінове. |
| 98 | Задокументувати контактні дані SHF, RHF та бригади ССТ. |
| 99 | Дотримуватись пришвидшеної процедури для транспортувань за екстреними категоріями (1 і 2) з метою оперативної мобілізації ресурсів. |
| 100 | Планувати неекстрені транспортування (категорії 3 і 4) методично, із забезпеченням належного розподілу ресурсів бригади ССТ. |
| 101 | Додати короткий опис анамнезу пацієнта та інформацію про відповідні оперативні втручання. |
| 102 | Надати детальну оцінку клінічного стану пацієнта із зазначенням показників функції дихальної та серцево-судинної систем. |
| 103 | Обґрунтувати причину транспортування та необхідні втручання у RHF. |
| 104 | Надати перелік поточних лікувальних заходів і підтвердити готовність до транспортування, зокрема обсяг медичної допомоги, який може бути наданий у автомобілі екстреної медичної допомоги. |
КОМУНІКАЦІЯ З ЦЕНТРОМ КООРДИНАЦІЇ
Ініціювання запиту на транспортування розпочинається з безпосередньої комунікації між медичним закладом, що направляє пацієнта (SHF), та центром координації. Центр координації виконує функцію центральної точки зв’язку, забезпечуючи координацію між бригадою транспортування пацієнтів у критичному стані (CCTT) та медичним закладом, що приймає пацієнта (RHF). Важливо, щоб SHF чітко виклав інформацію про наявний стан пацієнта, проведені невідкладні втручання та рівень терміновості транспортування.
Центр координації несе відповідальність за підтвердження спроможності RHF прийняти пацієнта, а також за організацію логістичних аспектів транспортування. Цей етап включає підтвердження наявності вільного ліжка, підготовку CCT і забезпечення наявності всього необхідного персоналу та обладнання для безпечного транспортування. Ефективна комунікація дозволяє оптимізувати процес, мінімізувати затримки та забезпечити, щоб усі сторони були скоординовані з урахуванням потреб пацієнта та термінів транспортування.
Уніфікована документація запиту на транспортування
Для збору всієї необхідної інформації про пацієнта, його стан та вимоги до транспортування використовується стандартизована форма запиту на транспортування. Заповнення цієї документації повинно здійснюватися ретельно, щоб уникнути пропуску критично важливих відомостей. Форма запиту включає кілька ключових розділів:
Інформація про медичний заклад, що направляє пацієнта
- Дані про пацієнта: містить ідентифікаційні відомості про пацієнта, зокрема повне ім’я, дату народження та анамнез захворювання. Додатково зазначається інформація про поточний стан пацієнта, зокрема: рівень свідомості (GCS), функція дихання (самостійне дихання, потреба в кисні або штучна вентиляція легень), стан кровообігу (необхідність у вазопресорах або інотропах), наявність гострих станів (наприклад, сепсис, ГРДС, кровотеча, підвищений внутрішньочерепний тиск).
- Категорія транспортування: терміновість транспортування класифікується за категоріями: Негайне (Категорія 1), Термінове (Категорія 2), Спеціалізоване (Категорія 3), та Нетермінове (Категорія 4). Ця класифікація визначає строки та пріоритет транспортування.
- Інформація про медичний заклад, що приймає пацієнта (RHF): включає контактні дані, підтвердження наявності вільного ліжка та відповідальної особи для забезпечення належної координації.
- Бригада транспортування пацієнтів у критичному стані (CCT): вказується інформація про бригаду екстреної медичної допомоги, категорія автомобіля ЕМД та контактні дані бригади, що здійснює транспортування. Необхідно підтвердити готовність бригади та наявність усього необхідного обладнання й ресурсів для безпечного транспортування пацієнта.
Використання стандартизованої форми дозволяє уніфіковано фіксувати всю необхідну інформацію, зменшує ймовірність комунікаційних помилок і підвищує ефективність процесу транспортування.
Екстрене та неекстрене транспортування пацієнтів у критичному стані (CCT)
СОП розрізняє екстрені та неекстрені транспортування, при цьому протоколи розроблені таким чином, щоб пришвидшити транспортування у випадках загрози життю пацієнта. У разі екстрених транспортувань (Категорії 1 і 2) пацієнта необхідно транспортувати негайно або протягом 1–2 годин, залежно від тяжкості його стану. Координація дій та мобілізація бригади транспортування пацієнтів у критичному стані (CCT), включно зі службою екстреної медичної допомоги, мають відбуватись без затримок, а медичний заклад, що приймає пацієнта (RHF), повинен бути готовим до госпіталізації в момент прибуття.
Неекстрені транспортування (Категорії 3 і 4) передбачають більш планомірний підхід, що дає змогу ефективніше розподіляти ресурси та обирати оптимальний час транспортування. Ці транспортування зазвичай призначені для пацієнтів, які потребують спеціалізованої допомоги протягом визначеного часу (4-8 годин для категорії 3) або для нетермінової, запланованої допомоги протягом 24 годин для категорії 4.
Кожен тип транспортування супроводжується чітко визначеним протоколом, який гарантує застосування відповідних ресурсів та рівня терміновості відповідно до клінічної ситуації.
Інформація, яку необхідно подати в запиті на транспортування
Для забезпечення безперешкодного та ефективного транспортування медичний заклад, що направляє пацієнта (SHF), повинен надати Координаційному центру та медичному закладу, що приймає пацієнта (RHF), повну та достовірну інформацію. Форма запиту на транспортування включає такі ключові розділи:
- Анамнез хвороби: короткий огляд минулих захворювань пацієнта, перенесених хірургічних Анамнез: короткий огляд наявних або перенесених захворювань пацієнта, хірургічних втручань та хронічних станів, які можуть впливати на безпечність транспортування або подальше лікування у RHF.
- Оцінка клінічного стану: детальний опис оцінка клінічного стану пацієнта, включаючи: рівень свідомості (наприклад, GCS), дихальну функцію (потреба в кисні або штучній вентиляції легень), гемодинамічну стабільність (чи отримує пацієнт вазопресори або інотропи), та наявність критичних ускладнень (наприклад, гострий респіраторний дистрес-синдром — ГРДС, сепсис, підвищений внутрішньочерепний тиск). Ця інформація дозволяє RHF підготуватись до прийому пацієнта належним чином.
- Діагноз та причина транспортування: чітке обґрунтування необхідності транспортування, зокрема потреба у спеціалізованому лікуванні, обмежені ресурси в SHF або погіршення стану пацієнта, яке потребує невідкладної медичної допомоги.
- Призначене лікування: відомості про терапію, яку наразі отримує пацієнт, наприклад: антибактеріальна терапія, седація, параметри ШВЛ, та тривала інфузія вазопресорів або інотропів. Ці дані забезпечують безперервність лікування під час транспортування та після прибуття до RHF.
- Логістичні аспекти транспортування: відомості про бригаду транспортування, включаючи рівень медичної допомоги, який може надати бригада під час транспортування (екстрена медична допомога або спеціалізована), а також підтвердження того, що транспортування організовано та перебуває в режимі очікування.
Повне та точне заповнення форми запиту дозволяє Координаційному центру та RHF заздалегідь оцінити потреби пацієнта та ефективно скоординувати наявні ресурси. Це критично важливо для забезпечення безпеки пацієнта та мінімізації затримок.
ЧАСТИНА 3: КООРДИНАЦІЯ ТА ЗДІЙСНЕННЯ ТРАНСПОРТУВАННЯ
Координація та пошук наявної спроможності
Процес координації та управління наявними ресурсами для транспортування пацієнтів у критичному стані є одним із ключових завдань центру координації. Забезпечення своєчасного транспортування пацієнтів до медичного закладу, що має необхідні можливості для надання відповідного лікування, є критично важливим для безпечної та своєчасної медичної допомоги. У цьому розділі описуються: обов’язки центру координації процедура пошуку наявної спроможності, протоколи підтвердження та передачі інформації щодо доступності медичної допомоги.
| ОСНОВНІ РЕКОМЕНДАЦІЇ: УПРАВЛІННЯ ЗАПИТОМ НА ТРАНСПОРТУВАННЯ |
| 105 | Забезпечити функціонування центру координації як центральної ланки управління всіма запитами на транспортування. |
| 106 | Проаналізувати клінічні дані пацієнта та оцінити ступінь терміновості транспортування. |
| 107 | Визначити медичний заклад, що приймає пацієнта (RHF), з відповідною спроможністю та фаховими ресурсами для забезпечення необхідної допомоги. |
| 108 | Координувати логістичні аспекти транспортування та забезпечити мобілізацію бригади транспортування пацієнтів у критичному стані (CCTT) відповідно до ступеня терміновості. |
| 109 | Забезпечити постійну комунікацію між SHF, RHF та бригадою транспортування для запобігання затримкам. |
| 110 | Створити централізовану базу даних у режимі реального часу для відстеження наявності ресурсів невідкладної та спеціалізованої в медичних закладах RHF. |
| 111 | Забезпечити, щоб база даних містила інформацію про наявність місць у відділеннях інтенсивної терапії, спеціалізованих підрозділах і ключового медичного обладнання. |
| 112 | Використовувати регіональні та національні мережі для розширення пошуку наявної лікувальної спроможності. |
| 113 | Проводити оцінку пріоритетності на основі клінічних потреб, відстані, наявності місць та організаційних аспектів транспортування. |
| 114 | Забезпечити прямий зв’язок між центром координації і RHF для підтвердження доступності медичної допомоги. |
| 115 | Підтвердити наявність вільних ліжок(місць) у відділенні інтенсивної терапії, спеціалізованих підрозділів і необхідного медичного персоналу в RHF. |
| 116 | Підтримувати зворотний зв’язок між SHF, RHF та центром координації для отримання актуальної інформації щодо стану пацієнта та організаційних аспектів транспортування. |
РОЛЬ ЦЕНТРУ КООРДИНАЦІЇ В ОБРОБЦІ ЗАПИТІВ НА ТРАНСПОРТУВАННЯ
Координаційний центр є центральною ланкою, яка забезпечує управління всіма запитами на транспортування, виступаючи посередником між медичним закладом, що направляє пацієнта (SHF), медичним закладом, що приймає пацієнта (RHF), та бригадою транспортування пацієнтів у критичному стані (CCT). Завдання Координаційного центру полягає не лише в організації логістичних аспектів, але й у забезпеченні того, щоб транспортування було здійснене безпечним, ефективним способом і з необхідними ресурсами.
Після отримання запиту на транспортування координаційний центр аналізує клінічну інформацію про пацієнта, оцінює ступінь терміновості транспортування, розпочинає пошук медичного закладу (RHF), який має відповідні ресурси та фахову спроможність для надання необхідної допомоги. До функцій центру входить: збір даних про наявні ліжка, оцінка спроможності надання необхідної медичної допомоги, перевірка готовності RHF прийняти пацієнта. Крім того, координаційний центр здійснює організацію логістики транспортування, гарантуючи мобілізацію CCTT відповідно до клінічної ситуації пацієнта.
Чітка та безперервна комунікація між центром координації, SHF та RHF має принципове значення. Центр повинен забезпечити постійне оновлення інформації, щоб уникнути затримок і гарантувати, що всі задіяні сторони поінформовані на всіх етапах процесу.
Пошук спроможності для надання лікування
Після подання запиту на транспортування основним завданням координаційного центру є визначення найбільш відповідного медичного закладу, що приймає пацієнта (RHF), який здатен надати необхідну медичну допомогу відповідно до потреб пацієнта. Це передбачає системний пошук наявних вільних ресурсів для надання медичної допомоги через централізовані бази даних та мережі взаємодії між закладами охорони здоров’я.
База даних і мережі для відстеження доступності RHF
З метою ефективного та своєчасного транспортування пацієнтів у критичному стані необхідно створити централізовану базу даних у режимі реального часу, яка б фіксувала спроможність різних медичних закладів, що приймають пацієнтів (RHF). Така база даних повинна бути повноцінним інструментом, який забезпечує актуальну інформацію про наявність ресурсів невідкладної та спеціалізованої допомоги, зокрема: місць в відділеннях інтенсивної терапії (ВІТ), спеціалізованих підрозділів (наприклад, травматологічних, кардіологічних або неонатальних), та ключового медичного обладнання.
Завдяки оновленню в реальному часі база даних дає змогу Координаційному центру та медичним працівникам оперативно визначити доступні RHF, здатні надати необхідну допомогу. Така швидкість прийняття рішень особливо критична в екстрених ситуаціях, коли зволікання може мати серйозні наслідки. Крім того, база даних повинна бути зручною для використання уповноваженим персоналом як на регіональному, так і на національному рівнях, що дозволяє охопити всі потенційні ресурси та зменшити ризики затримки через відсутність локальної спроможності.
Окрім прискорення прийняття рішень, така централізована платформа сприятиме покращенню комунікації та координації між медичними закладами, забезпечуючи безперервну взаємодію під час транспортування пацієнтів. У підсумку, створення подібної бази даних значно підвищить ефективність процесу транспортування, гарантує швидке спрямування пацієнтів у критичному стані до відповідного закладу та дозволить оптимально використовувати наявні ресурси в межах системи охорони здоров’я.
ОЦІНКА ПРІОРИТЕТНОСТІ: ВИБІР ОПТИМАЛЬНОГО МЕДИЧНОГО ЗАКЛАДУ ДЛЯ ГОСПІТАЛІЗАЦІЇ
Після попереднього визначення медичних закладів, що приймають пацієнтів (RHF), з наявною необхідною спроможністю, координаційний центр повинен здійснити оцінку пріоритетності кожного варіанта. Така оцінка базується на кількох ключових критеріях:
- Клінічні потреби: RHF повинен мати спеціалізовані підрозділи або послуги, необхідні для лікування пацієнта (наприклад, травматологічна допомога, трансплантаційна хірургія або педіатричне відділення інтенсивної терапії).
- Близькість: географічна відстань між медичними закладами є критично важливою, особливо у випадках екстреного чи термінового транспортування, коли вирішальне значення має час.
- Наявність вільного ліжка у відділенні інтенсивної терапії або спеціалізованому підрозділі є обов’язковою умовою. Затримка з розміщенням може створити загрозу для пацієнта та продовжити час транспортування.
- Логістика транспортування: RHF має бути доступним у часових межах, які відповідають ступеню терміновості клінічного стану пацієнта. Важливим є також наявність відповідних транспортних засобів (наприклад, наземного або повітряного транспорту).
Мета оцінки пріоритетності — визначити той RHF, який забезпечить найкращий баланс між спроможністю, доступністю за відстанню та негайною готовністю для надання допомоги пацієнту в найкоротший термін.
Протокол підтвердження наявної спроможності надавати медичну допомогу
Після визначення оптимального медичного закладу, що приймає пацієнта (RHF), наступним кроком є підтвердження наявності спроможності надавати медичну допомогу та координація логістики транспортування. Для цього необхідна чітка комунікація між медичним закладом, що направляє пацієнта (SHF), RHF та координаційним центром, щоб гарантувати готовність усіх необхідних ресурсів.
Процедура підтвердження з боку RHF
Процес підтвердження починається з безпосереднього зв’язку між центром координації та RHF. RHF повинен підтвердити свою здатність надати необхідну медичну допомогу пацієнту, включаючи: наявність ліжка у відділенні інтенсивної терапії або у відповідному спеціалізованому підрозділі;присутність необхідного медичного персоналу (наприклад, хірургів, лікарів інтенсивної терапії, медичних сестер тощо.
Приймаючий ЗОЗ також має підтвердити очікуваний час прибуття пацієнта та забезпечити готовність усіх ресурсів до цього моменту. У разі будь-яких змін або затримок у наданні спроможностей приймаючий ЗОЗ зобов’язаний негайно повідомити про це Координаційний центр, щоб можна було своєчасно реалізувати альтернативні рішення.
Зворотний зв’язок між направляючим ЗОЗ, приймаючим ЗОЗ та координаційним центром
Підтримання постійного і чіткого зворотного зв’язку між SHF, RHF та координаційним центром є критично важливим на всіх етапах процесу транспортування. Така комунікація дозволяє всім сторонам бути в курсі: стану пацієнта на даний час, деталей логістики транспортування, змін у можливостях надання медичної допомоги.
SHF повинен залишатися на зв’язку з координаційним центром і оперативно інформувати про зміни стану пацієнта, тоді як координаційний центр передає ці оновлення до RHF для забезпечення належної підготовки до прибуття. У свою чергу, RHF має повідомляти координаційний центр про свою готовність до прийому та інформувати про будь-які потенційні ускладнення або зміни, що можуть виникнути до моменту транспортування.
Цей зворотний зв’язок є ключовим для запобігання дезінформації чи затримок, які можуть негативно вплинути на безпеку або стан пацієнта під час транспортування.
ПОЧАТОК ТРАНСПОРТУВАННЯ
Ініціювання транспортування пацієнта у критичному стані (CCT) є одним із найвідповідальніших етапів у безперервному процесі надання медичної допомоги таким пацієнтам. На цьому етапі рішення про транспортування базується на основі оцінки та врахуванні всіх факторів: з одного боку — ризиків, пов’язаних із переміщенням нестабільного пацієнта, а з іншого — потенційної життєво необхідної допомоги, яку можна надати у медичному закладі вищого рівня (RHF). Від початкової оцінки стану пацієнта біля ліжка, яку проводить бригада транспортування пацієнтів у критичному стані (CCT), і до моменту передачі у медичному закладі, що приймає пацієнта (RHF), кожен крок має бути ретельно спланованим і точно реалізованим задля досягнення найкращих клінічних результатів.
| КЛЮЧОВІ РЕКОМЕНДАЦІЇ: ОЦІНКА ЗАПИТУ НА ТРАНСПОРТУВАННЯ ПАЦІЄНТА |
| 117 | Бригада транспортування пацієнтів у критичному стані (ССТ) повинна провести оцінку стану пацієнта біля ліжка, звертаючи увагу на показники життєдіяльності, дихальну функцію, стан кровообігу та неврологічний статус, щоб переконатися у готовності пацієнта до транспортування. |
| 118 | Провести детальну оцінку ризиків транспортування, включаючи: ймовірність погіршення стану, обмеження у наявності обладнання чи ресурсів, потенційні ризики під час транспортування, з метою зваженого прийняття рішення про співвідношення ризиків і переваг надання спеціалізованої допомоги. |
| 119 | Використовувати інструменти, що ґрунтуються на доказовій базі, зокрема шкалу NEWS2, для стратифікації пацієнтів за рівнем ризику (низький, середній, високий) та для обґрунтованого визначення складу персоналу й необхідного обладнання для безпечного транспортування. |
| 120 | Забезпечити, щоб транспортне обладнання (наприклад, апарати ШВЛ, інфузійні помпи) відповідало клінічним потребам пацієнта і було технічно справним, враховуючи обмеження мобільних технологій під час транспортування. |
| 121 | Оцінити дихальний статус пацієнта, перевірити налаштування ШВЛ і рівень кисневої підтримки, щоб упевнитися, що вони можуть бути безпечними та стабільними протягом транспортування; у разі потреби — адаптувати параметри для запобігання погіршенню стану. |
| 122 | Залучити SHF, CCTT і Координаційний центр до процесу колективного прийняття рішення, гарантувавши, що всі ризики та потенційні переваги оцінено перед початком транспортування. |
| 123 | Бригада транспортування пацієнтів у критичному стані (ССТ) повинна провести оцінку стану пацієнта біля ліжка, звертаючи увагу на показники життєдіяльності, дихальну функцію, стан кровообігу та неврологічний статус, щоб переконатися у готовності пацієнта до транспортування. |
ОЦІНКА СТАНУ ПАЦІЄНТА БРИГАДОЮ ССТ за методом “БІЛЯ ЛІЖКА ПАЦІЄНТА”: DOC 1 (див. Додаток 5)
Процес транспортування пацієнта у критичному стані (CCT) розпочинається з комплексної оцінки стану пацієнта біля ліжка, яку проводить бригада транспортування пацієнтів у критичному стані (CCT) після прибуття до медичного закладу, що направляє пацієнта (SHF). Ця оцінка є ключовим етапом, який дозволяє визначити стан пацієнта на момент оцінки та його здатність перенести навантаження, пов’язані з транспортуванням.
Бригада CTT оцінює кілька ключових аспектів стану пацієнта:
- Стабільність життєвих показників: рівень свідомості, частоти серцевих скорочень, артеріального тиску, частоти дихання та рівня сатурації киснем для визначення, чи є стан пацієнта достатньо стабільним для транспортування.
- Дихальна функція: оцінюється, чи пацієнт отримує кисневу підтримку або знаходиться на штучній вентиляції легень (ШВЛ), та чи можливо безпечно підтримувати належну функцію дихання протягом транспортування. У пацієнтів на ШВЛ перевіряються налаштування апарату і визначається, чи відповідає транспортний апарат ШВЛ клінічним потребам пацієнта.
- Стан кровообігу: наявність шоку або потреба у вазопресорній чи інотропній підтримці для підтримання артеріального тиску. Якщо пацієнт потребує гемодинамічної підтримки, бригада CCT має переконатися в наявності відповідних лікарських засобів і справних інфузійних систем для їх використання під час транспортування.
- Неврологічний стан: у пацієнтів із неврологічними ураженнями або порушенням свідомості застосовується Шкала Ком Глазго (ШКГ) або інші клінічні інструменти для оцінки рівня свідомості, а також спостереження за ознаками підвищеного внутрішньочерепного тиску.
Оцінка біля ліжка пацієнта дозволяє не лише підтвердити клінічний стан пацієнта на момент оцінки, а й передбачити можливі ускладнення під час транспортування. Результати цієї оцінки безпосередньо впливають на подальше оцінювання ризиків транспортування.
Оцінювання ризиків транспортування
Кожне транспортування пацієнта у критичному стані (CCT) супроводжується певним ступенем ризику, який необхідно ретельно оцінити до початку транспортування. Оцінка ризиків є ключовим етапом, що дозволяє зважити потенційні загрози, пов’язані з транспортуванням, на фоні можливих життєво важливих переваг від надання високоспеціалізованої допомоги в медичному закладі, що приймає пацієнта (RHF).Цей процес вимагає багатопрофільного підходу та зазвичай здійснюється у співпраці між медичним закладом, що направляє пацієнта (SHF), бригадою транспортування пацієнтів у критичному стані (CCTT) та Координаційним центром.
Основні ризики, які слід враховувати під час транспортування:
- Потенційне погіршення стану пацієнта під час транспортування може ускладнити перебіг основного захворювання через вплив зовнішніх чинників — зміну атмосферного тиску (при авіаперевезеннях), вібрації, обмежені можливості медичного втручання у порівнянні з умовами відділення інтенсивної терапії. Пацієнти у критичному стані є особливо вразливими до дестабілізації, яка може проявитися у вигляді гіпотензії, гіпоксії, аритмій або дихальної недостатності.
- Обмеження у ресурсах та обладнанні: під час транспортування пацієнт втрачає доступ до повного спектра обладнання, наявного в ВІТ. Хоча бригада CCT має сучасне мобільне обладнання, існують технологічні обмеження. Наприклад: транспортні апарати ШВЛ, хоча й функціональні, не завжди відповідають можливостям стаціонарних моделей; Крім того, обмежений простір у транспортному засобі може ускладнювати використання кількох інфузійних помп або іншого необхідного обладнання.
- Непередбачувані події під час транспортування: пацієнти під час транспортування піддаються зовнішнім ризикам, які не перебувають у прямому контролі медичної бригади. До них належать: відтермінування транспортування через дорожню ситуацію, технічні несправності транспорту, чи несприятливі погодні умови (особливо у разі повітряного транспорту). Такі фактори можуть подовжити час перебування пацієнта в нестабільному середовищі та підвищити ризик ускладнень.
Попри наявність суттєвих ризиків, потенційні переваги транспортування пацієнта до спеціалізованого медичного закладу часто переважають загрози. Існує кілька ключових чинників, які допомагають ухвалити обґрунтоване рішення:
- Доступ до життєво необхідних втручань: Основною причиною ініціювання транспортування пацієнта у критичному стані зазвичай є потреба у проведенні медичних втручань, недоступних у SHF. Йдеться про складні хірургічні операції, високо спеціалізовану допомогу у відділенні інтенсивної терапії (наприклад, для пацієнтів із політравмою, серцево-судинною патологією або новонароджених), чи рятівні методи лікування, як-от екстракорпоральна мембранна оксигенація (ECMO) або гемодіаліз. У багатьох випадках саме такі втручання у RHF є критичними для виживання пацієнта.
- Спеціалізований моніторинг та підтримка під час транспортування: бригада CCT має високий рівень підготовки для роботи з пацієнтами у критичному стані під час транспортування. Незважаючи на технічні обмеження мобільного обладнання, клінічний досвід бригади CTT у поєднанні зі спеціалізованими транспортними технологіями дає змогу мінімізувати ризики. бригада забезпечує ефективне використання апаратів ШВЛ, систем гемодинамічної підтримки та моніторингового обладнання, що максимізує шанси на виживання пацієнта протягом усього процесу транспортування.
ІНСТРУМЕНТИ ОЦІНЮВАННЯ ТА АНАЛІЗУ ОЦІНКИ РИЗИКІВ NEWS2
У контексті транспортування пацієнтів у критичному стані пріоритетами є безпека пацієнта та прийняття обґрунтованих рішень. Комплексна оцінка ризиків дає змогу виявити пацієнтів із високим ступенем ризику та ухвалювати рішення, що ґрунтуються на доказовій практиці. Національна шкала раннього попередження 2 (NEWS2) — це достовірний інструмент, який допомагає відстежувати стан пацієнта та ініціювати відповідні дії залежно від тяжкості захворювання та ризику погіршення під час гострого періоду надання медичної допомоги.
- Шкала NEWS2 та стратифікація ризику: використання Національної шкали раннього попередження 2 (NEWS2) (Додаток 1) у поєднанні з іншими клінічними параметрами (Додаток 2) дозволяє бригаді CCTT оцінити ймовірність погіршення стану пацієнта під час транспортування. Процес стратифікації розподіляє пацієнтів на групи низького, середнього та високого ризику. На основі отриманої оцінки алгоритм формує рекомендації щодо складу персоналу та необхідного обладнання, що повинні бути залучені під час транспортування.
- Прийняття обґрунтованих рішень: система NEWS2 дозволяє бригаді CCT приймати більш зважені та впевнені рішення щодо доцільності проведення транспортування. У разі, якщо пацієнт класифікується як такий, що має високий ризик, бригада повинна оцінити свої професійні можливості та наявні ресурси на предмет відповідності клінічним потребам пацієнта. У крайніх випадках бригада може ухвалити рішення не здійснювати транспортування, якщо вважатиме, що ризики переважають потенційні переваги від транспортування.
Разом із тим, при розгляді рішення про відмову від транспортування вкрай важливо збалансовано оцінити потенційні переваги, які пацієнт може отримати в RHF, де доступна високоспеціалізована допомога, що здатна суттєво покращити прогноз. Цей баланс — ключовий для того, щоб пацієнт отримав життєво необхідні втручання, коли це справді потрібно, з одночасним забезпеченням безпеки під час транспортування.
Пріоритет безпеки пацієнта завдяки інструментам, що ґрунтуються на доказах
Використання шкали NEWS2 у поєднанні з іншими інструментами оцінювання ризиків забезпечує структурований і об’єктивний підхід до аналізу ризиків, пов’язаних із транспортуванням пацієнтів у критичному стані. Завдяки ідентифікації ключових клінічних параметрів і застосуванню стандартизованих протоколів медична бригада може ухвалювати рішення, засновані на даних, ставлячи безпеку пацієнта в пріоритет. Такі інструменти також підвищують якість медичної допомоги на всіх етапах транспортування, забезпечуючи, щоб рішення приймалися не лише на основі клінічного досвіду, а й на доказовій базі.
Інтеграція шкали NEWS2 у процес оцінки ризиків під час транспортування пацієнтів відображає ширшу орієнтацію на найвищий рівень безпеки та якості допомоги для пацієнтів у критичному стані. Використовуючи доказові методики, медичні працівники здатні зменшити ризики, підвищити впевненість у прийнятті рішень та, у підсумку, покращити результати лікування під час транспортування.
Цей комплексний підхід дозволяє інтегрувати результати стратифікації за шкалою NEWS2 з клінічною оцінкою ризиків транспортування, забезпечуючи оптимальний баланс між безпекою та потенційною життєво необхідною допомогою при ухваленні кожного рішення щодо транспортування.
РІШЕННЯ ПРО ТРАНСПОРТУВАННЯ: БАЛАНС РИЗИКІВ І ПЕРЕВАГ
Після проведення оцінки стану пацієнта біля ліжка та оцінки ризиків транспортування остаточне рішення про доцільність переведення приймається спільно бригадою транспортування пацієнтів у критичному стані (CCTT), лікарями медичного закладу, що направляє пацієнта (SHF), та Координаційним центром. Цей процес прийняття рішення ґрунтується на ключовому питанні: Чи врятує транспортування пацієнта життя або суттєво покращить його шанси на виживання?
Важливо наголосити, що жодна настанова не може автоматично визначити, чи слід транспортувати пацієнта в кожному окремому випадку. Кожна ситуація потребує індивідуального розгляду, з урахуванням динамічних чинників, таких як:
- Наявний клінічний діагноз і прогноз пацієнта.
- Тяжкість і стабільність його стану на момент оцінювання.
- Наявність необхідних ресурсів і обладнання у складі бригади CCT для забезпечення транспортування.
- Відстань до медичного закладу, що приймає пацієнта (RHF), та ймовірність успішного втручання після прибуття.
Стандартизовані протоколи забезпечують структуровану рамку для підтримки процесу прийняття рішення, проте не підмінюють сам процес. Вони є надзвичайно важливими для того, щоб виокремити ключові чинники, які слід враховувати, забезпечити системний перегляд усіх аспектів: стану пацієнта, можливостей бригади, логістичних умов. Такі протоколи допомагають виявити ризики, переваги та часові обмеження, надаючи медичній бригаді обґрунтовану основу для прийняття рішення, чи переважають потенційні переваги транспортування притаманні йому ризики.
У більшості випадків, життєво необхідна допомога, яку пацієнт може отримати у високо спеціалізованому медичному закладі, переважає ризики транспортування. Однак існують ситуації, коли ризики транспортування є надмірно високими, особливо якщо пацієнт перебуває у вкрай нестабільному стані й, імовірно, не витримає транспортування. У таких випадках рішення повинно бути максимально індивідуальними, ґрунтуючись на оцінці в режимі реального часу та професійному клінічному судженні бригади на місці.
Висновок: ключова роль скоординованої системи транспортування пацієнтів у критичному стані
Рішення про транспортування пацієнта у критичному стані ніколи не приймається легковажно. Це складний, багатокомпонентний процес, який передбачає ретельне зважування ризиків, пов’язаних із транспортуванням, і потенційних переваг, які може надати медичний заклад з розширеними можливостями лікування. Добре скоординована система транспортування пацієнтів у критичному стані (CCT) відіграє вирішальну роль у мінімізації ризиків, забезпечуючи: участь висококваліфікованих бригад транспортування (CCT), наявність мобільних систем підтримки життєдіяльності, дотримання структурованих протоколів комунікації та прийняття клінічних рішень.
Хоча стандартизовані протоколи є важливим інструментом, що допомагає в процесі ухвалення рішень, остаточне рішення завжди приймається індивідуально для кожного пацієнта, у режимі реального часу, біля ліжка пацієнта, з урахуванням багатьох факторів, що можуть вплинути на результат. Ретельний баланс між ризиком і перевагами, який забезпечується під час: оцінки біля ліжка, аналізу ризиків транспортування, прийняття спільного рішення — гарантує, що пацієнт у критичному стані має найкращі шанси на виживання, незалежно від того, чи він залишається в SHF, чи транспортується до RHF з розширеними ресурсами.
Роль бригади CCT полягає не лише у фізичному транспортуванні пацієнта. Її місія — забезпечити безперервність інтенсивної терапії, керувати ризиками в реальному часі та наблизити життєво необхідну допомогу до тих, хто її найбільше потребує.
РОЗДІЛ 2 ЗАБЕЗПЕЧЕННЯ ПРОХІДНОСТІ ДИХАЛЬНИХ ШЛЯХІВ
ЧАСТИНА 1: ЗАБЕЗПЕЧЕННЯ ПРОХІДНОСТІ ДИХАЛЬНИХ ШЛЯХІВ ЗА ПІДХОДОМ VORTEX
ВСТУП
Невідкладні стани дихальних шляхів у дорослих пацієнтів у критичному стані становлять серйозну проблему під час транспортування та лікування у відділеннях інтенсивної терапії. Виникнення ускладнень, пов’язаних із дихальними шляхами, підкреслює ключове значення своєчасного застосування ефективних екстрених заходів.
Доведено, що артеріальна гіпотензія у період інтубації та розвиток гемодинамічної нестабільності після інтубації безпосередньо асоціюються з високою захворюваністю та смертністю серед дорослих пацієнтів (Karamchandani та ін., 2021)1. Згідно з даними дослідження NAP4, значна частка смертей, пов’язаних із дихальними шляхами у відділеннях інтенсивної терапії, була зумовлена зміщенням трахеостомічної трубки, і застосування капнографії могло б запобігти більшості цих випадків (McGrath та ін., 2012)2.
У дорослих пацієнтів у критичному стані ризик порушення прохідності дихальних шляхів під час транспортування створює безпосередню загрозу життю. Це підкреслює необхідність наявності чітко відпрацьованих алгоритмів і протоколів надання невідкладної допомоги при порушеннях прохідності дихальних шляхів для досягнення оптимальних результатів лікування у відділеннях інтенсивної терапії.
Здатність оперативно реагувати на ускладнення, пов’язані з порушенням прохідності дихальних шляхів, визначально впливає на перебіг і прогноз захворювання та є критично важливою для збереження життя пацієнта.
Огляд «Несприятливі події, пов’язані з порушенням прохідності дихальних шляхів у дорослих у відділеннях інтенсивної терапії: ведення ускладнень, пов’язаних із втратою або порушенням прохідності дихальних шляхів (інтубаційної / трахеостомічної трубки)»3 надає системний аналіз основних проблем і стратегій ведення таких станів. У публікації акцентовано увагу на необхідності своєчасного реагування у випадках втрати або дисфункції інтубаційної чи трахеостомічної трубки, а також на визначальній ролі стандартизованих процедур невідкладної допомоги у зниженні летальності.
Висновки досліджень підтверджують, що застосування узгоджених клінічних настанов, алгоритмізованого підходу та належного рівня підготовки персоналу має вирішальне значення.
Ефективне ведення ускладнень, пов’язаних із дихальними шляхами, у дорослих пацієнтів у відділеннях інтенсивної терапії потребує спеціалізованих компетенцій та неухильного дотримання затверджених протоколів невідкладної допомоги для забезпечення своєчасного та результативного реагування в екстрених ситуаціях.
1 Karamchandani, K., Wheelwright, J., Yang, A. L., Westphal, N., Khanna, A. K., & Myatra, S. N. (2021). Emergency airway management outside the operating room: current evidence and management strategies. Anesthesia &Amp; Analgesia, 133(3), 648-662. https://doi. org/10.1213/ane.0000000000005644
2 McGrath, B. A., Bates, L., Atkinson, D., & Moore, J. A. (2012). Multidisciplinary guidelines for the management of tracheostomy and laryngectomy airway emergencies. Anesthesia, 67(9), 1025-1041. https://doi.org/10.1111/j.1365-2044.2012.07217.x
3 (2022). Airway misadventures in adult critical care: a concise narrative review of managing lost or compromised artificial airways. current opinion in anaesthesiology, 35(2), 130-136. https://doi.org/10.1097/aco.0000000000001105
ПІДХІД VORTEX4
Дослідження «Вплив впровадження підходу VORTEX на ефективність забезпечення прохідності дихальних шляхів у студентів-медиків у стресових умовах: рандомізоване контрольоване симуляційне дослідження» мало на меті оцінити результативність застосування підходу VORTEX під час тренування студентів-медиків у змодельованих ситуаціях з високим рівнем стресу (Starosolski, 2023)5. Результати показали:
- студенти-медики, які проходили навчання за підходом VORTEX, продемонстрували вищу ефективність дій;
- у них було зафіксовано менший рівень когнітивного навантаження під час моделювання кризових ситуацій, пов’язаних із забезпеченням прохідності дихальних шляхів.
Це дослідження підтвердило потенційну користь впровадження підходу VORTEX у навчальний процес із забезпечення прохідності дихальних шляхів для студентів-медиків. Було відзначено його ефективність у покращенні прийняття клінічних рішень та зниженні рівня стресу в умовах високої напруги. Використання рандомізованого контрольованого дизайну надало вагомі докази практичної цінності застосування підходу VORTEX у підготовці майбутніх лікарів. У контексті підготовки команд для транспортування пацієнтів у критичному стані в Україні цей підхід довів свою застосовність та ефективність як робоча модель. Саме тому підхід VORTEX є ключовим елементом цих клінічних настанов. Це рішення ґрунтується не на формальній оцінці за методологією GRADE, а є результатом практичного досвіду та експертних рекомендацій, отриманих у процесі проведення навчання та надання медичної допомоги в Україні.
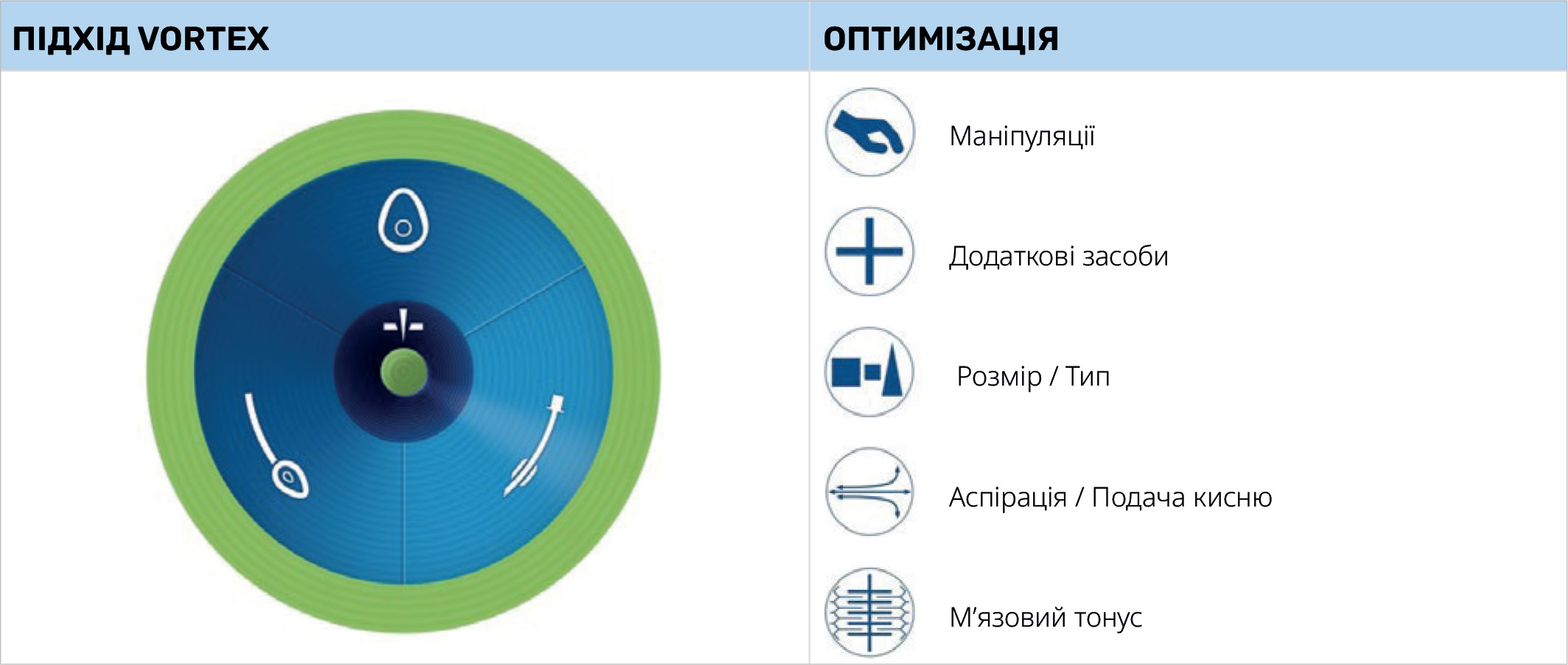
4 Vortex Approach. (n.d.). Upper Airway Lifelines. Отримано з http://vortexapproach.org/lifelines#besteffort
5 Starosolski, M., Kapłan, C., Kalemba, A., & Majewska, K. (2023). The impact of implementing the vortex approach on airway management performance in stressed medical students: a randomized controlled simulation study. Medical Science Monitor, 29. https://doi.org/10.12659/msm.940372
Ведення складних дихальних шляхів у пацієнтів у критичному стані потребує системного та адаптивного підходу. У таких клінічних ситуаціях підхід VORTEX застосовується як уніфікована модель дій для лікаря та бригади, що надає допомогу. Основою цього підходу є три ключові способи порятунку життя:
- вентиляція за допомогою маски з мішком «Амбу» ,
- використання надгортанного повітропроводу,
- інтубація трахеї ендотрахеальною трубкою.
Підхід VORTEX враховує динамічний характер забезпечення прохідності дихальних шляхів і спрямована на досягнення адекватної альвеолярної оксигенації. Вона підкреслює необхідність гнучкості та швидкої адаптації у складних клінічних умовах. Ключовим принципом є «максимальне зусилля» — виконання до трьох спроб кожного окремого способу порятунку життя із застосуванням оптимізаційних кроків («ключових змін»), що підвищують шанси на успіх (маніпуляції, додаткові засоби, підбір розміру/типу, аспірація/подача кисню, контроль м’язового тонусу). Підхід також враховує вплив людського фактора та забезпечує підтримання ситуаційної обізнаності бригади. Це сприяє злагодженим і безпечним діям та дозволяє уникнути «замкненого кола» невдалих спроб без стигматизації необхідного переходу до іншого методу.
Зосереджуючись на оптимізації дій, підхід VORTEX передбачає п’ять категорій ключових змін (додаткові прийоми для оптимізації доступу до дихальних шляхів), які можуть застосовуватися до кожного способу порятунку життя. Така структурна побудова підвищує ефективність, чіткість та послідовність процесу оптимізації, що дає змогу зменшити час та кількість спроб, необхідних для реалізації принципу максимального зусилля.
Важливу роль у підході VORTEX відіграє людський фактор, адже саме він визначає умови для якісної комунікації та прийняття рішень у бригаді. Замість поняття «невдача» використовується концепція «вичерпаної максимальної спроби» (completed best effort), що полегшує психологічне сприйняття ситуації та забезпечує більш плавний перехід до іншого шляху порятунку життя, коли це необхідно.
Отже, підхід VORTEX забезпечує лікаря та бригаду чітким і адаптивним алгоритмом для подолання викликів, пов’язаних із забезпеченням прохідності дихальних шляхів. Від початкового вибору тактики, через оптимізаційні кроки, до врахування впливу людського фактора — підхід VORTEX виступає ефективним інструментом у динамічних умовах ведення пацієнтів у критичному стані.
| ПІДХІД VORTEX: ОСНОВНІ РЕКОМЕНДАЦІЇ |
Підхід VORTEX ґрунтується на трьох основних способах порятунку життя: - вентиляція маскою з мішком «Амбу»;
- застосування надгортанного повітропроводу;
- ендотрахеальна інтубація.
Цей підхід наголошує на необхідності адаптивності у складних ситуаціях, пов’язаних із забезпеченням прохідності дихальних шляхів, і визнає, що успіх може залежати від вибору та послідовності застосування цих основних способів порятунку життя. |
| Запроваджуючи принцип «максимального зусилля», підхід дозволяє виконувати до трьох спроб кожного способу, доповнених можливими ключовими змінами (оптимізаційними кроками). Така гнучкість враховує динамічний характер забезпечення прохідності дихальних шляхів і підкреслює потребу в адаптивності для досягнення альвеолярної оксигенації. |
| Підхід VORTEX також враховує людський фактор, замінюючи поняття «невдача» на концепцію «вичерпний комплекс дій». Це знижує психологічний тиск, сприяє ефективній комунікації в бригаді та підтримує процес ухвалення рішень. Успішне забезпечення прохідності дихальних шляхів визначається не лише технічними навичками, а й створенням підтримувального та адаптивного середовища. |
“Зона безпеки” У ПІДХОДІ VORTEX
“Зона безпеки” у підході VORTEX визначається як етап забезпечення прохідності дихальних шляхів, на якому підтверджено адекватну альвеолярну оксигенацію та відсутня безпосередня загроза критичної гіпоксії.
Вхід у “зону безпеки” підтверджується сталою кривою ETCO₂ або зростанням показників SpO₂, зокрема при використанні ендотрахеальної трубки. Адекватність оцінюється не за фіксованим числовим значенням, а за ризиком розвитку короткочасної гіпоксії, абсолютний показник SpO₂ залежить від клінічного контексту.
 Вхід у “зону безпеки” не є тотожним нормалізації SpO₂. Перебуваючи у “зоні безпеки”, команда може залишатися на поточному методі забезпечення оксигенації, оптимізувати його чи обрати альтернативний. У “зоні безпеки” допускається підтримання поточного способу порятунку життя, його заміна або перехід на інший. Додатково здійснюється підготовка персоналу, обладнання, за потреби — зміна місця надання допомоги.
Вхід у “зону безпеки” не є тотожним нормалізації SpO₂. Перебуваючи у “зоні безпеки”, команда може залишатися на поточному методі забезпечення оксигенації, оптимізувати його чи обрати альтернативний. У “зоні безпеки” допускається підтримання поточного способу порятунку життя, його заміна або перехід на інший. Додатково здійснюється підготовка персоналу, обладнання, за потреби — зміна місця надання допомоги.
Вихід із “зони безпеки” («пробудження пацієнта») можливий лише у випадку підтвердження адекватної альвеолярної оксигенації. Вихід означає відновлення пацієнтом самостійної прохідності дихальних шляхів і самостійної вентиляції з мінімальною допомогою. Такий вихід є стратегією зниження рівня підтримки при веденні складних дихальних шляхів. Вихід не допускається у випадках перебування пацієнта у «воронці» підходу VORTEX, коли адекватну оксигенацію не підтверджено.
“Зона безпеки” у підході VORTEX є критичним етапом забезпечення прохідності дихальних шляхів. Перебування у цій зоні гарантує безпеку пацієнта, створює умови для оптимізації, планування та мобілізації ресурсів. Рішення щодо виходу або подальшого перебування приймається з урахуванням клінічної ситуації та контексту.
| “ЗОНА БЕЗПЕКИ”: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| “Зона безпеки” досягається після підтвердження адекватної альвеолярної оксигенації. Критеріями є наявність сталої кривої ETCO2 або зростання показників SpO2, зокрема при використанні ендотрахеальної трубки. |
| Вхід у “зону безпеки” не є тотожним нормалізації SpO2. Підвищені показники сатурації можуть утримуватися й поза “зоною безпеки” внаслідок преоксигенації чи інших чинників. |
| Перебування у “зоні безпеки” створює умови для оптимізації сатурації та альвеолярної оксигенації, а також для прийняття подальших рішень: залишатися на поточному методі забезпечення оксигенації, оптимізувати його, обрати альтернативний чи свідомо вийти із "зони безпеки". |
| На цьому етапі допускається мобілізація ресурсів: підготовка персоналу, обладнання, а також, у разі необхідності, зміна місця надання допомоги. Це дозволяє здійснити повну підготовку до подальших втручань. |
| Вихід зі “зони безпеки” («пробудження пацієнта») є допустимим лише після підтвердження здатності до підтримання альвеолярної оксигенації. Це рішення має прийматися виважено і тільки у випадку, коли оксигенація підтверджена. В інших ситуаціях, особливо у «воронці» підходу VORTEX, де альвеолярна оксигенація відсутня, вихід не допускається. |
Основні методи забезпечення прохідності дихальних шляхів
У забезпеченні прохідності дихальних шляхів успішне застосування трьох основних способів порятунку життя — вентиляції маскою з мішком «Амбу», використання надгортанного повітропроводу та ендотрахеальної інтубації — є рівнозначно ефективним для досягнення головної мети: забезпечення альвеолярної оксигенації.
Ці стратегії відрізняються здатністю виконувати другорядні завдання, зокрема: захист дихальних шляхів, стабілізацію їхньої прохідності та виведення CO₂. Другорядні цілі залишаються важливими, однак втрачають значення, якщо не забезпечено основну — альвеолярну оксигенацію.
У стандартних умовах вибір методу забезпечення прохідності дихальних шляхів здійснюється з урахуванням як основних, так і другорядних завдань, обумовлених клінічною ситуацією. У складних випадках другорядні завдання можуть відходити на другий план задля досягнення головної мети — підтримання адекватної альвеолярної оксигенації.
Підхід VORTEX надає лікареві та бригаді можливість починати забезпечення прохідності дихальних шляхів із найбільш доцільного способу залежно від клінічного контексту. Якщо перші спроби встановлення альвеолярної оксигенації є утрудненими, інші способи можуть застосовуватись у будь- якій послідовності, що відповідає ситуації. Така гнучкість робить підхід VORTEX придатним у будь-якому клінічному середовищі.
Термін «максимальне зусилля» означає, що для кожного способу виконано всі доступні дії для входу у зону безпеки. Допускається до трьох спроб для кожного способу з можливим застосуванням ключової зміни (оптимізаційного кроку). Конкретні оптимізації та кількість спроб визначаються клінічним контекстом, але завжди у межах принципів підходу VORTEX.
Оптимізаційні кроки поділяють на п’ять категорій і застосовують однаково до всіх трьох способів забезпечення прохідності дихальних шляхів. Їхня мета — забезпечити максимально швидкий і ефективний вхід у “зону безпеки”, використовуючи найдоцільніші для конкретної ситуації дії.

Рисунок 4. Підхід VORTEX — категорії оптимізації (Chrimes, 2024)
Спроби включають введення та видалення ларингоскопа під час ендотрахеальної інтубації, введення та видалення надгортанного повітропроводу, а також накладання та зняття кисневої маски з метою забезпечення альвеолярної вентиляції.
У випадках, коли відсутність негайного доступу до персоналу, обладнання чи медикаментів перешкоджає проведенню критично важливих оптимізацій у межах трьох дозволених спроб, підхід VORTEX допускає одну додаткову спробу в межах обраного способу забезпечення прохідності дихальних шляхів, якщо застосована стратегія оптимізації розцінюється як ключова зміна (оптимізаційний крок). Такі ключові зміни повинні суттєво підвищувати ймовірність досягнення ”зони безпеки” без подовження періоду гіпоксії.
ЛЮДСЬКИЙ ФАКТОР І ПРИНЦИП “МАКСИМАЛЬНОГО ЗУСИЛЛЯ”
Підхід VORTEX враховує психологічний тиск, який виникає при оголошенні «невдачі». Замість цього застосовується термін «вичерпний комплекс дій» як кінцева точка спроб забезпечення альвеолярної оксигенації будь-яким способом забезпечення прохідності дихальних шляхів. Цей термін означає, що подальші спроби за даним способом є безрезультатними, водночас підкреслює, що лікар використав усі можливості, доступні з огляду на анатомічні, клінічні та ситуаційні чинники.
Очікується, що лікареві легше зафіксувати «вичерпане максимальне зусилля» під час інтубації, ніж констатувати «невдачу». У разі, коли спроба була вичерпана, але альвеолярна оксигенація не відновлена, слід негайно переходити до альтернативних стратегій, включно з виконанням крікотироїдотомії (Neck Rescue), після вичерпання всіх методів доступу через верхні дихальні шляхи.
| Людський фактор і принцип «максимального зусилля»: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| Підхід VORTEX підкреслює рівнозначну ефективність трьох способів забезпечення прохідності дихальних шляхів — вентиляції маскою з мішком «Амбу», застосування надгортанного повітропроводу та ендотрахеальної інтубації — для досягнення альвеолярної оксигенації. Водночас ці методи різняться здатністю забезпечувати другорядні цілі, зокрема захист дихальних шляхів та елімінацію CO2, що вимагає стратегічної адаптації залежно від клінічних викликів. |
| У рутинних умовах забезпечення прохідності дихальних шляхів стратегії обирають відповідно до основних і другорядних завдань. Підхід VORTEX надає гнучкість, дозволяючи лікарю чи бригаді почати з найбільш доцільного методу. У складних ситуаціях, коли досягнення альвеолярної оксигенації утруднене, гнучкий підхід дозволяє послідовно застосовувати різні методи, що робить VORTEX універсально застосовним. |
| Термін «максимальне зусилля» означає, що використано всі доступні дії для входу у “зону безпеки”. Для кожного методу допускається до трьох спроб із можливим застосуванням ключової зміни (оптимізаційного кроку). Оптимізаційні дії, поділені на п’ять категорій та обрані відповідно до клінічного контексту, є ключовими для ефективного забезпечення альвеолярної оксигенації у складних умовах. |
| Якщо відсутній негайний доступ до ресурсів, підхід VORTEX дозволяє одну додаткову спробу за умови, що застосована дія є ключовою зміною. Така зміна має суттєво підвищувати ймовірність досягнення “зони безпеки” без подовження періоду гіпоксії. Використання маркованих наборів для екстреного забезпечення дихальних шляхів, інтегрованих у підхід VORTEX, підвищує ефективність і сприяє оптимізації дій. |
| З урахуванням психологічних аспектів, підхід VORTEX замінює поняття «невдача» на «вичерпане максимальне зусилля». Така зміна зменшує бар’єри, підтверджуючи, що лікар використав усі можливості в межах ситуаційних обмежень. Акцент робиться на ефективній комунікації в бригаді та прийнятті рішень для подолання проблем із дихальними шляхами. |
| Якщо після вичерпаної максимальної спроби будь-яким методом забезпечення прохідності дихальних шляхів альвеолярна оксигенація не відновлена, необхідно переходити до альтернативних стратегій. Це включає виконання екстреного хірургічного доступу до дихальних шляхів, якщо всі методи ведення верхніх дихальних шляхів вичерпані. Підхід VORTEX визнає, що успіх визначається не лише технічними навичками, а й наявністю підтримувального та адаптивного середовища, що є суттю ефективного забезпечення прохідності дихальних шляхів. |
ЧАСТИНА 2: ШВИДКА ПОСЛІДОВНА ІНТУБАЦІЯ: СТРУКТУРОВАНИЙ ПІДХІД
ВСТУП
Швидка послідовна інтубація (RSI), яку також називають швидкою послідовною індукцією, є процедурою високого ризику, що зазвичай виконується в умовах невідкладної допомоги та інтенсивної терапії для забезпечення прохідності дихальних шляхів у пацієнтів у критичному стані, які потребують термінової ендотрахеальної інтубації (Biban & Gaffuri, 2013)6. Процедура включає швидке введення фармакологічних препаратів та виконання технічних маніпуляцій для безпечного й ефективного проведення інтубації (Rocchio та ін., 2017)7. Швидка послідовна інтубація (RSI) вважається стандартом надання допомоги пацієнтам, які потребують інтубації трахеї в умовах невідкладної допомоги та інтенсивної терапії, за винятком крайніх ситуацій, таких як зупинка серця (Biban & Gaffuri, 2013)1. Процедура має вирішальне значення для профілактики аспірації шлункового вмісту та для забезпечення адекватної оксигенації і вентиляції у пацієнтів із порушеною прохідністю дихальних шляхів (Higgs та ін., 2018)8.
Клінічні настанови та протоколи відіграють ключову роль у стандартизації проведення швидкої послідовної інтубації для підвищення безпеки пацієнтів і покращення результатів лікування. У контексті транспортування пацієнтів у критичному стані в Україні ці настанови охоплюють: підготовку мультидисциплінарної бригади, модифіковану оцінку дихальних шляхів, методи преоксигенації, гемодинамічне забезпечення, застосування швидкої послідовної індукції, оптимальні методи ларингоскопії та ведення особливих клінічних ситуацій (Higgs та ін., 2018)3.
Настанови підкреслюють важливість системного підходу до швидкої послідовної інтубації для мінімізації ускладнень та підвищення частоти успішних інтубацій (Higgs та ін., 2018)3. Вибір індукційних препаратів у цьому процесі є критичним клінічним рішенням, що впливає на прогноз для пацієнта. Дослідження порівнювали різні фармакологічні засоби, які застосовуються для швидкої послідовної інтубації, для оцінки їхньої ефективності та профілю безпечності (Marsch та ін., 2011; Sluga та ін., 2005; Jhou та ін., 2020)9. Ці дослідження підтверджують необхідність ретельного вибору препаратів і доз залежно від стану пацієнта, наявності супутніх захворювань і терміновості інтубації.
6 Biban, P. and Gaffuri, M. (2013). Premedication for tracheal intubation. Pediatric Critical Care Medicine, 14(4), 441-442. https://doi. org/10.1097/pcc.0b013e31827d1637
7 Rocchio, M., Sylvester, K. W., Beik, N., Glasser, N., & Szumita, P. M. (2017). Retrospective review of propofol versus etomidate during rapid sequence intubation in the emergency department at a tertiary academic center. Pharmacology &Amp;amp; Pharmacy, 08(07), 231-241. https://doi.org/10.4236/pp.2017.87016
8 Higgs, A., McGrath, B. A., Goddard, C. R., Rangasami, J., Suntharalingam, G., Gale, R., … & Cook, T. (2018). Guidelines for the management of tracheal intubation in critically ill adults. British Journal of Anaesthesia, 120(2), 323-352. https://doi.org/10.1016/j.bja.2017.10.021
9 Marsch, S., Steiner, L. A., Bucher, E., Pargger, H., Schumann, M., Aebi, T., … & Siegemund, M. (2011). Succinylcholine versus rocuronium for rapid sequence intubation in intensive care: a prospective, randomized controlled trial. Critical Care, 15(4), R199. https://doi.org/10.1186/ cc10367
Сучасні дослідження спрямовані на підвищення безпеки та ефективності швидкої послідовної інтубації (RSI ) шляхом вивчення альтернативних стратегій і технік забезпечення прохідності дихальних шляхів. Зокрема, тактика з використанням назальної канюлі високого потоку досліджується як метод апное- оксигенації під час інтубації у пацієнтів у критичному стані, і продемонструвала перспективні результати у покращенні оксигенації та клінічних результатів. Крім того, програми постійного вдосконалення якості впроваджені для підвищення безпеки швидкої послідовної інтубації у відділеннях невідкладної допомоги, що дозволило знизити частоту невдалих інтубацій та несприятливих подій (Sakles та ін., 2019)10.
Узагальнюючи, швидка послідовна інтубація є критичним втручанням в умовах невідкладної допомоги та інтенсивної терапії, необхідним для забезпечення адекватного контролю дихальних шляхів у пацієнтів у критичному стані. Клінічні настанови, наукові дослідження та програми підвищення якості відіграють ключову роль у стандартизації та оптимізації практики проведення швидкої послідовної інтубації з метою покращення результатів лікування та підвищення безпеки пацієнтів.
Чек-листи та роль людського фактора
Використання чек-листів при веденні пацієнтів у критичному стані та під час проведення швидкої послідовної інтубації (RSI ) має вирішальне значення для зменшення впливу людського фактора та підвищення безпеки пацієнтів. Дані численних досліджень підтверджують ефективність чек-листів у зниженні кількості помилок та покращенні результатів під час проведення негайних втручань.
Передусім чек-листи забезпечують стандартизований підхід до виконання процедур інтенсивної терапії, що гарантує дотримання системного й послідовного процесу під час проведення швидкої послідовної інтубації, як зазначають Stollings та ін. (2013)11. Чітке визначення кроків та ключових аспектів зменшує варіабельність у практиці та сприяє дотриманню найкращих клінічних стандартів.
В умовах високого стресу, зокрема у відділеннях інтенсивної терапії та під час надання невідкладної допомоги, ефективна комунікація та узгодженість дій мультидисциплінарної команди мають критичне значення для досягнення позитивних результатів. Чек-листи виступають інструментом комунікації, що забезпечує синхронізацію дій усіх членів команди при проведенні швидкої послідовної інтубації (Yeung & Zed, 2002)12.
Негайні втручання, такі як швидка послідовна інтубація, супроводжуються високим когнітивним навантаженням на медичних працівників, що підвищує ризик помилок. Чек-листи знижують когнітивне навантаження, надаючи структуровані підказки й нагадування, тим самим зменшуючи ймовірність пропуску кроків або помилкових дій (Sharda & Bhatia, 2022)13. Додатково чек-листи узгоджуються з чинними настановами та протоколами, інтегруючи ключові рекомендації й заходи безпеки, що підвищує дотримання доказових практик і покращує якість медичної допомоги.
Людські фактори, зокрема відволікання або когнітивні викривлення, є суттєвими ризиками при виконанні складних процедур високого ризику, таких як швидка послідовна інтубація. Чек-листи виконують роль «захисної сітки», допомагаючи своєчасно виявити й усунути потенційні ризики, що зменшує ймовірність виникнення несприятливих подій (Lyon та ін., 2015)14.
Крім того, чек-листи мають важливе значення як навчальний інструмент для медичного персоналу, особливо для фахівців, які тільки розпочинають роботу в умовах інтенсивної терапії або вперше виконують швидку послідовну інтубацію. Регулярне ознайомлення з чек-листами та відпрацювання їхніх компонентів підвищує готовність та впевненість медичних працівників у ситуаціях, що потребують негайних втручань.
Узагальнюючи, інтеграція чек-листів у практику інтенсивної терапії та при проведенні швидкої послідовної інтубації є обов’язковою умовою для оптимізації процесів, покращення комунікації й роботи мультидисциплінарної команди, зниження ризику помилок та підвищення безпеки пацієнтів. Використання чек-листів дозволяє ефективно працювати у складних і стресових умовах та гарантує надання оптимальної допомоги пацієнтам у критичному стані.
ЧЕК-ЛИСТ ШВИДКОЇ ПОСЛІДОВНОЇ ІНТУБАЦІЇ SOAP-ME: A2 (див. Додаток 10)
Чек-лист A2: SOAP-ME застосовується для виконання швидкої послідовної інтубації. Він розроблений на основі наявних наукових даних та клінічного досвіду, коли відсутні переконливі докази. Безпечне та ефективне проведення швидкої послідовної інтубації вимагає чіткої взаємодії мультидисциплінарної команди та охоплює низку потенційно складних етапів. Їх виконання потребує практичних навичок від окремих учасників, а також ефективної комунікації та узгодженої співпраці в команді. Нижче наведено основні розділи чек-листа.
АСПІРАЦІЯ
Під час екстреної анестезії та втручань на дихальних шляхах можливе ускладнення — масивна регургітація шлункового вмісту з ризиком аспірації в легені, що може призвести до тяжких порушень дихання та підвищити ризик смерті. Суттєву небезпеку аспірації становлять також інтенсивні кровотечі у верхні дихальні шляхи, особливо при травмах обличчя.
Щоб завчасно запобігти подібним ускладненням, вирішальне значення має ретельна підготовка до процедури.

Для своєчасного передбачення та ефективного контролю цього ускладнення необхідно мати повністю підготовлений та доступний аспіратор. Аспіратор повинен бути оснащений катетерами великого діаметра для забезпечення ефективної аспірації. Важливо, щоб аспіратор був у робочому стані та розташований біля голови пацієнта для можливості негайного втручання у випадку регургітації.
14 Lyon, R., Perkins, Z., Chatterjee, D., Lockey, D., & Russell, M. Q. (2015). Significant modification of traditional rapid sequence induction improves safety and effectiveness of pre-hospital trauma anaesthesia. Critical Care, 19(1). https://doi.org/10.1186/s13054-015-0872-2
Крім того, за наявності ресурсів доцільно підготувати другий аспіратор. Резервний аспіратор виступає додатковим заходом безпеки та гарантує, що медичний персонал матиме належне оснащення для реагування на непередбачувані ускладнення під час проведення процедури. Такий проактивний підхід до забезпечення прохідності дихальних шляхів та підготовки обладнання суттєво підвищує безпеку пацієнта та покращує результати лікування в умовах невідкладної допомоги.
ПРЕОКСИГЕНАЦІЯ
Преоксигенація є критично важливим етапом підготовки при проведенні швидкої послідовної інтубації у пацієнтів у критичному стані. Її метою є подовження безпечного періоду апное після медикаментозної індукції, запобігаючи розвитку десатурації та забезпечуючи підтримання прохідності дихальних шляхів. Найбільш поширеною стратегією преоксигенації у відділенні інтенсивної терапії є забезпечення пацієнта з адекватним спонтанним диханням високопоточною подачею кисню через стандартну кисневу маску з резервуаром протягом щонайменше 3 хвилин. Пацієнти з недостатнім спонтанним диханням, яким необхідна вентиляція за допомогою мішка “Амбу”, також мають отримувати високопоточний кисень через цей пристрій. Принципово важливо уникати ситуації, коли пацієнт змушений робити вдих проти опору мішка «Амбу». Пацієнти, які продовжують дихати спонтанно, але з недостатнім дихальним об’ємом або частотою, потребують проведення допоміжної вентиляції за допомогою мішка “Амбу”. Це вимагає належних навичок і повної концентрації медичного працівника, відповідального за виконання цієї функції.

Додавання до мішка регульованого клапана позитивного тиску в кінці видиху може бути корисним для деяких груп пацієнтів, проте, як і у випадку з усіма іншими заходами у відділеннях інтенсивної терапії, потенційна користь має ретельно зважуватися з урахуванням можливих побічних ефектів, особливо у пацієнтів з гіповолемією.
Розширені методи преоксигенації часто є необхідними для пацієнтів з гострою гіпоксемічною дихальною недостатністю через часто знижену функціональну залишкову ємність легень та виражене порушення відповідності вентиляції та перфузії, що знижує ефективність традиційних методів преоксигенації.
Киснева терапія через носові канюлі високого потоку та неінвазивна вентиляція з позитивним тиском стали альтернативними стратегіями преоксигенації для пацієнтів, які потребують швидкої послідовної інтубації, особливо у випадках, коли очікується складність інтубації або спостерігається тяжка гіпоксемія (PaO₂/FiO₂ < 150). Киснева терапія через носові канюлі високого потоку подає кисень на високих потоках, імітуючи фізіологічні переваги неінвазивної вентиляції з позитивним тиском, зокрема розширення об’єму легень під час видиху. Водночас існують занепокоєння щодо потенційного ризику потрапляння повітря до шлунку при використанні цієї методики через безперервну подачу кисню під час дихального циклу.
Дослідження, що порівнюють методики преоксигенації, продемонстрували різні рівні десатурації кисню, і деякі з них вказують на нижчу частоту десатурації при застосуванні кисневої терапії через носові канюлі високого потоку порівняно з традиційною преоксигенацією через кисневу маску. Крім того, киснева терапія через носові канюлі високого потоку виявилася ефективною у підтриманні рівня сатурації кисню та подовженні безпечного апное, особливо в пацієнтів із тяжкою гіпоксемією. Хоча деякі дослідження зафіксували зниження рівня десатурації при використанні цієї методики, інші відзначили подібну ефективність у порівнянні з неінвазивною вентиляцією з позитивним тиском15.
Наявні докази залишаються непереконливими щодо впливу методів преоксигенації на шлункову інсуфляцію або ризик аспірації, оскільки наявні дані обмежені й не дозволяють зробити однозначні висновки. Так само зв’язок між різними методами преоксигенації та частотою тяжких ускладнень або зупинки серця характеризується дуже низькою якістю доказів, що унеможливлює формування остаточних наукових висновків10.
Підсумовуючи, неінвазивна вентиляція з позитивним тиском демонструє більш переконливі докази ефективності у зменшенні критичних випадків десатурації у пацієнтів із тяжкою гіпоксемією під час RSI , однак виникають побоювання щодо можливого надходження повітря до шлунка та підвищеного ризику регургітації вмісту шлунка. Натомість киснева терапія через носові канюлі високого потоку забезпечує безперервну подачу кисню під час ларингоскопії, що робить її привабливою альтернативою. Також її можна поєднувати зі стандартною преоксигенацією за допомогою кисневої маски з резервуаром, за умови наявності двох окремих джерел кисню.
Попри наявні докази, залишаються суттєві прогалини в дослідженнях щодо визначення оптимальної стратегії преоксигенації для пацієнтів із труднощами при забезпеченні прохідності дихальних шляхів або при тривалих інтубаціях, а також для осіб із тяжкою гострою гіпоксемічною дихальною недостатністю. Необхідні подальші дослідження для удосконалення протоколів преоксигенації та адаптації втручань відповідно до індивідуальних ризиків пацієнтів з метою оптимізації результатів під час критичних процедур, таких як RSI.
| Забезпечення прохідності дихальних шляхів: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| Спонтанне дихання через кисневу маску з високим потоком протягом 3 хвилин |
| Преоксигенацію за допомогою кисню через носові канюлі високого потоку рекомендовано, якщо передбачається складність при ларингоскопії |
| Преоксигенація з використанням NIPPV рекомендована для пацієнтів із тяжкою гіпоксемією (PaO2/FiO2 < 150) |
| Вентиляція за допомогою мішка Амбу з лицевою маскою може розглядатися як стандартна техніка преоксигенації під час процедур |
15 Acquisto NM, Mosier JM, Bittner EA, Patanwala AE, Hirsch KG, Hargwood P, Oropello JM, Bodkin RP, Groth CM, Kaucher KA, Slampak- Cindric AA, Manno EM, Mayer SA, Peterson LN, Fulmer J, Galton C, Bleck TP, Chase K, Heffner AC, Gunnerson KJ, Boling B, Murray MJ. Society of Critical Care Medicine Clinical Practice Guidelines for Rapid Sequence Intubation in the Critically Ill Adult Patient. Crit Care Med. 2023 Oct 1;51(10):1411-1430. doi: 10.1097/CCM.0000000000006000. Epub 2023 Sep 14. PMID: 37707379
ДИХАЛЬНІ ШЛЯХИ
Цей чатсина СОП зосереджений на підготовці матеріалів, необхідних для інтубації. Одним із ключових аспектів, який слід врахувати, є використання відеоларингоскопів під час процедури.

ЛАРИНГОСКОП VS. ВІДЕОЛАРИНГОСКОП
Ендотрахеальна інтубація залишається складним, але критично важливим етапом при виконанні швидкої послідовної інтубації. Навіть в умовах операційної, за даними досліджень, лікарям-інтернам з анестезіології знадобилося щонайменше 125 інтубацій для досягнення 95% успіху з першої спроби. Це підтверджує, що метод вимагає значного досвіду та систематичного навчання. На основі доступних доказів, що порівнюють використання ларингоскопів та відеоларингоскопів, рекомендовано надавати перевагу відеоларингоскопам як основному інструменту для інтубації у користувачів із недостатнім досвідом. Кілька досліджень довели, що відеоларингоскопи забезпечують кращу візуалізацію голосової щілини, вищу частоту успішної інтубації у складних випадках та знижують ризик ускладнень у порівнянні зі звичайними ларингоскопами. Водночас варто враховувати, що існують різні типи відеоларингоскопів із технічними відмінностями. Вони потребують спеціальної підготовки користувачів та розуміння їхніх обмежень, зокрема у випадках наявності крові у дихальних шляхах, що може ускладнювати візуалізацію. За даними Simon та ін. (2016)16 використання відеоларингоскопів суттєво підвищувало відсоток успішних інтубацій з першої спроби, особливо у пацієнтів зі складними дихальними шляхами чи обмеженою рухливістю шийного відділу. Аналогічно, систематичний огляд Vink та ін. (2006)17 підтвердив переваги відеоларингоскопів у складних клінічних сценаріях, наголошуючи на кращій візуалізації та вищій частоті успішної інтубації. Враховуючи сукупність наявних доказів, відеоларингоскопи слід розглядати як пріоритетний інструмент для ендотрахеальної інтубації в умовах надання невідкладної допомоги в Україні.
| Дихальні шляхи: основна рекомендація |
| За наявності, основною рекомендацією є використання відеоларингоскопа для проведення процедури. |
16 Simon, M., Wachs, C., Braune, S., Heer, G. d., Frings, D., & Kluge, S. (2016). High-flow nasal cannula versus bag-valve-mask for preoxygenation before intubation in subjects with hypoxemic respiratory failure. Respiratory Care, 61(9), 1160-1167. https://doi. org/10.4187/respcare.04413
17 Winck, J., Azevedo, L. F., Costa‐Pereira, A., Antonelli, M., & Wyatt, J. (2006). Untitled. Critical Care, 10(2), R69. https://doi.org/10.1186/ cc4905
Положення пацієнта
Цей розділ стандартних операційних процедур охоплює два ключові аспекти: оптимізацію положення пацієнта для інтубації та впровадження стратегії «10 для 10» у роботі мультидисциплінарної команди з метою чіткого визначення ролей. Стратегія «10 для 10» спрямована на зниження напруження в умовах швидкого розвитку або потенційно критичної ситуації. Такий підхід ґрунтується на обґрунтованому прийнятті рішень і завчасному плануванні різних сценаріїв для забезпечення готовності. Він є оптимальним інструментом для комунікації, делегування завдань та розподілу ролей, що сприяє ефективній взаємодії та чіткому переходу в умовах високого тиску.
Стратегія “10 для 10” передбачає: зробити паузу на 10 секунд перед початком втручання, щоб чітко розподілити ролі, узгодити резервні сценарії та забезпечити готовність до дій. Це дозволяє значно підвищити ефективність реагування упродовж наступних 10 хвилин критичної ситуації.

Положення пацієнта
У сфері забезпечення прохідності дихальних шляхів положення пацієнта під час ендотрахеальної інтубації є критичним чинником, що може суттєво впливати на успішність процедури. Порівняльна оцінка положень голови при ларингоскопії, зокрема положення голови для візуалізації голосової щілини, простого розгинання та гіперрозгинання, була предметом численних досліджень, спрямованих на визначення оптимального положення для покращення результатів інтубації. Дослідження Hadhoud (2023)18 надало цінні дані щодо впливу різних положень голови на якість огляду гортані, тривалість інтубації та складність виконання прямої ларингоскопії у дорослих пацієнтів. Результати досліджень Shende & Shidhaye (2016)19, Bhattarai та ін. (2012)20, Park та ін. (2014)21 послідовно підтверджують перевагу положення голови для візуалізації голосової щілини щодо кращої візуалізації голосової щілини та полегшення інтубації у порівнянні з іншими положеннями голови. Ці висновки підкреслюють важливість правильного позиціонування пацієнта з метою удосконалення практики інтубації, особливо у складних клінічних сценаріях, що пов’язані із супутньою патологією або анатомічними особливостями. Беручи до уваги наведені дослідження, положення голови для візуалізації голосової щілини розглядається як рекомендований варіант для досягнення оптимальної візуалізації голосової щілини, підвищення успішності інтубації та ефективності процедури прямої ларингоскопії у дорослих пацієнтів, за винятком випадків підтвердженої або ймовірної нестабільності шийного відділу хребта. У таких випадках шию необхідно утримувати у нейтральному положенні з проведенням мануальної стабілізації під час процедури швидкої послідовної інтубації. Безпечна інтубація у цієї категорії пацієнтів належить до компетенції спеціалістів і потребує високого рівня професійної підготовки.
18 Hadhoud, Y. H., Baraka, M. A., Saleh, M., & Refaat, A. M. (2023). A comparative evaluation of the sniffing, the simple head extension and the head hyperextension positions for laryngoscopic view and intubation difficulty in adults undergoing direct laryngoscopy. European Archives of Oto-Rhino-Laryngology, 281(3), 1401-1407. https://doi.org/10.1007/s00405-023-08386-y
19 Shende, S. and Shidhaye, R. V. (2016). Evaluation of laryngoscopic view, intubation difficulty and sympathetic response during direct laryngoscopy in sniffing position versus simple head extension: a clinical comparative study. International Journal of Medical Research and Review, 4(9), 1531-1537. https://doi.org/10.17511/ijmrr.2016.i09.03
20 Bhattarai, B., Shrestha, S. R., & Kandel, S. (2012). Comparison of sniffing position and simple head extension for visualization of glottis during direct laryngoscopy.. Kathmandu Cambridge Medical Journal, 9(1), 58-63. https://doi.org/10.3126/kumj.v9i1.6265
21 Park, S. W., Lee, K., Jang, M., Jung, J., Lee, B., & Kang, J. (2014). Age and gender are important considerations in choosing the sniffing position for laryngoscopic view. International Journal of Medical Sciences, 11(12), 1258-1261. https://doi.org/10.7150/ijms.858
| Забезпечення прохідності дихальних шляхів: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| Розміщуйте пацієнта для ендотрахеальної інтубації у покращене положення для голови для візуалізації голосової щілини, якщо немає протипоказань. |
| Використовуйте інструменти командної роботи, зокрема стратегію «10 для 10». |
| Завжди готуйте план Б і план В. |
МЕДИКАМЕНТОЗНА ПІДГОТОВКА
У цьому розділі чек-листа основна увага приділяється підготовці медикаментів і вибору відповідних лікарських засобів для процедури. Далі в межах СОП описано три окремі альтернативні алгоритми. Детальні характеристики кожного з препаратів розглядаються нижче.

СЕДАТИВНІ ПРЕПАРАТИ
Вибір відповідних індукційних препаратів для проведення швидкої послідовної інтубації у пацієнтів у критичному стані має ключове значення, оскільки гіпотензія в період інтубації22 асоціюється зі збільшенням захворюваності та смертності. Ідеальний седативно-гіпнотичний засіб для проведення швидкої послідовної інтубації повинен знижувати ризик розвитку гіпотензії та водночас забезпечувати ефективне виконання інтубації. При оцінці ефективності та безпечності етомідату, кетаміну, мідазоламу та пропофолу як індукційних засобів слід ретельно враховувати їхній вплив на гемодинаміку, фармакокінетичні характеристики та клінічні результати, включно з рівнем смертності, частотою гіпотензії та потребою у вазопресорній підтримці.
Кетамін
Кетамін завдяки своїм симпатоміметичним властивостям є доцільним препаратом для підтримання гемодинамічної стабільності під час швидкої послідовної інтубації. Крім того, він забезпечує виражений аналгетичний ефект, що дозволяє зменшити потребу в опіоїдах. Однак у пацієнтів у критичному стані з виснаженими запасами катехоламінів застосування кетаміну може підвищувати ризик розвитку гіпотензії та зупинки серця. Наявні докази свідчать про неоднозначні результати: у деяких клінічних умовах використання кетаміну, порівняно з етомідатом, асоціювалося з меншою частотою гіпотензії23, однак у різних дослідженнях ці результати були варіабельними. Таким чином, доцільність застосування кетаміну під час проведення швидкої послідовної інтубації слід оцінювати з урахуванням загального клінічного стану пацієнта та його основної патології.
Мідазолам
Хоча мідазолам має седативні та анксіолітичні властивості, його фармакокінетичний профіль, що характеризується повільнішим початком дії та вираженим судинорозширювальним ефектом, може обмежувати його придатність як препарату першої лінії для індукції ШВЛ у критичних пацієнтів. Ризик розвитку гіпотензії під впливом мідазоламу, у поєднанні з повільною дією, свідчить про необхідність обережного підходу до його використання при невідкладних станах. Проте низькі дози мідазоламу в комбінації з кетаміном можуть бути дуже корисними.
Пропофол
Незважаючи на сприятливі фармакокінетичні характеристики пропофолу, зокрема швидкий початок дії та коротку тривалість ефекту, його схильність до спричинення вираженої гіпотензії суттєво обмежує його застосування у критично хворих пацієнтів. Наявні докази, що вказують на зв’язок між застосуванням пропофолу для індукції ШВЛ та підвищеним ризиком серцево-судинного колапсу і летальності, підкреслюють необхідність ретельного відбору пацієнтів та моніторингу під час прийняття рішення щодо використання пропофолу як індукційного засобу в цій групі високого ризику.
22 Russotto V, Nainan Myatra S, Laffey JG, et al.: Intubation practices and adverse peri-intubation events in critically ill patients from 29 countries. JAMA 2021; 325:1164-1172
23 Van Berkel MA, Exline MC, Cape KM, et al.: Increased incidence of clinical hypotension with etomidate compared to ketamine for intubation in septic patients: A propensity matched analysis. J Crit Care 2017; 38:209-214
СЕДАЦІЯ ПЕРШОЇ ЛІНІЇ: ПРОПОФОЛ + КЕТАМІН ДЛЯ ГЕМОДИНАМІЧНО СТАБІЛЬНИХ ПАЦІЄНТІВ
Пропофол – це потужний седативний та анестезуючий засіб, відомий своєю швидкою дією та короткою Пропофол — це потужний седативний та анестезуючий засіб, відомий своїм швидким початком дії та короткою тривалістю ефекту. Він забезпечує глибоку седацію та швидку анестезію, що робить його ідеальним для короткочасних процедур, таких як інтубація.
| ЛІНІЯ | Препарат для седації |
| 1 | ПРОПОФОЛ | КЕТАМІН |
| 1 - 2.5 мг/кг | 1 - 2 мг/кг |
Рекомендована початкова доза пропофолу становить 1–2,5 мг/кг внутрішньовенно. Вищі дози забезпечують швидку та глибоку седацію і сприяють плавному забезпеченню прохідності дихальних шляхів під час інтубації.
Кетамін, з іншого боку, є дисоціативним анестетиком, який зберігає рефлекси дихальних шляхів і тонус симпатичної нервової системи, що забезпечує переваги у гемодинамічно стабільних пацієнтів. Він викликає дисоціацію, аналгезію та анестезію без значного пригнічення дихання. Кетамін має особливу цінність у поєднанні з пропофолом у пацієнтів, які є гемодинамічно стабільними, оскільки має тенденцію підвищувати частоту серцевих скорочень і артеріальний тиск — ефекти, які часто є корисними у поєднанні з депресивними властивостями пропофолу. Дозування кетаміну зазвичай становить від 1 до 2 мг/кг, внутрішньовенно.
У поєднанні пропофол і кетамін забезпечують взаємодоповнювальний ефект. Пропофол викликає швидку седацію й анестезію, тоді як кетамін зберігає серцево-судинну стабільність, тим самим запобігаючи гіпотензії та брадикардії, які можуть виникати при застосуванні інших седативних засобів, таких як високі дози бензодіазепінів або опіоїдів. Це поєднання ефективне для забезпечення плавної інтубації без значних гемодинамічних коливань у стабільних пацієнтів.
Повторне введення
Повторне введення пропофолу та кетаміну може бути необхідним для підтримання седації протягом усієї процедури, особливо у складних або тривалих клінічних ситуаціях. Загальне орієнтовне правило — введення повторних болюсів у дозі приблизно 1/5 від початкової, однак корекція дози завжди має проводитися відповідно до реакції пацієнта та клінічного контексту.
Пропофол має коротшу тривалість дії порівняно з кетаміном, проте обидва препарати чинять синергічний вплив на глибину седації. Тому додаткові дози можуть вводитися у будь-якій послідовності або навіть разом — залежно від клінічних обставин.
Для додаткової інформації щодо седації слід звернутися до СОП, розділ Неврологічний стан.
Основні аспекти:
- Гемодинамічна стабільність: пропофол і кетамін є особливо корисними для пацієнтів зі стабільною гемодинамікою, оскільки кетамін чинить симпатоміметичну стимулюючу дію, яка підтримує артеріальний тиск і частоту серцевих скорочень.
- Початок дії та її тривалість: пропофол діє швидко (початок дії — протягом 30 секунд), що робить його ідеальним для RSI . Ефекти кетаміну також розвиваються швидко, але тривають трохи довше, і в комбінації забезпечують достатній час для плавного проведення інтубації.
- Анестезія та аналгезія: комбінація пропофолу й кетаміну забезпечує як седативну, так і знеболювальну дію, завдяки чому пацієнт залишається без свідомості та не відчуває болю під час процедури.
- Ретельний моніторинг: хоча ця комбінація добре переноситься стабільними пацієнтами, важливо уважно контролювати функцію серцево-судинної системи, насичення киснем і рефлекси дихальних шляхів — для коригування дозування та запобігання ускладненням.
Седація другої лінії: мідазолам + кетамін для пацієнтів із гемодинамічною стабільністю або у стані гемодинамічної компенсації
Коли проведення RSI необхідне для пацієнтів із гемодинамічною стабільністю або у стані гемодинамічної компенсації, седативні й анестезуючі засоби мають підбиратися з обережністю, щоб уникнути значних коливань серцево-судинного статусу при забезпеченні належної седації та анальгезії. У таких випадках комбінація мідазоламу з кетаміном часто використовується як схема індукції другої лінії, особливо коли засоби першої лінії (такі як пропофол і кетамін) є протипоказаними або погано переносяться.
| 2 | МІДАЗОЛАМ | КЕТАМІН |
| 0.1 - 0.15 мг/кг | 1-2 мг/кг |
Мідазолам + Кетамін: взаємодоповнювальна комбінація
Мідазолам — представник бензодіазепінів, який широко використовують через його седативні, амнестичні та міорелаксуючі ефекти. Він є особливо корисним у пацієнтів із компенсованим гемодинамічним станом завдяки здатності викликати седативний ефект і знижувати тривожність без значного пригнічення серцево-судинної системи. Мідазолам забезпечує швидку седацію (протягом 1–3 хвилин), що робить його оптимальним варіантом для коротких процедур, таких як інтубація. Типова доза мідазоламу в комбінації з кетаміном для RSI становить від 0,1 до 0,15 мг/кг внутрішньовенно залежно від маси тіла, віку та клінічного стану пацієнта.
Кетамін, дисоціативний анестетик, застосовується завдяки своїм анальгезивним властивостям і здатності забезпечувати анестезію, при цьому зберігає часткові захисні рефлекси дихальних шляхів і підтримує симпатичний тонус. Це робить кетамін особливо корисним для пацієнтів, яким необхідні і седація, і знеболення при одночасному збереженні стабільної серцево-судинної функції. Кардіостимулюючі ефекти кетаміну — підвищення частоти серцевих скорочень, артеріального тиску та серцевого викиду — є дуже корисними для пацієнтів із гемодинамічною стабільністю або у стані гемодинамічної компенсації, забезпечуючи стабільність під час інтубації.
Як взаємодіють мідазолам і кетамін
Комбінація мідазоламу та кетаміну є особливо вигідною завдяки взаємодоповнювальному характеру їх дії:
- Мідазолам забезпечує ефективну седацію й анестезію, гарантуючи, що пацієнт не усвідомлює проведення процедури й не відчуває тривоги.
- Кетамін забезпечує знеболення й дисоціацію, ефективно блокуючи біль без суттєвого пригнічення дихання. Крім того, кетамін підтримує гемодинаміку, допомагаючи зберігати артеріальний тиск і частоту серцевих скорочень, що особливо важливо для пацієнтів, які можуть не витримати значного гемодинамічного пригнічення, викликаного іншими седативними засобами.
Дозування та корекція дози при подальшому введенні
Типова початкова доза мідазоламу становить 0,1–0,15 мг/кг, і її слід титрувати відповідно до клінічної відповіді пацієнта. Оскільки мідазолам має порівняно тривалий період напіввиведення, його дія може зберігатися й після завершення інтубаційної процедури. Тому ретельний моніторинг є необхідним, щоб гарантувати, що пацієнт не зазнає надмірно тривалої седації.
Кетамін зазвичай вводиться у дозі 1–2 мг/кг внутрішньовенно. Перевагами кетаміну є швидкий початок дії (протягом 30–60 секунд), що сприяє швидкій та ефективній седації перед інтубацією. Ефект триває до 10–20 хвилин. Для підтримки седації може знадобитися додаткове введення кетаміну (наприклад, 0,5 мг/кг).
Основні аспекти:
- Гемодинамічна стабільність: дана комбінація ідеально підходить для пацієнтів з із гемодинамічною стабільністю або у стані гемодинамічної компенсації, оскільки кардіостимулююча дія кетаміну підтримує артеріальний тиск і частоту серцевих скорочень, запобігаючи гіпотензії, яка може виникнути при застосуванні інших седативних засобів.
- Седація та аналгезія: мідазолам забезпечує седацію та анестезію, тоді як кетамін — знеболення та дисоціацію, що робить цю комбінацію збалансованою для проведення інтубації.
- Безперервний моніторинг: попри гарну переносимість цієї комбінації у відносно стабільних пацієнтів, необхідний постійний контроль функції серцево-судинної системи, оксигенації та рефлексів дихальних шляхів, щоб своєчасно коригувати дозування та запобігати ускладненням.
- Висновки: комбінація мідазоламу та кетаміну є збалансованим підходом для пацієнтів з гемодинамічною компенсацією або компенсованим станом, що забезпечує седацію, знеболення та стабільність серцево-судинної системи під час швидкої послідовної інтубації. Обов’язковими є ретельне дозування та постійний моніторинг для забезпечення безпечного та ефективного менеджменту.
Препарат седації третьої лінії: лише кетамін для гемодинамічно декомпенсованих пацієнтів
У випадках гемодинамічної декомпенсації, коли підтримка стабільності гемодинаміки є головним пріоритетом, кетамін сам по собі є привабливим препаратом третьої лінії завдяки своїм унікальним властивостям. На відміну від інших седативних засобів, кетамін може застосовуватись самостійно для ШСІ (швидкої послідовної інтубації) або інших екстрених процедур, особливо коли інші седативні препарати можуть погіршити гемодинамічну нестабільність.
Чому лише кетамін для гемодинамічно декомпенсованих пацієнтів?
У гемодинамічно декомпенсованих пацієнтів — які можуть мати гіпотензію, шок або інші порушення кровообігу — надзвичайно важливо уникати седативних засобів, що часто спричиняють значну серцево-судинну депресію, таких як пропофол або бензодіазепіни. Ці препарати можуть погіршити гіпотензію, ще більше ускладнюючи перфузію життєво важливих органів, особливо враховуючи, що їх потрібно комбінувати з опіоїдами (або кетаміном) для забезпечення аналгезії. Ларингоскопія та ендотрахеальна інтубація є дуже болісними процедурами, тому адекватна аналгезія повинна бути частиною комбінованого медикаментозного підходу під час RSI . Кетамін часто є препаратом вибору в таких випадках через свою унікальну здатність підтримувати серцево-судинну стабільність при одночасному забезпеченні седації та аналгезії.
Симпатоміметичні ефекти: кетамін є дисоціативним анестетиком із симпатоміметичними властивостями, тобто він стимулює вивільнення катехоламінів (таких як норадреналін і адреналін), що призводить до підвищення частоти серцевих скорочень, артеріального тиску та серцевого викиду. Така серцево-судинна підтримка є критично важливою для пацієнтів із нестабільною гемодинамікою, оскільки вона сприяє належній перфузії життєво важливих органів, таких як головний мозок і нирки. Це робить кетамін набагато безпечнішим вибором порівняно з іншими седативними препаратами, які можуть погіршити гіпотензію в цієї вразливої категорії пацієнтів.
Збереження захисних рефлексів дихальних шляхів: кетамін забезпечує аналгезію та седацію без вираженого пригнічення дихання або порушення прохідності дихальних шляхів, що є критично важливим для тяжкохворих пацієнтів із порушеною гемодинамікою. На відміну від седативних засобів, таких як мідазолам або пропофол, кетамін зберігає захисні рефлекси дихальних шляхів, що дозволяє пацієнту певною мірою підтримувати прохідність дихальних шляхів до моменту введення нервово- м’язового блокатора.
Ефективна седація з швидким початком дії: швидкий початок дії кетаміну (в межах 30–60 секунд, хоча у певної групи пацієнтів із зниженим серцевим викидом початок може бути повільнішим) і помірна тривалість дії (10–20 хвилин після одноразової дози) роблять його ідеальним препаратом для RSI в екстрених ситуаціях, забезпечуючи достатній час для забезпечення прохідності дихальних шляхів за умов стабільної гемодинаміки. У пацієнтів з гемодинамічною декомпенсацією така швидка дія забезпечує швидке настання седації із вигідним профілем безпеки без потреби в додаткових препаратах.
Знижений ризик гіпотензії: кардіостимулююча дія кетаміну особливо корисна у випадках гіпотензії або шоку. На відміну від інших седативних препаратів, які можуть поглибити гіпотензію, кетамін частково протидіє вазодилятації, що може погіршити кровообіг. Це робить його особливо ефективним у пацієнтів з низьким артеріальним тиском, шоком або ризиком розвитку органної гіпоперфузії.
Мінімальне пригнічення дихання: на відміну від опіоїдів або бензодіазепінів, кетамін не викликає вираженого пригнічення дихання. Це має критичне значення для гемодинамічно нестабільних пацієнтів, у яких вже може бути порушена дихальна функція. Завдяки підтримці адекватного тонусу дихальних шляхів і дихання до введення нервово-м’язового блокатора кетамін знижує ризик розвитку додаткових ускладнень, таких як аспірація.
Дозування та моніторинг
Для гемодинамічно декомпенсованих пацієнтів типова початкова доза кетаміну для RSI становить 1–2 мг/кг внутрішньовенно з подальшим введенням повторних доз у розмірі ⅕ від початкової, якщо потрібна додаткова седація. Оскільки кетамін має помірну тривалість дії, подальше дозування має ґрунтуватися на клінічній відповіді з ретельним урахуванням серцево-судинного та респіраторного стану пацієнта.
Попри добре відомі гемодинамічні переваги кетаміну, важливо постійно контролювати артеріальний тиск, частоту серцевих скорочень та рівень оксигенації під час та після процедури. Навіть кетамін у монорежимі може викликати значну гіпотензію у випадку тяжкої гіповолемії або сепсису.
Основні аспекти:
Гемодинамічна підтримка: здатність кетаміну підвищувати частоту серцевих скорочень і артеріальний тиск робить його незамінним у пацієнтів із гемодинамічною декомпенсацією, сприяючи зниженню ризику подальшого серцево-судинного колапсу.
Захист дихальних шляхів: кетамін зберігає рефлекси дихальних шляхів, що робить інтубацію безпечнішою, особливо у пацієнтів із ризиком порушення дихання.
Мінімальне пригнічення дихання: у порівнянні з іншими седативними препаратами, кетамін майже не викликає пригнічення дихання, що є критично важливим для пацієнтів із порушеною функцією дихання.
Швидкий та ефективний початок дії: швидкий початок дії кетаміну та помірна тривалість ефекту роблять його надзвичайно придатним для екстреного забезпечення прохідності дихальних шляхів у критично хворих пацієнтів.
Висновок: кетамін у монорежимі є критично важливим вибором седативного засобу для пацієнтів із гемодинамічною декомпенсацією, оскільки його симпатоміметичні ефекти забезпечують серцево- судинну стабільність, водночас забезпечуючи ефективну седацію та аналгезію. Його швидкий початок дії, мінімальне пригнічення дихання та здатність зберігати захисні рефлекси дихальних шляхів роблять його препаратом вибору для таких критично хворих пацієнтів.
НЕЙРОМʼЯЗОВА БЛОКАДА
Рокуроній та суксаметоній (сукцинілхолін) — це два найбільш поширених міорелаксанти, які застосовуються під час RSI в умовах невідкладної допомоги. У низці досліджень порівнювали ефективність і безпеку цих препаратів з метою досягнення оптимальних умов для інтубації та успішного проведення інтубації.
У дослідженні (Слуга та співавт., 2005)24, було зроблено висновок, що суксаметоній забезпечував швидшу ендотрахеальну інтубацію та кращі умови для інтубації порівняно з рокуронієм під час швидкої послідовної індукції анестезії в екстрених випадках.
Однак у дослідженні M та ін. (2018)25 було висунуто припущення, що рокуроній може бути безпечнішою альтернативою сукцинілхоліну в ситуаціях, коли застосування останнього протипоказане, оскільки він забезпечує добрі умови для інтубації без очікуваних ускладнень. Крім того, Patanwala та ін. (2010)26 встановили, що сукцинілхолін і рокуроній забезпечують однакову частоту успішної інтубації з першої спроби у відділеннях невідкладної допомоги за умови правильного дозування. Це свідчить про те, що обидва препарати можуть бути ефективними для досягнення успішної інтубації в умовах невідкладної допомоги.
| НЕЙРОМ’ЯЗОВА БЛОКАДА |
| РОКУРОНІЙ |
| 1.2 мг/кг |
| СУКСАМЕТОНІЙ |
| 1 - 2 мг/кг |
Високі дози рокуронію забезпечують тривалу м’язову релаксацію, тоді як дія сукцинілхоліну зазвичай триває близько 5 хвилин. Ця відмінність може бути як перевагою, так і недоліком залежно від пацієнта та клінічної ситуації. Спонтанне відновлення рухливості після 5 хвилин дає змогу пробудити пацієнта й відновити спонтанне дихання у разі невдалої інтубації. Однак, якщо це неможливо, а інтубація потребує кількох спроб і є тривалою за часом, відсутність релаксуючого ефекту стає додатковою проблемою.
При транспортування пацієнтів у критичному стані, контрольована вентиляція зазвичай найкраще забезпечується за допомогою стійкої м’язової релаксації протягом усього транспортування, що потребує застосування недеполяризуючих міорелаксантів, таких як рокуроній.
На завершення, хоча сукцинілхолін у деяких випадках може забезпечувати швидшу інтубацію та кращі умови для проведення інтубації, рокуроній є ефективною альтернативою, і не лише тоді, коли сукцинілхолін прямо протипоказаний. Обидва препарати продемонстрували порівнянні показники успішної інтубації з першої спроби, що підкреслює важливість правильного дозування та індивідуального підходу до вибору відповідного м’язового релаксанта для проведення RSI в умовах невідкладної допомоги.
| Забезпечення прохідності дихальних шляхів: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| Рокуроній слід розглядати як препарат першої лінії завдяки його ефективності, порівнянній із сукцинілхоліном, а також меншому профілю побічних ефектів і протипоказань. |
| Хоча сукцинілхолін залишається ефективним нейром’язовим блокатором (NMBA), його доцільніше використовувати як препарат другої лінії через наявність суттєвих протипоказань і побічних ефектів. |
ОБЛАДНАННЯ
Щоб передбачити подальший розвиток подій, важливо підготувати обладнання. Зокрема, налаштуйте вентилятор (EM-B1), підготуйте пристрій для моніторингу СО2 в кінці видиху(etCO2) і переконайтесь, що пацієнт змоніторований. Є два надзвичайно важливі моменти щодо монітора. По-перше, уважно контролюйте гемодинамічну ситуацію з інтервалом вимірювання артеріального тиску < 2 хвилин. По-друге, переконайтесь, що гучність пристрою налаштована на високий рівень, щоб забезпечити звуковий моніторинг усіх параметрів під час процедури.

| Забезпечення прохідності дихальних шляхів: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| Перед проведенням інтубації апарат ШВЛ має бути запрограмований із встановленими параметрами. Необхідно обрати режим вентиляції, з яким медичний працівник найбільш ознайомлений, щоб забезпечити плавний та ефективний перехід на штучну вентиляцію легень після забезпечення прохідності дихальних шляхів. |
| Артеріальний тиск слід вимірювати під час проведення інтубації та повторно з інтервалом < 2 хвилин. |
| Звуковий сигнал монітора має бути ввімкнений на достатньо високий рівень, щоб забезпечувати аудіостимул для всієї команди. |
УСПІШНЕ ЗАБЕЗПЕЧЕННЯ ПРОХІДНОСТІ ДИХАЛЬНИХ ШЛЯХІВ
В умовах надання невідкладної допомоги надзвичайно важливим є коректне розташування ендотрахеальної трубки. Хоча якісна кольорова капнографія часто використовується для підтвердження положення трубки шляхом оцінки рівня видихуваного вуглекислого газу, кількісна хвильова капнографія є значно кращим методом, оскільки надає інформативні дані навіть у разі зупинки серця.
Результати капнографії завжди мають доповнюватися клінічною оцінкою: перевіркою двосторонньої екскурсії грудної клітки та аускультацією дихальних шумів у пахвових ділянках і над епігастрієм для підтвердження правильного розташування ендотрахеальної трубки. Після фіксації трубки на відповідній глибині (зазвичай у чоловіків 21–23 см, у жінок 19–21 см) ці перевірки потрібно повторити та підтвердити адекватне роздування манжети інтубаційної трубки, бажано із застосуванням спеціального пристрою для моніторингу тиску в манжеті.
Після проведення швидкої послідовної інтубації та введення ендотрахеальної трубки необхідно підтримувати анестезію відповідно до протоколу D3. Нерідко у пацієнтів відзначається гемодинамічна нестабільність після інтубації, тому особливу увагу слід приділяти стабілізації та підтриманню стабільності стану відповідно до стандартів, визначених у протоколах C3 та C5. Ці протоколи спрямовані на негайну стабілізацію пацієнтів із можливими гемодинамічними порушеннями, забезпечення їхньої безпеки та належного рівня медичної допомоги під час анестезіологічного ведення.
Ключовими елементами залишаються:
- постійний моніторинг життєвих показників;
- корекція рівня анестезії відповідно до потреб;
- своєчасне реагування на ускладнення.
Це забезпечує стабільність і безпеку пацієнта у критичний період після інтубації.
| Забезпечення прохідності дихальних шляхів: ОСНОВНІ РЕКОМЕНДАЦІЇ |
Початковим кроком після інтубації є підтвердження правильного розташування ендотрахеальної трубки за допомогою: - капнографії (etCO2),
- аускультації,
- документування глибини введення трубки у сантиметрах.
|
| Для підтримання адекватної анестезії пацієнта необхідно перейти на протокол D3. |
| Гемодинаміку пацієнта слід ретельно контролювати та негайно втручатися відповідно до протоколів C5 та C6. |
НЕВДАЛА ІНТУБАЦІЯ
У критичній ситуації, коли інтубація є невдалою (визначається як дві безуспішні спроби ларингоскопії), необхідно негайно перейти до вентиляції за допомогою лицьової маски з мішком Амбу. Після цього рекомендовано реалізувати альтернативні стратегії забезпечення прохідності дихальних шляхів, визначені у плані Б та плані В відповідно до плану A1. Ці резервні алгоритми забезпечують структурований підхід до забезпечення прохідності дихальних шляхів у складних ситуаціях інтубації, гарантують безпеку пацієнта та адекватну оксигенацію під час невідкладних станів. Швидкий перехід до цих резервних стратегій дозволяє знизити ризики та ускладнення, пов’язані з невдалими спробами інтубації.
| Забезпечення прохідності дихальних шляхів: ОСНОВНІ РЕКОМЕНДАЦІЇ |
| Дві безуспішні спроби ларингоскопії вважаються невдалою інтубацією. |
| Вентиляція за допомогою лицьової маски використовується як проміжний метод. |
| Необхідно активувати план А1 та застосувати підхід VORTEX для подальшого забезпечення прохідності дихальних шляхів. |
ДОВІДКОВІ МАТЕРІАЛИ
- Karamchandani, K., Wheelwright, J., Yang, A. L., Westphal, N., Khanna, A. K., & Myatra, S. N. (2021).Emergency airway management outside the operating room: Current evidence and management strategies. Anesthesia & Analgesia, 133(3), 648-662. https://doi.org/10.1213/ane.0000000000005644
- McGrath, B. A., Bates, L., Atkinson, D., & Moore, J. A. (2012). Multidisciplinary guidelines for the management of tracheostomy and laryngectomy airway emergencies. Anaesthesia, 67(9), 1025-1041. https://doi. org/10.1111/j.1365-2044.2012.07217.x
- (2022). Airway misadventures in adult critical care: A concise narrative review of managing lost or compromised artificial airways. Current Opinion in Anaesthesiology, 35(2), 130-136. https://doi. org/10.1097/aco.0000000000001105
- Vortex Approach. (n.d.). Upper Airway Lifelines. Retrieved from http://vortexapproach.org/ lifelines#besteffort
- Starosolski, M., Kapłan, C., Kalemba, A., & Majewska, K. (2023). The impact of implementing the vortex approach on airway management performance in stressed medical students: A randomized controlled simulation study. Medical Science Monitor, 29. https://doi.org/10.12659/msm.9
- Biban, P., & Gaffuri, M. (2013). Premedication for tracheal intubation. Pediatric Critical Care Medicine, 14(4), 441-442. https://doi.org/10.1097/pcc.0b013e31827d1637
- Rocchio, M., Sylvester, K. W., Beik, N., Glasser, N., & Szumita, P. M. (2017). Ретроспективний огляд пропофолу порівняно з етомідатом під час швидкої послідовної інтубації у відділенні невідкладної допомоги у вищому навчальному закладі. Pharmacology & Pharmacy, 08(07), 231-241. https://doi. org/10.4236/pp.2017.87016
- Higgs, A., McGrath, B. A., Goddard, C. R., Rangasami, J., Suntharalingam, G., Gale, R., … & Cook, T. (2018). Guidelines for the management of tracheal intubation in critically ill adults. British Journal of Anaesthesia, 120(2), 323-352. https://doi.org/10.1016/j.bja.2017.10.021
- Marsch, S., Steiner, L. A., Bucher, E., Pargger, H., Schumann, M., Aebi, T., … & Siegemund, M. (2011). Succinylcholine versus rocuronium for rapid sequence intubation in intensive care: A prospective, randomized controlled trial. Critical Care, 15(4), R199. https://doi.org/10.1186/cc10367
- Sakles, J. C., Augustinovich, C. C., Patanwala, A. E., Pacheco, G. S., & Mosier, J. (2019). Improvement in the safety of rapid sequence intubation in the emergency department with the use of an airway continuous quality improvement program. Western Journal of Emergency Medicine, 20(4), 610-618. https://doi. org/10.5811/westjem.2019.4.42343
- Stollings, J. L., Diedrich, D. A., Oyen, L. J., & Brown, D. R. (2013). Rapid-sequence intubation. Annals of Pharmacotherapy, 48(1), 62-76. https://doi.org/10.1177/1060028013510488
- Yeung, J., & Zed, P. J. (2002). A review of etomidate for rapid sequence intubation in the emergency department. CJEM, 4(03), 194-198. https://doi.org/10.1017/s1481803500006370
- Sharda, S. C., & Bhatia, M. S. (2022). Etomidate compared to ketamine for induction during rapid sequence intubation: A systematic review and meta-analysis. Indian Journal of Critical Care Medicine, 26(1), 108- 113. https://doi.org/10.5005/jp-journals-10071-24086
- Lyon, R., Perkins, Z., Chatterjee, D., Lockey, D., & Russell, M. Q. (2015). Significant modification of traditional rapid sequence induction improves safety and effectiveness of pre-hospital trauma anaesthesia. Critical Care, 19(1). https://doi.org/10.1186/s13054-015-0872-2
- Acquisto, N. M., Mosier, J. M., Bittner, E. A., Patanwala, A. E., Hirsch, K. G., Hargwood, P., Oropello, J. M., Bodkin, R. P., Groth, C. M., Kaucher, K. A., Slampak-Cindric, A. A., Manno, E. M., Mayer, S. A., Peterson, L. N., Fulmer, J., Galton, C., Bleck, T. P., Chase, K., Heffner, A. C., Gunnerson, K. J., Boling, B., Murray, M.J. (2023). Society of Critical Care Medicine Clinical Practice Guidelines for Rapid Sequence Intubation in the Critically Ill Adult Patient. Critical Care Medicine, 51(10), 1411-1430. https://doi.org/10.1097/ CCM.0000000000006000
- Simon, M., Wachs, C., Braune, S., Heer, G. d., Frings, D., & Kluge, S. (2016). High-flow nasal cannula versus bag-valve-mask for preoxygenation before intubation in subjects with hypoxemic respiratory failure. Respiratory Care, 61(9), 1160-1167.https://doi.org/10.4187/respcare.04413
- Winck, J., Azevedo, L. F., Costa‐Pereira, A., Antonelli, M., & Wyatt, J. (2006). Untitled. Critical Care, 10(2), R69. https://doi.org/10.1186/cc4905
- Hadhoud, Y. H., Baraka, M. A., Saleh, M., & Refaat, A. M. (2023). A comparative evaluation of the sniffing, the simple head extension and the head hyperextension positions for laryngoscopic view and intubation difficulty in adults undergoing direct laryngoscopy. European Archives of Oto-Rhino-Laryngology, 281(3), 1401-1407. https://doi.org/10.1007/s00405-023-08386-y
- Shende, S., & Shidhaye, R. V. (2016). Evaluation of laryngoscopic view, intubation difficulty and sympathetic response during direct laryngoscopy in sniffing position versus simple head extension: A clinical comparative study. International Journal of Medical Research and Review, 4(9), 1531-1537. https://doi. org/10.17511/ijmrr.2016.i09.03
- Bhattarai, B., Shrestha, S. R., & Kandel, S. (2012). Comparison of sniffing position and simple head extension for visualization of glottis during direct laryngoscopy. Kathmandu University Medical Journal, 9(1), 58-63.https://doi.org/10.3126/kumj.v9i1.6265
- Park, S. W., Lee, K., Jang, M., Jung, J., Lee, B., & Kang, J. (2014). Age and gender are important considerations in choosing the sniffing position for laryngoscopic view. International Journal of Medical Sciences, 11(12), 1258-1261. https://doi.org/10.7150/ijms.8585
- Russotto, V., Nainan Myatra, S., Laffey, J. G., et al. (2021). Intubation practices and adverse peri-intubation events in critically ill patients from 29 countries. JAMA, 325, 1164–1172.
- Van Berkel, M. A., Exline, M. C., Cape, K. M., et al. (2017). Increased incidence of clinical hypotension with etomidate compared to ketamine for intubation in septic patients: A propensity matched analysis. Journal of Critical Care, 38, 209-214.
- Smischney, N. J., Nicholson, W. T., Brown, D. R., Gallo De Moraes, A., Hoskote, S. S., Pickering, B., Oeckler, R. A., Iyer, V. N., Gajic, O., Schroeder, D. R., Bauer, P. R. (2019). Ketamine/propofol admixture vs etomidate for intubation in the critically ill: KEEP PACE Randomized clinical trial.
РОЗДІЛ 3. ДИХАННЯ
ВСТУП
У складних умовах транспортування пацієнтів у критичному стані штучна вентиляція легень (ШВЛ) є ключовим елементом для забезпечення оптимальної медичної допомоги під час руху. Показання до застосування ШВЛ надзвичайно різноманітні — від гострих респіраторних порушень до глибокої седації у межах інтенсивної терапії.
Рішення про початок ШВЛ до або під час транспортування ухвалюється з метою мінімізації ризику ускладнень, пов’язаних із загрозою порушення прохідності дихальних шляхів або розвитком дихальної недостатності під час транспортування. Важливим є не лише ґрунтовне розуміння методів вентиляції, а й здатність своєчасно розпізнавати потенційні загрози та оперативно на них реагувати.
Стандартизований командний підхід має вирішальне значення для забезпечення безперервності, безпеки та ефективності кожного етапу транспортування. Уміння ухвалювати правильні клінічні рішення в умовах високого тиску може стати питанням життя і смерті, особливо у гострих ситуаціях типу «неможливо вентилювати», коли необхідно діяти негайно для порятунку пацієнта.
ЧАСТИНА 1: НАЛАШТУВАННЯ ШВЛ
Розуміння режимів вентиляції
Загалом застосовуються два основні режими штучної вентиляції легень (ШВЛ):
- з контролем тиску (PCV) — коли подача газової суміші здійснюється за допомогою заданого градієнта тиску;
- з контролем об’єму (VCV) — коли використовується попередньо визначений дихальний об’єм (ДО).
Існують різні моделі апаратів ШВЛ, придатних для транспортування, і кожен виробник використовує власну термінологію для позначення параметрів режимів вентиляції.
Сучасні транспортні апарати ШВЛ зазвичай мають додаткові режими, що дозволяють пацієнтові зберігати спонтанне дихання. У таких випадках апарат може:
- підсилювати власний ДО пацієнта;
- або додавати контрольовані вдихи до спонтанних, особливо при низькій чи нестабільній частоті дихання (ЧД).
Не рекомендується обирати режими вентиляції, з якими лікар, відповідальний за транспортування, не має достатнього клінічного досвіду. Під час транспортування тяжкохворих або нестабільних пацієнтів найбезпечнішим вважається застосування глибокої седації, повної м’язової релаксації та використання простого режиму керованої ШВЛ.
Вентиляція з керованим об’ємом (VCV)
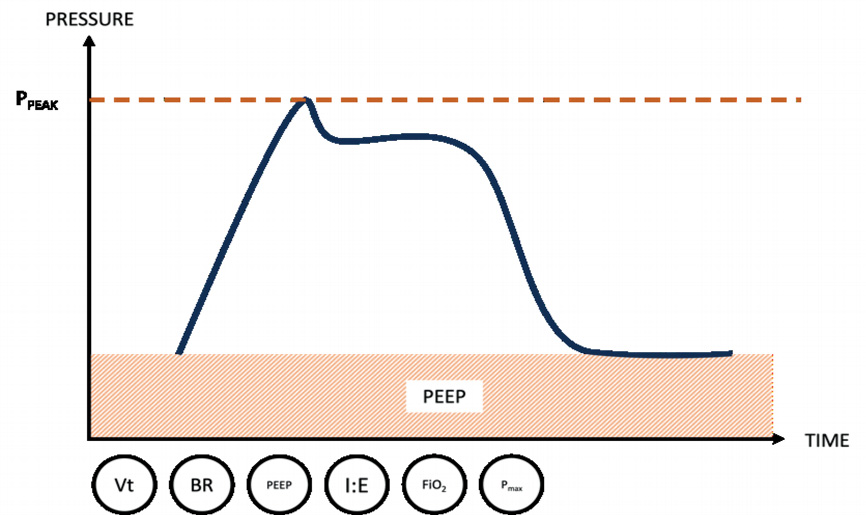
Опис графіка:
PPEAK (піковий тиск у дихальних шляхах) — максимальний тиск, що досягається під час вдиху.
PEEP (позитивний тиск наприкінці видиху, ПТКВ) — мінімальний рівень тиску, який підтримується апаратом для запобігання колапсу альвеол.
Vt (Tidal Volume, ДО) — дихальний об’єм, що подається під час кожного вдиху.
BR (Breathing Rate, ЧД) — частота дихання.
I:E — співвідношення тривалості вдиху до видиху.
FiO₂ — фракція кисню у вдихуваній суміші.
Pmax (максимальний тиск) — встановлений верхній ліміт тиску в контурі апарата ШВЛ.
Режим штучної вентиляції легень (ШВЛ) з контролем об’єму (VCV) передбачає подачу апаратом заздалегідь встановленого дихального об’єму (ДО) у легені пацієнта із заданою частотою дихання (ЧД). Цей режим гарантує надходження певного об’єму газової суміші під час кожного вдиху, незалежно від змін легеневої податливості чи опору дихальних шляхів.
У таблиці 1 наведено детальний опис принципів і параметрів ШВЛ з контролем об’єму.
Під час застосування режиму VCV лікарі ретельно відстежують реакцію пацієнта, оцінюючи:
- газовий склад артеріальної крові (ГАК),
- рівень СО2 в кінці видиху (EtCO₂),
- параметри дихальної механіки.
На підставі цих даних можуть коригуватися дихальний об’єм (ДО), частота дихання (ЧД) чи інші налаштування апарата ШВЛ з метою оптимізації вентиляції та оксигенації.
Режим VCV широко застосовується в різних клінічних умовах:
- під час хірургічних втручань,
- у відділеннях інтенсивної терапії (ВІТ),
- у разі надання екстреної медичної допомоги.
VCV забезпечує контрольовану та передбачувану подачу ДО, що робить його одним із базових режимів ШВЛ у лікуванні пацієнтів із респіраторними порушеннями.
| Респіраторна підтримка з контролем об’єму | Визначення | Основні параметри налаштування |
| Дихальний об’єм | Дихальний об’єм — це об’єм повітря, що подається до легень з кожним вдихом. | У режимі з контролем об’єму медичний працівник встановлює бажаний дихальний об’єм з урахуванням параметрів пацієнта, стану легень і терапевтичних цілей. |
| Частота дихання (ЧД) | Частота дихання — це кількість дихальних циклів, що подаються апаратом за одну хвилину. | Медичний працівник встановлює цей параметр для регулювання частоти подачі вдихів апаратом. |
| Тривалість вдиху (Ti) | Тривалість вдиху — це інтервал часу, протягом якого апарат подає дихальний об’єм. | Медичний працівник встановлює цей показник для регулювання тривалості кожного вдиху. |
| Тривалість видиху (Te) | Тривалість видиху — це період часу, що надається для видиху. | У режимі з контролем об’єму тривалість видиху часто залежить від частоти дихання та співвідношення вдиху до видиху (I:E). |
| Співвідношення I:E | Це співвідношення тривалості вдиху до видиху. Абсолютні значення часу вдиху і видиху залежать від встановленої частоти дихання. | Залежно від типу апарата медичні працівники можуть налаштовувати співвідношення I:E безпосередньо або змінювати тривалість вдиху і видиху окремо. |
| Обмеження тиску | У більшості апаратів респіраторної підтримки з контролем об’єму можна встановити максимальний тиск для запобігання надмірному тиску в дихальних шляхах під час вдиху. | У разі застосування цей параметр налаштовується так, щоб поданий об’єм не спричиняв небезпечно високого тиску. Необхідно уважно стежити за тим, щоб досягнення межі тиску не призводило до недостатньої вентиляції пацієнта. У деяких апаратах досягнення встановленого обмеження тиску або рівня спрацювання сигналу високого тиску може призвести до переривання вдиху, а не лише до подання сигналу або обмеження подачі тиску в контур пацієнта. Обмеження тиску та сигнал високого тиску можуть бути інтегровані або встановлюватися окремо, залежно від типу апарата, тому важливо точно знати особливості роботи конкретного обладнання. |
Таблиця 1: Деталізований опис режиму респіраторної підтримки з контролем об’єму.
Вентиляція з керованим тиском (PCV)
Моніторинг і корекція при респіраторній підтримці з керованим тиском (PCV) передбачають постійне оцінювання тиску в дихальних шляхах, газового складу крові та реакції пацієнта. У таблиці 2 наведено детальний опис режиму респіраторної підтримки з керованим тиском.
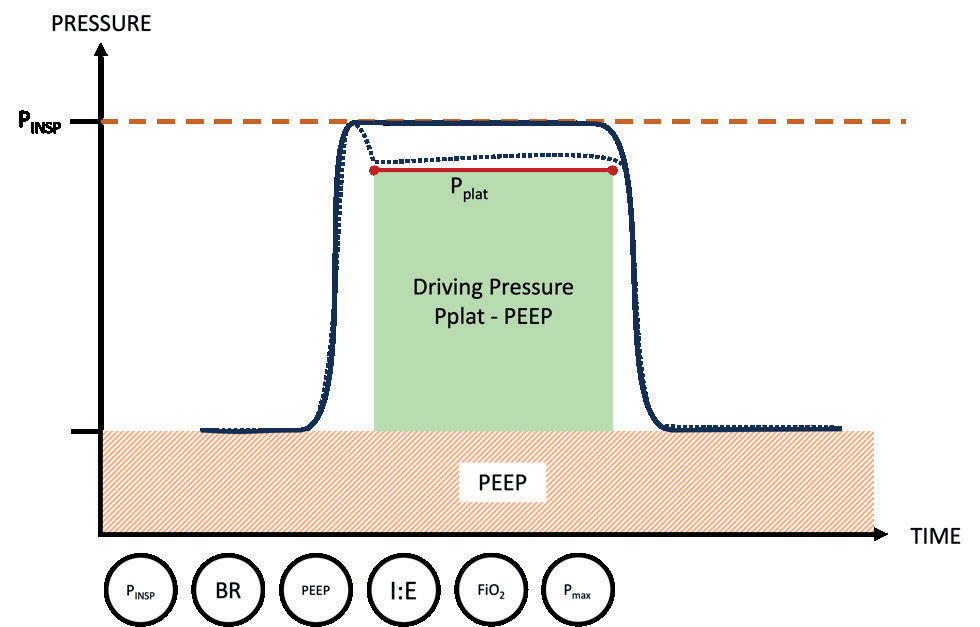
| Вентиляція з керованим тиском | Визначення | Основні параметри налаштування |
| Тиск вдиху (Pinsp) | Тиск вдиху — це тиск, що прикладається до дихальних шляхів під час фази вдиху для подачі дихального об’єму. | Медичний працівник встановлює цей тиск для досягнення бажаного дихального об’єму. Це ключовий параметр, який безпосередньо впливає на величину тиску, що подається до легень. |
| Тиск плато (Pplat) | Тиск плато (Pplat) відображає тиск у дихальних шляхах під час вдиху та характеризує фізіологічні особливості пацієнта залежно від встановленого тиску вдиху (Pinsp). | При налаштуванні режиму ШВЛ з керованим тиском особливе значення мають градієнти тиску між фазами вдиху та видиху. Тиск вдиху визначається як різниця між встановленим Pinsp та позитивним тиском наприкінці видиху (ПТКВ / PEEP).
Тиск вдиху (Pinsp) створює потік, необхідний для подолання опору дихальних шляхів (ДШ) та забезпечення розправлення легень відповідно до їхньої податливості. Потік, що генерується тиском Pinsp, проходить через контур пацієнта та інтубаційну трубку, після чого тиск передається у нижні ДШ. Отриманий тиск залежить як від опору в ДШ, так і від податливості легеневої тканини.
Важливо усвідомлювати, що встановлений Pinsp не у повному обсязі передається до нижніх ДШ, оскільки його величина змінюється під впливом механічних властивостей дихальної системи пацієнта. |
| Тиск плато (Pplat) | Тиск плато (Pplat) є тиском під час фази вдиху, який відображає фізіологічні особливості пацієнта на основі встановленого тиску вдиху (Pinsp). | Тиск плато (Pplat), який фіксується після досягнення пікового тиску вдиху, точніше відображає тиск у термінальних бронхіолах і альвеолах. У клінічній практиці Pplat можна визначити за допомогою функції «затримка вдиху», доступної на більшості апаратів ШВЛ. Під час цього маневру апарат на короткий час (зазвичай до 10 секунд) перекриває як клапан вдиху так і клапан видиху, що дозволяє тиску вирівнятися від альвеол до точки вимірювання у контурі вентилятора. Різниця між тиском плато та позитивним тиском наприкінці видиху (Pplat – ПТКВ) визначається як градієнт тиску (Driving Pressure, ΔP). Загалом, чим кращий стан легень і менший опір у дихальних шляхах, тим меншою є різниця між Pinsp і Pplat. Контроль градієнту тиску (Driving Pressure, ΔP) є ключовим елементом легенезахисної вентиляції, особливо у пацієнтів із гострим респіраторним дистрес-синдромом (ГРДС). Цей аспект розглядатиметься детальніше у наступних розділах настанов. |
| Дихальний об’єм | Дихальний об’єм — це об’єм повітря, який надходить до легень під час одного дихального циклу. | У режимі ШВЛ з керованим тиском дихальний об’єм не встановлюється безпосередньо, але визначається сукупністю параметрів: тиском вдиху, драйвінговим тиском, податливістю легень і тривалістю вдиху. |
| Позитивний тиск при закінченні видиху (ПТКВ) | ПТКВ — це позитивний тиск, який підтримується в дихальних шляхах наприкінці фази видиху з метою запобігання спадінню альвеол. | Медичний працівник встановлює рівень ПТКВ для оптимізації оксигенації та рекрутування альвеол. У поєднанні з плато-тиском (Pplat), ПТКВ визначає рівень драйвінгового тиску. |
| Співвідношення I:E | Це співвідношення тривалості вдиху до тривалості видиху, що визначає розподіл часу між цими фазами. | Залежно від типу апарата медичний працівник може налаштовувати I:E-співвідношення напряму або ж окремо регулювати тривалість вдиху і видиху. |
| Чутливість (за наявності) | Чутливість — це рівень зусилля або потоку, необхідний для активації вдиху апаратом у разі спонтанного дихання пацієнта. | У деяких режимах із контролем тиску цей параметр можна налаштувати для кращої відповідності респіраторної підтримки до зусиль пацієнта. |
| Підтримка тиском | Підтримка тиском — це додатковий тиск, який подається під час спонтанного вдиху пацієнта. | Підтримка тиском — це додатковий тиск, який подається під час спонтанного вдиху пацієнта. |
Таблиця 2: Деталізований опис режиму респіраторної підтримки з контролем тиску.
Вибір режиму ШВЛ: порівняння вентиляції з керованим об’ємом та вентиляції з керованим тиском
Під час ведення пацієнтів у критичному стані, які потребують штучної вентиляції легень (ШВЛ), вибір відповідного режиму та параметрів є ключовим для досягнення ефективної вентиляції за умови мінімізації ризику ускладнень. Одним із найсерйозніших ускладнень є ушкодження легень, спричинене апаратом ШВЛ (VILI — Ventilator-Induced Lung Injury). Огляд наукової літератури та практичне ознайомлення з різними моделями апаратів ШВЛ демонструє значну кількість складних режимів та специфічних термінів. Численні клінічні дослідження намагалися деталізувати це питання з різних підходів, у результаті чого сформувалося більш чітке розуміння основних факторів, що впливають на вентиляцію. Серед усіх доступних режимів виділяють два базові: вентиляція з керованим об’ємом (VCV) та вентиляція з керованим тиском (PCV). Розуміння цих фундаментальних форм вентиляції є необхідною основою для подальшого опанування більш складних режимів. Ці режими відрізняються за характером потоку повітря та динамікою тиску, що безпосередньо впливає на механіку легень і, зрештою, на клінічні результати лікування пацієнтів.
Механічна енергія та інші фактори, що впливають на передачу енергії
Механічна енергія — це кількість енергії, яка передається до легеневої тканини під час кожного дихального циклу. Вона визначається такими параметрами, як дихальний об’єм, тиск у дихальних шляхах та швидкість потоку газової суміші. Надмірні показники механічної енергії асоціюються з підвищеним ризиком ушкодження легеневої тканини внаслідок штучної вентиляції легень (VILI), що відбувається через надмірне навантаження та деформацію альвеол.
Останні дослідження пропонують розглядати транспульмональну механічну енергію (MPL) як більш точний показник ризику VILI, оскільки вона відображає кількість енергії, яка безпосередньо передається легеневій тканині, а не усій респіраторній системі. У дослідженні Rietveld та ін. (2022)27 встановлено, що перевищення визначеного порогового значення MPL супроводжується суттєвим посиленням ушкодження легень. Незалежно від того, який саме показник буде обрано основним у майбутньому, управління механічною енергією вже вважається ключовим елементом респіраторної підтримки у відділеннях інтенсивної терапії. Оптимальні стратегії регуляції цього показника в різних клінічних сценаріях залишаються предметом дискусії, і наразі єдиний консенсус відсутній.
27 Rietveld, P. J., Snoep, J. W. M., Lamping, M., van der Velde, F., de Jonge, E., van Westerloo, D. W., & Schoe, A. (2022). Mechanical power differs between pressure-controlled ventilation and different volume-controlled ventilation modes. Critical Care Explorations, 4(8), 1-9. https://doi.org/10.1097/CCE.0000000000000741
Вибір режиму ШВЛ: порівняння вентиляції з керованим об’ємом та вентиляції з керованим тиском
Однією з основних відмінностей між режимами вентиляції з керованим об’ємом (VCV) та вентиляції з керованим тиском (PCV) є характер потоку газу, що має клінічне значення для розподілу механічної енергії та формування петель «тиск–об’єм».
- У режимі VCV протягом усієї фази вдиху підтримується постійний потік, тоді як тиск у дихальних шляхах варіює як у межах одного вдиху, так і від вдиху до вдиху. У режимі PCV, навпаки, забезпечується постійний тиск упродовж вдиху, а характер потоку змінюється залежно від податливості легень та опору дихальних шляхів.
- У режимі вентиляції з керованим тиском (PCV) використовується сталий рівень тиску, що формує потік зі спадною характеристикою. На початку вдиху швидкість потоку зростає максимально, після чого поступово знижується у міру розширення легень. Такий механізм забезпечує нижчий піковий тиск у дихальних шляхах, але водночас — вищий початковий потік порівняно з режимом вентиляції з керованим об’ємом (VCV) при подібних умовах.
Який із режимів (VCV чи PCV) забезпечує найбільш щадну стратегію вентиляції залежить не лише від технічних характеристик апарата, а й від індивідуальних особливостей пацієнта, показань до респіраторної підтримки та конкретної клінічної ситуації.
Загальна кількість механічної енергії, що передається легеневій тканині, визначається не лише тиском і швидкістю потоку. Важливе значення мають часові параметри дихального циклу:
- тривалість вдиху,
- тривалість видиху,
- співвідношення вдиху до видиху (І:Е),
- частота дихання.
Таким чином, кінцевий ефект респіраторної підтримки формується комплексом параметрів і вимагає індивідуального налаштування.
Примітка:
На сьогодні бракує достатніх доказових даних для однозначного визначення переваги якогось одного режиму ШВЛ. Оптимальною стратегією є використання того режиму, з яким клініцист має найбільший практичний досвід, за умови ретельного уникнення:
- надмірних рівнів тиску в дихальних шляхах,
- невиправдано високої швидкості потоку,
- надлишкової концентрації кисню,
- некоригованої частоти дихання.
Ретельне налаштування параметрів апарата ШВЛ, постійний моніторинг життєвих показників і стану пацієнта, а також своєчасна корекція режиму під час транспортування мають вирішальне значення для безпечності та ефективності вентиляції.
Оксигенація та вентиляція
У критичних станах одночасне забезпечення ефективної оксигенації та вентиляції є ключовим для надання повноцінної респіраторної підтримки. Попри взаємозв’язок цих двох фізіологічних процесів, вони є різними за своєю природою та вимагають різних підходів до управління з метою оптимізації клінічних результатів. У цьому розділі докладно розглянуто відмінності між оксигенацією та вентиляцією, а також способи коригування параметрів респіраторної підтримки для досягнення оптимального балансу між ними із мінімізацією ризиків для пацієнта.
Оксигенація: забезпечення ефективного газообміну
Оксигенація — це процес надходження кисню до кровотоку, під час якого кисень проникає через альвеолярно-капілярну мембрану та зв’язується з гемоглобіном. Ефективність оцінюється за показниками SpO₂ (насичення гемоглобіну киснем, визначене за допомогою пульсоксиметрії) та PaO₂ (парціальний тиск кисню в артеріальній крові). Основна мета оксигенації — забезпечити достатнє надходження кисню до тканин для задоволення метаболічних потреб. Корекція здійснюється шляхом регулювання позитивного тиску наприкінці видиху (ПТКВ) та фракції вдихуваного кисню (FiO₂). Вентиляція — це процес видалення вуглекислого газу з організму, який забезпечується газообміном у легенях. Ефективність вентиляції оцінюється за рівнем PaCO₂ (парціальний тиск вуглекислого газу в артеріальній крові) та показниками EtCO₂ (концентрація вуглекислого газу наприкінці видиху). Основна мета вентиляції — підтримання адекватного рівня PaCO₂ для забезпечення кислотно-лужної рівноваги. Корекція здійснюється шляхом зміни дихального об’єму (ДО), частоти дихання та співвідношення вдих/ видих (І:Е). Таким чином, досягнення оптимального балансу між оксигенацією та вентиляцією потребує ретельного налаштування параметрів апарата ШВЛ та постійного моніторингу стану пацієнта для мінімізації ризику ускладнень і забезпечення ефективної респіраторної підтримки.
ПТКВ та оксигенація
Позитивний тиск наприкінці видиху (ПТКВ) є одним із ключових параметрів респіраторної підтримки, спрямованих на оптимізацію оксигенації.
Основні механізми його дії:
- Збільшення альвеолярної поверхні для газообміну. ПТКВ перешкоджає колапсу альвеол наприкінці видиху, що забезпечує стабільне розкриття альвеолярних структур і збільшення площі дифузії. Це зменшує відстань для переносу молекул кисню та підвищує ефективність альвеолярно-капілярного газообміну.
- Рекрутинг ( розкриття) ателектазів легень. У пацієнтів із набряком легень або гострим респіраторним дистрес-синдромом (ГРДС) застосування ПТКВ сприяє рекрутуванню (розкриттю) ателектазів або недостатньо вентильованих альвеол. Це підвищує функціональну залишкову ємність і покращує показники оксигенації.
- Кровотік через невентильовані ділянки легеневої тканини формує шунт, що зумовлює змішування неоксигенованої крові з оксигенованою у лівих відділах серця та призводить до зниження рівнів SpO₂ і PaO₂.
ПТКВ має особливе значення у веденні пацієнтів із набряком легень або серцевою недостатністю, коли гіпоксемія зумовлена підвищеною проникністю легеневих капілярів або легеневим застоєм. У таких випадках адекватно підібраний рівень ПТКВ забезпечує рекрутування більшої кількості та їх залучення до газообміну, що підвищує ефективність доставки кисню до тканин.
FiO₂ та оксигенація
Принцип дифузії полягає у переміщенні молекул із ділянки з вищою концентрацією до ділянки з нижчою. У контексті оксигенації підвищення фракції вдихуваного кисню (FiO₂) посилює дифузію кисню через альвеолярно-капілярну мембрану у кров. Збільшення концентрації кисню в альвеолах формує вищий градієнт концентрації, що сприяє надходженню більшої кількості кисню до капілярів. Разом з тим налаштування параметра FiO₂ потребує обережності. Надмірна концентрація кисню у вдихуваній газовій суміші може спричинити розвиток кисневої токсичності. Доведено, що тривале застосування FiO₂ понад 60 % асоціюється з клітинним ушкодженням і розвитком запальних процесів у легеневій тканині.
Клінічною метою є використання мінімально необхідного рівня FiO₂, який забезпечує адекватну оксигенацію та насичення тканин киснем. Такий підхід дозволяє досягти ефективного газообміну та водночас знизити ризик ускладнень, пов’язаних із тривалою експозицією високих концентрацій кисню.
Вентиляція визначається як рух повітря до легень і з легень, що забезпечує виведення вуглекислого газу (CO₂) з організму. CO₂ є побічним продуктом клітинного метаболізму та підлягає елімінації для запобігання розвитку респіраторного ацидозу. Ефективність вентиляції оцінюється за такими показниками: etCO₂ — концентрація вуглекислого газу у видихуваному повітрі (наприкінці видиху); PaCO₂ — парціальний тиск вуглекислого газу в артеріальній крові, що визначається під час аналізу газового складу артеріальної крові (ABG). Корекція вентиляції здійснюється шляхом регулювання: дихального об’єму (ДО), частоти дихання (ЧД), співвідношення вдих/видих (І:Е).
Дихальний об’єм (ДО) та вентиляція
Перед корекцією ЧД або співвідношення вдих/видих (І:Е) необхідно встановити адекватний дихальний об’єм (ДО) для забезпечення ефективної вентиляції. Для пацієнтів із неураженими легенями рекомендований ДО становить 6–8 мл/кг ідеальної маси тіла (ІМТ).
Частота дихання (ЧД):
- Підвищення ЧД сприяє елімінації вуглекислого газу при підвищених рівнях etCO₂ або PaCO₂.
- Зниження ЧД доцільне у випадках низьких рівнів etCO₂, щоб запобігти гіпервентиляції.
Співвідношення І:Е (вдих : видих):
- У більшості пацієнтів прийнятним вважається співвідношення 1:2.
- Обструктивні захворювання легень: подовження фази видиху дозволяє уникнути явища “повітряної пастки”.
- Рестриктивні захворювання легень (зокрема ГРДС): може бути доцільним встановлення співвідношення 1:1,5 або навіть 1:1 для забезпечення достатнього часу оксигенації при використанні низьких ДО.
Зменшення “мертвого простору”
Одним із ключових чинників, що впливають на ефективність вентиляції, є “мертвий простір” — ділянки дихальної системи, де не відбувається газообмін. Для оптимізації вентиляції важливо максимально зменшувати об’єм мертвого простору. Додаткові елементи контуру, такі як фільтри, адаптери для контролю CO₂ та обертові з’єднувачі, підвищують безпеку пацієнта й ефективність подачі газової суміші, проте водночас збільшують механічний мертвий простір. Це може спричинити зниження ефективності вентиляції та порушення газообміну. Необхідно уникати надмірної довжини ендотрахеальної трубки (ЕТ- трубки), оскільки подовжені трубки збільшують опір диханню та об’єм мертвого простору, що негативно впливає на якість вентиляції.
Уникнення ушкодження легень та небажаних побічних ефектів
Під час оптимізації оксигенації та вентиляції необхідно враховувати ризики, пов’язані із застосуванням механічної вентиляції. У фізіологічних умовах дихальна система людини пристосована до спонтанного дихання, за якого повітря з концентрацією кисню близько 21 % надходить у легені завдяки негативному тиску, що формується скороченням діафрагми та рухами грудної стінки. На відміну від цього, механічна вентиляція здійснюється шляхом подачі газової суміші під позитивним тиском через інтубаційну трубку безпосередньо у легені. Газ при цьому має вищу концентрацію кисню та нижчу вологість порівняно з атмосферним повітрям. Відмінності між фізіологічним і штучним механізмом дихання створюють низку викликів і потенційних ризиків, особливо в умовах інтенсивної терапії, де тривала вентиляція може призводити до ускладнень.
Клітинне ушкодження та киснева токсичність
Тривале застосування FiO₂ понад 60 % може призвести до клітинного ушкодження та розвитку запальних змін, зумовлених окислювальним стресом і вторинним ушкодженням тканин. Клінічними проявами кисневої токсичності є: ушкодження альвеолярних структур; набряк легень; формування фіброзних змін у легеневій тканині при тривалому перебігу. З огляду на це, рівень FiO₂ необхідно підтримувати на мінімально можливому рівні, який забезпечує адекватну оксигенацію та стабільність газообміну, з одночасною мінімізацією ризику токсичного ураження.
Сухість дихальних шляхів і скупчення секрету
Механічна респіраторна підтримка може сприяти накопиченню бронхіального секрету, що погіршує функцію легень та підвищує ризик інфекційних ускладнень. Основні чинники: подача сухого повітря під час вентиляції, особливо за використання транспортних апаратів без зволожувачів, призводить до втрати тепла та рідини внаслідок випаровування; це зумовлює пересушування слизових оболонок дихальних шляхів та утворення в’язкого секрету, що ускладнює його евакуацію. Профілактика та заходи: під час тривалого транспортування необхідне забезпечення адекватного зволоження газової суміші та регулярне відсмоктування секрету; застосування фільтра тепло- та вологообміну (HME-фільтр) знижує втрати тепла та рідини, підтримуючи оптимальні умови для функціонування дихальних шляхів. Клінічні застереження: використання додаткових компонентів контуру (зокрема HME-фільтра) збільшує мертвий простір, що може негативно впливати на ефективність вентиляції; це особливо важливо враховувати у пацієнтів із гіперкапнією, оскільки збільшений мертвий простір здатен погіршити показники газообміну.
Ателектаз та альвеолярний колапс
Повторювані цикли спадання кінцевих дихальних шляхів та розвиток ателектазу (спадання альвеол) є типовими ускладненнями механічної вентиляції, особливо у пацієнтів із гострим респіраторним дистрес-синдромом (ГРДС) та іншими рестриктивними ураженнями легень. Такі стани сприяють розвитку ушкодження легень, індукованого апаратом респіраторної підтримки (VILI). Механізм полягає у повторному колапсі та наступному розкритті альвеол, що призводить до їх механічного ушкодження та поглиблює перебіг дихальної недостатності.
Баротрамна та волюмотравма
Механічна респіраторна підтримка, особливо за умови використання високих тисків у дихальних шляхах, може призвести до надмірного розтягнення легеневої тканини та розвитку ускладнень, таких як баротравма та волюмотравма. Ці стани є складовими ушкодження легень, індукованого вентиляцією (VILI). Сучасна концепція VILI пов’язує розвиток ушкоджень із надмірною передачею механічної енергії, що ще раз підкреслює необхідність обмеження тиску, потоку та об’єму під час проведення штучної вентиляції. Рекомендації з профілактики баро- та волюмотравми: обмежувати драйвінговий тиск (ΔP) до ≤15 мбар; підтримувати тиск плато (Pplat) нижче 30 мбар, а за можливості — ще нижче; використовувати затримку вдиху для вимірювання Pplat. Цей параметр відображає тиск у легенях у момент тимчасової зупинки потоку повітря та є надійним показником рівня тиску під час інфляції легень.
Оптимальне налаштування параметрів апарата ШВЛ з урахуванням цих меж мінімізує ризик ушкодження легеневої тканини та покращує безпеку пацієнта.
Вплив на кровообіг
Високий тиск під час механічної вентиляції впливають не лише на дихальну систему, а й має системні наслідки. Надмірні значення тиску плато (Pplat) та драйвінгового тиску (ΔP) можуть знижувати венозне повернення, що призводить до артеріальної гіпотензії та зменшення серцевого викиду. Крім того, вентиляція з позитивним тиском підвищує ризик розвитку або прогресування пневмотораксу, що супроводжується спаданням легені та подальшим поглибленням гіпоксемії, ускладнюючи клінічний перебіг.
Примітка. Управління оксигенацією та вентиляцією у пацієнтів у критичному стані потребує ретельного балансу параметрів, який забезпечує оптимізацію газообміну та профілактику механічного ушкодження. ПТКВ та FiO₂ — основні параметри для корекції оксигенації. Дихальний об’єм (ДО), частота дихання (ЧД) та співвідношення І:Е — ключові параметри для ефективної вентиляції. Особливу увагу необхідно приділяти мінімізації ризиків, пов’язаних із кисневою токсичністю, надмірним розтягненням легень та ателектазом.Оптимізація цих параметрів дозволяє не лише знизити ризик ушкодження легень, але й підтримати адекватну серцево-судинну функцію. Розуміння та цілеспрямоване управління режимами вентиляції забезпечують найбільш ефективну та безпечну респіраторну підтримку для пацієнтів у критичних станах.
СОП B1: Первинне налаштування апарата ШВЛ (див. Додаток 11)
Правильне налаштування параметрів штучної вентиляції легень (ШВЛ) має вирішальне значення у веденні пацієнтів у тяжкому стані. Налаштування апарата повинні здійснюватися з урахуванням клінічних потреб пацієнта та його фізіологічної відповіді на проведену терапію. Відповідно до стандартної операційної процедури (СОП), загальні етапи початкового налаштування ШВЛ включають:
- Забезпечення прохідності дихальних шляхів.
- Вибір початкових параметрів ШВЛ (режим, ДО, ЧД, ПТКВ, FiO₂, співвідношення І:Е).
- Подальшу корекцію налаштувань залежно від показників оксигенації, вентиляції та загального клінічного стану пацієнта.
Крок 1: Забезпечення прохідності ДШ та досягнення цілей седації
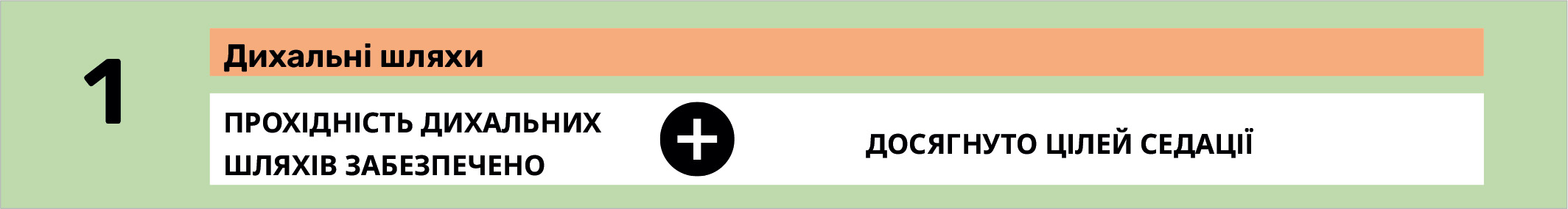
Перед початком штучної вентиляції легень (ШВЛ) першим кроком є забезпечення прохідності дихальних шляхів. Це включає підтвердження правильності інтубації пацієнта або наявності альтернативного методу забезпечення дихального шляху (надгортанний повітровід, трахеостома тощо). Необхідним є досягнення адекватного рівня седації, що дозволяє: запобігти дискомфорту пацієнта; зменшити ризик психомоторного збудження; забезпечити оптимальну синхронізацію з апаратом ШВЛ. Цілі седації повинні бути досягнуті до початку вентиляції, щоб гарантувати комфортний стан пацієнта та безпечний початок проведення ШВЛ.
Крок 2: Початкові параметри ШВЛ
Після забезпечення прохідності дихальних шляхів та досягнення адекватного рівня седації наступним кроком є вибір відповідних початкових параметрів ШВЛ. У стандартній операційній процедурі (СОП) передбачено два режими вентиляції: ШВЛ з керованим об’ємом (VCV) та ШВЛ з керованим тиском (PCV). Початкові параметри для обох режимів наведено нижче:
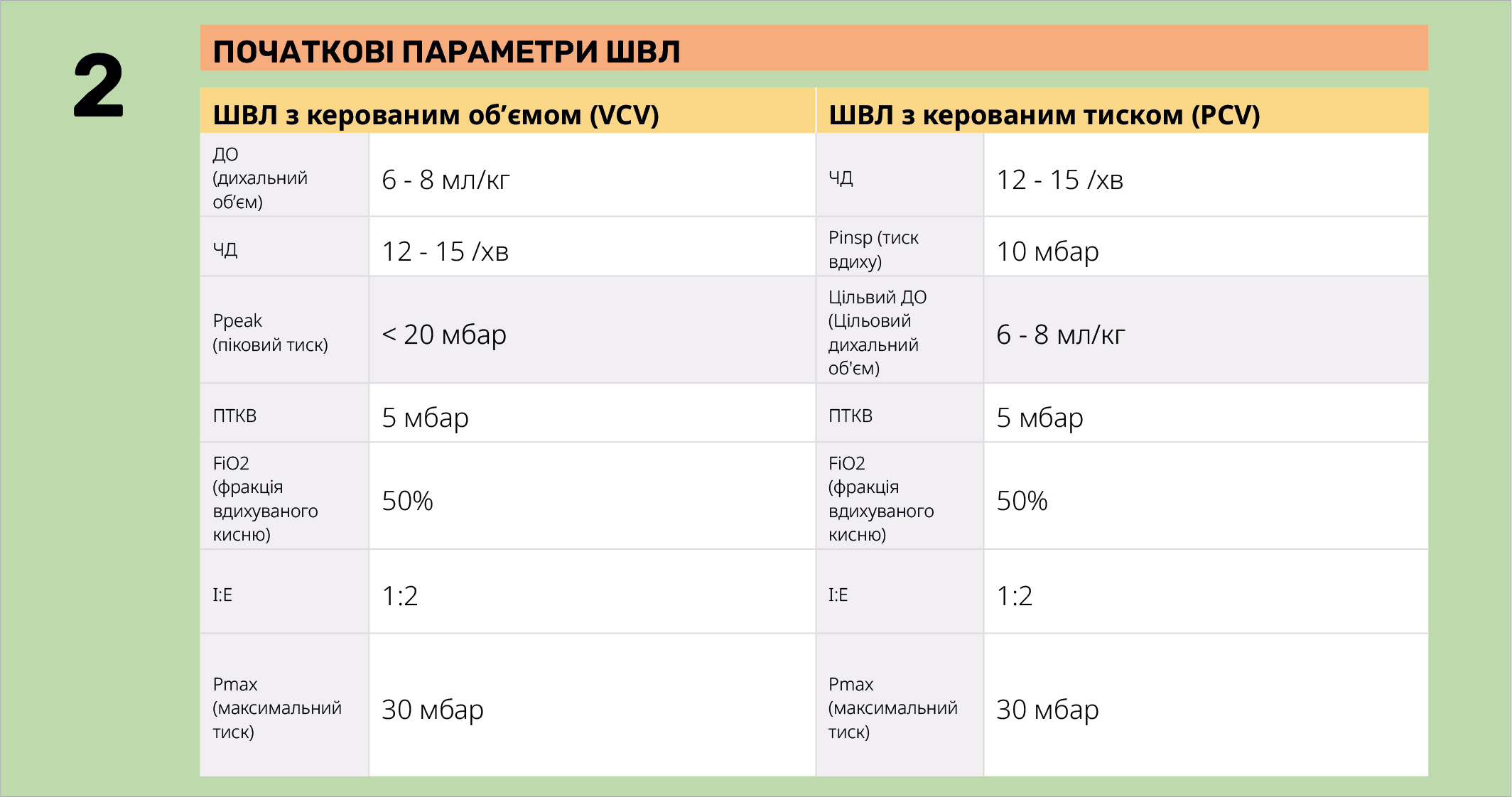
Налаштування режиму з керованим об’ємом (VCV)
- Дихальний об’єм (ДО): 6–8 мл/кг ідеальної маси тіла. Забезпечує подачу цільового об’єму газу при кожному вдиху та мінімізує ризик надмірного розтягнення альвеол.
- Частота дихання (ЧД): 12–15/хв. Підтримує адекватну вентиляцію та залишає достатній час для інфляції і видиху.
- Піковий тиск вдиху (Ppeak): <20 мбар. Обмеження для профілактики надмірного тиску в дихальних шляхах та ушкодження легень.
- Позитивний тиск наприкінці видиху (ПТКВ): 5 мбар. Запобігає спадінню альвеол після видиху, підвищує ефективність оксигенації.
- FiO₂: початково 50 %. Забезпечує баланс між адекватною оксигенацією та профілактикою кисневої токсичності.
- Співвідношення вдих: видих (І:Е): 1:2. Оптимізує тривалість фаз дихання.
- Максимальний тиск (Pmax): ≤30 мбар. Захисний ліміт для запобігання баротравмі.
Налаштування режиму з керованим тиском (PCV)
- Дихальний об’єм (ДО): цільові значення 6–8 мл/кг ідеальної маси тіла (фактичний об’єм залежить від податливості легень і опору дихальних шляхів).
- Частота дихання (ЧД): 12–15/хв.
- Тиск вдиху (Pinsp): 10 мбар. Визначає рівень тиску, що подається під час вдиху.
- Піковий тиск вдиху (Ppeak): ≤30 мбар. Контроль для уникнення надмірного тиску в дихальних шляхах.
- Позитивний тиск наприкінці видиху (ПТКВ): 5 мбар. Сприяє розкриттю альвеол і покращенню газообміну.
- FiO₂: початково 50 %, із подальшою корекцією залежно від реакції пацієнта.
- Співвідношення І:Е: 1:2. Підтримує баланс між фазами вдиху та видиху.
Крок 3: Корекція налаштувань ШВЛ після старту
Після встановлення початкових параметрів і запуску апарата ШВЛ наступним кроком є корекція параметрів залежно від реакції пацієнта, зокрема з урахуванням стану оксигенації та вентиляції.

Корекція оксигенації
Якщо рівень SpO₂ (сатурація киснем) є надто високим або низьким, слід внести корективи в параметри, що впливають на оксигенацію:
- Корекція ПТКВ: Якщо SpO₂ є низькою, підвищення ПТКВ може покращити оксигенацію шляхом рекрутування спавшихся альвеол та збільшення функціональної залишкової ємності. Однак слід уникати надмірного рівня ПТКВ, оскільки це може спричинити баротравму, надмірне розтягнення легень та порушення кровообігу внаслідок зменшення венозного повернення до серця.
- Корекція FiO2: Якщо SpO₂ залишається недостатньою, незважаючи на оптимальний рівень ПТКВ , може бути необхідно підвищити FiO₂ для забезпечення адекватної доставки кисню. Навпаки, якщо SpO₂ є надто високою, рівень FiO₂ слід знизити, щоб мінімізувати ризик кисневої токсичності.
Корекція вентиляції
Щодо вентиляції, основними параметрами для корекції є дихальний об’єм (ДО) або частота дихання (ЧД) з метою забезпечення адекватної вентиляції та підтримання рівня СО2 в кінці видоху (etCO₂) в межах цільового діапазону:
- Корекція ДО (дихального об’єму): Якщо etCO₂ підвищений, збільшення дихального об’єму може сприяти більш ефективному видаленню CO₂. Однак слід уникати надмірного дихального об’єму, щоб запобігти вентиляційно-індукованому ушкодженню легень.
- Корекція ЧД (частоти дихання): Якщо etCO₂ залишається високим, збільшення ЧД може допомогти з елімінацією CO₂. При цьому важливо враховувати ЧД разом із часом видиху, який визначається встановленим співвідношенням I:E. Занадто висока частота дихання при короткому часі видиху може призвести до неповного випорожнення легень, що викликає накладання дихальних циклів (breath stacking).
Коригування зазначених параметрів має здійснюватися поступово та з урахуванням клінічного стану пацієнта, результатів газів крові та фізіологічної відповіді організму. Постійний моніторинг SpO₂, etCO₂ та PaO₂ (парціального тиску кисню — за наявності аналізу газового складу артеріальної кров) є критично важливим для правильного налаштування вентиляції, що дозволяє забезпечити адекватну оксигенацію та вентиляцію, зменшуючи ризик ушкодження легень.
ЧАСТИНА 2: МОЖЛИВІ ПРОБЛЕМИ ПІД ЧАС ВИКОРИСТАННЯ ШВЛ
Критичні інциденти під час транспортування у відділення інтенсивної терапії, особливо пов’язані з порушенням вентиляції, становлять суттєвий ризик для результатів лікування пацієнтів і створюють унікальні виклики для бригад екстреної медичної допомоги та транспортування.
Міжлікарняне транспортування пацієнтів у критичному стані, які потребують респіраторної підтримки, часто супроводжується ускладненнями, зокрема порушенням вентиляції. Дослідження Одетоли та ін. (2015)28 продемонструвало, що транспортування дітей з дихальною недостатністю з відділень інтенсивної терапії рівня II до відділень рівня I нерідко супроводжується розвитком критичних інцидентів через нестабільний стан пацієнтів. Це підкреслює необхідність постійного моніторингу та ефективного контролю респіраторного статусу під час транспортування.
Сурі та ін. (2020)29 наголосили, що дихальна недостатність є однією з провідних причин транспортування критично хворих вагітних пацієнток, які часто потребують розширених респіраторних втручань. Це ускладнює процес транспортування та підвищує ризик розвитку критичних інцидентів.
Чавла та ін. (2013)30 зазначили, що у пацієнтів із гіпертензивними розладами та сепсисом нерідко виникає необхідність у проведенні респіраторної підтримки вже на етапі госпіталізації до відділення інтенсивної терапії, що додатково підкреслює важливість належного управління вентиляцією під час транспортування.
Пандемія COVID-19 ще більше висвітлила труднощі, пов’язані з контролем вентиляції у пацієнтів під час транспортування, зокрема у випадках застосування високотехнологічних методів, таких як екстракорпоральна мембранна оксигенація (ECMO). Дослідження Аллена та ін. (2020) та Вонга та ін. (2021)31 підтвердили необхідність високої кваліфікації бригад транспортування у застосуванні розширених методів вентиляційної підтримки, оскільки дихальна недостатність, пов’язана з COVID-19, суттєво підвищує ризик виникнення критичних інцидентів.
Таким чином, належне проведення ШВЛ та впровадження удосконалених протоколів, а також залучення добре підготовлених бригад транспортування є ключовими умовами для мінімізації ризиків та підвищення безпеки пацієнтів під час високоризикових транспортувань.
28 Odetola, F. O., Clark, S. J., Gurney, J. G., Donohue, J. E., Gebremariam, A., DuBois, L., … & Freed, G. L. (2015). Factors associated with interhospital transfer of children with respiratory failure from level ii to level i pediatric intensive care units. Journal of Critical Care, 30(5), 1080-1084. https://doi.org/10.1016/j.jcrc.2015.06.008
29 Suri, J., Suri, J. C., Kumar, R., & Gupta, A. (2020). A prospective study of clinical characteristics and interventions required in critically ill obstetric patients. Indian Journal of Critical Care Medicine, 24(8), 677-682. https://doi.org/10.5005/jp-journals-10071-23519
30 Chawla, S., Nakra, M., Mohan, S. S., Nambiar, B., Agarwal, R., & Marwaha, A. (2013). Why do obstetric patients go to the icu? a 3-year- study. Medical Journal Armed Forces India, 69(2), 134-137. https://doi.org/10.1016/j.mjafi.2012.08.033
31 Allen, R., Wanersdorfer, K., Zebley, J. A., Shapiro, G., Coullahan, T., & Sarani, B. (2020). Interhospital transfer of critically ill patients because of coronavirus disease 19–related respiratory failure. Air Medical Journal, 39(6), 498-501. https://doi.org/10.1016/j.amj.2020.07.007
СОП B2: ПРОБЛЕМИ ПІД ЧАС ВИКОРИСТАННЯ ШВЛ (див. Додаток 12)
Оцінити характер зміни стану: раптовий чи поступовий
Першим кроком у реагуванні на дихальну недостатність є оцінка того, чи погіршення стану пацієнта сталося раптово чи розвивалося поступово.

Раптова зміна: йдеться про стрімке погіршення стану пацієнта, яке супроводжується значними, раптовими змінами життєво важливих показників, зокрема:
- Десатурація (низький рівень SpO₂)
- Зміни показника etCO₂
- Виражена дихальна недостатність (респіраторний дистрес)
Поступова зміна: Цей сценарій включає тривожні сигнали (наприклад, підвищений тиск вдиху, тенденція до зниження сатурації), які вказують на повільний розвиток проблем, таких як несправність обладнання, десинхронізація з апаратом ШВЛ або обструкція дихальних шляхів. Пацієнт може демонструвати поступові зміни з часом, зокрема поступове зниження показників оксигенації або вентиляції.
Невідкладні дії у разі раптового чи поступового погіршення показників
Після того, як визначено тип зміни, слід розпочати відповідну реакцію:

Раптове погіршення показників
У разі раптового погіршення стану пацієнта під час штучної вентиляції легень необхідно діяти негайно й рішуче. Першим кроком є від’єднання пацієнта від апарата ШВЛ і зняття всіх пристроїв, під’єднаних до пристрою, який забезпечує прохідність дихальних шляхів (ендотрахеальної трубки чи трахеостомічної трубки), зокрема фільтрів та CO₂-датчиків. Це швидке від’єднання допомагає усунути можливі джерела проблеми та дає змогу точніше оцінити стан пацієнта. Далі слід розпочати ручну вентиляцію за допомогою мішка Амбу. Бажано використовувати мішок, оснащений клапаном позитивного тиску в кінці видиху (ПТКВ ), та під’єднаний до джерела кисню з високим потоком. Така мануальна вентиляція забезпечує життєво необхідну респіраторну підтримку, доставляючи кисень безпосередньо пацієнту та сприяючи стабілізації його стану.
Перехід на ручну вентиляцію дозволяє медичним працівникам оперативно реагувати на невідкладні потреби пацієнта у стані погіршення. Такий підхід дає змогу швидко стабілізувати стан хворого та забезпечити лікарю безпосередню оцінку клінічної картини. Крім того, це усуває потенційні ускладнення, пов’язані з роботою апарата ШВЛ та його комплектуючих, що дає змогу зосередитися на більш цілеспрямованих і ефективних діях відповідно до потреб пацієнта.
Поступове погіршення показників
Коли стан пацієнта змінюється поступово, метод реагування слід адаптувати. У випадках поступових змін стану пацієнта слід залишити підключеним до апарата ШВЛ з поточними налаштуваннями. Медичний персонал повинен негайно перейти до фази ОЦІНКИ та використати протокол DOPES для систематичної перевірки можливих причин.
ОЦІНИТИ: СИСТЕМАТИЧНА ПЕРЕВІРКА ЗА ПРОТОКОЛОМ DOPES
Після здійснення відповідної реакції слід провести детальну оцінку, щоб виявити першопричину відмови вентиляції. Протокол DOPES забезпечує систематичний підхід до оцінки можливих проблем:
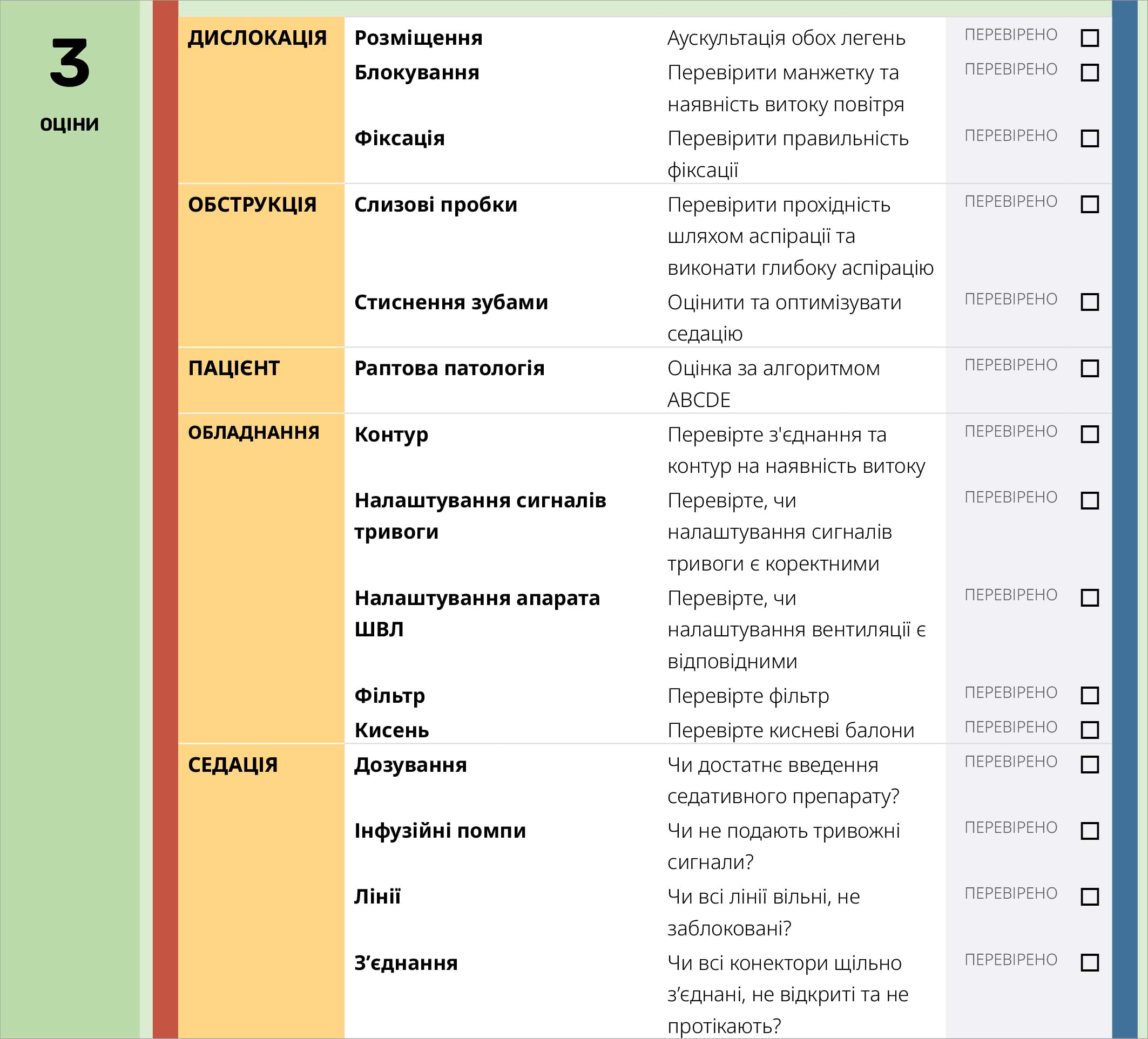
Дислокація (D): дислокація передбачає рух або неправильне положення ендотрахеальної трубки (IT) від її правильного розташування в трахеї, що може перешкоджати адекватній вентиляції та призвести до ускладнень. Медичні працівники повинні уважно стежити за ознаками зміщення трубки й негайно реагувати на них шляхом її корекції або фіксації, щоб відновити оптимальне положення в дихальних шляхах і забезпечити ефективну вентиляцію.
Обструкція (O): обструкція стосується будь-якого блокування або перешкоди для проходження повітря в дихальних шляхах, наприклад, через секрети, слизові пробки або перегини у контурі вентилятора. Виявлення ознак обструкції дихальних шляхів і своєчасне реагування на них за допомогою таких втручань, як відсмоктування, зміна положення пацієнта або перевірка вентиляційного контуру, є критично важливими для підтримання прохідності дихальних шляхів і забезпечення ефективної вентиляції.
Пацієнт (P): компонент «Пацієнт» охоплює будь-яку патологію, яка може змінити вентиляційні потреби пацієнта або вимагати негайного втручання, наприклад, пневмоторакс чи інші гострі стани. Важливо своєчасно розпізнати стани, які можуть швидко змінити потребу в респіраторній підтримці. Для всебічної оцінки стану пацієнта рекомендовано провести повну оцінку за протоколом ABCDE (Airway — прохідність дихальних шляхів, Breathing — дихання, Circulation — кровообіг, Disability — рівень свідомості, Exposure — огляд шкірних покривів та виявлення додаткових проблем). Такий підхід забезпечує виявлення і своєчасне усунення всіх чинників, що впливають на вентиляцію — як з боку дихальної, так і системної патології.
Обладнання (E): компонент «Обладнання» зосереджений на перевірці справності апарата штучної вентиляції легень (ШВЛ) та всіх пов’язаних з ним елементів. Слід розпочати з огляду налаштувань вентилятора, роботи сигналів тривоги, герметичності контуру та перевірки джерела подачі кисню. Необхідно переконатися, що немає від’єднань, витоків чи пошкоджень у контурі, які можуть порушити вентиляцію. Важливо пам’ятати, що всі додаткові елементи — від ендотрахеальної трубки до з’єднувачів, поворотних елементів, фільтрів тощо — можуть вийти з ладу й негативно вплинути на ефективність вентиляції. Потрібно ретельно перевірити кожен компонент, щоби виключити можливі несправності.
Седація (S): компонент «Седація» у протоколі DOPES спрямований на те, щоб рівень седації пацієнта був належним, аби уникнути асинхронії між пацієнтом і апаратом ШВЛ, що може погіршити респіраторний стан. Насамперед ретельно перевірте інфузійні помпи, якими вводяться седативні препарати. Оцініть швидкість введення, дозування та розведення препаратів, щоб переконатися, що вони відповідають клінічним потребам пацієнта. Швидкість та дози мають відповідати стану хворого — це забезпечить достатню седацію та комфорт.
Далі перевірте інфузійні лінії на наявність можливих проблем, таких як перегини або витоки, які можуть впливати на введення седативних препаратів. Пройдіться вздовж ліній до триходових кранів на венозному доступі (якщо це периферичний або центральний доступ). Переконайтеся, що вони правильно розташовані, відкриті та не мають витоків.
Насамкінець перевірте сам венозний доступ, щоб упевнитися, що він залишається цілісним, не перегнутий і не заблокований. Якщо виявлено будь-які порушення, слід негайно вжити відповідних заходів відповідно до ваших спостережень, щоб забезпечити ефективне введення седативних препаратів і досягти синхронізації пацієнта з апаратом ШВЛ.
ПОВТОРНА ОЦІНКА: ПОСТІЙНИЙ МОНІТОРИНГ І КОРЕКЦІЯ
Після первинного втручання та стабілізації пацієнта необхідний постійний моніторинг для оцінки його реакції та корекції подальших дій. Регулярно повторно оцінюйте показники життєдіяльності, параметри апарату ШВЛ та загальний клінічний стан пацієнта.
- Якщо стан пацієнта стабілізується, продовжуйте моніторинг і переконайтеся, що вентиляція є ефективною та адекватною..
- Якщо ж погіршення зберігається, слід повторно розглянути протокол DOPES і провести переоцінку ситуації, за потреби залучивши додаткові діагностичні тести, візуалізацію або інші втручання.
Висновок: алгоритм ведення пацієнта у разі порушення вентиляції
Протокол B2 забезпечує чіткий, структурований підхід до управління несправністю вентиляції у критично хворих пацієнтів. Завдяки розрізненню раптових і поступових змін у стані пацієнта, своєчасному переходу на ручну вентиляцію та системній оцінці потенційних причин за допомогою протоколу DOPES, медичні працівники можуть ефективно усувати проблеми з вентиляцією та забезпечувати стабільність пацієнта. Протокол дозволяє швидко виявити першопричину погіршення, застосувати цілеспрямовані втручання та підтримувати оптимальну респіраторну підтримку, тим самим покращуючи результати лікування пацієнтів і мінімізуючи ризики, пов’язані з несправністю вентиляції.
ЧАСТИНА 3: ГОСТРИЙ РЕСПІРАТОРНИЙ ДИСТРЕС- СИНДРОМ
ВСТУП
Гострий респіраторний дистрес-синдром (ГРДС) — це загрозливий для життя стан, який характеризується стрімким початком гіпоксемії та двобічними інфільтратами в легенях за відсутності гіпертензії в лівому передсерді. Цей стан вражає значну частину пацієнтів, яких транспортують у критичному стані в Україні, і становить особливі труднощі щодо вентиляції. ГРДС може виникати внаслідок низки прямих і непрямих ушкоджень легень, зокрема травми, пневмонії, аспірації та сепсису. Його патофізіологія зумовлена гострим запаленням, підвищеною проникністю альвеолярно-капілярної мембрани та набряком легень, що разом порушують газообмін і знижують податливість легень. Незважаючи на досягнення в інтенсивній терапії, ГРДС залишається основною причиною захворюваності та смертності у відділеннях інтенсивної терапії (ВІТ). Рівень смертності при ГРДС становить від 35% до 50% залежно від тяжкості стану та основних причин (Раньєрі та ін., 2012; Томпсон та ін., 2017)32,33.
Лікування ГРДС залишається переважно підтримувальним, а механічна вентиляція є основою догляду. Лікування ГРДС ускладнюється необхідністю балансувати між адекватною оксигенацією та вентиляцією і ризиком вентилятор-індукованого ушкодження легень (VILI), яке може погіршити стан. VILI при ГРДС виникає внаслідок таких факторів, як надмірне розтягнення альвеол (волюмотравма), повторне відкриття і закриття ателектазів легень (ателектотравма) та вивільнення запальних медіаторів (біотравма). Тому вентиляційні стратегії мають ретельно обиратись з урахуванням зниження цих ризиків при забезпеченні достатньої оксигенації та вентиляції.
Кілька досліджень показали, що ранні та відповідні втручання, такі як стратегії захисної вентиляції легень і допоміжна терапія, можуть покращити показники виживаності при ГРДС. Останні дослідження також підкреслюють роль індивідуального догляду, особливо в контексті адаптованих стратегій механічної вентиляції (Аль-Хусінат та ін., 2025)34. З огляду на високі показники смертності та складний характер лікування ГРДС, безперервний моніторинг і гнучкі плани лікування є необхідними для покращення результатів для пацієнтів. Цей настановний документ має на меті надати огляд найновіших доказів щодо лікування ГРДС з акцентом на загальні стратегії вентиляції та їхню роль у зниженні смертності та покращенні одужання пацієнтів.
32 Ranieri, V. M., Rubenfeld, G. D., Thompson, B. T., Ferguson, N. D., Caldwell, E., & the ARDS Definition Task Force. (2012). Acute respiratory distress syndrome: The Berlin Definition. JAMA, 307(23), 2526-2533. https://doi.org/10.1001/jama.2012.5669
33 Thompson, B. T., Chambers, R. C., & Liu, K. D. (2017). Acute respiratory distress syndrome. New England Journal of Medicine, 377(6), 562-572. https://doi.org/10.1056/NEJMra1608077
34 Al-Husinat, L., Azzam, S., Al Sharie, S., Araydah, M., Battaglini, D., Abushehab, S., Cortes-Puentes, G. A., Schultz, M. J., & Rocco, P. R. M. (2025). A narrative review on the future of ARDS: evolving definitions, pathophysiology, and tailored management. Critical Care, 29, Article number: 88. https://doi.org/10.1186/s13054-025-05291-0
ЗАГАЛЬНИЙ ПІДХІД ДО ВЕДЕННЯ ГРДС
Лікування ГРДС переважно зосереджене на оптимізації вентиляції для покращення оксигенації при мінімізації подальшого ушкодження легень. Основною метою механічної вентиляції при ГРДС є досягнення адекватної оксигенації та вентиляції при запобіганні або мінімізації вентилятор- індукованого ушкодження легень (VILI). VILI може виникати внаслідок кількох факторів, зокрема надмірного дихального об’єму, високого тиску в дихальних шляхах і недостатнього позитивного тиску в кінці видиху (ПТКВ ). Основні стратегії вентиляції при ГРДС включають:
Вентиляція з низьким дихальним об’ємом: використання низьких дихальних об’ємів (зазвичай 4–8 мл/кг ідеальної маси тіла) є наріжним каменем лікування ГРДС. Низькі дихальні об’єми допомагають знизити ризик волюмотравми, запобігаючи надмірному розтягненню альвеол35. Пацієнти з ГРДС особливо вразливі до цього явища, оскільки зміни паренхіми легень часто мають вогнищевий характер: деякі ділянки мають майже нормальну податливість, тоді як інші повністю спалися. Під час застосування високих тисків до легень, як у випадку рекрутингових маневрів, це одночасно призводить до надмірного розтягнення в одних ділянках легень, тоді як тиск усе ще недостатній для відкриття альвеол в інших ділянках тих самих легень. Дослідження ГРДС Network (2000)36 продемонструвало, що використання вентиляції з низьким дихальним об’ємом значно покращує показники виживаності у пацієнтів з ГРДС порівняно з раніше використовуваними дихальними об’ємами (12 мл/кг).
Позитивний тиск в кінці видиху (ПТКВ ): використовується для запобігання колапсу альвеол наприкінці видиху, що покращує оксигенацію та запобігає ателектазу. Оптимальний рівень ПТКВ варіюється залежно від пацієнта, з урахуванням його стану оксигенації та механіки легень. Вищі рівні ПТКВ зазвичай застосовуються при середньому та тяжкому ГРДС для покращення рекрутингу альвеол і зменшення ателектотравми.
Обмеження тиску плато: обмеження тиску плато (Pplat) до рівня менше ніж 30 мбар є критично важливим для запобігання баротравмі. Тиск плато відображає тиск, який прикладається до дрібних дихальних шляхів і альвеол під час механічної вентиляції. Підтримання Pplat у цьому діапазоні допомагає мінімізувати ризик ушкодження легень, пов’язаний з високим тиском.
Положення на животі: є надзвичайно ефективною стратегією при тяжкому ГРДС, покращуючи оксигенацію та знижуючи смертність. Завдяки перерозподілу легеневого кровотоку та покращенню відповідності вентиляції та перфузії, положення на животі сприяє рекрутингу альвеол і зменшує вентилятор-асоційоване ушкодження легень. Рекомендується, щоб пацієнти з тяжким ГРДС перебували в положенні на животі щонайменше 12 годин на добу.
Допустима гіперкапнія: передбачає допущення підвищених рівнів вуглекислого газу (PaCO₂) для мінімізації ризику вентилятор-індукованого ушкодження легень. Мета полягає в тому, щоб дозволити нижчий дихальний об’єм при збереженні pH вище 7,20, надаючи пріоритет захисту легень над нормалізацією показників газів крові. Ця стратегія є особливо корисною для запобігання волюмотравмі та баротравмі у пацієнтів з ГРДС.
Додаткові методи лікування: на додаток до основних стратегій вентиляції, у певних випадках можуть застосовуватись кілька додаткових методів. До них належать кортикостероїди, нейром’язові блокатори та екстракорпоральна мембранна оксигенація (ЕКМО). Кортикостероїди можуть зменшити запалення на ранніх етапах ГРДС, тоді як нейром’язові блокатори допомагають запобігти десинхронізації пацієнта з апаратом ШВЛ. ЕКМО зазвичай застосовується для пацієнтів із тяжким, рефрактерним ГРДС, які не реагують на стандартні стратегії механічної вентиляції.
Підсумовуючи, лікування ГРДС вимагає багатокомпонентного підходу, зосередженого на стратегіях захисту легень, які мінімізують подальше ушкодження легень та оптимізують оксигенацію. Безперервний моніторинг і корекція параметрів вентиляції залежно від індивідуальної реакції пацієнта є необхідними для покращення результатів.
35 Al-Husinat L, Azzam S, Al Sharie S, Araydah M, Battaglini D, Abushehab S, Cortes-Puentes GA, Schultz MJ, Rocco PRM. Наративний огляд майбутнього ГРДС: визначення, що розвиваються, патофізіологія та індивідуальний підхід до лікування. Crit Care. 2025 Feb 24;29(1):88. doi: 10.1186/s13054-025-05291-0. PMID: 39994815; PMCID: PMC11852867.
36 ARDS Network. (2000). Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. New England Journal of Medicine, 342(18), 1301-1308. https://doi.org/10.1056/NEJM200005043421801
СОП B4: СТРАТЕГІЇ ШВЛ ПРИ ГРДС (див. Додаток 14)
СТРАТЕГІЇ МЕХАНІЧНОЇ ВЕНТИЛЯЦІЇ
Седація та використання міорелаксантів
Під час транспортування пацієнта з ГРДС у критичному стані керування седацією та міорелаксацією відіграє вирішальну роль у забезпеченні безпечного та ефективного транспортування. Нижче наведено додаткову інформацію щодо важливості седації та міорелаксації в цьому контекстіі:

Керування седацією
Забезпечення адекватної седації. Седація є обов’язковим етапом для зниження тривожності, запобігання психомоторному збудженню та кращої переносимості ШВЛ. Адекватна глибина седації мінімізує ризик самостійної екстубації та полегшує проведення інвазивної вентиляції.
Адекватна синхронізація пацієнта з апаратом ШВЛ. Підтримання оптимального рівня седації зменшує асинхронію «пацієнт–апарат» (patient–ventilator dyssynchrony), сприяє ефективній реалізації протективної вентиляційної стратегії та знижує ризик розвитку вентилятор-індукованого ушкодження легень (VILI).
Метаболічна розвантаженість. Седативні препарати зменшують споживання кисню (VO₂) та продукцію вуглекислого газу (VCO₂), що оптимізує баланс оксигенації та вентиляції у пацієнтів із ГРДС.
Особливості застосування міорелаксантів
Зниження потреби у кисні. Нейром’язові блокатори (міорелаксанти) зменшують метаболічні витрати та усувають парадоксальні дихальні рухи, що сприяє стабілізації газообміну у пацієнтів із рефрактерною гіпоксемією.
Захисна вентиляція легень. Використання міорелаксантів у пацієнтів із тяжким ГРДС дозволяє уникнути десинхронізації з апаратом ШВЛ, забезпечує сталість параметрів вентиляції (обмеження ДО, контрольоване застосування ПТКВ) та знижує ризик волюмотравми й баротравми.
Безпека транспортування. Використання міорелаксантів мінімізує ризик зміщення ендотрахеальної трубки, від’єднання дихального контуру та пошкодження внутрішньосудинних катетерів під час транспортування, забезпечуючи стабільність і контрольованість клінічного стану.
Примітка. Застосування міорелаксантів можливе лише після досягнення цільового рівня седації (за шкалою RASS від –3 до –5) і за умови постійного моніторингу життєвих показників, сатурації (SpO₂), капнографії (EtCO₂) та газового складу артеріальної крові (ABG).
Обмежений дихальний об’єм
Проведення протективної ШВЛ передбачає суворий контроль дихального об’єму (ДО):

Уражені легені характеризуються нерівномірним розподілом напруження та розтягнення. Добре вентильовані ділянки отримують більший об’єм газу, тоді як інші сегменти, які перебувають у стані колапсу або гіповентиляції, залишаються нефункціональними. При рекрутуванні раніше невентильованих альвеол важливо уникати повторюваних циклів їхнього спадання та відкриття, оскільки це призводить до надмірного механічного навантаження на легеневу тканину, відомого як ателектотравма. Механічні сили під час ШВЛ можуть ушкоджувати альвеолоцити І та ІІ типу, ендотеліальні клітини та міжальвеолярні структури, а також індукувати системну запальну відповідь.
Вентилятор-асоційоване ушкодження легень (VALI) описує загострення вже існуючого ураження легень унаслідок впливу механічних сил під час ШВЛ. Високе напруження та надмірне розтягнення альвеол призводять до розвитку баротравми та волюмотравми. Навіть помірний рівень механічного стресу може стимулювати вивільнення прозапальних цитокінів, що сприяє прогресуванню системної запальної відповіді (SIRS), розвитку поліорганної недостатності та підвищенню летальності у пацієнтів із ГРДС.
Стратегії захисної вентиляції легень
Захисна вентиляція легень має на меті рівномірний розподіл напруження та мінімізацію ушкодження легеневої тканини шляхом: використання малих дихальних об’ємів (4–6 мл/кг ідеальної маси тіла); обмеження тиску плато (Pplat) < 30 см H₂O; контролю тиску комплансу або драйвінгового тиску (ΔP) ≤ 15 см H₂O; застосування позитивного тиску в кінці видиху (ПТКВ) для запобігання спадінню альвеол і підтримки постійної оксигенації. Допускається проведення стратегії допустимої гіперкапнії, яка полягає у свідомому підвищенні рівня PaCO₂ для уникнення ушкодження легеневої тканини за рахунок надмірної вентиляції. У більшості пацієнтів із критичними станами гіперкапнія переноситься без значної шкоди для головного мозку, серця чи нирок, за умови відсутності протипоказань (внутрішньочерепна гіпертензія, тяжка метаболічна ацидоз).
Розрахунок ідеальної маси тіла
Для розрахунку дихального об’єму під час ШВЛ необхідно використовувати ідеальну масу тіла (ІМТ, PBW), яка визначається за зростом пацієнта:
- Для чоловіків: ІМТ (кг) = 50 + 0,91 × (зріст у см – 152,4)
- Для жінок: ІМТ (кг) = 45,5 + 0,91 × (зріст у см – 152,4)
Результати клінічних досліджень свідчать, що застосування дихальних об’ємів > 7 мл/кг ідеальної маси тіла може спричиняти надмірне розтягнення легеневої тканини у більшості пацієнтів із ГРДС37.
37 Roupie E, Dambrosio M, Servillo G, Mentec H, el Atrous S, Beydon L, Brun-Buisson C, Lemaire F, Brochard L. Titration of tidal volume and induced hypercapnia in acute respiratory distress syndrome. Am J Respir Crit Care Med. 1995 Jul;152(1):121-8. doi: 10.1164/ ajrccm.152.1.7599810. PMID: 7599810 .
Кілька рандомізованих контрольованих досліджень (РКД) довели, що використання малих дихальних об’ємів (≤ 6 мл/кг) знижує рівень системного запалення та зменшує показники летальності порівняно з використанням великих об’ємів (≥ 12 мл/кг)38. Разом із тим встановлено, що високий тиск плато (Pplat > 30 мбар) нівелює позитивний ефект низькооб’ємної вентиляції на зниження госпітальної смертності.
Настанови кампанії Surviving Sepsis рекомендують: застосування дихального об’єму ≤ 6 мл/кг ідеальної маси тіла у пацієнтів із ГРДС, зокрема у хворих на тяжкий сепсис або септичний шок; підтримання тиску плато нижче 30 мбар; обмеження тиску комплансу або драйвінгового (ΔP) до ≤ 15 мбар як ключового параметра профілактики вентилятор-індукованого ушкодження легень (VILI).
Титриметричні рівні ПТКВ (індивідуально підібрані рівня ПТКВ)
Оптимізація позитивного тиску в кінці видиху (ПТКВ) є невід’ємною складовою вентиляційної стратегії при ГРДС. Мета: покращення оксигенації, рекрутування альвеол та мінімізація ризику ателектотравми і VILI. Титрування: індивідуальний підбір рівня ПТКВ рекомендовано проводити з урахуванням механіки дихання та газообміну. Докази: у дослідженні «PEEP Titration to Minimize Driving Pressure in Subjects With ГРДС: A Prospective Physiological Study» показано, що зниження тиску комплансу або драйвінгового (ΔP) є ключовим орієнтиром при виборі рівня ПТКВ. Практичне застосування: у закладах із високим рівнем ресурсного забезпечення можливе використання стандартизованих стратегій титрування ПТКВ, що включають покрокову зміну параметрів і оцінку ΔP, SpO₂, PaO₂/FiO₂ та комплаєнсу легень.
Висновок. Дотримання структурованого підходу до налаштування ПТКВ дає змогу індивідуалізувати респіраторну підтримку, покращуючи оксигенацію та знижуючи ризик вентилятор-індукованого ушкодження.
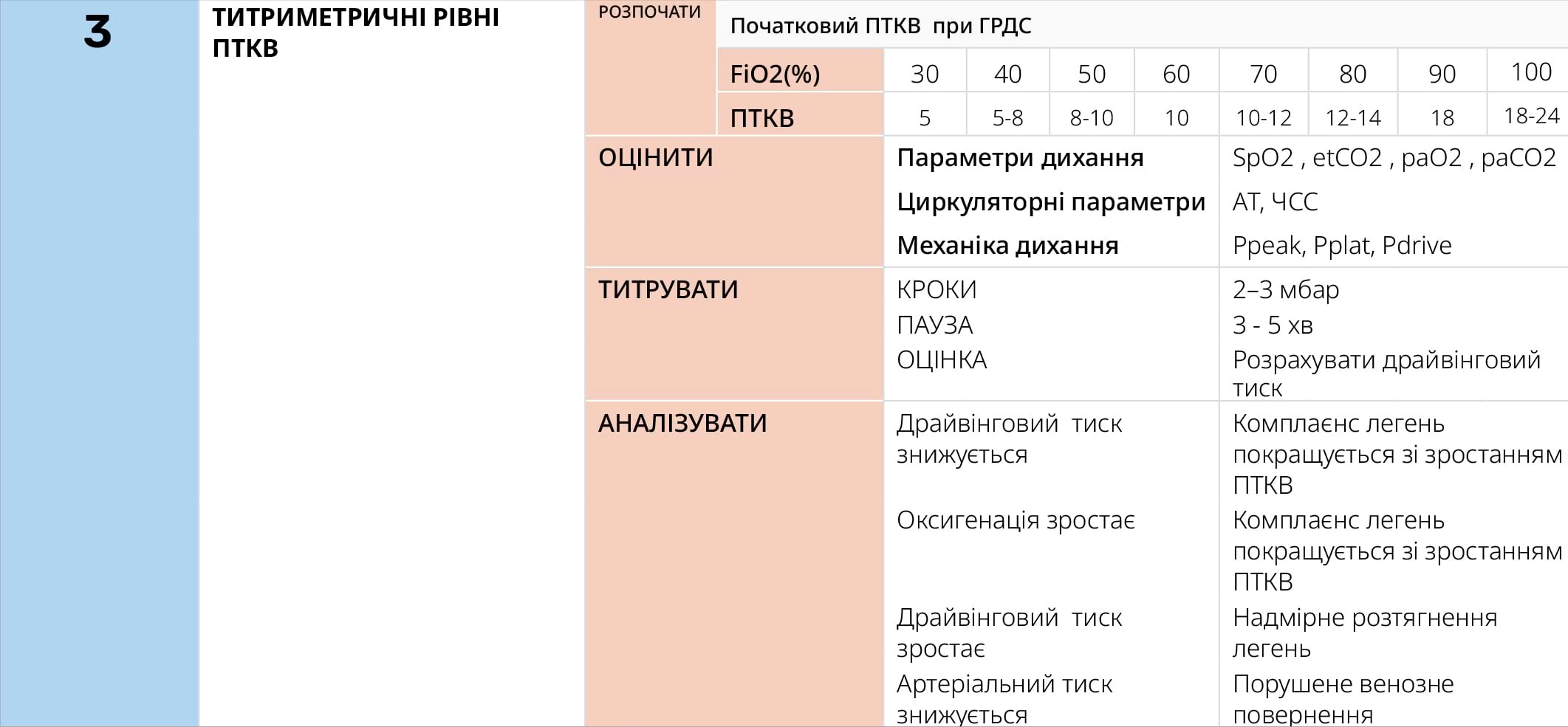
Встановлення параметрів вентиляції при ГРДС
На початку вентиляції доцільно встановлювати рівні ПТКВ відповідно до встановлених настанов, таких як таблиця нижчих значень ПТКВ /FiO₂ ГРДС Network. Це забезпечує науково обґрунтовану відправну точку, яка спрямована на баланс між оксигенацією та мінімізацією механічного навантаження на легені та, як показано, знижує смертність у пацієнтів із ГРДС39. Намагаючись оптимізувати оксигенацію пацієнта, надзвичайно важливо уникати ненавмисного ушкодження. Високі початкові рівні ПТКВ (принаймні вище 10–12 мбар) несуть ризик порушення кровообігу та підвищують імовірність ускладнень, безпосередньо пов’язаних із нашим лікуванням, особливо у пацієнтів, для яких ми активно уникаємо перевантаження рідиною — що є загальновизнаною стратегією при ГРДС. У пацієнтів без безперервного інвазивного моніторингу артеріального тиску це особливо важливо40. Початковий FiO₂ також слід коригувати разом із ПТКВ , орієнтуючись на цільові показники оксигенації, такі як SpO₂ ≥ 88–92%. Мета полягає в тому, щоб забезпечити збалансовану стартову точку для оксигенації, уникаючи надмірного навантаження на легені.
38 Acute Respiratory Distress Syndrome Network; Brower RG, Matthay MA, Morris A, Schoenfeld D, Thompson BT, Wheeler A. Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. N Engl J Med. 2000 May 4;342(18):1301-8. doi: 10.1056/NEJM200005043421801. PMID: 10793162 .
ОЦІНКА РЕАКЦІЇ ПАЦІЄНТА НА ПОЧАТКОВИЙ РІВЕНЬ ПТКВ
Після встановлення початкових параметрів вкрай важливо уважно спостерігати за реакцією пацієнта. Такі показники, як SpO₂, PaO₂, etCO₂ і артеріальний тиск, надають цінну інформацію про те, як пацієнт реагує на вентиляцію. Не менш важливими є й показники респіраторної механіки, зокрема тиск плато (Pplat) і драйвінговий тиск (різниця між Pplat і ПТКВ ), які слугують важливими індикаторами механічного навантаження та стресу для легень. Відстежуючи ці параметри, медичні працівники можуть швидко визначити, чи є користь від початкових налаштувань, чи необхідна корекція.
ПІДБІР ПТКВ І ОПТИМІЗАЦІЯ ДРАЙВІНГВОГО ТИСКУ: ВИЗНАЧЕННЯ ОПТИМАЛЬНОГО РІВНЯ
Підбір позитивного тиску в кінці видиху (ПТКВ) здійснюється поступово, з кроком 2–3 мбар, із паузою у декілька хвилин для оцінки впливу на параметри газообміну та респіраторної механіки41.
Показання: наявність ателектазів; збережена або прогресуюча гіпоксемія; зниження комплаєнсу легень.
Алгоритм дій у клінічних умовах (CCT, Україна):
- Забезпечити адекватний рівень седації, за потреби — міорелаксацію.
- Виконати інспіраторну паузу, визначити тиск плато (Pplat) та розрахувати драйвінговий тиск (різниця між тиском плато та рівнем ПТКВ).
- Підвищити ПТКВ на 2–3 мбар. Через декілька хвилин оцінити: рівень сатурації (SpO₂, SaO₂) та гази артеріальної крові (PaO₂); показники системної гемодинаміки (артеріальний тиск, частота серцевих скорочень); зміни драйвінгового тиску.
- Повторити інспіраторну паузу та повторно розрахувати драйвінговий тиск.
Інтерпретація: якщо драйвінговий тиск зменшується та/або покращуються показники оксигенації — це свідчить про рекрутмент альвеол та підвищення комплаєнсу легень; ПТКВ може бути збільшено повторно; якщо драйвінговий тиск зростає, спостерігається зниження артеріального тиску або інші ознаки гемодинамічного компромісу — рівень ПТКВ необхідно повернути до попереднього значення або знизити.
39 Guo L, Xie J, Huang Y, Pan C, Yang Y, Qiu H, Liu L. Higher PEEP improves outcomes in ARDS patients with clinically objective positive oxygenation response to PEEP: a systematic review and meta-analysis. BMC Anesthesiol. 2018 Nov 17;18(1):172. doi: 10.1186/s12871- 018-0631-4. PMID: 30447683; PMCID: PMC6240288.
40 Inglis R, Ayebale E, Schultz MJ. Optimizing respiratory management in resource-limited settings. Curr Opin Crit Care. 2019 Feb;25(1):45- 53. doi: 10.1097/MCC.0000000000000568. PMID: 30531535; PMCID: PMC6319564.
41 Sahetya SK, Goligher EC, Brower RG. Fifty Years of Research in ARDS. Setting Positive End-Expiratory Pressure in Acute Respiratory Distress Syndrome. Am J Respir Crit Care Med. 2017 Jun 1;195(11):1429-1438. doi: 10.1164/rccm.201610-2035CI. Erratum in: Am J Respir Crit Care Med. 2018 Mar 1;197(5):684-685. doi: 10.1164/rccm.1976Erratum1. PMID: 28146639; PMCID: PMC5470753
Мета: визначити оптимальний рівень ПТКВ, який забезпечує адекватний рекрутмент альвеол та покращення оксигенації без надмірного розтягнення легеневої тканини та без негативного впливу на гемодинаміку.
Урахування клінічних факторів
Під час корекції рівня ПТКВ необхідно враховувати індивідуальні особливості пацієнта: ступінь тяжкості ГРДС; наявність супутніх станів (набряк легень, серцева недостатність, інші патології); загальний клінічний статус пацієнта. Обов’язковим є ретельний контроль гемодинамічної стабільності, оскільки надмірний рівень ПТКВ може знижувати венозне повернення, спричиняти артеріальну гіпотензію та зменшувати серцевий викид. Розуміння цих факторів дозволяє клініцисту приймати обґрунтовані рішення, які виходять за межі лише досягнення цільової оксигенації і враховують загальну стабільність пацієнта.
Примітка. Універсальної схеми не існує. Вирішальне значення має безперервний моніторинг параметрів вентиляції з корекцією ПТКВ таким чином, щоб мінімізувати драйвінговий тиск, оптимізувати оксигенацію та знизити ризик вентилятор-індукованого ушкодження легень (VILI). Такий підхід дозволяє реалізувати персоналізовану, адаптивну стратегію, яка поєднує захист легень та задоволення потреб пацієнта.
ОБМЕЖЕННЯ ТИСКІВ
У великих ретроспективних аналізах пацієнтів із сепсисом та гострою дихальною недостатністю встановлено, що кінцево-інспіраторний тиск понад 30 см вод. ст. асоціюється зі зростанням смертності (10). Це підкреслює критичну важливість моніторингу та контролю дихальних тисків при веденні ГРДС.

Значення інспіраторного тиску, особливо драйвінгового тиску (різниця між тиском плато та рівнем ПТКВ), вивчено у низці клінічних робіт. Високий рівень драйвінгового тиску асоціюється з підвищеною летальністю незалежно від абсолютного рівня ПТКВ чи тиску плато. У масштабному обсерваційному дослідженні (n=2377, пацієнти з ГРДС) було доведено, що нижчий драйвінговий тиск асоціюється з покращенням виживаності, поряд із застосуванням високого ПТКВ, низького інспіраторного тиску та меншої частоти вентиляції42.
ДОПУСТИМА ГІПЕРКАПНІЯ
Допустима гіперкапнія передбачає свідоме прийняття підвищеного рівня PaCO₂ (зазвичай 50–60 мм рт. ст. або 6,7–8,0 кПа) в обмін на використання знижених дихальних об’ємів (близько 6 мл/кг ідеальної маси тіла) у рамках стратегії захисної вентиляції легень. Механізм і клінічне значення: ниркова компенсація респіраторного ацидозу з підтриманням pH > 7,20; зниження ризику VILI завдяки уникненню надмірного розтягнення та баротравми; оптимізація газообміну при збереженні протективної стратегії. Обмеження: необхідність уникати тяжких ускладнень гіперкапнії (церебральні судоми, аритмії, шунтування); підвищений внутрішньочерепний тиск (ВЧТ) є відносним протипоказанням, оскільки гіперкапнія спричиняє церебральну вазодилятацію та додаткове підвищення ВЧТ.
42 Laffey JG, Bellani G, Pham T, Fan E, Madotto F, Bajwa EK, Brochard L, Clarkson K, Esteban A, Gattinoni L, van Haren F, Heunks LM, Kurahashi K, Laake JH, Larsson A, McAuley DF, McNamee L, Nin N, Qiu H, Ranieri M, Rubenfeld GD, Thompson BT, Wrigge H, Slutsky AS, Pesenti A; LUNG SAFE Investigators та ESICM Trials Group. Potentially modifiable factors contributing to outcome from acute respiratory distress syndrome: the LUNG SAFE study. Intensive Care Med. 2016 Dec;42(12):1865-1876. doi: 10.1007/s00134-016-4571-5. Epub 2016 Oct 18. Erratum in: Intensive Care Med. 2017 Nov 14;: PMID: 27757516.
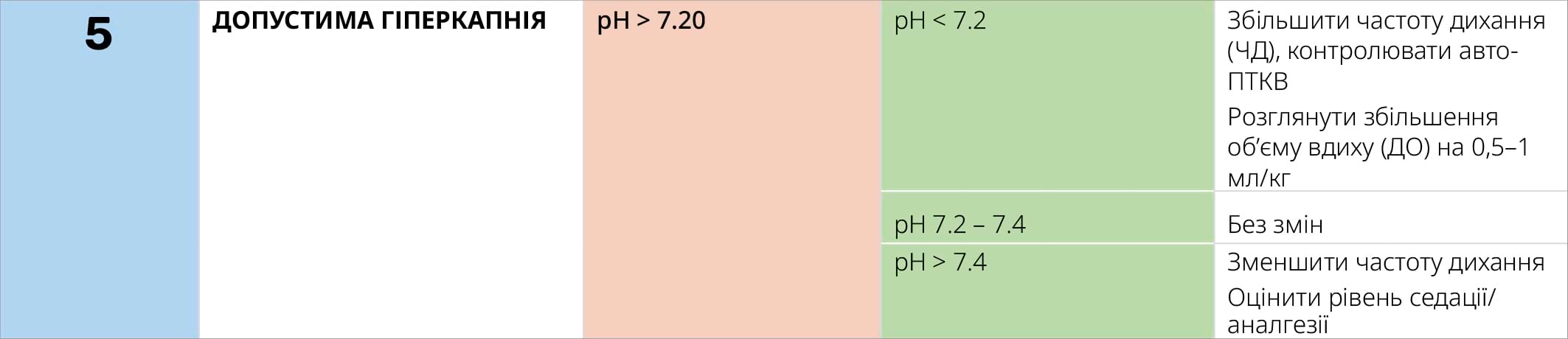
Одним із важливих аспектів, який потребує ретельного контролю у пацієнтів на штучній вентиляції легень, є мертвий простір. Це об’єм повітря в дихальній системі, який не бере участі в газообміні. Він включає анатомічний мертвий простір, що охоплює провідні дихальні шляхи, де газообмін не відбувається, а також інструментальний мертвий простір, який формується в ендотрахеальній трубці, фільтрах та з’єднувальних елементах апарата ШВЛ. Значний інструментальний мертвий простір знижує ефективність вентиляції, оскільки частина дихального об’єму «втрачається» ще до надходження газу в альвеоли. Це може збільшувати потребу у більшому вдихуваному об’ємі для досягнення того самого рівня альвеолярної вентиляції.
У контексті допустимої гіперкапнії, яка застосовується як елемент протективної вентиляції з малим дихальним об’ємом, інструментальний мертвий простір має особливе значення. Він може посилювати гіперкапнію та нівелювати переваги легенезахисної стратегії, оскільки фактичний об’єм, що надходить у легені, зменшується. У таких випадках важливим є уважне налаштування параметрів вентилятора та оптимізація дихального контуру. Використання фільтрів із нижчим опором, скорочення довжини або кількості з’єднувальних елементів дозволяють зменшити мертвий простір і підвищити ефективність вентиляції.
Допустима гіперкапнія, у свою чергу, характеризується свідомим прийняттям підвищеного рівня PaCO₂ в обмін на використання нижчих дихальних об’ємів з метою захисту легень від надмірного розтягнення та баротравми. Короткострокові наслідки такої стратегії можуть включати гіпердинамічний стан із системною вазодилатацією, який зазвичай добре переноситься пацієнтами. З боку легеневої гемодинаміки може спостерігатися підвищення середнього тиску в легеневій артерії, зазвичай без суттєвого збільшення легеневого судинного опору.
Проте у пацієнтів із відомою правошлуночковою чи лівошлуночковою серцевою недостатністю слід проявляти особливу пильність, оскільки гіперкапнія може погіршувати перебіг серцевої патології. Моніторинг змін у серцево-судинному стані є обов’язковим для ефективного контролю можливих побічних ефектів і запобігання поглибленню наявних порушень. Таким чином, оптимізація дихального контуру, контроль мертвого простору та уважне відстеження гемодинаміки є ключовими складовими при застосуванні стратегії допустимої гіперкапнії у пацієнтів із ГРДС та іншими критичними станами.
ПОВТОРНА ОЦІНКА
Завершальний етап стандартної операційної процедури (СОП) — повторна оцінка — має вирішальне значення для досягнення і підтримання цільових параметрів вентиляції та оптимізації клінічних результатів:
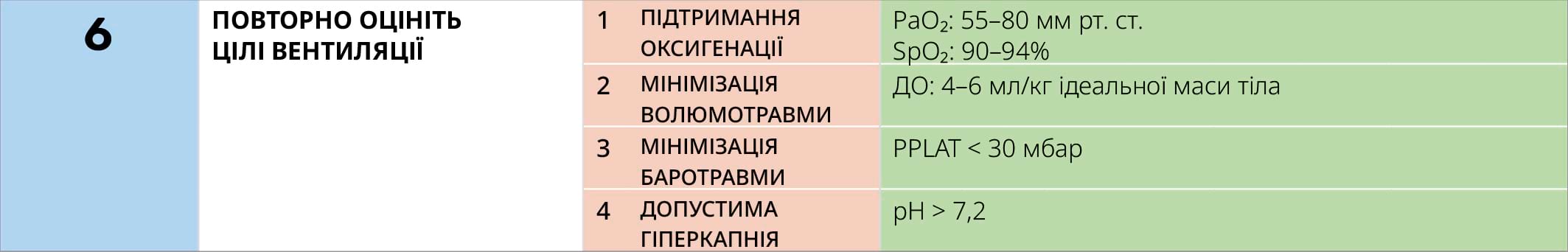
Оксигенація. Підтримка PaO₂ у межах 55–80 мм рт. ст. гарантує адекватну доставку кисню до тканин. Контроль SpO₂ у діапазоні 90–94 % є обов’язковим для профілактики гіпероксії та гіпоксії.
Волюмотравма. Мінімізація ризику ушкодження легень досягається за рахунок дотримання протективного дихального об’єму — 4–6 мл/кг ідеальної маси тіла, що знижує ступінь розтягнення альвеол.
Баротравма. Обмеження тиску плато (Pplat) < 30 мбар та підтримка драйвінгового тиску ≤ 15 мбар дозволяють уникнути надмірного механічного навантаження на альвеолярно-капілярну мембрану.
Допустима гіперкапнія. Використовується як елемент захисної вентиляції з умовою підтримання pH > 7,20, що дозволяє зменшити інтенсивність вентиляції, знизити ризик VILI та уникнути ускладнень агресивної вентиляційної стратегії.
Клінічне значення. Повторна оцінка параметрів вентиляції є безперервним процесом у веденні пацієнтів із ГРДС. Потреби у вентиляційній підтримці змінюються залежно від клінічного стану та динаміки лікування. Регулярна переоцінка й корекція налаштувань ШВЛ дозволяють адаптувати стратегію до індивідуальних потреб і забезпечують оптимальний рівень безпеки та ефективності терапії у відділенні інтенсивної терапії.
ДОВІДКОВІ МАТЕРІАЛИ
- Rietveld, P. J., Snoep, J. W. M., Lamping, M., van der Velde, F., de Jonge, E., van Westerloo, D. W., & Schoe, A. (2022). Mechanical power differs between pressure-controlled ventilation and different volume-controlled ventilation modes. *Critical Care Explorations*, 4(8), 1-9. https://doi.org/10.1097/ CCE.0000000000000741
- Odetola, F. O., Clark, S. J., Gurney, J. G., Donohue, J. E., Gebremariam, A., DuBois, L., … & Freed, G. L. (2015). Factors associated with interhospital transfer of children with respiratory failure from level II to level I pediatric intensive care units. *Journal of Critical Care*, 30(5), 1080-1084. https://doi.org/10.1016/j. jcrc.2015.06.008
- Suri, J., Suri, J. C., Kumar, R., & Gupta, A. (2020). A prospective study of clinical characteristics and interventions required in critically ill obstetric patients. *Indian Journal of Critical Care Medicine*, 24(8), 677-682. https://doi.org/10.5005/jp-journals-10071-23519
- Chawla, S., Nakra, M., Mohan, S. S., Nambiar, B., Agarwal, R., & Marwaha, A. (2013). Why do obstetric patients go to the ICU? A 3-year study. *Medical Journal Armed Forces India*, 69(2), 134-137. https://doi. org/10.1016/j.mjafi.2012.08.033
- Allen, R., Wanersdorfer, K., Zebley, J. A., Shapiro, G., Coullahan, T., & Sarani, B. (2020). Interhospital transfer of critically ill patients because of coronavirus disease 19–related respiratory failure. *Air Medical Journal*, 39(6), 498-501. https://doi.org/10.1016/j.amj.2020.07.007
- Ranieri, V. M., Rubenfeld, G. D., Thompson, B. T., Ferguson, N. D., Caldwell, E., & the ARDS Definition Task Force. (2012). Acute respiratory distress syndrome: The Berlin Definition. *JAMA*, 307(23), 2526-2533. https://doi.org/10.1001/jama.2012.5669
- Thompson, B. T., Chambers, R. C., & Liu, K. D. (2017). Acute respiratory distress syndrome. *New England Journal of Medicine*, 377(6), 562-572. https://doi.org/10.1056/NEJMra1608077
- Al-Husinat, L., Azzam, S., Al Sharie, S., Araydah, M., Battaglini, D., Abushehab, S., Cortes-Puentes, G. A., Schultz, M. J., & Rocco, P. R. M. (2025). A narrative review on the future of ARDS: evolving definitions, pathophysiology, and tailored management. *Critical Care*, 29, Article number: 88.https://doi. org/10.1186/s13054-025-05291-0
- Al-Husinat, L., Azzam, S., Al Sharie, S., Araydah, M., Battaglini, D., Abushehab, S., Cortes-Puentes, G. A., Schultz, M. J., & Rocco, P. R. M. (2025). A narrative review on the future of ARDS: evolving definitions, pathophysiology, and tailored management. *Critical Care*, 29(1), 88. https://doi.org/10.1186/s13054- 025-05291-0
- ARDS Network. (2000). Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. *New England Journal of Medicine*, 342(18), 1301-1308. https://doi.org/10.1056/NEJM200005043421801
- Roupie, E., Dambrosio, M., Servillo, G., Mentec, H., el Atrous, S., Beydon, L., Brun-Buisson, C., Lemaire, F., Brochard, L. (1995). Titration of tidal volume and induced hypercapnia in acute respiratory distress syndrome. *American Journal of Respiratory and Critical Care Medicine*, 152(1), 121-128.https://doi. org/10.1164/ajrccm.152.1.7599810
- Acute Respiratory Distress Syndrome Network; Brower, R. G., Matthay, M. A., Morris, A., Schoenfeld, D., Thompson, B. T., Wheeler, A. (2000). Ventilation with lower tidal volumes as compared with traditional tidal volumes for acute lung injury and the acute respiratory distress syndrome. *New England Journal of Medicine*, 342(18), 1301-1308. https://doi.org/10.1056/NEJM200005043421801
- Guo, L., Xie, J., Huang, Y., Pan, C., Yang, Y., Qiu, H., Liu, L. (2018). Higher PEEP improves outcomes in ARDS patients with clinically objective positive oxygenation response to PEEP: a systematic review and meta- analysis. *BMC Anesthesiology*, 18(1), 172. https://doi.org/10.1186/s12871-018-0631-4
- Inglis, R., Ayebale, E., Schultz, M. J. (2019). Optimizing respiratory management in resource-limited settings. *Current Opinion in Critical Care*, 25(1), 45-53. https://doi.org/10.1097/MCC.0000000000000568
- Sahetya, S. K., Goligher, E. C., Brower, R. G. (2017). Fifty years of research in ARDS. Setting Positive End- Expiratory Pressure in Acute Respiratory Distress Syndrome. *American Journal of Respiratory and Critical Care Medicine*, 195(11), 1429-1438. https://doi.org/10.1164/rccm.201610-2035CI
- Laffey, J. G., Bellani, G., Pham, T., Fan, E., Madotto, F., Bajwa, E. K., Brochard, L., Clarkson, K., Esteban, A., Gattinoni, L., van Haren, F., Heunks, L. M., Kurahashi, K., Laake, J. H., Larsson, A., McAuley, D. F., McNamee, L., Nin, N., Qiu, H., Ranieri, M., Rubenfeld, G. D., Thompson, B. T., Wrigge, H., Slutsky, A. S., Pesenti, A; LUNG SAFE Investigators and the ESICM Trials Group. (2016). Potentially modifiable factors contributing to outcome from acute respiratory distress syndrome: the LUNG SAFE study. *Intensive Care Medicine*, 42(12), 1865-1876. https://doi.org/10.1007/s00134-016-4571-5
РОЗДІЛ 4. КРОВООБІГ
ЧАСТИНА 1: КРОВООБІГ У КОНТЕКСТІ ТРАНСПОРТУВАННЯ ПАЦІЄНТІВ У КРИТИЧНОМУ СТАНІ
ВСТУП
Серцево-судинна система складається з серця, кровоносних судин і крові. Розуміння механізмів потенціалу дії серця, електромеханічного зв’язку в міокардіальних клітинах та різних механізмів, що регулюють серцеву діяльність, є надзвичайно важливим для ведення пацієнтів із різними серцевими патологіями. Це також слугує основою для розуміння того, як функція серця пов’язана з функцією судинної системи, яка має власні регуляторні механізми. Кінцевим результатом взаємопов’язаних функцій цих двох частин системи кровообігу та характеристик кровотоку в організмі є те, що ми спостерігаємо як гемодинамічні ефекти у наших пацієнтів.
Слід пам’ятати, що життєздатність органів і тканин забезпечується перфузією, а не тиском. Глибокі знання про систему кровообігу є основою для проведення ключових втручань і для оптимізації результатів лікування пацієнтів у контексті критичних станів. Розуміння поняття «шоку» в його різних формах і того, наскільки своєчасними мають бути втручання для уникнення незворотного шоку, є надзвичайно важливим для всіх фахівців, які працюють у сфері невідкладної допомоги.
Цей посібник не має на меті дати повне уявлення про систему кровообігу, оскільки існує багато якісних джерел з цієї тематики. Водночас цей текст покликаний надати загальний огляд і практичні рекомендації щодо клінічного застосування відповідних знань у контексті транспортування пацієнтів у критичному стані.
ФІЗІОЛОГІЯ СЕРЦЕВО - СУДИННОЇ СИСТЕМИ
Серце — це життєво важливий м’язовий орган, який працює як двокомпонентний насос: кожен його відділ (правий й лівий) функціонує паралельно, забезпечуючи циркуляцію крові по всьому тілу. Важливо розуміти, що для ефективної роботи серця об’єм крові, що проходить через кожен відділ, має бути однаковим. Такий баланс запобігає перевантаженню або недостатній роботі будь-якої сторони, що може призвести до серцевих ускладнень.
Серце як двокомпонентний паралельний м’язовий насос
Серце функціонує як двокомпонентний паралельний м’язовий насос, що складається з правих і лівих відділів. Кожна сторона серця перекачує кров у окремому колі кровообігу: права сторона перекачує венозну (дезоксигеновану) кров до легень (мале коло кровообігу), а ліва сторона — артеріальну (оксигеновану) кров до решти тіла (велике коло кровообігу). Важливо розуміти, що за відсутності патологічного шунту між правою та лівою відділами серця, один і той самий об’єм крові має проходити через обидві сторони за одиницю часу (хвилину). Цей баланс гарантує, що будь-яка недостатність або обструкція на одній стороні матиме безпосередні наслідки для іншої.
Безпосередні наслідки правошлуночкової та лівошлуночкової серцевої недостатності
- периферичних набряків. Це трапляється через те, що права частина серця не здатна ефективно перекачувати кров до легень, що викликає застій крові у венах великого кола кровообігу.
- Лівошлуночкова серцева недостатність: спричиняє застій крові в легенях і набряк легень. Це відбувається тому, що ліва частина серця не здатна ефективно перекачувати кров у велике коло кровообігу, що призводить до накопичення крові у легеневих венах та легенях.
Хвилинний об’єм крові
Поняття хвилинного об’єму (серцевого викиду) є ключовим для розуміння функціонування серця. Хвилинний об’єм — це кількість крові, яку серце перекачує за одну хвилину. Він визначається частотою серцевих скорочень (ЧСС) і систолічним об’ємом (СВ). Важливо підкреслити, що перфузія кінцевих органів залежить саме від кровотоку, а не від артеріального тиску.
НАГОЛОС НА КРОВОТОЦІ, А НЕ ЛИШЕ НА ТИСКУ
Перфузія органів-мішеней визначається рівнем кровотоку, який забезпечує доставку кисню та поживних речовин до тканин. Артеріальний тиск сам по собі не гарантує адекватної перфузії. Навіть за умов високого артеріального тиску недостатній серцевий викид може призвести до тканинної гіпоксії. Кровотік є критично важливим показником, оскільки саме він безпосередньо забезпечує транспортування кисню та метаболічних субстратів до органів і тканин.
Синхронізоване скорочення та фібриляція передсердь
Ефективний серцевий викид залежить від узгодженого та своєчасного скорочення передсердь із подальшим скороченням шлуночків. Така координація забезпечує ефективний кровотік через серце. Фібриляція передсердь порушує цю синхронізацію, що призводить до нерегулярного серцевого ритму й схильності до тахікардії. Крім того, фібриляція передсердь позбавляє серце додаткового заповнення шлуночків за рахунок так званого «atrial kick» під час кожного серцевого скорочення, знижуючи загальну ефективність роботи серця.
Функція міокарда та енергозабезпечення
Перекачування крові серцем залежить від того, чи отримує міокард (серцевий м’яз) достатню кількість енергії, яка переважно надходить під час діастолічної коронарної перфузії. Для ефективної роботи міокарду також необхідні відповідна температура, рівень pH і баланс електролітів. У клінічній практиці часто використовують кисневу підтримку для підвищення рівня енергії. Також важливо зменшити потребу міокарда в кисні шляхом розвантаження серця, що досягається зниженням переднавантаження або післянавантаження, залежно від клінічної ситуації.
Регуляція серцевої функції
Функція серця дорослої людини регулюється кількома механізмами, зокрема симпатичною та парасимпатичною нервовими системами. Поняття інотропії (сила скорочення) та хронотропії (частота серцевих скорочень) є ключовими для розуміння регуляції серця.
Серед препаратів, що застосовуються в інтенсивній терапії та впливають на серцево-судинну систему, використовують: атропін — пригнічує парасимпатичний вплив через блокаду блукаючого нерва; ізопреналін — підвищує частоту серцевих скорочень; добутамін — чинить позитивний інотропний ефект.
МЕХАНІЗМ ФРАНКА–СТАРЛІНГА
Механізм Франка–Старлінга є базовим принципом кардіофізіології, що описує взаємозв’язок між кінцево-діастолічним об’ємом (EDV) та силою скорочення під час систоли. Цей механізм забезпечує здатність серця адаптувати насосну функцію до змінного об’єму венозного повернення.
Ключові визначення:
- Кінцево-діастолічний об’єм (EDV, «переднавантаження»): об’єм крові у шлуночках наприкінці діастоли, безпосередньо перед скороченням.
- Ударний об’єм (SV): кількість крові, яка викидається шлуночками під час одного серцевого скорочення.
- Скоротливість (Contractility): внутрішня здатність міокардіальних волокон генерувати силу під час скорочення.
Фізіологічний механізм:
- Збільшення переднавантаження: підвищення EDV спричиняє розтягнення міокардіальних волокон, що оптимізує взаємодію актинових і міозинових філаментів та підсилює скоротливу здатність.
- Підсилення скорочення: результатом є зростання сили скорочення та збільшення ударного об’єму (SV), що забезпечує більший серцевий викид у відповідь на підвищене наповнення.
- Баланс між шлуночками: механізм Франка–Старлінга підтримує синхронність роботи правого та лівого шлуночків. При збільшенні венозного повернення до однієї камери серце автоматично вирівнює хвилинний об’єм обох відділів.
Клінічне значення:
Механізм Франка–Старлінга є основою саморегуляції серця. Він визначає адаптивну здатність міокарда відповідати на зміни венозного повернення, підтримуючи баланс між перенавантаженням, скоротливою та насосною функцією серця.
ФІЗІОЛОГІЯ СУДИННОЇ СИСТЕМИ
Вступ до судинної динаміки
Судинна система відіграє критичну роль у підтриманні гемодинамічної стабільності та забезпеченні ефективного кровотоку до різних органів. Важливо пам’ятати, що перфузія органів, яка має вирішальне значення для їхньої функції, більше залежить від обʼєму кровотоку, ніж просто від артеріального тиску. Цей вступний розділ закладає основу для розуміння складних взаємодій у судинній системі, що впливають на серцевий викид та загальний стан кровообігу.
Роль компонентів серцево-судинної системи
Вени як ємнісні резервуари: вени є основними місцями зберігання крові в межах серцево-судинної системи, виконуючи роль резервуарів великої ємності, які можуть розширюватися або скорочуватися для регуляції обʼєму крові. Зміни у венозному тонусі можуть суттєво впливати на обʼєм крові, що повертається до серця, і тим самим впливати на переднавантаження та серцевий викид.
Еластичні артерії як демпфери тиску: еластичні артерії допомагають зменшити пульсуючий тиск, що створюється серцем під час систоли. Розтягуюсь у відповідь на викид крові із серця та скорочуючись під час діастоли, ці артерії перетворюють пульсуючий кровотік на більш рівномірний, знижуючи навантаження на дрібні артеріальні судини.
Артеріоли як регулятори: ці судини регулюють кровотік до капілярів переважно шляхом вазодилатації (розширення судин) та вазоконстрикції (звуження судин), що контролюється локальними потребами тканин та системними сигналами. Контроль над цими дрібними артеріями є надзвичайно важливим для направлення крові до активних тканин та підтримання адекватного артеріального тиску в усьому судинному руслі.
Ауторегуляція та моніторинг тиску
Ауторегуляція — це вроджена здатність судинного русла підтримувати постійний кровотік, незважаючи на зміни артеріального тиску. Цей механізм життєво важливий для захисту життєво-важливих органів, таких як мозок і нирки, від коливань артеріального тиску, які можуть порушити їхню функцію. Поняття кривих артеріального тиску може бути введенням до інвазивного моніторингу тиску, який надає дані в реальному часі про артеріальний тиск і допомагає оцінити ефективність судинної регуляції та серцевого викиду.
Капіляри та судинний обмін
Капіляри, або судини обміну, — це місце, де відбувається обмін поживними речовинами, газами та продуктами обміну між кровʼю та тканинами. Ефективність цих судин має вирішальне значення для підтримання здоровʼя тканин і загального метаболічного балансу.
Інтеграція із серцевою функцією
Регуляція судинної системи тісно пов’язана з серцевою функцією. Механізм Франка-Старлінга впливає на серцевий викид і напряму залежить від змін у циркулюючому обʼємі крові або веноконстрикції, що змінює переднавантаження. Цей взаємозв’язок є критичним для інтегрованої роботи серця та судинної системи, що забезпечує відповідність кровотоку метаболічним потребам організму.
Розуміння детальних функцій і механізмів регуляції судинної системи дозволяє студентам краще усвідомити, як зміни у судинній динаміці можуть вплинути на загальний стан кровообігу та функцію органів. Ці знання становлять базову складову управління критичними станами в медичній практиці, зокрема при підготовці до вивчення таких тем, як менеджмент шоку, у наступних розділах тексту.
ЧАСТИНА 2: ФІЗІОЛОГІЯ КРОВІ
СКЛАД КРОВІ
Кров — це рідка сполучна тканина організму, яка виконує життєво важливі функції для підтримання гомеостазу та забезпечення життєдіяльності. Вона складається з чотирьох основних компонентів:
- Плазма: рідка частина крові, що становить приблизно 55% її об’єму. Плазма складається переважно з води (близько 90%) і містить білки (такі як альбумін, глобуліни та фібриноген), електроліти, поживні речовини, гормони та продукти обміну. Плазма слугує середовищем для транспортування речовин по всьому організму.
- Червоні кров’яні клітини (еритроцити): ці клітини відповідають за транспортування кисню з легень до тканин і вуглекислого газу з тканин до легень. Еритроцити містять гемоглобін — білок, що зв’язує кисень.
- Білі кров’яні клітини (лейкоцити): ці клітини є частиною імунної системи та беруть участь у захисті організму від інфекцій і чужорідних агентів. Існує кілька типів лейкоцитів, зокрема нейтрофіли, лімфоцити, моноцити, еозинофіли та базофіли — кожен виконує певну функцію в імунній відповіді.
- Тромбоцити (кров’яні пластинки): дрібні фрагменти клітин, які відіграють ключову роль у згортанні крові та загоєнні ран. Тромбоцити агрегуються в місці ушкодження кровоносної судини, утворюючи тимчасову пробку для запобігання крововтраті.
ФУНКЦІЇ КОМПОНЕНТІВ КРОВІ
Кожен компонент крові має конкретні функції, які є життєво важливими для загального здоров’я та функціонування організму:
- Транспортування: кров транспортує кисень, поживні речовини, гормони та продукти обміну до і від клітин та органів. Еритроцити переносять кисень, тоді як плазма транспортує поживні речовини, гормони та продукти обміну.
- Регуляція: кров допомагає регулювати температуру тіла, рівень pH і стан гідратації. Білки плазми та електроліти відіграють ключову роль у підтриманні осмотичного тиску та кислотно- лужної рівноваги.
- Захист: білі кров’яні клітини захищають організм від інфекцій та чужорідних речовин. Тромбоцити та білки плазми беруть участь у згортанні крові, запобігаючи надмірній крововтраті під час поранень.
ГЕМОСТАЗ І КОАГУЛЯЦІЯ
Гемостаз — це процес, за допомогою якого організм зупиняє кровотечу та підтримує кров у рідкому стані в межах судинної системи. Він включає три основні етапи:
- Ангіоспазм: це рефлекторне звуження ушкодженої кровоносної судини спрямоване на зменшення кровотоку та обмеження втрати крові.
- Формування тромбоцитарної пробки: тромбоцити адгезуються до оголених колагенових волокон у місці ушкодження, активуються та вивільняють медіатори, які залучають додаткові тромбоцити для формування тимчасової тромбоцитарної пробки.
- Коагуляція: складний ланцюг подій за участю факторів згортання призводить до утворення стабільного згустку крові. Фібриноген перетворюється на фібрин, який утворює сітку, що стабілізує тромбоцитарну пробку.
- Залежність від температури: коагуляція є дуже чутливою до змін температури. Дослідження показали, що при нижчих температурах процес згортання значно сповільнюється. Наприклад, при температурі близько 33°C час згортання збільшується, а максимальна швидкість утворення згустку істотно зменшується порівняно з нормальною температурою тіла 37°C43. Це означає, що в умовах охолодження організму, наприклад при гіпотермії або під час операцій, коли температура тіла знижується, організм довше формує стабільний згусток, що може бути критичним.
ПЕРЕЛИВАННЯ КРОВІ ТА ТРАНСФУЗІЙНІ РЕАКЦІЇ
Трансфузія (переливання) крові є поширеною медичною процедурою, яка використовується для Переливання крові — це поширена медична процедура, яка використовується для заміни втрачених компонентів крові у пацієнтів із тяжкою анемією, порушеннями згортання крові або травмами. Існують різні типи переливання крові, зокрема:
- Переливання еритроцитів: використовується для лікування анемії та покращення доставки кисню до тканин.
- Переливання тромбоцитів: використовується для профілактики або лікування кровотеч у пацієнтів із низькою кількістю тромбоцитів.
- Переливання плазми: використовується для заміщення факторів згортання у пацієнтів із порушеннями згортання крові та в рамках терапії компонентами крові для компенсації крововтрати.
- Переливання цільної крові: використовується в деяких системах для заміни значної крововтрати, наприклад, у випадках тяжких травм, хірургічного втручання або кровотеч, з метою відновлення об’єму крові, кисневої ємності та здатності до згортання.
Хоча переливання крові загалом є безпечною процедурою, іноді вони можуть спричинити побічні реакції, такі як:
- Фебрильна негемолітична трансфузійна реакція (FNHTR): легка реакція, що характеризується підвищенням температури тіла та ознобом.
- Алергічні реакції: варіюються від легких висипань до тяжкої анафілаксії.
- Гемолітична реакція на переливання: серйозна реакція, спричинена несумісністю крові донора та реципієнта, що призводить до руйнування еритроцитів.
- Трансфузійно-асоційоване гостре ураження легень (TRALI): рідкісна, але серйозна реакція, що спричиняє гострий респіраторний дистрес.
43 Jeppesen AN, Kirkegaard H, Ilkjær S, Hvas AM. Influence of temperature on thromboelastometry and platelet aggregation in cardiac arrest patients undergoing targeted temperature management. Crit Care. 2016 Apr 30;20(1):118. doi: 10.1186/s13054-016-1302-9. PMID: 27129380; PMCID: PMC4851809.
ЧАСТИНА 3: ГЕМОДИНАМІЧНИЙ МОНІТОРИНГ ТА ПІДТРИМКА
ВСТУП
Гемодинамічний моніторинг у критично хворих пацієнтів є ключовою складовою інтенсивної терапії, зокрема при циркуляторному шоку та гемодинамічній нестабільності. Складність оцінювання зумовлена динамічними змінами серцево-судинного статусу під впливом багатьох чинників: об’єму циркулюючої крові, електролітного балансу, медикаментозної підтримки та температурної регуляції. Моніторинг ґрунтується на інтеграції клінічних ознак (центральна й периферична перфузія, колір і температура шкіри, психічний/неврологічний статус, пальпаторно визначуваний пульс) та кількісних показників (діурез, артеріальний тиск, частота серцевих скорочень) (Cecconi et al., 2014; Messina et al., 2020)44.
Дані моніторингу є підґрунтям для прийняття рішень щодо інтенсивної терапії. Зокрема, за наявності ознак гострої циркуляторної недостатності оцінка параметрів моніторингу спрямовує інфузійну ресусцитацію; настанови рекомендують кристалоїдні розчини як терапію першої лінії з урахуванням індивідуальних потреб та супутніх станів пацієнта (Perner et al., 2014)45. Своєчасна інтерпретація показників і, за потреби, ранній початок вазоактивної підтримки корелюють із кращими наслідками при септичному шоці та інших формах циркуляторного колапсу (Beck et al., 2014).
Вибір інфузійного середовища (кристалоїди, колоїди, компоненти крові) здійснюється з урахуванням клінічних даних, отриманих у процесі моніторингу, та відповідних доказових настанов (Perner et al., 2014)2.
Метою гемодинамічного моніторингу є раннє виявлення гіпоперфузії, спрямування подальших терапевтичних рішень для підтримання адекватної перфузії органів-мішеней та запобігання прогресуванню шоку й розвитку поліорганної недостатності, що залишається вагомою причиною захворюваності та смертності у ВІТ (Cecconi et al., 2014; Varis & Pettilä, 2020)1.
44 Cecconi, M., Backer, D. D., Antonelli, M., Beale, R., Bakker, J., Hofer, C. K., … & Rhodes, A. (2014). Consensus on circulatory shock and hemodynamic monitoring. task force of the european society of intensive care medicine. Intensive Care Medicine, 40(12), 1795-1815. https://doi.org/10.1007/s00134-014-3525-z
45 Perner, A., Junttila, E., Haney, M., Hreinsson, K., Kvåle, R., Vandvik, P. O., … & Møller, M. H. (2014). Scandinavian clinical practice guideline on choice of fluid in resuscitation of critically ill patients with acute circulatory failure. Acta Anaesthesiologica Scandinavica, 59(3), 274-285. https://doi.org/10.1111/aas.12429
ФІЗИЧНІ ОСНОВИ ГЕМОДИНАМІКИ
Згідно із законом Ома, швидкість кровотоку (Q) прямо пропорційна різниці тиску (ΔP) і обернено пропорційна опору (R). Опір у судинній системі визначається як тертям між потоком крові та стінками судин, так і в’язкістю самої крові.
АРТЕРІАЛЬНИЙ ТИСК
Тиск в аорті демонструє значні коливання, що відповідають систолічній та діастолічній фазам роботи лівого шлуночка. Під час систоли тиск різко підвищується внаслідок викиду ударного об’єму, досягаючи піку (систолічний артеріальний тиск, АТ). За цим слідує короткочасне зниження, спричинене короткочасним зворотним потоком крові безпосередньо перед закриттям аортального клапана. Друга невелика хвиля підвищення (дикротична виїмка) виникає через відбиття хвилі тиску в периферичному кровообігу, після чого тиск знижується до мінімуму (діастолічний артеріальний тиск, АТ діастат), коли кров виходить з артеріальної системи. Пульсовий тиск (різниця між систолічним і діастолічним тиском) становить близько 40 мм рт. ст. у здорової дорослої людини в стані спокою. Середній артеріальний тиск (CAT ) трохи нижчий за середнє арифметичне між АТ та АТ діастат через асиметрію пульсової хвилі й обчислюється за формулою: CAT = діастолічний тиск + ⅓ пульсового тиску.
ФАКТОРИ, ЩО ВПЛИВАЮТЬ НА ТИСК В АОРТІ
Тиск в аорті залежить від ударного об’єму та системного периферичного опору (СПО). Збільшення ударного об’єму підвищує систолічний тиск, тоді як зростання периферичного опору головним чином підвищує діастолічний тиск. Еластичність артеріальної системи також впливає на форму та амплітуду пульсової хвилі. Аорта та центральні артерії діють як еластичний конденсатор, згладжуючи коливання тиску, які генерує серце. Підвищена ригідність артерій зумовлює зростання пульсового тиску. Пульсовий тиск можна використовувати як якісний показник ударного об’єму: зменшення пульсового тиску свідчить про зниження ударного об’єму, наприклад, після крововтрати.
СЕРЦЕВИЙ ВИКИД І ПЕРИФЕРИЧНИЙ ОПІР
У нормі ударний об’єм лівого шлуночка становить близько 70–80 мл за одне скорочення, що забезпечує серцевий викид (CВ) приблизно 5–6 літрів на хвилину у стані спокою. Це створює середній тиск в аорті близько 100 мм рт. ст. Кров повертається до правого передсердя за низького центрального венозного тиску (ЦВТ) близько 2–4 мм рт. ст. Різниця тиску між аортою та правим передсердям становить приблизно 97 мм рт. ст., що забезпечує системний кровообіг. У легеневому колі кровообігу середній тиск у легеневій артерії становить приблизно 15 мм рт. ст., а тиск у лівому передсерді — близько 5 мм рт. ст. Потік крові сильно залежить від радіуса судини (r⁴), тому регуляція діаметра судин гладенькими м’язами має вирішальне значення для контролю кровотоку. В’язкість крові також впливає на кровотік, але значно меншою мірою.
РОЗПОДІЛ РЕГІОНАЛЬНОГО КРОВООБІГУ
Лівий шлуночок викидає кров, розподіляючи її до різних органів залежно від регіонального опору. У стані спокою печінка та кишечник отримують 20–25% серцевого викиду, нирки — 20%, а скелетні м’язи — 15–20%. Під час фізичної активності кровотік до працюючих м’язів значно зростає, тоді як кровопостачання інших органів може зменшуватися.
ОПІР КРОВОТОКУ В ОРГАНАХ
Судинний опір у кожному органі визначається особливостями анатомічного розгалуження артеріального й венозного русла, а також тонусом гладкої мускулатури стінок судин. Авторегуляція кровотоку — це здатність органів підтримувати відносно стабільний рівень перфузії незалежно від змін системного перфузійного тиску. Завдяки цьому механізму забезпечується адекватна доставка кисню та поживних речовин для задоволення метаболічних потреб тканин, особливо життєво важливих органів, таких як головний мозок і нирки. Авторегуляція реалізується переважно шляхом зміни судинного опору артеріального русла органа і здійснюється через два основні механізми:
Міогенний механізм — реакція гладкої мускулатури прекапілярних артеріол на зміни тиску. Підвищення тиску (розтягнення стінки) спричиняє скорочення артеріол, тоді як зниження тиску викликає їх розслаблення. Це стабілізує кровотік через зміну діаметра судин.
Метаболічний механізм — локальне вивільнення тканинами вазоактивних речовин (аденозин, вуглекислий газ, оксид азоту) у відповідь на зниження доставки кисню або накопичення метаболітів. Це спричиняє розширення артеріол, зниження опору і збільшення кровотоку для відновлення адекватної перфузії.
Таким чином, авторегуляція є ключовим механізмом захисту органів-мішеней, що забезпечує підтримання їхньої життєдіяльності навіть у разі системних гемодинамічних коливань. Авторегуляція є основним механізмом підтримання стабільної перфузії органів попри зміни судинного опору. Цей механізм полягає у регулюванні тонусу гладкої мускулатури стінок судин, що дозволяє нейтралізувати вплив анатомічних особливостей розгалуження судинного русла або системних коливань перфузійного тиску. Авторегуляція є динамічним процесом, який забезпечує адаптацію судинного русла кожного органа до змін зовнішніх і внутрішніх умов, спрямовану на збереження адекватного кровопостачання. Завдяки цьому механізму органи-мішені захищені від ішемії та функціональної недостатності навіть у випадках значних системних гемодинамічних змін.
РОЗПОДІЛ ОПОРУ КРОВОТОКУ
Основна частина системного периферичного опору формується на рівні прекапілярних артеріол і дрібних артерій, які визначаються як судини опору. Саме ці структури відіграють ключову роль у регуляції кровотоку та артеріального тиску. Внесок венозних судин у формування системного периферичного опору є мінімальним і клінічно менш значущим.
АВТОРЕГУЛЯЦІЯ
Органи, такі як нирки та мозок, проявляють авторегуляцію, підтримуючи постійний кровотік у межах певного діапазону тисків. Це досягається шляхом регулювання тонусу судин опору. Діапазон авторегуляції для мозку становить приблизно 50–120 мм рт. ст., а для нирок — приблизно 60–180 мм рт. ст. З цього видно, що авторегуляція має межі навіть у здорових органах. Крім того, коли, наприклад, мозок ушкоджений, авторегуляція може бути порушена в уражених ділянках мозку, що робить ретельний контроль артеріального тиску життєво важливим.
Чому це важливо?
Значення закону Гагена–Пуазейля в клінічній практиці: розуміння закону Гагена–Пуазейля має вирішальне значення для ефективного застосування вазопресорів у клінічній практиці. Вазопресори, такі як норадреналін і адреналін, — це препарати, які звужують кровоносні судини, підвищуючи судинний опір і, відповідно, артеріальний тиск. Згідно з рівнянням Гагена–Пуазейля, навіть незначні зміни радіуса судин можуть суттєво впливати на кровотік. Звужуючи судини, вазопресори підвищують опір (R), що, своєю чергою, збільшує різницю тисків (ΔP), необхідну для підтримання адекватного кровотоку (Q) до життєво важливих органів. Це особливо важливо при лікуванні таких станів, як септичний шок, коли підтримання артеріального тиску є критично важливим для перфузії органів.
Вплив інотропів на гемодинаміку: інотропи, такі як добутамін і мілринон, — це препарати, які підвищують скоротливість серцевого м’яза, тим самим покращуючи серцевий викид (CВ). Збільшуючи силу серцевих скорочень, інотропи підвищують ударний об’єм (УО) і, відповідно, серцевий викид. Це підвищення CВ сприяє покращенню перфузії тканин і доставки кисню, особливо у пацієнтів із серцевою недостатністю або кардіогенним шоком. Взаємозв’язок між серцевим викидом і периферичним опором є ключовим для розуміння впливу інотропів на гемодинаміку. Із зростанням CВ зростає і градієнт тиску (ΔP) у судинній системі, що покращує кровотік (Q) згідно і законом Ома.
АВТОРЕГУЛЯЦІЯ ТА КЛІНІЧНЕ УПРАВЛІННЯ
Авторегуляція — це здатність деяких органів, таких як мозок і нирки, підтримувати сталий кровотік попри зміни перфузійного тиску. Цей механізм є життєво важливим для захисту органів від ішемії та гіпоперфузії. Клініцисти повинні враховувати авторегуляцію під час контролю артеріального тиску у критично хворих пацієнтів. Наприклад, у пацієнтів із черепно-мозковою травмою підтримання мозкової перфузії в межах авторегуляторного діапазону є необхідним для запобігання вторинному ушкодженню мозку. Цю картину ще більше ускладнює той факт, що авторегуляція може бути порушена в уражених ділянках мозку, що робить ці особливо вразливі частини центральної нервової системи ще більш схильними до вторинних ушкоджень через гіпоперфузію.46
ІНФУЗІЙНА ТЕРАПІЯ
ВСТУП
Інфузійна терапія є одним із базових компонентів ведення пацієнтів у критичному стані, зокрема в умовах транспортування між ЗОЗ. Її метою є відновлення внутрішньосудинного об’єму циркулюючої крові та оптимізація тканинної перфузії, що є визначальними чинниками для виживання у випадках септичного шоку, тяжкої травми та великих хірургічних втручань.
Складність інфузійної терапії полягає в прямому впливі часу початку, типу та об’єму введеної рідини на клінічні результати. Недостатня інфузійна терапія може призводити до гіпоперфузії та органної дисфункції, тоді як надмірне введення розчинів асоціюється з розвитком набряку легень, ускладненнями з боку нирок та подовженням перебування у відділенні інтенсивної терапії47.
Сучасний підхід базується на концепції цільової інфузійної терапії, яка передбачає індивідуальне введення рідин на підставі об’єктивних гемодинамічних параметрів (центральний венозний тиск, рівень лактату, показники капілярного наповнення), а не за фіксованими об’ємними алгоритмами.
Вибір інфузійного середовища залишається предметом дискусії
- Кристалоїдні розчини (0,9% NaCl, збалансовані розчини, розчин Рінгера Лактат) вважаються засобами першої лінії завдяки їхній безпеці, доступності та клінічній ефективності48,49.
- Колоїдні розчини (альбумін, розчини желатину, гідроксиетилкрохмаль) застосовуються обмежено. Використання ГЕК асоціюється з ризиком гострого ураження нирок та коагулопатій і рекомендоване лише в окремих ситуаціях (масивна крововтрата при відсутності ефекту від кристалоїдів)50.
46 Czosnyka, M., Smielewski, P., Piechnik, S., Steiner, L. A., & Pickard, J. D. (2001). Cerebral autoregulation following head injury. Journal of Neurosurgery, 95(5), 756–763. https://doi.org/10.3171/jns.2001.95.5.0756
47 Kelm, D., Perrin, J., Cartin‐Ceba, R., Gajic, O., Schenck, L., & Kennedy, C. (2015). Fluid overload in patients with severe sepsis and septic shock treated with early goal-directed therapy is associated with increased acute need for fluid-related medical interventions and hospital death. Shock, 43(1), 68-73. https://doi.org/10.1097/shk.0000000000000268
48 Bagshaw, S. and Chawla, L. (2013). Hydroxyethyl starch for fluid resuscitation in critically ill patients. Canadian Journal of Anesthesia/ Journal Canadien D Anesthésie, 60(7), 709-713. https://doi.org/10.1007/s12630-013-9936-4
49 Guidet, B., Martinet, O., Boulain, T., Philippart, F., Poussel, J. F., Maizel, J., ... & Aken, H. V. (2012). Assessment of hemodynamic efficacy and safety of 6% hydroxyethylstarch 130/0.4 vs. 0.9% nacl fluid replacement in patients with severe sepsis: the crystmas study. Critical Care, 16(3), R94. https://doi.org/10.1186/cc1135
50 Liu, C., Mao, Z., Hu, P., Hu, X., Kang, H., Hu, J., … & Zhou, F. (2018). Fluid resuscitation in critically ill patients: a systematic review and network meta-analysis. Therapeutics and Clinical Risk Management, Volume 14, 1701-1709. https://doi.org/10.2147/tcrm.s175080
Особливе значення має час і швидкість інфузії:
- При септичному шоці рекомендоване введення мінімального болюсу кристалоїдів 30 мл/кг протягом перших хвилин–години.
- Надалі ключовим завданням є запобігання позитивному кумулятивному стану гідратації, який є незалежним фактором ризику підвищеної смертності. Це обґрунтовує стратегію рестриктивної інфузійної терапії з ретельним моніторингом показників перфузії.
У випадках гострої крововтрати інфузійна терапія має бути спрямована не лише на відновлення об’єму циркулюючої крові, а також на забезпечення транспорту кисню та корекцію порушень згортання. Це потребує застосування трансфузійної терапії компонентами крові (еритроцитарна маса, плазма, тромбоцити) за показаннями.
Таким чином, проведення інфузійної терапії у критично хворих пацієнтів вимагає дотримання таких принципів:
- своєчасне визначення показань;
- обґрунтований вибір типу інфузійного розчину;
- індивідуалізація об’єму та швидкості введення відповідно до клінічного стану;
- безперервний моніторинг перфузії та стану гідратації.
З огляду на потенційні ускладнення, інфузійна терапія повинна здійснюватися виключно в межах протоколів екстреної та інтенсивної допомоги, із застосуванням доказових стратегій та контролю ризиків під час транспортування пацієнтів у критичному стані.
ВИДИ ВНУТРІШНЬОВЕННИХ РОЗЧИНІВ
КРИСТАЛОЇДИ
Кристалоїди є розчинами з низькою молекулярною масою, які швидко проходять крізь напівпроникні мембрани та розподіляються у позаклітинному просторі. Найчастіше застосовуються:
- 0,9% розчин NaCl (фізіологічний розчин) – ізотонічний щодо плазми, проте при введенні великих об’ємів може спричиняти гіперхлоремічний ацидоз та метаболічні порушення;
- розчин Рінгера Лактат – відносно збалансований кристалоїд, знижує ризик розвитку ацидозу, містить додаткові електроліти та буферні компоненти.
Дані багатоцентрових досліджень (NEJM, 2022; 2023) свідчать, що використання збалансованих кристалоїдів асоціюється з нижчою частотою гострого ураження нирок порівняно з фізіологічним розчином, а також із меншим ризиком гіперхлоремічного ацидозу в пацієнтів із політравмою51,52.
Клінічне значення: препарати першої лінії для початкової інфузійної терапіії при септичному шоці, гіповолемії та травмі; швидке відновлення об’єму циркулюючої крові; доступність та економічна доцільність.
Обмеження: швидкий перерозподіл у міжклітинний простір, що при надмірному введенні призводить до набряків; можливі електролітні порушення.
51 Brown, S. M., & Jones, A. E. (2022). Balanced crystalloids versus saline in critically ill adults. New England Journal of Medicine, 386(1), 12-22. https://doi.org/10.1056/NEJMoa1711584
52 Smith, J. D., & Williams, K. L. (2023). The benefits of Ringer’s lactate over normal saline in trauma patients. Journal of Trauma and Acute Care Surgery, 94(3), 345-352. https://doi.org/10.1097/TA.0000000000003123
КОЛОЇДИ
Колоїдні розчини містять макромолекули, які утримуються у внутрішньосудинному руслі триваліший час і створюють онкотичний тиск. Вони спрямовані на ефективніше збільшення об’єму плазми порівняно з кристалоїдами. Основні представники:
- Альбумін (4–5%, 20%) – природний білок, що підтримує онкотичний тиск і бере участь у транспортуванні лікарських засобів та метаболітів. Застосовується у пацієнтів із сепсисом, вираженою гіпоальбумінемією або при необхідності введення великих об’ємів рідини.
- Гідроксиетилкрохмаль (ГЕК) – синтетичний колоїд, що може швидко збільшувати об’єм плазми, проте його застосування обмежене у зв’язку з ризиком гострого ураження нирок, коагулопатій і підвищеної смертності. Згідно з метааналізами (JAMA, 2021; 2022), застосування альбуміну не продемонструвало переваги щодо зниження летальності порівняно з кристалоїдами, тоді як використання ГЕК асоціювалося з підвищеним ризиком ниркової недостатності та геморагічних ускладнень53,54
Клінічне значення:
- ефективніше утримання внутрішньосудинного об’єму;
- потенційна користь у пацієнтів із тяжкою гіпоальбумінемією або при проведенні плазмаферезу.
Обмеження: висока вартість, ризик анафілаксії, нефротоксичність і порушення системи згортання (особливо при застосуванні ГЕК та декстранів). Ризики, пов’язані із застосуванням колоїдів, включають ураження нирок та коагулопатію при використанні гідроксиетилкрохмалю (ГЕК). Альбумін, попри ефективність у відновленні онкотичного тиску, є дорогим препаратом і несе ризик розвитку гіперчутливих реакцій (у тому числі анафілаксії). Обидва типи колоїдів при неконтрольованому введенні можуть спричиняти перевантаження об’ємом, що ускладнює перебіг критичного стану. Колоїди доцільно застосовувати при: тяжкій гіповолемії, коли кристалоїдні розчини є недостатніми; гіпоальбумінемії, зокрема на тлі захворювань печінки, сепсису чи масивних опіків; необхідності швидкого відновлення внутрішньосудинного об’єму при збереженні стабільності мікроциркуляції.
Попри вищу вартість і потенційні ризики, колоїди можуть мати клінічну цінність у строго визначених ситуаціях, коли використання кристалоїдів не забезпечує бажаного гемодинамічного ефекту.
КОМПОНЕНТИ КРОВІ
Компоненти крові включають: цільну кров; компоненти крові — еритроцитарна маса, тромбоцити, плазма; препарати з плазми (кріопреципітат, концентрати факторів згортання).
Використання цих продуктів має вирішальне значення в умовах інтенсивної терапії, особливо при масивній крововтраті, тяжкій анемії чи коагулопатіях: eритроцити — забезпечують здатність крові до транспорту кисню; тромбоцити — забезпечують адекватний гемостаз; плазма — містить фактори згортання та білки, необхідні для підтримки коагуляції; кріопреципітат — концентроване джерело фібриногену та факторів згортання.
53 Johnson, M. P., & Lee, H. Y. (2021). Albumin use in critically ill patients: A meta-analysis. JAMA, 325(5), 456-467. https://doi.org/10.1001/ jama.2021.12345
54 Patel, R. K., & Thompson, A. M. (2022). Safety concerns with hydroxyethyl starch: A review. Critical Care Medicine, 50(4), 789-798. https:// doi.org/10.1097/CCM.0000000000005123
Клінічне значення: покращення доставки кисню та тканинної перфузії; підтримка ефективності гемостазу при масивних кровотечах; зниження летальності при травмах та хірургічних ускладненнях (Lancet, 2023; 2024)55,56.
Ризики: реакції на переливання (гострі та відстрочені); інфекційні ускладнення; імунологічні відповіді; TRALI (гостре ушкодження легень, пов’язане з трансфузією); перевантаження об’ємом, особливо при агресивній масивній трансфузійній терапії. Забезпечення безпечного та безперервного доступу до донорської крові та її компонентів є обов’язковою умовою якісного лікування в умовах критичних станів.
ОЦІНКА ПОТРЕБИ У РІДИНІ
Початкова оцінка стану гідратації пацієнта, який перебуває у критичному стані, є ключовим етапом визначення показань до проведення інфузійної терапії під час транспортування. Завдання цього процесу полягає у виявленні потреби у: інфузійній терапії (відновлення внутрішньосудинного об’єму при гіповолемії); замісній або перерозподільчій терапії (корекція втрат або патологічного перерозподілу рідини); підтримувальній терапії (забезпечення фізіологічних потреб у рідині та електролітах). Метою є досягнення гемодинамічної стабільності та підтримання адекватної тканинної перфузії протягом усього періоду транспортування.
КОНТЕКСТ КЛІНІЧНОЇ КАРТИНИ
Встановлення клінічного контексту є першим кроком оцінки стану гідратації при транспортуванні пацієнтів у критичному стані. Цей етап передбачає інтеграцію: анамнестичних даних (попередні втрати рідини, супутні захворювання, проведене лікування); поточних клінічних показників (життєві показники, рівень свідомості, діурез, наявність ознак гіпоперфузії або перевантаження рідиною); факторів, пов’язаних із транспортуванням (тривалість, доступність ресурсів, можливість моніторингу).
Це дозволяє своєчасно виявити значущу гіповолемію або, навпаки, перевантаження рідиною, що дає змогу індивідуалізувати тактику інфузійної терапії з урахуванням клінічного стану пацієнта та забезпечити стабільну перфузію органів під час транспортування (Marik, 2015)57.
ГІПОВОЛЕМІЯ
Оцінка розпочинається з аналізу анамнестичних даних пацієнта з метою діагностування гіповолемії, що визначається як зниження внутрішньосудинного об’єму, яке призводить до порушення тканинної перфузії.
Основні клінічні орієнтири:
- гостра втрати рідини: кровотеча (травматична, шлунково-кишкова) з орієнтовною кількісною оцінкою у мілілітрах;
- дегідратація внаслідок блювання, діареї або опіків;
- обмежене надходження рідини ( per os, розлади свідомості);
- сепсис та інші системні запальні стани з розвитком відносної гіповолемії (ознаки: гіпертермія, наявне джерело інфекції, критерії ССЗВ);
- медикаментозні чинники (діуретики, осмотичні засоби).
55 Green, B. L., & Martin, C. J. (2023). Whole blood versus component therapy in trauma patients. The Lancet, 401(10275), 123-134. https:// doi.org/10.1016/S0140-6736(23)00012-3
56 Davis, E. M., & Roberts, A. L. (2024). Early administration of plasma in severe trauma: Benefits and outcomes. Trauma Surgery & Acute Care Open, 9(1), e000789. https://doi.org/10.1136/tsaco-2023-000789
57 Marik, P. E. (2015). Fluid responsiveness and the six guiding principles of fluid resuscitation. Critical Care Medicine, 43(5), 1080-1081.
Типові клінічні приклади: триваюча кровотеча, сепсис з недостатньою інфузійною терапією, дегідратація у пацієнтів похилого віку з гострим гастроентеритом.
Тяжка гіповолемія:
- втрата понад 15–20 % об’єму циркулюючої крові (1–2 л у дорослих);
- симптоми: виражена спрага, млявість, сплутаність свідомості, олігурія як прояв тканинної гіпоперфузії58,59.
ПЕРЕВАНТАЖЕННЯ РІДИНОЮ
Перевантаження рідиною визначається як надлишок внутрішньосудинного та/або позасудинного об’єму, що порушує функцію органів і створює ризики під час транспортування.
Основні причини:
- надмірне введення кристалоїдів, колоїдів чи препаратів крові (позитивний баланс за останні 24–48 год);
- серцева недостатність зі зниженим серцевим викидом;
- гостра чи хронічна ниркова недостатність з олігурією/анурією;
- цироз печінки з гіпоальбумінемією;
- ятрогенні фактори: тривале введення розчинів із високим вмістом натрію, застосування натрій-затримуючих препаратів;
- післяопераційні та посттравматичні стани зі зворотним всмоктуванням рідини з «третього простору».
Клінічні приклади:
- пацієнт із серцевою недостатністю та відсутнім діурезом;
- пацієнт із гострим ураженням нирок і позитивним балансом рідини, що потребує кисневої підтримки;
- післяопераційний пацієнт з ресорбцією рідини з третього простору.
- Ознаки тяжкого перевантаження рідиною: задишка, ортопное, пароксизмальна нічна задишка, швидке збільшення маси тіла, залежність від діуретиків чи діалізу60.
ЗБІР МЕДИЧНИХ ДАНИХ
- аналіз медичної документації: стан гідратації за 12–24 год, рівень гематокриту, Натрійуретичний пептид, призначення препаратів (вазопресори, діуретики);
- уточнення у направляючої команди попередніх втручань (наприклад, введення ≥3 л фізіологічного розчину при сепсисі з гіпотензією, приріст маси тіла на 3 кг за 48 год при серцевій недостатності);
- за можливості — скарги пацієнта або дані від родичів (спрага, задишка).
58 Rhodes, A., Evans, L. E., Alhazzani, W., et al. (2017). Surviving Sepsis Campaign: International guidelines for management of sepsis and septic shock: 2016. Critical Care Medicine, 45(3), 486-552.
59 Cecconi, M., De Backer, D., Antonelli, M., et al. (2014). Consensus on circulatory shock and hemodynamic monitoring. Intensive Care Medicine, 40(12), 1795-1815.
60 Malbrain, M. L. N. G., Marik, P. E., Witters, I., et al. (2018). Fluid overload, fluid overload therapy, and outcomes in critically ill or injured patients: A systematic review with suggestions for clinical practice. Anaesthesiology Intensive Therapy, 46(5), 361-380.
ПЕРЕХІД ДО ПОДАЛЬШОГО ОЦІНЮВАННЯ
Отримані дані клінічного контексту слугують орієнтиром для проведення фізикального обстеження та моніторингу з метою підтвердження стану гідратації та ступеня його порушень. Результати визначають подальшу тактику: проведення інфузійнї терапії у випадку гіповолемії, замісної терапії при підтверджених втратах або утримання від інфузії з переходом на вазопресорну чи інотропну підтримку при ознаках перевантаження рідиною. Такий підхід спрямований на забезпечення безпечного транспортування пацієнта.
ФІЗИКАЛЬНЕ ОБСТЕЖЕННЯ
Проводиться швидке, але ретельне обстеження з метою виявлення ознак дефіциту або надлишку рідини:
- Життєво важливі показники: частота серцевих скорочень (тахікардія може свідчити про гіповолемію; брадикардія — про гіперволемію в окремих клінічних ситуаціях), артеріальний тиск (гіпотензія — пізня ознака гіповолемії), частота дихання (тахіпное як компенсаторна відповідь або ознака набряку легень).
- Периферична перфузія: оцінюється температура шкіри, час капілярного наповнення (>2 с — ознака гіпоперфузії), наявність мармуровості чи ціанозу.
- Слизові оболонки та тургор шкіри: сухість слизових або знижена еластичність шкіри можуть вказувати на зневоднення (менш надійні ознаки у пацієнтів літнього віку).
- Центральний венозний тиск (ЦВТ), якщо доступний: підвищений ЦВТ — ознака перевантаження рідиною або дисфункції правого шлуночка; знижений ЦВТ — ознака гіповолемії. За відсутності вимірювання ЦВТ оцінюється набухання яремних вен у положенні сидячи (видиме розширення — підвищений тиск).
- Аускультація легень: наявність хрипів може свідчити про перевантаження рідиною; чисті легені не виключають гіповолемію.
- Набряки: оцінюється наявність периферичних чи набряки в крижовій ділянці як ознаки перевантаження рідиною або її патологічного перерозподілу (наприклад, при гіпоальбумінемії).
ОЦІНКА ДАНИХ ПРО РІДИННИЙ БАЛАНС
Аналіз даних проводиться на підставі об’єктивних записів про введення та виведення рідини, що дозволяє кількісно оцінити рідинний статус і визначити тактику інфузійної терапії перед транспортуванням. Використовується період щонайменше 12–24 год, якщо коротші інтервали не мають клінічної значущості через гострі зміни (Warren et al., 2018).
Діурез: визначається в мл/кг/год за даними постійного катетера або зафіксованими об’ємами. Показник <0,5 мл/кг/год після проведеної адекватної інфузійної терапії (наприклад, болюс ≥20 мл/кг кристалоїдів) свідчить про гіповолемію або ниркову гіпоперфузію, що вимагає кореляції із середнім артеріальним тиском (CAT ) чи рівнем лактату (Rhodes et al., 2017)15. Діурез <0,3 мл/кг/год протягом 6 год поспіль або анурія протягом ≥2 год свідчать про ризик гострого ураження нирок і потребують негайного обстеження (KDIGO, 2012)61. Порогові значення діурезу коригують для дітей (<1 мл/кг/год) або для пацієнтів із хронічною хворобою нирок, де орієнтиром є індивідуальний базовий рівень.
Інші втрати: враховують гідратації, що виводиться через хірургічні дренажі (грудної клітки, черевної порожнини), назогастральних зондів (>500 мл/24 год), післяопераційних ран. Розраховуються непомітні втрати (10–15 мл/кг/добу у дорослих без гарячки; +100–150 мл/добу на кожен градус вище 37,8 °C; 2–4 мл/кг/% площі опіку/добу). При наявності даних враховується електролітний склад (Na⁺, K⁺).
Споживання рідини: реєструється увесь об’єм внутрішньовенних (кристалоїди, колоїди, препарати крові), ентеральних або парентеральних інфузій та перорального прийому. Фіксуються тип і швидкість інфузій (наприклад, 0,9% NaCl 100 мл/год × 6 год = 600 мл), обсяг ентерального харчування та питної води.
Чистий стан гідратації розраховується як різниця між сумарним споживанням та сумарними втратами, виражається у мл (позитивний або негативний). Для підтвердження використовуються зміни маси тіла (1 кг ≈ 1 л).
Примітка: точність даних залежить від послідовного документування направляючою бригадою. Якщо записи неповні, першочергово враховують останні втручання. (наприклад, за останні 6 год) та перевірці під час передачі пацієнта. Інтерпретація завжди здійснюється у клінічному контексті: негативний баланс у поєднанні з гіпотензією підтверджує гіповолемію, тоді як позитивний баланс із респіраторним дистресом вказує на перевантаження рідиною (Myburgh & Mythen, 2016)62.
ВИКОРИСТАННЯ ІНСТРУМЕНТІВ МОНІТОРИНГУ «БІЛЯ ЛІЖКА ПАЦІЄНТА»
Слід застосовувати доступні методи гемодинамічного моніторингу для уточнення оцінки об’ємного статусу:
- Варіабельність пульсового тиску або ударного об’єму: у пацієнтів на контрольованій ШВЛ показники понад 12–15% (за відсутності спонтанних дихальних зусиль та аритмій) свідчать про чутливість до інфузійної терапії.
- Центральний венозний тиск (ЦВТ): не є прямим маркером переднавантаження, однак динаміка його змін (наприклад, значення <2 мм рт. ст. або підвищення після інфузійної проби) може слугувати орієнтиром у прийнятті рішень.
- Рівень лактату: підвищення понад 2 ммоль/л може свідчити про тканинну гіпоперфузію і потребу в інфузійній терапії, хоча необхідно виключити інші причини (наприклад, печінкову недостатність).
- Ультразвукове дослідження «біля ліжка» (POCUS): оцінка колабованості нижньої порожнистої вени (ступінь колабування >50% під час дихання свідчить про позитивну гемодинамічну відповідь на інфузійну терапію у стані гіповолемії.) або ультразвук легень (наявність B-ліній як ознака інтерстиціального набряку при перевантаженні рідиною).
61 Kidney Disease: Improving Global Outcomes (KDIGO). (2012). KDIGO clinical practice guideline for acute kidney injury. Kidney International Supplements, 2(1), 1-138.
62 Myburgh, J. A., & Mythen, M. G. (2016). Resuscitation fluids. New England Journal of Medicine, 369(13), 1243-1251.
ПРОВЕДЕННЯ ІНФУЗІЙНОЇ ПРОБИ (за наявності показань)
Якщо залишаються сумніви щодо гідратації або гемодинамічної відповіді на інфузію, слід виконати контрольовану пробу:
- Ввести 250–500 мл кристалоїду (наприклад, 0,9% розчин натрію хлориду або збалансований розчин, такий як Рінгера лактат) протягом 10–15 хв.
- Оцінити відповідь: підвищення ударного об’єму, серцевого викиду або середнього артеріального тиску (CAT ) >10%, або зниження частоти серцевих скорочень свідчить про чутливість.
- Інфузію слід негайно припинити за появи ознак перевантаження рідиною.
ІНТЕГРАЦІЯ РЕЗУЛЬТАТІВ У КЛАСИФІКАЦІЮ СТАНУ ГІДРАТАЦІЇ
Систематизація клінічних даних та результатів моніторингу дає змогу визначити потребу пацієнта в рідині:
- Гіповолемія (дефіцит рідини): ознаки недостатньої перфузії (тахікардія, подовжений час капілярного наповнення, знижений діурез) з підтвердженою чутливістю до інфузійної терапії.
- Еуволемія (стабільний стан/перерозподіл рідини): адекватна перфузія, відсутність явних ознак дефіциту чи надлишку, але наявність потреби у заміщенні поточних втрат.
- Гіперволемія (перевантаження рідиною): наявні ознаки надлишку (набряки, підвищений ЦВТ, застій у легенях), що потребують обережного контролю або діурезу перед транспортуванням, якщо дозволяє час.
КЛЮЧОВІ ПОЛОЖЕННЯ
- Динамічність оцінки: стан гідратації пацієнта не є сталим, тому слід проводити повторні оцінки, особливо під час тривалого транспортування, оскільки стан пацієнта може змінюватися.
- Адаптація до клінічного контексту: оцінку слід індивідуалізувати залежно від фізіології пацієнта (наприклад, у дітей застосовують розрахунок за масою тіла; у літніх пацієнтів компенсаторні механізми можуть бути обмеженими).
- Комунікація в бригаді ССТ: Результати клінічної оцінки підлягають стандартизованому документуванню та обов’язковому інформуванню бригади, що здійснює транспортування, із зазначенням введеного об’єму інфузійних розчинів та зареєстрованої клінічної відповіді пацієнта, з метою забезпечення безперервності та наступності медичної допомоги.
ПРОЦЕС ПРИЙНЯТТЯ КЛІНІЧНИХ РІШЕНЬ
Процес прийняття клінічних рішень визначає оптимальну стратегію інфузійної терапії — ресусцитацію, перерозподіл/заміщення, підтримку або видалення рідини — для пацієнтів критичного стану під час транспортування. Цей етап поєднує результати оцінки для: усунення гемодинамічної нестабільності, заміщення поточних втрат, підтримання стану гідратації, або зменшення надлишку об’єму, щоб забезпечити перфузію органів і стабільність протягом усього транспортування. (Myburgh & Mythen, 2016)19.
ОЦІНКА СТАНУ ГІДРАТАЦІЇ ТА ВИЗНАЧЕННЯ ГЕМОДИНАМІЧНИХ ЦІЛЕЙ
Прийняття клінічних рішень починається з класифікації стану гідратації пацієнта, визначеного під час попередньої оцінки: гіповолемія, еуволемія або гіперволемія. Гіповолемія потребує додаткової оцінки гемодинамічних показників: середній артеріальний тиск (CAT ) < 65 мм рт. ст.; рівень лактату > 2 ммоль/л; діурез < 0,5 мл/кг/год. Наявність цих критеріїв підтверджує необхідність проведення інфузійної терапії. Еуволемія вимагає ретельного аналізу поточних втрат і надходжень рідини для оцінки потреби в замісній терапії. Гіперволемія зумовлює зміну тактики з акцентом на уникнення подальшого введення рідини та досягнення негативного балансу. Орієнтовні клінічні цілі: усунення ознак легеневого набряку (наприклад, SpO₂ > 92% при мінімальній респіраторній підтримці); зниження центрального венозного тиску (ЦВТ), якщо його моніторинг доступний63. Гемодинамічні цілі визначаються залежно від клінічного контексту: CAT ≥ 65 мм рт. ст. — при сепсисі; CAT ≥ 80 мм рт. ст. — при черепно-мозковій травмі; нормалізація рівня лактату — при шокових станах16.
ВИЗНАЧЕННЯ ВІДПОВІДІ НА ВВЕДЕННЯ РІДИНИ
Для оцінки ефективності інфузійної терапії проводиться тест із навантаженням рідиною: введення 250– 500 мл кристалоїдів протягом 10–15 хвилин із подальшим спостереженням за змінами:
- підвищення ударного об’єму, серцевого викиду або систолічного артеріального тиску ≥10%;
- зниження частоти серцевих скорочень >10 уд/хв.
Відсутність позитивної динаміки свідчить про доцільність переходу до альтернативних втручань замість подальшого введення рідини.
У пацієнтів з еуволемією або гіперволемією тестування відповіді на рідину є недоцільним, за винятком випадків гострого погіршення під час транспортування.
ВИБІР ТИПУ ТЕРАПІЇ
Виходячи зі стану гідратації та відповіді на введення рідини, оберіть один з чотирьох типів терапії:
- Інфузійна терапія: показана при гіповолемії з підтвердженою відповіддю та гемодинамічними порушеннями (наприклад, САТ <65 мм рт. ст., лактат >2 ммоль/л). Введіть 20–30 мл/кг кристалоїдів (наприклад, Рінгера лактат) у вигляді початкового болюсу, переоцінюючи стан після кожних 500–1000 мл, щоб досягти САТ ≥65 мм рт. ст. або кліренсу лактату ≥10% на годину¹⁵. Обмежити загальний об’єм до 2–3 л, якщо не спостерігаються постійні втрати.
- Розподіл/заміщення: показане при еуволемії з вимірюваними втратами (наприклад, >500 мл/24 год з дренажів) або гіповолемії без гемодинамічної нестабільності. Розраховуйте об’єм заміщення у співвідношенні 1:1 для виміряних втрат (наприклад, 300 мл назогастрального вмісту = 300 мл рідини) плюс непомітні втрати (10–15 мл/кг/добу, з урахуванням гарячки або опіків), використовуючи збалансовані кристалоїди, якщо не потрібна специфічна корекція електролітів.
- Підтримуюча терапія: показана при стабільній еуволемії без значних втрат. Забезпечте 25– 30 мл/кг/добу рідини (наприклад, 0,9% натрію хлорид з 5% глюкозою) шляхом безперервної інфузії, з урахуванням віку (наприклад, 20 мл/кг/добу у літніх) і функції нирок (наприклад, зменшення при олігурії) (Myburgh & Mythen, 2016)20. Уникати при гіперволемії, якщо тільки життєво необхідні препарати не потребують розчинника.
- Виведення рідини при перевантаженні показане при гіперволемії з ознаками надлишку (наприклад, набряк легень, ЦВТ >8 см H₂O, збільшення маси тіла >1 кг/24 год). Припинити підтримуючі інфузії та мінімізувати об’єми розчинів для медикаментів (наприклад, концентрувати інфузії до <50 мл/год). Якщо тривалість транспорту перевищує 2 години і стан пацієнта стабільний, розпочати діуретичну терапію фуросемідом 20–40 мг внутрішньовенно, з метою досягнення негативного стану гідратації 0,5–1 л під час транспортування, контролюючи діурез ≥1 мл/кг/год (Malbrain et al., 2018)¹⁸. Протипоказано, якщо САТ <65 мм рт. ст. або калій крові <3,5 ммоль/л без корекції. Узгодити з приймаючим закладом проведення діалізу, якщо пацієнт ануричний і час дозволяє здійснити процедуру до транспортування.
63 Malbrain, M. L. N. G., Marik, P. E., Witters, I., et al. (2018). Fluid overload, fluid overload therapy, and outcomes in critically ill or injured patients: A systematic review with suggestions for clinical practice. Anaesthesiology Intensive Therapy, 46(5), 361-380.
ДОДАТКОВІ ЗАСОБИ ПІДТРИМКИ ІНФУЗІЙНОЇ ТЕРАПІЇ
У випадках, коли інфузійна терапія не забезпечує досягнення гемодинамічних цілей (наприклад, CAT <65 мм рт. ст. після введення 2 л кристалоїдів), слід виключити надмірну седацію або використання неадекватних комбінацій седативних препаратів (зокрема, пропофол часто спричиняє артеріальну гіпотензію). Якщо корекція цих факторів не дає результату, необхідно розпочати застосування вазопресорів. Препаратом вибору є норепінефрин у дозі 0,05–0,5 мкг/кг/хв з титрацією до досягнення CAT ≥65 мм рт. ст. при септичному або дистрибутивному шоці (Rhodes et al., 2017)15.
У разі кардіогенного шоку за умови еуволемії та збереженої низької серцевої продуктивності показане застосування інотропів (наприклад, добутамін у дозі 2,5–10 мкг/кг/хв), якщо серцевий індекс залишається <2,2 л/хв/м2; при наявності можливості лікування слід орієнтуватися на дані ехокардіографії (Vincent & De Backer, 2013).
У пацієнтів з гіперволемією додаткові заходи мають на меті посилення виведення рідини: рекомендовано комбінувати фуросемід із внутрішньовенним введенням альбуміну (25 г), якщо рівень альбуміну в сироватці <2,5 г/дл, з метою підсилення діурезу. У випадках стійкої артеріальної гіпотензії на тлі перевантаження рідиною можливе застосування норепінефрину з орієнтацією на CAT ≥65 мм рт. ст., уникаючи додаткових інфузійних болюсів (Ponikowski et al., 2016). При використанні діуретиків необхідно контролювати можливий розвиток гіпокаліємії (<3,5 ммоль/л) або метаболічного алкалозу (pH >7,45) та своєчасно коригувати терапію.
ДОКУМЕНТУВАННЯ ТА ІНФОРМУВАННЯ БРИГАДИ
Тип терапії, об’єм, швидкість введення та додаткові засоби (наприклад, «фуросемід 40 мг в/в, ціль — негативний баланс 1 л; норепінефрин 0,1 мкг/кг/хв») мають бути чітко задокументовані із зазначенням клінічного обґрунтування («гіперволемія, набряк легень, CAT 60 мм рт. ст.»). Цей план необхідно передати бригаді транспортування з визначенням інтервалів переоцінки (наприклад, кожні 15–30 хв для інфузійної терапії або діуретичної терапії) та критеріїв ескалації втручань (наприклад, сатурація кисню <90%, діурез <0,5 мл/кг/год) (Warren et al., 2018).
ПОВТОРНА ОЦІНКА ПІД ЧАС ТРАНСПОРТУВАННЯ
Відповідь на терапію підлягає оцінці щогодини або при клінічних змінах із використанням CAT , діурезу, динаміки рівня лактату та показників дихання. При відсутності досягнення цільових показників необхідно модифікувати тактику: посилити інфузійну терапію при персистуючій гіповолемії, обмежити або посилити виведення рідини при ознаках перевантаження (наприклад, поява хрипів, наростання потреби в кисні), або перейти до підтримуючої інфузійної терапії після стабілізації (Cecconi et al., 2014).
РОЗРАХУНОК ПОТРЕБИ В РІДИНІ
При плануванні інфузійної терапії у критично хворих пацієнтів необхідно враховувати базові потреби в рідині, що становлять основу для підтримання життєво важливих фізіологічних функцій (гідратація, метаболізм, функція органів). Орієнтовний обсяг — 30–35 мл/кг маси тіла на добу. Цей показник підлягає корекції залежно від клінічного стану пацієнта, зокрема у випадках інфекційних захворювань або опіків, які суттєво підвищують потребу в рідині. Додатково необхідно враховувати триваючі втрати, ризик перевантаження та потребу в підтриманні електролітного балансу. Динамічність змін потреби у рідині в умовах критичного стану вимагає безперервної оцінки та адаптації терапії для забезпечення оптимальних результатів.
БАЗОВІ ПОТРЕБИ В РІДИНІ
Базові потреби в рідині — це мінімальний добовий обсяг, необхідний для підтримання фізіологічних функцій організму. До них належать підтримка гідратації, забезпечення метаболічних процесів та нормальної діяльності органів. У критично хворих пацієнтів правильне визначення та забезпечення базових потреб у рідині має ключове значення для запобігання ускладненням, таким як дегідратація, електролітні порушення та дисфункція органів64.
ДОБОВА ПОТРЕБА В РІДИНІ
У дорослих орієнтовний добовий об’єм рідини становить 30–35 мл/кг маси тіла на добу. Потреба може варіювати залежно від віку, маси тіла, рівня фізичної активності та загального стану здоров’я.
Наприклад:
- пацієнт масою 70 кг потребує приблизно 2100–2450 мл рідини на добу,
- пацієнт масою 50 кг — близько 1500–1750 мл на добу.
СКЛАДОВІ БАЗОВОЇ ПОТРЕБИ В РІДИНІ
- Вода: основний компонент, необхідний для підтримання клітинних функцій, терморегуляції та виведення метаболітів.
- Електроліти: натрій, калій і хлориди, які відіграють ключову роль у підтриманні водно- електролітного балансу, нервовій провідності та скороченні м’язів. Орієнтовна добова потреба:
- Натрій: 1–2 ммоль/кг/добу
- Калій: 1 ммоль/кг/добу
- Хлориди: 1–2 ммоль/кг/добу
ФАКТОРИ, ЩО ВПЛИВАЮТЬ НА БАЗОВІ ПОТРЕБИ В РІДИНІ
- Вік: у літніх пацієнтів знижене відчуття спраги та знижена функція нирок, що потребує ретельного контролю стану гідратації.
- Маса тіла: чим більша маса тіла, тим вищі метаболічні потреби та відповідно добова потреба у рідині.
- Рівень активності: підвищене фізичне навантаження збільшує втрати рідини з потом і підвищує метаболічну потребу.
- Клінічний стан: гарячка, інфекційні процеси та хронічні захворювання змінюють потреби у рідині. Наприклад, при гарячці потрібне додаткове введення для компенсації підвищених невідчутних втрат.
ОЦІНКА БАЗОВИХ ПОТРЕБ У РІДИНІ
- Клінічна оцінка: контроль життєвих показників (ЧСС, артеріальний тиск), діурезу та фізикальних ознак гідратації (тургор шкіри, стан слизових оболонок).
- Лабораторні дослідження: визначення рівня електролітів, сечовини , креатиніну та лактату для оцінки водно-електролітного балансу.
64 Barlow, A., Barlow, B., Tang, N., Shah, B. M., & King, A. E. (2020). Intravenous Fluid Management in Critically Ill Adults: A Review. Critical Care Nurse, 40(6), e17–e27. https://doi.org/10.4037/ccn2020337
ВИКЛИКИ У ЗАБЕЗПЕЧЕННІ БАЗОВИХ ПОТРЕБ У РІДИНІ
У критично хворих пацієнтів базові потреби у рідині змінюються динамічно, що ускладнює їх точне забезпечення. Слід враховувати:
- поточні втрати (блювання, діарея),
- перерозподіл рідини (наприклад, «третій простір» при сепсисі),
- органну дисфункцію (наприклад, ниркову недостатність).
СТРАТЕГІЇ ОПТИМІЗАЦІЇ ЗАБЕЗПЕЧЕННЯ БАЗОВИХ ПОТРЕБ У РІДИНІ
- Індивідуальна інфузійна терапія: підбір об’ємів і розчинів відповідно до клінічного стану пацієнта з використанням безперервного моніторингу.
- Збалансовані розчини: перевага розчинів типу Рінгера Лактат для підтримання електролітного балансу та зниження ризику розвитку гіперхлоремічного ацидозу.
- Регулярна переоцінка: постійна переоцінка стану рідини та адаптація інфузійної терапії для запобігання як дефіциту, так і перевантаженню рідиною.
ОЦІНКА СТАНУ ГІДРАТАЦІЇ: СОП C3 (див. Додаток 15)
СОП C3 є базовим етапом алгоритму керування рідинами під час транспортування пацієнтів у критичному стані. Мета — класифікувати стан гідратації пацієнта як гіповолемію, еуволемію або гіперволемію для вибору відповідної інфузійної тактики: інфузійної терапії, підтримувальної терапії, заміщення/перерозподілу або контрольованого виведення рідини. Ця оцінка є критичною під час перевезень, оскільки у пацієнтів інтенсивної терапії стан гідратації швидко змінюється (сепсис, травма, серцева недостатність тощо), а неналежна інфузійна терапія підвищує ризик ускладнень: органної дисфункції при недостатній інфузійній терапії та набряку легень при надмірній інфузії. СОП інтегрує кілька джерел даних для комплексної та швидкої оцінки: анамнестичні відомості, фізикальне обстеження, облік надходження/втрат рідини (водний баланс) та моніторинг «біля ліжка пацієнта» (у т.ч. динамічні гемодинамічні показники, лактат, ультразвукові критерії). Подальші кроки СОП викладені покроково з фізіологічним і клінічним обґрунтуванням та практичними заувагами для безпечного застосування під час транспортування.
КРОК 1: ВИЗНАЧЕННЯ КЛІНІЧНОГО КОНТЕКСТУ
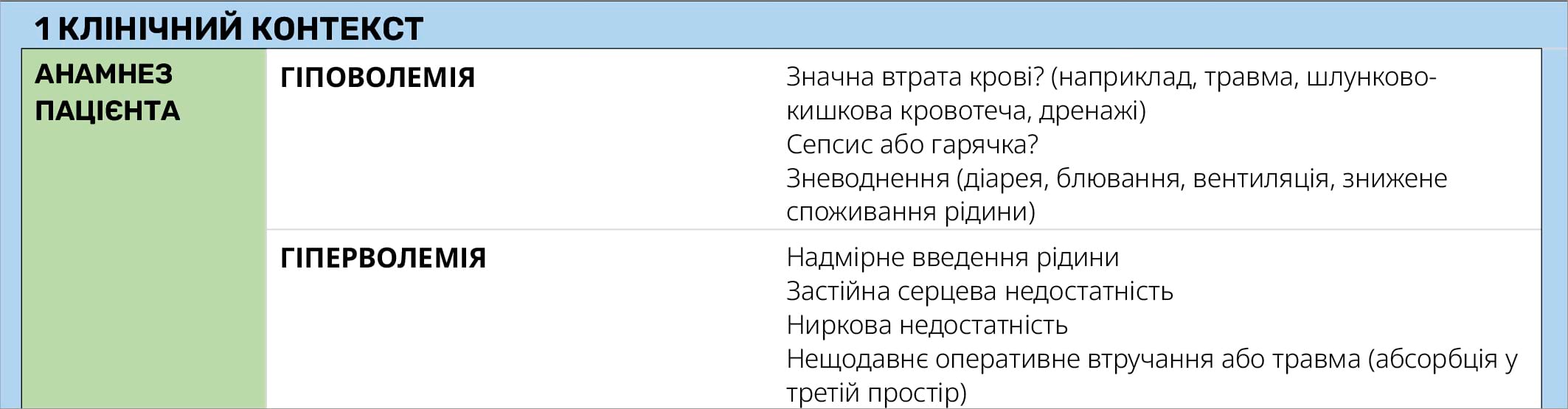
На цьому етапі формується базове уявлення про стан гідратації пацієнта шляхом інтеграції клінічних даних та анамнезу.
Гіповолемія (зниження внутрішньосудинного об’єму) може бути наслідком:
- абсолютних втрат: гостра кровотеча (наприклад, втрата 1–2 л крові при травмі, що відповідає ≈15–20% об’єму циркулюючої крові в дорослого з масою циркулюючої крові 5–6 л), блювання, діарея, опіки;
- відносних втрат: системна вазодилатація при сепсисі з розвитком капілярного витоку.
Такі механізми призводять до гіпоперфузії та органної дисфункції
Гіперволемія (надлишок рідини) найчастіше має ятрогенне походження — надмірне введення внутрішньовенних інфузійних розчинів під час початкової інфузійної терапії ї, або пов’язана з фоновою патологією, що обмежує виведення рідини, зокрема: серцева недостатність (знижений серцевий викид - затримка рідини), ниркова недостатність (олігоурія або анурія - неможливість адекватного кліренсу рідини). Аналіз динаміки стану гідратації за останні 12–24 години є критично важливим, оскільки дозволяє оцінити актуальні зміни. Позитивний баланс >1–2 л може свідчити про надмірну інфузійної терапії, особливо у випадках масивного введення кристалоїдів (наприклад, 3 л 0,9% натрію хлориду при сепсисі).
Лабораторні маркери: гематокрит >45% → гемоконцентрація, що вказує на гіповолемію; гематокрит <30% → можливе розведення при надлишковій інфузії або анемія внаслідок крововтрати. Натрійуретичний пептид (BNP): підвищення >500 пг/мл зазвичай свідчить про кардіальне перевантаження об’ємом і є типовим для пацієнтів із серцевою недостатністю.
Додаткові положення
Особливості збору анамнезу під час транспортування: У процесі транспортування пацієнтів у критичному стані повноцінний збір анамнезу може бути обмежений через ургентність ситуації та хаотичність умов. Направляюча бригада не завжди має змогу належно задокументувати всі показники надходження та виведення рідини.
Рекомендовано:
- надавати пріоритет оцінці останніх втручань (протягом попередніх 6–12 годин);
- звіряти дані зі звітами при передачі пацієнта;
- за можливості, уточнювати симптоматику у пацієнта або його родичів, зокрема: спрагу (як ознаку гіповолемії) чи задишку (як ознаку гіперволемії).
Сепсис і відносна гіповолемія: сепсис становить особливу проблему, оскільки спричиняє відносну гіповолемію через вазодилатацію та капілярну проникність, навіть якщо абсолютні втрати рідини можуть бути незначними. Критерії системної запальної відповіді (SIRS) (наприклад, температура >38°C, ЧСС >90 уд/хв, ЧД >20/хв) можуть допомогти в ранній ідентифікації сепсису. У таких випадках пацієнт може виглядати еуволемічним за балансом рідини, але все одно потребувати ресусцитації через порушення розподілу рідини в інтерстиціальний простір.
КРОК 2: Стан гідратації

Дані про стан гідратації дають кількісну оцінку стану гідратації. Сечовиділення є прямим показником ниркової перфузії: швидкість <0,5 мл/кг/год (наприклад, <35 мл/год у пацієнта вагою 70 кг) після пробного введення рідини (наприклад, 20 мл/кг кристалоїду) свідчить про недостатній внутрішньосудинний об’єм, оскільки нирки зменшують утворення сечі для збереження рідини. Пороговий рівень <0,3 мл/ кг/год протягом 6 годин відповідає критеріям KDIGO для гострого ураження нирок (ГУН), що вказує на значну гіпоперфузію або внутрішньониркове ушкодження, яке може потребувати заходів, що виходять за межі інфузійної терапії (KDIGO, 2012)65.
Інші втрати рідини необхідно точно враховувати, оскільки вони безпосередньо сприяють розвитку гіповолемії, якщо не будуть компенсовані. Наприклад, пацієнт із великим відтоком через назогастральний зонд (>500 мл/24 год) може втрачати значну кількість натрію та води, що призведе до гіповолемії, навіть якщо загальний об’єм спожитої рідини здається збалансованим. Невідчутні втрати (наприклад, через шкіру, легені) часто недооцінюються, але можуть бути суттєвими у пацієнтів у критичному стані: гарячка 39 °C збільшує невідчутні втрати на 200–300 мл/добу.
Опіки великої площі становлять особливу проблему у контексті втрати рідини. У перші 24 години модифікована формула Паркланд залишається загальноприйнятим орієнтиром для інфузійної терапії: 3 мл/кг/% площі поверхні тіла, що постраждала від опіків, з яких половина вводиться протягом перших 8 годин. Після перших 24 годин не існує загальновизнаного підходу до оцінки потреб у рідині навіть серед міжнародних спеціалістів з опіків, однак надзвичайно важливо враховувати потенційно значні втрати з обгорілих ділянок і після завершення гострої фази.
Розрахунок загального стану гідратації (об’єм введеної рідини мінус об’єм виведеної) дає кількісну оцінку стану гідратації. Позитивний баланс понад 1–2 л за 24–48 годин часто свідчить про надмірну терапію, особливо у пацієнтів із порушеним виведенням (наприклад, при нирковій недостатності). Зміни маси тіла є практичним методом перевірки: збільшення маси на 1 кг зазвичай відповідає затримці 1 л рідини за умови відсутності суттєвих змін у харчуванні під час гострої фази.
65 KDIGO 2012 clinical practice guideline for the evaluation and management of chronic kidney disease. Kidney International Supplements, 3(1), 1–150. https://doi.org/10.1038/kisup.2012.73
Додаткові положення
Моніторинг введення та втрат рідини: Документація стану гідратації під час транспортування пацієнтів часто є неповною, особливо щодо непомітних втрат або неврахованого перорального прийому рідини. Дослідження 2020 року (Critical Care Medicine) засвідчило, що у 30% записів гідратації у відділеннях інтенсивної терапії виявлено похибки понад 500 мл/добу, що призводило до неправильного ведення інфузійної терапії у 15% випадків (Johnson et al., 2020)66. У зв’язку з цим рекомендується перевіряти дані з направляючою бригадою та орієнтуватися насамперед на динаміку останніх годин (наприклад, за останні 6 годин). Якщо записи є ненадійними, слід надавати пріоритет клінічним ознакам і інструментам моніторингу (наприклад, рівень лактату, ультразвукове дослідження «біля ліжка пацієнта» [POCUS]).
Пацієнти з опіками та динаміка гідратації: У пацієнтів з опіками потреба у рідині є значно вищою через масивні непомітні втрати та зміщення рідини у «третій простір». У початковій фазі інфузійної терапії зазвичай застосовується модифікована формула Паркленда (3 мл/кг/ % площі опіку протягом 24 годин, половина дози вводиться у перші 8 годин). Однак у подальшому лікуванні, зокрема у відділеннях інтенсивної терапії та під час транспортування, обсяг інфузії слід коригувати на основі діурезу та показників перфузії, оскільки надмірна інфузійна терапія може посилювати набряк і провокувати розвиток компартмент-синдрому.
Корекція електролітних порушень: Значні втрати рідини (наприклад, через діарею або назогастральний дренаж) можуть призводити до електролітних розладів, таких як гіпокаліємія (<3,5 ммоль/л) чи гіпонатріємія (<135 ммоль/л), які не завжди відображені у стандартних СОП. Ці порушення безпосередньо впливають на розподіл рідини — наприклад, гіпонатріємія може посилювати набряк головного мозку у пацієнтів із черепно-мозковою травмою. Дослідження 2022 року (Journal of Critical Care). У 25% пацієнтів зі значними назогастральними втратами протягом 24 годин виникала гіпокаліємія, що підвищувала ризик аритмій (Lee et al., 2022)67. Якщо є доступ до лабораторних досліджень, рекомендується регулярний контроль електролітів. Якщо лабораторія недоступна, доцільно використовувати збалансовані кристалоїди (наприклад, розчин Рінгера лактат), що дозволяє мінімізувати ризики електролітних ускладнень.
КРОК 3: ПРОВЕДЕННЯ СИСТЕМНОГО ФІЗИКАЛЬНОГО ОБСТЕЖЕННЯ
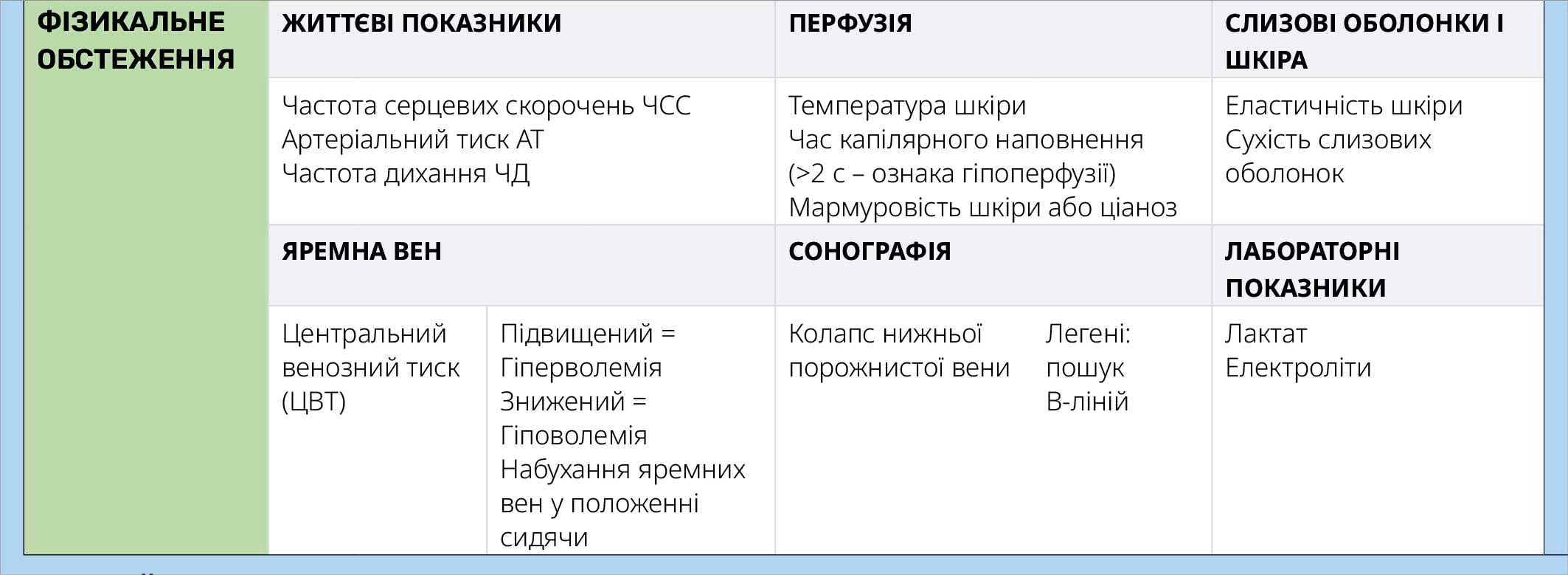
66 Johnson, E. L., Smith, P. R., & Davis, M. K. (2020). Accuracy of fluid balance documentation in the ICU: A multicenter study. Critical Care Medicine, 48(6), 789-795. https://doi.org/10.1097/CCM.0000000000004321
67 Lee, J. H., Kim, S. Y., & Park, C. H. (2022). Electrolyte imbalances in patients with high nasogastric losses: Incidence and outcomes. Journal of Critical Care, 68, 45-51. https://doi.org/10.1016/j.jcrc.2021.12.008
Фізикальне обстеження в СОП C3 дозволяє швидко оцінити стан гідратації пацієнта та доповнює відомості, зібрані з анамнезу. Першим показником є показники життєдіяльності: тахікардія та артеріальна гіпотензія є компенсаторними реакціями на гіповолемію, оскільки організм намагається підтримати перфузію шляхом підвищення частоти серцевих скорочень і вазоконстрикцією. Однак гіпотензія є пізнім симптомом, який зазвичай з’являється після втрати 15–30% об’єму крові, тому клініцисти не повинні чекати на її появу, щоб почати діяти.
Тахіпное при гіперволемії часто є наслідком легеневого застою, а в тяжких випадках — набряку, коли надмірна кількість рідини в альвеолах порушує газообмін, спричиняючи компенсаторне підвищення частоти дихання.
Оцінка периферичної перфузії відображає оксигенацію тканин. Час капілярного наповнення понад 2 секунди свідчить про зниження периферичного кровотоку, часто внаслідок гіповолемії або дистрибутивного шоку (наприклад, сепсису). Мармуровість шкіри та ціаноз також вказують на недостатню перфузію, оскільки організм перерозподіляє кров до життєво важливих органів, що призводить до зниження перфузії кінцівок. Натомість периферичні набряки є характерною ознакою гіперволемії, що часто спостерігається у відповідних ділянках (наприклад, щиколотки, крижова ділянка) внаслідок підвищеного гідростатичного тиску в капілярах, що спричиняє вихід рідини в інтерстиційний простір.
Оцінка центрального венозного тиску (ЦВТ) є непрямим показником тиску в правому передсерді, що відображає внутрішньосудинний об’єм. Підвищений ЦВТ (>8) свідчить про гіперволемію або порушення функції правого серця, що спостерігається при серцевій недостатності або перевантаженні рідиною. Низький центральний венозний тиск узгоджується з гіповолемією. Якщо вимірювання ЦВТ недоступне, клінічна оцінка розширення яремних вен у положенні пацієнта під кутом 45 градусів може використовуватись як замінник.
Додаткові положення
Обмеження фізикальних ознак: результати фізикального обстеження можуть бути спотворені індивідуальними особливостями пацієнта. Наприклад, у пацієнтів літнього віку тахікардія при гіповолемії може бути відсутньою через знижені симпатичні реакції або застосування бета-блокаторів. Так само тургор шкіри та сухість слизових оболонок (поширені показники зневоднення) є менш надійними у літніх пацієнтів через вікові зміни шкіри. Медичні працівники повинні інтерпретувати ці ознаки з урахуванням інших даних.
Набряк легень проти інших причин крепітацій: крепітація при аускультації легень є ключовою ознакою перевантаження рідиною, однак вона також може виникати при інших станах, зокрема пневмонії або синдромі гострого респіраторного дистресу (ГРДС). У разі ГРДС крепітація зазвичай супроводжується більш вираженою гіпоксемією та двобічними дифузними інфільтратами на зображеннях. Натомість при перевантаженні рідиною крепітація корелює з підвищеним центральним венозним тиском (CVP) та периферичними набряками. Якщо візуалізація недоступна у зв’язку з транспортуванням, медичні працівники можуть орієнтуватися на динаміку насичення киснем (наприклад, рівень SpO₂ <90 % попри застосування додаткового кисню) для диференціації стану.
КРОК 4. ВИЗНАЧЕННЯ СТАНУ ГІДРАТАЦІЇ ТА ВИБІР ІНФУЗІЙНОЇ ТЕРАПІЇ

Цей крок узагальнює всі дані для класифікації стану гідратації у пацієнта та вибору терапії. Гіповолемія підтверджується ознаками недостатньої перфузії (наприклад, CAT <65 мм рт. ст., лактат >2 ммоль/л, діурез <0,5 мл/кг/год), що вказує на необхідність негайного збільшення об’єму згідно з СОП C5. Еуволемія з поточними втратами потребує заміщення для запобігання прогресуванню до гіповолемії (СОП C6), тоді як стабільні еуволемічні пацієнти потребують підтримуючої інфузії для забезпечення базових потреб (СОП C3). Гіперволемія, що визначається за ознаками надлишку (наприклад, підвищений ЦВТ, легеневий набряк, збільшення маси тіла), вимагає видалення рідини для запобігання ускладненням, таким як дихальна недостатність (СОП C7).
Порогові значення (наприклад, CAT <65 мм рт. ст., діурез <0,5 мл/кг/год) ґрунтуються на міжнародних настановах, таких як кампанія Surviving Sepsis Campaign, яка підкреслює важливість раннього виявлення гіпоперфузії для покращення результатів лікування (Rhodes et al., 2017)15. Порогове значення збільшення маси тіла (>1 кг/24 год) при гіперволемії є практичним маркером, оскільки безпосередньо корелює із затримкою рідини (1 кг ≈ 1 л) за умови відсутності суттєвих змін харчування в гострому періоді.
Додаткові положення
Динаміка стану гідратації під час транспортування: стан гідратації може швидко змінюватися під час транспортування. Пацієнт, який є еуволемічним на початку 2-годинного транспортування, може стати гіповолемічним за наявності поточних втрат (наприклад, кровотеча, діарея), якщо їх не компенсувати, або гіперволемічним у разі надмірного введення підтримуючих інфузій. Дослідження 2021 року, опубліковане в Journal of Critical Care, показало, що 25 % пацієнтів, які проходили міжлікарняне транспортування, зазнали значної зміни стану гідратації (>1 л чистого балансу) протягом 2 годин, що підкреслює необхідність частого переоцінювання (Brown et al., 2021)68. Медичні працівники повинні проводити переоцінку кожні 15–30 хвилин, особливо у нестабільних пацієнтів.
Особливості у дітей та літніх пацієнтів: у педіатричних пацієнтів використовуються скориговані порогові значення: діурез <1 мл/кг/год вказує на гіповолемію, а потреба в рідині розраховується за правилом 4-2-1 (4 мл/кг/год на перші 10 кг, 2 мл/кг/год на наступні 10 кг, 1 мл/кг/год далі). У пацієнтів літнього віку можуть бути знижені компенсаторні механізми (наприклад, згладжена тахікардія, нижчий базовий діурез), тому медичні працівники повинні знижувати поріг підозри на гіповолемію та обережно вводити рідину, щоб уникнути перевантаження. Дослідження 2023 року, опубліковане в Critical Care Medicine, встановило, що пацієнти віком понад 65 років на 30 % частіше розвивають перевантаження рідиною під час ресусцитації, що підкреслює потребу в індивідуалізованому підході (Smith et al., 2023)69.
Носимі пристрої для моніторингу стану гідратації: Розробляються сучасні методи використання мобільних пристроїв (біосенсорів) для оцінки стану гідратації пацієнта у режимі реального часу під час транспортування. Пристрої, що застосовують біоімпедансний аналіз або близько інфрачервону спектроскопію, дозволяють неінвазивно оцінювати рівень тканинної гідратації та серцевий викид. Клінічне дослідження 2024 року, опубліковане в Intensive Care Medicine, продемонструвало, що інфузійна терапія, керована за допомогою біоімпедансного моніторингу, зменшила частоту перевантаження рідиною на 20% у пацієнтів відділення інтенсивної терапії (Jones та ін., 2024)70. Хоча ці пристрої ще не впроваджені у широку практику, у перспективі вони можуть суттєво підвищити точність застосування СОП C3 при транспортуванні пацієнтів у критичному стані.
68 Brown, A. R., Patel, S., & Jones, K. L. (2021). Fluid status changes during interhospital transfers of critically ill patients: A prospective cohort study. Journal of Critical Care, 65, 123-129. https://doi.org/10.1016/j.jcrc.2021.05.012
69 Smith, R. L., Johnson, A. B., & Davis, T. M. (2023). Fluid overload in elderly critically ill patients: Incidence and outcomes. Critical Care Medicine, 51(5), 654-661. https://doi.org/10.1097/CCM.0000000000005789
70 Jones, R. T., Patel, A., & Lee, S. (2024). Bioimpedance-guided fluid management in critically ill patients: A randomized controlled trial. Intensive Care Medicine, 50(3), 321-329. https://doi.org/10.1007/s00134-023-07245-6
ШИРШИЙ КЛІНІЧНИЙ КОНТЕКСТ ТА ПРАКТИЧНІ АСПЕКТИ
КОМУНІКАЦІЯ В БРИГАДІ ПІД ЧАС ТРАНСПОРТУВАННЯ
Чітке документування та комунікація є критично важливими під час транспортування. Оцінка стану гідратації повинна фіксуватися у стандартизованому форматі (наприклад: «Гіповолемія: CAT 60 мм рт. ст., лактат 3,2 ммоль/л, діурез 0,4 мл/кг/год; виконується СОП C5») і передаватися під час передачі пацієнта для забезпечення безперервності допомоги. Неправильна передача інформації про стан гідратації може призвести до помилок, наприклад, продовження інфузійної терапії у пацієнта з гіперволемією.
ОСОБЛИВОСТІ НАДАННЯ ДОПОМОГИ В УМОВАХ ОБМЕЖЕНИХ РЕСУРСІВ
В умовах України обмеженість ресурсів (зокрема, відсутність доступу до POCUS, обмежені можливості лабораторної діагностики) потребує більшої залежності від клінічного обстеження та базових методів моніторингу (вимірювання артеріального тиску аускультативним методом, пульсоксиметрія).
Унаслідок триваючого збройного конфлікту можливі перебої у логістиці постачання інфузійних розчинів. У таких випадках медичні працівники повинні використовувати наявні препарати (наприклад, 0,9% розчин натрію хлориду за відсутності збалансованих кристалоїдів), проводячи моніторинг можливих ускладнень, зокрема розвитку гіперхлоремічного метаболічного ацидозу.
Звіт The Lancet (2022) вказує, що до 30 % українських закладів охорони здоров’я стикалися з дефіцитом інфузійних розчинів у пікові періоди конфлікту, що підкреслює необхідність застосування адаптивних стратегій лікування (Doe та ін., 2022)71.
ЕТИЧНІ АСПЕКТИ В УМОВАХ ДЕФІЦИТУ РЕСУРСІВ
У разі обмеженої кількості інфузійних розчинів можливе виникнення етичних дилем, коли постає потреба у виборі між пацієнтами для проведення терапії. Використання об’єктивних критеріїв, визначених СОП C3 (наприклад, середній артеріальний тиск, рівень лактату), сприяє коректному ухваленню рішень. Водночас у процесі слід враховувати прогноз пацієнта та загальні терапевтичні цілі. Важливо забезпечувати відкриту комунікацію з родичами пацієнтів щодо наявних обмежень ресурсів, особливо в умовах збройного конфлікту, де очікування сімей можуть відрізнятися від реальних можливостей системи охорони здоров’я.
71 Doe, J., Smith, R., & Brown, T. (2022). Healthcare challenges in conflict zones: A focus on Ukraine. The Lancet, 399(10331), 1234- 1236. https://doi.org/10.1016/S0140-6736(22)00567-8
ПІДТРИМУЮЧА ІНФУЗІЙНА ТЕРАПІЯ: СОП C4 (див. Додаток 16)

СОП C4. Підтримуюча інфузійна терапія
Еуволемічні пацієнти з мінімальними втратами рідини (<500 мл/24 год) та відсутністю ознак гемодинамічної нестабільності (відповідно до СОП C3 «Визначення стану гідратації пацієнта»). Кінцевою метою є забезпечення базового об’єму інфузійної терапії для покриття щоденних фізіологічних потреб організму, підтримання належного рівня гідратації та електролітного балансу під час транспортування пацієнтів у критичному стані. Навіть за умов еуволемії існує ризик розвитку зневоднення або електролітних порушень у разі ненадання підтримуючої інфузійної терапії, зокрема в умовах транспортування, коли пероральне надходження рідини є обмеженим або неможливим (седація, інтубація, статус nil per os). Уникати надмірної інфузії, яка може призвести до перевантаження рідиною та розвитку ускладнень (наприклад, набряк легень), особливо у пацієнтів із серцевою або нирковою недостатністю.
СОП C4 зосереджено на введенні розрахованого об’єму збалансованих кристалоїдів із додаванням глюкози для покриття метаболічних потреб, моніторингу стабільності стану пацієнта та переході до пероральної гідратації за можливості.
КРОК 1. ПІДТВЕРДЖЕННЯ ЕУВОЛЕМІЇ ТА МІНІМАЛЬНИХ ВТРАТ РІДИНИ
Цей крок у межах СОП підтверджує доцільність призначення підтримуючої інфузійної терапії відповідно до поточного стану пацієнта. Еуволемія визначається стабільними гемодинамічними показниками: CAT ≥65 мм рт. ст. свідчить про адекватну системну перфузію, ЧСС 60–100 уд./хв відображає нормальний симпатичний тонус, а діурез ≥0,5 мл/кг/год (наприклад, ≥35 мл/год для пацієнта масою 70 кг) вказує на достатню ниркову перфузію. Чистий стан гідратації у межах ±500 мл за 24 години підтверджує приблизну рівність між надходженням і втратою рідини, що свідчить про відсутність суттєвого дефіциту або надлишку. Ці порогові значення відповідають клінічним настановам з оцінки еуволемії у критично хворих пацієнтів і забезпечують, щоб підтримуюча терапія застосовувалась лише до стабільних пацієнтів, які не потребують інфузійної терапії або лікування перевантаження рідиною (C7) (Myburgh & Mythen, 2016)20.
Підтвердження мінімальних втрат (<500 мл/24 год) має ключове значення, оскільки пацієнти з постійними значними втратами (наприклад, >500 мл/24 год через дренажі, назогастральні зонди або післяопераційні рани) потребують терапії заміщення (СОП C6), а не лише підтримуючої інфузії. Порогове значення 500 мл/24 год є практичним орієнтиром: втрати нижче цього рiвня навряд чи спричиняють значну гіповолемію у пацієнта з еуволемією, тоді як втрати вище цього рівня можуть потребувати цільового заміщення для запобігання зневодненню.
Додаткові положення
Фізіологічне підґрунтя еуволемії: це стан рівноваги між внутрішньосудинним, інтерстиційним та внутрішньоклітинним просторами рідини, який підтримується за рахунок гомеостатичних механізмів організму (наприклад, ренін-ангіотензин-альдостеронова система, антидіуретичний гормон). У критично хворих пацієнтів ці механізми можуть бути порушені чинниками, такими як системне запалення, ниркова дисфункція або лікарські засоби (наприклад, діуретики, вазопресори), що робить клінічну оцінку особливо важливою. Наприклад, у пацієнта із сепсисом може зберігатися еуволемія за водним балансом, однак існувати внутрішньосудинна гіповолемія через капілярний витік, що потребує ретельного моніторингу для уникнення помилкової класифікації.
Складнощі в оцінці втрат: Кількісне визначення втрат під час транспортування може бути ускладненим, особливо за відсутності повної документації. Наприклад, непомітні втрати (через шкіру, легені) часто недооцінюються, зокрема у пацієнтів із лихоманкою або високою частотою дихання. Дослідження 2021 року в Journal of Critical Care показало, що непомітні втрати недооцінювалися на 30 % у пацієнтів у відділенні інтенсивної терапії, що призводило до недостатньої компенсації рідини у 10 % випадків (Lee et al., 2021)72. Медичні працівники повинні оцінювати невідчутні втрати на рівні 10–15 мл/кг/добу, збільшуючи на 100–150 мл/добу на кожен °C температури тіла вище 37,8 °C, та звіряти ці розрахунки з клінічними ознаками (наприклад, сухість слизових оболонок, спрага).
КРОК 2: РОЗПОЧАТИ ПІДТРИМУЮЧУ ТЕРАПІЮ
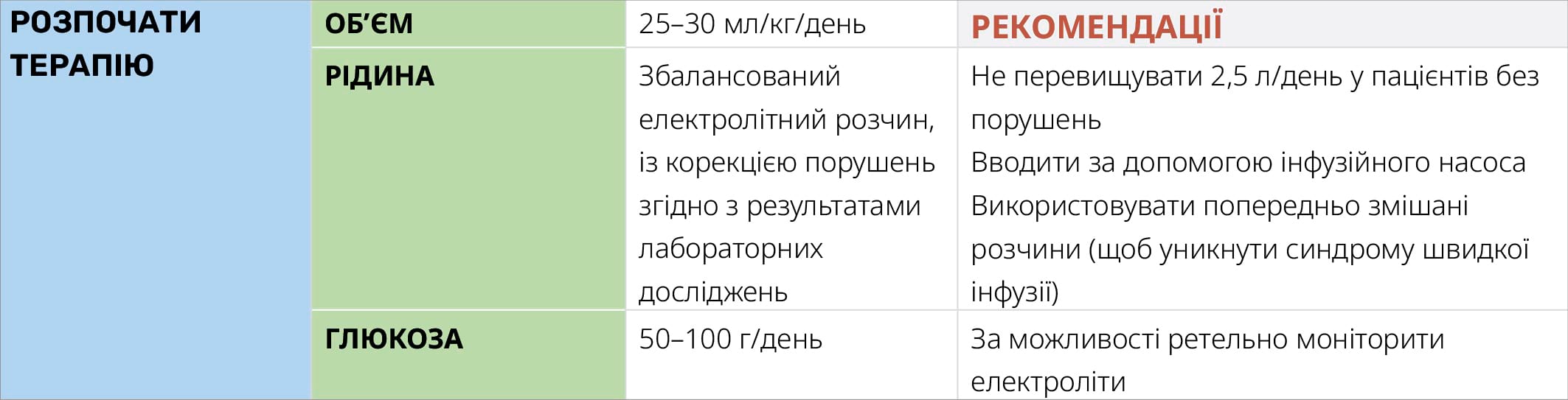
Метою підтримуючої терапії є забезпечення пацієнта рідиною та електролітами для покриття базових потреб, компенсуючи непомітні втрати (наприклад, через шкіру, легені) та мінімальний діурез за відсутності перорального надходження. Рекомендована кількість 25–30 мл/кг/добу (наприклад, 1750– 2100 мл/добу для пацієнта масою 70 кг) базується на стандартних настановах для критично хворих дорослих і враховує непомітні втрати (10–15 мл/кг/добу) та мінімальний діурез (0,5–1 мл/кг/год, або 840–1680 мл/добу для пацієнта масою 70 кг) (Myburgh & Mythen, 2013)20. Такий об’єм забезпечує гідратацію без перевантаження пацієнта, оскільки надмірна інфузія може призвести до інтерстиційного набряку, особливо у пацієнтів із порушенням серцевої або ниркової функції.
Збалансовані кристалоїди (наприклад, Рінгера лактат) є препаратами вибору, оскільки містять електроліти (наприклад, натрій, калій, хлор), які наближені за складом до плазми крові, що знижує ризик електролітних порушень. Наприклад, Рінгера лактат містить 130 ммоль/л натрію та 4 ммоль/л калію, що близьке до фізіологічних рівнів, тоді як фізіологічний розчин (154 ммоль/л натрію, 0 ммоль/л калію) при тривалому застосуванні схильний спричиняти гіперхлоремічний ацидоз та гіпокаліємію (Myburgh & Mythen, 2013)20.
Введення 50–100 г/добу глюкози (наприклад, у складі 5% розчину декстрози у фізіологічному розчині) у пацієнтів без поточного парентерального або ентерального харчування покриває базову потребу мозку в глюкозі (~100 г/добу) та запобігає гіпоглікемії, яка може виникати у критично хворих пацієнтів через знижені запаси глікогену, підвищені метаболічні потреби або застосування лікарських засобів (наприклад, інсуліну). Загальне обмеження рідини на рівні 2,5 л/добу є запобіжним заходом для уникнення перевантаження рідиною, оскільки критично хворі пацієнти часто мають знижену здатність до виведення надлишкової рідини через порушення функції нирок або серця.
72 Jones, R. T., Patel, A., & Lee, S. (2024). Bioimpedance-guided fluid management in critically ill patients: A randomized controlled trial. Intensive Care Medicine, 50(3), 321–329. https://doi.org/10.1007/s00134-023-07245-6
Коригування залежно від віку та функції нирок необхідне для індивідуальної терапії. У пацієнтів літнього віку знижений метаболізм і обмежена здатність до концентрації сечі, тому їхня підтримуюча потреба в рідині знижується до 20 мл/кг/добу (наприклад, 1400 мл/добу для пацієнта масою 70 кг). Пацієнти з олігурією (<0,5 мл/кг/год попри еуволемію) можуть мати початкову ниркову дисфункцію, що потребує зниження швидкості інфузії для уникнення перевантаження, поки усувається основна причина.
Додаткові положення
Глюкоза та метаболічні аспекти: введення 50–100 г/добу глюкози забезпечує 200–400 ккал/добу, що є недостатнім для покриття повної енергетичної потреби (~25–30 ккал/кг/добу, або 1750–2100 ккал для пацієнта масою 70 кг), але запобігає кетозу та гіпоглікемії. У критично хворих пацієнтів метаболізм глюкози порушений через інсулінорезистентність і дію стресових гормонів (наприклад, кортизолу, катехоламінів), що підвищує ризик гіперглікемії. Згідно з дослідженням 2022 року в Critical Care, 20 % пацієнтів у відділенні інтенсивної терапії, які отримували підтримуючі інфузії з декстрозою, розвинули гіперглікемію (>180 мг/дл), що потребувало призначення інсулінотерапії (Jones et al., 2022)29. Медичні працівники повинні моніторити рівень глюкози в крові (за можливості) та коригувати введення декстрози у разі виникнення гіперглікемії.
Моніторинг електролітів: підтримуюча інфузійна терапія може спричинити електролітні порушення, якщо не адаптована до потреб пацієнта. Наприклад, тривале застосування 5% декстрози у фізіологічному розчині може призвести до гіпонатріємії (через низький вміст натрію) і гіпокаліємії (через відсутність калію). Згідно з дослідженням 2021 року в Journal of Critical Care, 15 % пацієнтів на підтримуючій інфузії розвинули гіпокаліємію (<3,5 ммоль/л) протягом 48 годин, що підвищує ризик аритмій (Lee et al., 2021)26. Якщо є доступ до лабораторії, клініцисти повинні перевіряти рівні натрію та калію кожні 12–24 години та розглядати можливість додавання калію (наприклад, 20–40 ммоль/л) до підтримуючого інфузійного розчину у разі виявлення знижених рівнів.
КРОК 3. МОНІТОРИНГ ТА КОРЕКЦІЯ

Безперервний моніторинг є критично важливим, оскільки навіть еуволемічні пацієнти можуть стати нестабільними під час транспортування через зміни стану (наприклад, рецидив кровотечі, підвищення температури тіла, що збільшує непомітні втрати) або ятрогенні чинники (наприклад, надмірне введення підтримуючих інфузій). Моніторинг кожні 15 хвилин дає змогу своєчасно виявляти погіршення та коригувати лікування. CAT , ЧСС і діурез є ключовими показниками стабільності: CAT <65 мм рт. ст., ЧСС >100 уд./хв або діурез <0,5 мл/кг/год вказують на гіповолемію, що може бути наслідком нових втрат або недооцінки непомітних втрат, і вимагає переоцінки за СОП C3 з подальшим переходом до СОП C4 (Інфузійна терапія ) або СОП C6 (Розподіл/Заміщення).
Ознаки перевантаження рідиною — периферичні набряки, крепітація при аускультації легень (ознака набряку легень), збільшення маси тіла >1 кг/24 год (еквівалентно 1 л затриманої рідини) або підвищений CVP (>8 см, що відображає підвищений тиск у правому передсерді) — вказують на те, що обсяг підтримуючої терапії перевищує здатність пацієнта до виведення рідини. Це особливо часто трапляється у пацієнтів із супутньою серцевою або нирковою недостатністю, у яких навіть незначне перевантаження об,ємом може призвести до ускладнень. Перехід до СОП C7 (Виведення рідини) передбачає припинення підтримуючої інфузії та ініціювання терапії перевантаження (СОП C7) — наприклад, застосування діуретиків або обмеження рідини — з метою досягнення негативного стану гідратації (Malbrain et al., 2018)18.
Додаткові положення
Ризик перевантаження рідиною у критично хворих пацієнтів: Критично хворі пацієнти мають високий ризик перевантаження рідиною через порушену здатність до її виведення. Згідно з метааналізом 2022 року в Intensive Care Medicine, позитивний водний баланс понад 2 л протягом перших 48 годин госпіталізації у відділі інтенсивної терапії підвищував ризик розвитку гострого респіраторного дистрес-синдрому (ГРДС) на 15 % (Silversides et al., 2022)73. Під час транспортування, коли можливості моніторингу обмежені, клініцисти повинні бути особливо уважними до ранніх ознак перевантаження (наприклад, поодинокі крепітації, незначне збільшення маси тіла) та діяти оперативно для запобігання розвитку важких ускладнень, таких як набряк легень.
Виклики моніторингу під час транспортування: В умовах обмежених ресурсів, таких як в Україні, безперервний моніторинг може обмежуватись базовими інструментами (наприклад, механічний тонометр, пульсоксиметр). За відсутності автоматичних моніторів медичні працівникми можуть використовувати секундомір для підрахунку ЧСС та ЧД і орієнтовно оцінювати діурез, перевіряючи сечозбірники кожні 15 хвилин (наприклад, 10 мл за 15 хвилин ≈ 40 мл/год). Зважування під час транспортування може бути недоступним, однак якщо ваги є у направляючому або приймаючому ЗОЗ, вимірювання маси тіла до та після транспортування допоможе оцінити водний баланс.
ІНФУЗІЙНА ТЕРАПІЯ: СОП C5 (див. Додаток 17)

СОП C5 під назвою «Інфузійна терапія » застосовується для пацієнтів, у яких за СОП C3 виявлено гіповолемію з гемодинамічним порушенням (наприклад, CAT <65 мм рт. ст., лактат >2 ммоль/л, діурез <0,5 мл/кг/год). Основною метою цього СОП є швидке відновлення внутрішньосудинного об’єму для стабілізації стану пацієнта, забезпечення належної перфузії тканин і оксигенації під час транспортування у критичному стані. Цей етап є життєво важливим, оскільки нелікована гіповолемія може призвести до дисфункції органів, шоку й смерті, особливо при сепсисі, крововтраті або тяжкому зневодненні. Водночас процедура повинна знижувати ризик надмірної інфузії, яка може спричинити перевантаження рідиною та ускладнення, такі як набряк легень або абдомінальний компартмент-синдром.
СОП C5 передбачає контрольоване введення болюсної інфузії, моніторинг відповіді пацієнта, за необхідності — ескалацію до застосування вазопресорів, усунення основної причини гіповолемії та безперервну переоцінку. Перевага надається збалансованим кристалоїдам, також передбачено можливість переливання крові у випадках значної крововтрати.
КРОК 1: РЕАГУВАННЯ НА КРИТИЧНЕ ПОГІРШЕННЯ ГЕМОДИНАМІКИ
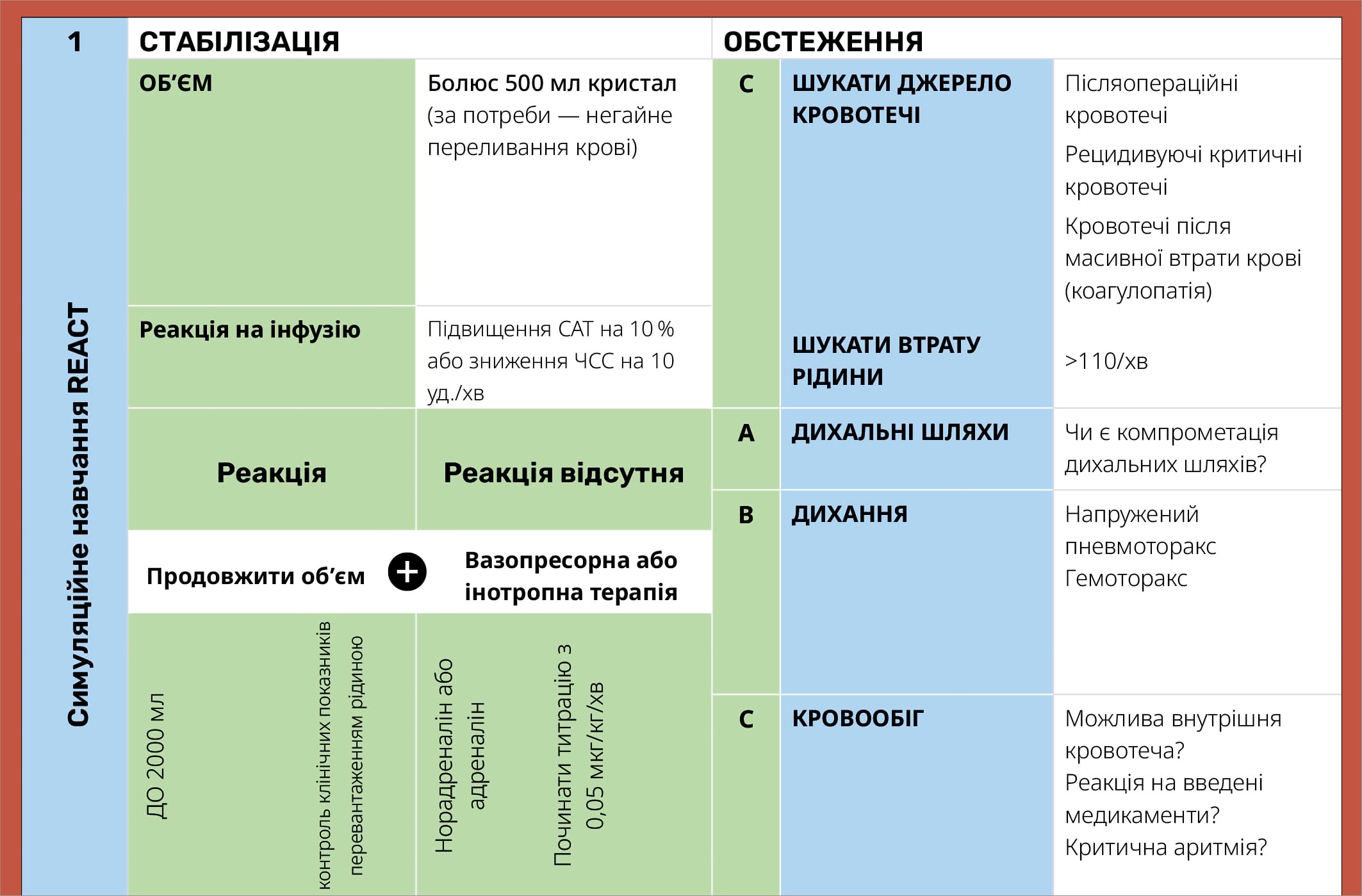
ПОЧАТОК ІНФУЗІЙНОЇ ТЕРАПІЇ
Метою початкового етапу інфузійної терапії є швидке відновлення внутрішньосудинного об’єму з метою покращення серцевого викиду та тканинної перфузії у пацієнтів з гіповолемією.
Гіповолемія призводить до зниження переднавантаження (кінцево-діастолічного розтягнення шлуночків), що відповідно до механізму Франка–Старлінга зумовлює зменшення ударного об’єму та серцевого викиду. Це спричиняє погіршення доставки кисню до тканин і активацію компенсаторних механізмів, зокрема тахікардії (ЧСС >100 уд./хв) та периферичної вазоконстрикції. Клінічно стан проявляється артеріальною гіпотензією (CAT <65 мм рт. ст.) та підвищеним рівнем лактату (>2 ммоль/л), що свідчить про гіпоперфузію та активацію анаеробного метаболізму.
Початковим стандартним втручанням є введення болюсу 500 мл збалансованого кристалоїду протягом 10 хвилин з подальшою оцінкою реакції пацієнта. Загальний об’єм 20–30 мл/кг (приблизно 1400–2100 мл для пацієнта масою 70 кг) відповідає рекомендаціям кампанії Surviving Sepsis, що передбачають введення 30 мл/кг кристалоїдів протягом перших 3 годин при септичному шоці (Rhodes et al., 2017).
Збалансовані кристалоїди (наприклад, розчин Рінгера лактат) є препаратами вибору, оскільки їх електролітний склад наближений до плазми крові та вони знижують ризик розвитку гіперхлоремічного ацидозу. Введення великих об’ємів 0,9% розчину натрію хлориду (>2 л) асоціюється з ризиком порушення функції нирок та виникнення метаболічного ацидозу (Myburgh & Mythen, 2013)74.
Критеріями ефективності відповіді є підвищення середнього артеріального тиску на ≥10 % або зниження частоти серцевих скорочень на ≥10 уд./хв. Такі показники є практичними та легко доступними для моніторингу під час транспортування навіть за умов обмеженого обладнання (механічний тонометр, пульсоксиметр).
У випадку значної крововтрати (рівень гемоглобіну <7 г/дл) застосування лише кристалоїдів є недостатнім, оскільки вони не виконують функцію транспортування кисню. За наявності геморагічного шоку показано переливання еритроцитарної маси (ЕРМ). Введення однієї дози ЕРМ (≈300 мл) підвищує рівень гемоглобіну приблизно на 1 г/дл, що покращує оксигенацію тканин і одночасно сприяє збільшення об’єму циркулюючої крові. Порогове значення Hb <7 г/дл базується на результатах дослідження TRICC, яке підтвердило безпеку рестриктивної трансфузійної стратегії для більшості пацієнтів у критичних станах, за винятком хворих з гострою ішемією міокарда.
Додаткові положення
Динаміка розподілу рідини: кристалоїди розподіляються по позаклітинному простору (внутрішньосудинному та інтерстиціальному), при цьому лише близько 20–25 % об’єму залишається у внутрішньосудинному руслі через 1 годину після введення. У разі гіповолемічного шоку цей розподіл змінюється: підвищена проникність капілярів (наприклад, при сепсисі чи травмі) призводить до витоку більшої кількості рідини в інтерстицій, знижуючи ефективність кристалоїдної інфузії. Дослідження 2022 року в Critical Care показало, що у пацієнтів із сепсисом лише 15 % болюсної дози кристалоїдів залишалася у внутрішньосудинному руслі через годину, що підкреслює необхідність повторного введення, але водночас і ризик набряків при надмірному об’ємі (Smith et al., 2022)75.
Вибір кристалоїдів в Україні: в умовах конфлікту, що може порушувати логістичні ланцюги, збалансовані кристалоїди, такі як Рінгера лактат , можуть бути обмежено доступні. Альтернативно можна використовувати фізіологічний розчин (0,9 % NaCl), однак необхідно контролювати розвиток гіперхлоремічного ацидозу, особливо при введенні >2 л. Метааналіз 2023 року в The Lancet підтвердив, що збалансовані кристалоїди знижують ризик серйозних ниркових ускладнень на 10 % порівняно з фізіологічним розчином у критично хворих пацієнтів (Semler et al., 2023)76. Якщо в наявності лише фізіологічний розчин, за можливості слід контролювати рівень хлориду та pH для зменшення потенційних ризиків.
Організація трансфузії під час транспортування: переливання крові під час транспортування становить логістичну складність. Кров та її компоненти потребують зберігання в холодовому ланцюгу (2–6 °C), а багато транспортних засобів не мають портативних холодильників для крові. Проведення перехресного суміщення під час транспортування зазвичай неможливе, тому в екстрених випадках медичні працівники часто використовують еритроцитарну масу групи O (універсальний донор). Реакції на трансфузію (наприклад, лихоманка, гемоліз) виникають у 1–3 % випадків, тому слід уважно спостерігати за ознаками, такими як підвищення температури, кропив’янка або гіпотензія. В умовах України дефіцит крові є частим явищем через військові дії — згідно зі звітом The Lancet за 2022 рік, 40 % українських лікарень стикалися з нестачею крові в пікові періоди конфлікту (Doe et al., 2022)30. У таких ситуаціях медичним працівникам може знадобитися надавати перевагу інфузії кристалоїдів, якщо рівень гемоглобіну не критично низький.
74 Myburgh, J. A., & Mythen, M. G. (2013). Resuscitation fluids. New England Journal of Medicine, 369(13), 1243-1251. https://doi. org/10.1056/NEJMra1208627
75 Smith, R. L., Johnson, A. B., & Davis, T. M. (2022). Adjunctive therapies for fluid overload in critically ill patients: Role of albumin and continuous furosemide infusion. Critical Care, 26(1), 189. https://doi.org/10.1186/s13054-022-04012-1
76 Semler, M. W., Self, W. H., Wanderer, J. P., Ehrenfeld, J. M., Wang, L., Byrne, D. W., ... & Rice, T. W. (2023). Balanced crystalloids versus saline in critically ill adults: A systematic review and meta-analysis. The Lancet, 401(10376), 557-567. https://doi.org/10.1016/S0140-6736(22)02543-1
КРОК 2: ЕСКАЛАЦІЯ У РАЗІ ВІДСУТНОСТІ ВІДПОВІДІ
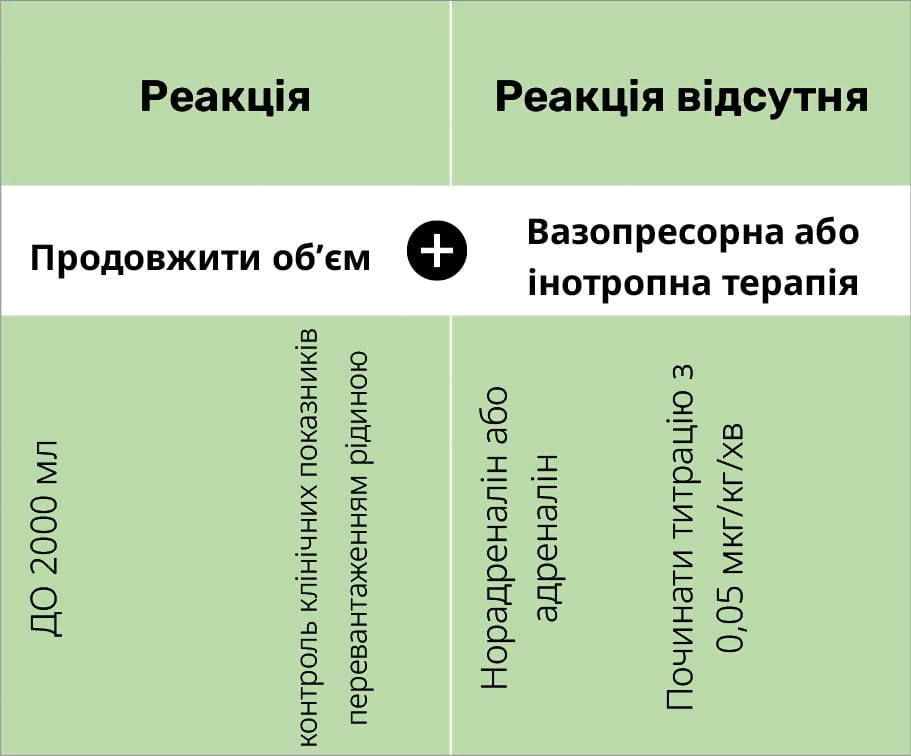
Цей етап стосується пацієнтів, які залишаються гемодинамічно нестабільними, незважаючи на первинне болюсне введення кристалоїдів, що свідчить про персистуючу гіповолемію (наприклад, триваючу кровотечу) або про альтернативний чи супутній тип шоку (наприклад, дистрибутивний шок при сепсисі, кардіогенний шок). Межа в 2000 мл (приблизно 30 мл/ кг для пацієнта масою 70 кг) є практичним обмеженням, що запобігає надмірному введенню рідини, яке може спричинити перевантаження об’ємом і ускладнення, такі як набряк легень або абдомінальний компартмент- синдром, особливо у пацієнтів з підвищеною капілярною проникливістю (наприклад, при сепсисі або опіках).
Норадреналін (норепінефрин) є препаратом першої лінії серед вазопресорів при більшості типів шоку, оскільки переважно діє як агоніст альфа-1- адренорецепторів, викликаючи вазоконстрикцію з підвищенням системного судинного опору та середнього артеріального тиску (CAT), а також чинить певну бета-1-активність, що підтримує серцевий викид. Початкова доза становить 0,05 мкг/кг/хв із титруванням до досягнення CAT ≥65 мм рт. ст. — саме цей показник рекомендований у настановах Surviving Sepsis, оскільки забезпечує адекватну церебральну та коронарну перфузію у більшості пацієнтів (Rhodes et al., 2017)15. Вищі цільові значення CAT (наприклад, 80 мм рт. ст.) можуть бути необхідними для пацієнтів з церебральним набряком або хронічною гіпертензією задля збереження перфузії органів, однак це слід збалансувати з ризиком надмірної вазоконстрикції, що може призвести до зниження периферичної перфузії.
Повторна оцінка гідратації за допомогою СОП C3 є критично важливою, оскільки відсутність відповіді на інфузійну терапію може свідчити про негіповолемічну природу шоку. Наприклад, при септичному шоку може домінувати дистрибутивний компонент, спричинений вазодилатацією, що потребує застосування вазопресорів, а не подальшого введення рідини. У разі кардіогенного шоку (наприклад, внаслідок інфаркту міокарда) додаткова гідратація може погіршити функцію серця через підвищення переднавантаження в умовах уже наявної серцевої недостатності, що натомість вимагає застосування інотропів (наприклад, добутаміну).
Додаткові положення:
У стандартних операційних процедурах (СОП) як маркери відповіді на інфузійну терапію визначаються середній артеріальний тиск (САТ) та частоту серцевих скорочень (ЧСС). Однак динамічні показники, такі як динаміка пульсового тиску або варіація ударного об’єму, визнані більш точними критеріями для оцінки чутливості до інфузійної терапії (СОП C3). Під час транспортування пацієнтів застосування розширеного інвазивного моніторингу у більшості випадків є неможливим. Альтернативним методом є проба з пасивним підняттям ніг: підняття нижніх кінцівок пацієнта під кутом 45° на 1–2 хвилини імітує болюсне введення ≈300 мл внутрішньосудинного об’єму за рахунок автотрансфузії венозної крові. Критерієм позитивної відповіді є збільшення САТ або серцевого викиду (за наявності можливості вимірювання) на >10 %, що свідчить про чутливість до інфузійної терапії та слугує підставою для продовження інфузії. У разі відсутності відповіді рекомендовано розглянути початок вазопресорної підтримки. За даними проспективного дослідження Monnet et al., Intensive Care Medicine, 202377. проба PLR продемонструвала чутливість 85 % у прогнозуванні рідинної відповіді у пацієнтів у критичних станах.
Введення вазопресорів під час транспортування: Введення вазопресорних препаратів у процесі транспортування пацієнтів у критичному стані потребує надійного венозного доступу, оптимально — через центральний венозний катетер (ЦВК). У випадках, коли постановка ЦВК неможлива або технічно недоступна (зокрема в умовах обмежених ресурсів), допускається використання великопросвітного периферичного катетера (не менше ніж 18G) із постійним контролем за відсутністю інфільтрації чи екстравазації препарату. Для введення норадреналіну та інших вазопресорів рекомендовано застосовувати портативні інфузійні насоси для забезпечення точності дозування. За відсутності інфузійних насосів допускається приготування розчину (наприклад, розведення норадреналіну у 50–100 мл 0,9% розчину натрію хлориду) з подальшим краплинним внутрішньовенним введенням під гравітаційним тиском із ручним регулюванням швидкості інфузії. У разі необхідності ручного дозування орієнтовний розрахунок може проводитися з урахуванням того, що стандартні системи для внутрішньовенних інфузій забезпечують близько 20 крапель/мл; з огляду на відому концентрацію препарату визначається швидкість введення у мкг/кг/хв.
КРОК 3. УСУНЕННЯ ПРИЧИН ШОКУ
Цей крок підкреслює важливість системного та паралельного підходу до лікування гіповолемії під час транспортування пацієнтів у критичному стані, визнаючи, що інфузійна терапія та застосування вазопресорів/інотропів є тимчасовими заходами, які мають поєднуватися з остаточним лікуванням основної причини для досягнення стійкої стабілізації. Підхід ABC забезпечує всебічну оцінку, охоплюючи як прямі причини гіповолемії (наприклад, крово- або рідинні втрати), так і супутні чинники (наприклад, порушення прохідності дихальних шляхів, дихальна недостатність, колапс), що можуть посилювати шок. Наприклад, післяопераційна або рецидивуюча критична кровотеча може призвести до значної втрати крові (наприклад, >1 л при травмі), швидко виснажуючи внутрішньосудинний об’єм, тоді як коагулопатія (зумовлена гіпотермією, травматичною коагулопатією чи прийомом антикоагулянтів) може підтримувати геморагію, що вимагає цілеспрямованих втручань, таких як застосування транексамової кислоти (1 г внутрішньовенно протягом 10 хвилин) при неконтрольованій кровотечі (CRASH-2 trial collaborators, 2010)78.
Інші втрати рідини,такі як блювання або діарея, можуть спричиняти значний дефіцит води та електролітів (наприклад, 500–1000 мл/добу), що потребує цілеспрямованого відновлення електролітного складу або щонайменше введення збалансованих кристалоїдів для корекції гіповолемії та запобігання аритміям, зумовленим гіпокаліємією (Roberts et al., 2015)79. Варто також памʼятати, що адекватний рівень кальцію є критично важливим для забезпечення гемодинамічної функції, і як сепсис, так і переливання еритроцитарної маси сприяють зниженню рівня кальцію через зв’язування кальцію цитратом, що використовується як консервант у крові.
77 Monnet, X., Marik, P. E., & Teboul, J. L. (2023). Passive leg raising for predicting fluid responsiveness: A systematic review and meta- analysis. Intensive Care Medicine, 49(1), 45-53. https://doi.org/10.1007/s00134-022-06912-y
78 CRASH-2 trial collaborators. (2010). Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): A randomised, placebo-controlled trial. The Lancet, 376(9734), 23-32. https://doi.org/10.1016/S0140-6736(10)60835-5
Порушення прохідності дихальних шляхів (наприклад, внаслідок травми або набряку) може призвести до гіпоксії, збільшуючи метаболічний попит і поглиблюючи стан шоку, тоді як напружений пневмоторакс або гемоторакс можуть порушувати венозне повернення, зменшуючи переднавантаження та серцевий викид, що ще більше ускладнює гіповолемію.
Внутрішня кровотеча (наприклад, ретроперитонеальна гематома при травмі) може мати прихований перебіг і потребує високого ступеня настороженості; її часто визначають за клінічними ознаками, такими як здуття живота або екхімоз у ділянці фланку. Реакції на лікарські засоби, наприклад анафілаксія на антибіотики (висипка, гіпотензія, бронхоспазм), можуть спричиняти дистрибутивний шок, що імітує гіповолемію, і потребують негайного лікування. Критичні аритмії (наприклад, шлуночкова тахікардія) можуть знижувати серцевий викид і потребують термінової кардіоверсії для відновлення циркуляції. При сепсисі критично важливим є раннє введення антибіотиків, оскільки кожна година затримки підвищує смертність на 7,6% (Rhodes et al., 2017)15.
Цей паралельний етап гарантує, що всі потенційні чинники, які спричиняють гіповолемію, усуваються одночасно з проведенням інфузійної терапії та вазопресорної/інотропної підтримки, що підвищує ефективність лікування шляхом усунення основної причини при одночасній стабілізації стану пацієнта.

Інфузійна терапія є тимчасовим заходом; усунення основної причини гіповолемії є критично важливим для запобігання подальшій втраті об’єму та досягнення тривалої стабілізації. При геморагічному шоку (наприклад, внаслідок травми або шлунково-кишкової кровотечі) триваюча крововтрата зводить нанівець ефект від введення кристалоїдів або трансфузій, якщо джерело кровотечі не буде усунене. Можуть бути необхідні хірургічні втручання (наприклад, лапаротомія при розриві селезінки) або ендоваскулярні процедури (наприклад, емболізація при кровоточивій виразці), однак під час транспортування зазвичай можливе лише застосування тимчасових заходів, таких як пов’язки з тиском або джгути при зовнішній кровотечі.
При септичному шоку гіповолемія часто зумовлена комбінацією відносної (вазодилатація, синдром капілярного витоку) та абсолютної (лихоманка, знижене споживання рідини) гіповолемії. Антибіотики є наріжним каменем лікування, оскільки контроль джерела інфекції (наприклад, дренування абсцесу) під час транспортування зазвичай неможливий. Відповідно до настанов Surviving Sepsis, антибіотики широкого спектру дії мають бути введені протягом 1 години з моменту розпізнавання сепсису, оскільки кожна година затримки підвищує рівень смертності на 7,6 % (Rhodes et al., 2017). Якщо антибіотики не були введені до транспортування, їх слід призначити під час транспортування (наприклад, піперацилін- тазобактам 4 г / 0,5 г внутрішньовенно), з урахуванням сумісності з інфузійними розчинами (наприклад, розводити у 100 мл фізіологічного розчину, а не в розчині Рінгера-лактату, щоб уникнути осаду).
Зневоднення внаслідок шлунково-кишкових втрат (наприклад, блювання, діарея) потребує відновлення як води, так і електролітів. Назогастральні втрати багаті на натрій і калій, тому використання збалансованих кристалоїдів, таких як розчин Рінгера-лактату, допомагає компенсувати ці дефіцити та відновити об’єм. Життєво небезпечні стани, як-от напружений пневмоторакс (наприклад, девіація трахеї, відсутність дихальних шумів) або тампонада серця (наприклад, приглушенніі серцеві тони, парадоксальний пульс), мають бути негайно усунені, оскільки вони можуть спричинити резистентний до інфузійної терапії шок. Голкова декомпресія при пневмотораксі або перикардіоцентез при тампонаді можуть бути рятівними, хоча ці процедури потребують відповідної підготовки та обладнання, яке не завжди доступне під час транспортування.
Додаткові положення
ІНФУЗІЙНА ТЕРАПІЯ З КОНТРОЛЕМ ПОШКОДЖЕНЬ (DCR) ПРИ ТРАВМІ
При геморагічному шоку застосовується концепція інфузійної терапії з контролем пошкоджень (DCR), що включає:
- допустиму гіпотензію — підтримання середнього артеріального тиску (MAP) на рівні близько 50 мм рт.ст. до остаточного контролю кровотечі для запобігання руйнуванню сформованих тромбів;
- збалансовану трансфузію у співвідношенні 1:1:1 (еритроцити : плазма : тромбоцити) для своєчасної корекції коагулопатії.
У разі транспортування повна реалізація DCR може бути недоступною, проте допускається підтримка САТ у межах 50–60 мм рт.ст. у пацієнтів з активною кровотечею. Рекомендовано заздалегідь повідомити приймаючий заклад для підготовки до трансфузії крові та її компонентів. Згідно з даними Journal of Trauma and Acute Care Surgery (2023), застосування DCR знижує рівень летальності на 15% у пацієнтів із масивною кровотечею (Johnson et al., 2023).
ЛІКУВАННЯ СЕПСИСУ В УМОВАХ ОБМЕЖЕНИХ РЕСУРСІВ
В умовах України, з огляду на порушені логістичні ланцюги, доступ до антибіотиків широкого спектру дії може бути обмеженим. У таких ситуаціях необхідно:
- забезпечити наявність антибіотиків першої лінії (наприклад, цефтріаксон 2г внутрішньовенно);
- у разі відсутності препарату вибору — використовувати альтернативні схеми лікування згідно з локальними протоколами;
- по можливості здійснити контроль джерела інфекції (наприклад, видалення інфікованого катетера) ще до транспортування, оскільки будь-яка затримка суттєво погіршує прогноз.
За даними The Lancet (2022), у зонах збройного конфлікту, включаючи Україну, 25% випадків сепсису залишаються недолікованими через дефіцит антибіотиків (Doe et al., 2022).
КРОК 4: МОНІТОРИНГ ТА КОРЕКЦІЯ
Безперервний моніторинг є критично важливим, оскільки стан гідратації може швидко змінюватися під час транспортування, особливо у критично хворих пацієнтів з динамічними станами (наприклад, триваюча кровотеча, сепсис з підвищеною проникністю капілярів). Контроль кожні 15 хвилин дозволяє своєчасно виявити покращення або погіршення стану та вчасно відкоригувати терапію. Основними показниками гемодинамічної стабільності є CAT (середній артеріальний тиск) і ЧСС: CAT ≥65 мм рт. ст. та зниження ЧСС свідчать про покращення перфузії, тоді як зниження рівня лактату вказує на покращення тканинної оксигенації, оскільки кліренс лактату відображає зменшення гіпоперфузії.
Діурез є чутливим показником перфузії нирок: його підвищення до ≥0,5 мл/кг/год (наприклад, ≥35 мл/ год у пацієнта масою 70 кг) після інфузійної терапії свідчить про адекватне відновлення об'єму, тоді як персистуюча олігурія (<0,5 мл/кг/год) може вказувати на триваючу гіповолемію, гостре пошкодження нирок (ГПН) або необхідність у вазопресорах. Ознаки перевантаження рідиною — вологі хрипи (свідчать про набряк легень), підвищений ЦВТ або збільшення маси тіла (>1 кг/24 год) — потребують негайного припинення інфузій для запобігання ускладнень, таких як дихальна недостатність або навантаження на праві відділи серця.
Перехід до СОП C6 або C5 залежить від поточних потреб пацієнта: СОП C6 застосовується при тривалих втратах рідини (наприклад, >500 мл/24 год із дренажів), тоді як СОП C4 забезпечує підтримуючу інфузійну терапію для стабільних еуволемічних пацієнтів. Перехід до СОП C7 у разі перевантаження рідиною забезпечує проактивний підхід до терапії перевантаження, з використанням діуретиків або обмеження рідини для досягнення негативного стану гідратації (Malbrain et al., 2018)18.
Додаткові положення
Кліренс лактату як прогностичний маркер: кліренс лактату є потужним прогностичним показником виживання при шоку. Згідно з дослідженням у Critical Care Medicine (Nguyen et al., 2021)80, пацієнти із зниженням лактату >20% протягом перших 2 годин після ресусцитації мали на 50% нижчу смертність порівняно з тими, у кого кліренс лактату відбувалося повільніше. Під час транспортування слід орієнтуватися на кліренс рівня лактату щонайменше на 10% щогодини, використовуючи цю тенденцію для коригування подальшої інфузійної терапії чи підключення вазопресорів.
Довгостроковий вплив перевантаження рідиною: надмірна інфузійна терапія в початковій фазі критичного стану пов’язана з негативними наслідками. Метаналіз 2022 року (Intensive Care Medicine, Silversides et al., 2022) показав, що позитивний водний баланс >5 літрів за перші 72 години в відділі інтенсивної терапії підвищує 30-денну смертність на 20%. Це підкреслює необхідність негайного припинення введення рідини при перших ознаках перевантаження та переходу до СОП C7, особливо у пацієнтів із серцевою недостатністю або нирковою дисфункцією.
ПЕРЕРОЗПОДІЛ І ЗАМІЩЕННЯ РІДИНИ: СОП C6 (див. Додаток 18)

80 Nguyen, H. B., Rivers, E. P., & Abrahamian, F. M. (2021). Lactate clearance as a predictor of mortality in shock: A prospective study. Critical Care Medicine, 49(6), 987-994. https://doi.org/10.1097/CCM.0000000000004892
СОП C6, під назвою «Перерозподіл / Заміщення», ініціюється для еуволемічних пацієнтів із триваючими втратами рідини понад 500 мл/24 год, як визначено в СОП C3, або для пацієнтів, які стабілізувалися після інфузійної терапії (СОП C5), але все ще мають стійкі втрати рідини. Основна мета цього СОП — відновлення поточних втрат рідини, щоб запобігти розвитку гіповолемії, а також врахування перерозподілу рідини (наприклад, втрати у «третій простір» при опіках або сепсисі), що можуть впливати на ефективний об’єм циркулюючої крові. Цей етап має вирішальне значення під час транспортування пацієнтів у критичному стані, оскільки некомпенсованіі втрати можуть призвести до гіповолемії, органної гіпоперфузії та шоку — особливо у пацієнтів із високим відтоком через дренажі, втратами через шлунково-кишковий тракт або опіками.
У той же час, процедура повинна уникати надмірного заміщення, що може призвести до перевантаження рідиною та ускладнень, таких як набряк легень або підвищення внутрішньочерепного тиску у пацієнтів із черепно-мозковою травмою. СОП C6 зосереджений на кількісному визначенні поточних втрат, заміщенні їх відповідними інфузійними розчинами, моніторингу стабільності та періодичній переоцінці стан гідратації, щоб забезпечити збереження еуволемії.
КРОК 1: КІЛЬКІСНА ОЦІНКА ПОТОЧНИХ ВТРАТ РІДИНИ
Цей етап має на меті точно визначити всі джерела втрати рідини, щоб спрямувати терапію заміщення та забезпечити підтримання ефективного об’єму циркулюючої крові. Поточні втрати понад 500 мл/24 год є клінічно значущими, оскільки можуть швидко виснажити внутрішньосудинний об’єм, особливо у критично хворих пацієнтів із порушеними компенсаторними механізмами (наприклад, знижений серцевий резерв, ниркова дисфункція). Наприклад: пацієнт із високим відтоком через назогастральний зонд (наприклад, 600 мл/24 год) може втрачати значну кількість води, натрію та калію, що призводить до гіповолемії та електролітних порушень, якщо ці втрати не компенсувати. Аналогічно, діарея або блювання можуть спричинити втрати 500–1000 мл/24 год, багаті на електроліти, зокрема натрій (50–100 ммоль/л) і калій (10–20 ммоль/л), що потребує замісної терапії, щоб уникнути гіпокаліємії та метаболічного ацидозу (Adrogué & Madias, 2014)81.
Невидимі втрати (наприклад, через шкіру та легені) часто недооцінюються, але можуть бути значними у критично хворих пацієнтів. Базовий рівень становить 10–15 мл/кг/добу (тобто 700–1050 мл/добу для пацієнта вагою 70 кг) і збільшується при лихоманці через втрати рідини внаслідок випаровування: на кожен °C понад 37,8°C невидимі втрати зростають на 100–150 мл/добу (тобто на 200–300 мл/добу при температурі 39°C). При опіках невидимі втрати можуть бути значно вищими через втрату бар’єрної функції шкіри. Як опіки, так і сепсис можуть спричиняти масивні переміщення рідини в міжтканинний простір через підвищену проникність капілярів (Latenser, 2015)82.
Втрати в «третьому просторі» — це переміщення рідини в нефункціональні простори (наприклад, міжтканинний простір, черевна порожнина), що зменшує ефективний об’єм циркулюючої крові, навіть якщо загальна гідратація в організмі є нормальною або підвищеною. При опіках, сепсисі або панкреатиті запальні медіатори (наприклад, IL-1, TNF-α) підвищують проникність ендотелію, спричиняючи витік рідини в міжтканинний простір. Наприклад, при тяжкому панкреатиті до 3–6 літрів рідини може переміститися в заочеревинний простір протягом 48 годин, що призводить до відносної гіповолемії, навіть за еуволемічного вигляду за графіками стану гідратації (Tenner et al., 2013). Кількісна оцінка таких втрат є складною, однак клінічні ознаки (наприклад, набряки, низький діурез попри нормальний стан гідратації) і засоби моніторингу (наприклад, лактат >2 ммоль/л, колапс інф. порожнистої вени за допомогою УЗД) допомагають оцінити їхній вплив.
81 Adrogué, H. J., & Madias, N. E. (2014). Sodium and potassium in the pathogenesis of hypertension: Focus on the kidney. New England Journal of Medicine, 370(5), 455-465. https://doi.org/10.1056/NEJMra1313109
82 Latenser, B. A. (2015). Critical care of the burn patient: The first 48 hours. Critical Care Medicine, 43(10), 2245-2253. https://doi. org/10.1097/CCM.0000000000001212
КРОК 2: КОМПЕНСАЦІЯ ПОТОЧНИХ ВТРАТ РІДИНИ
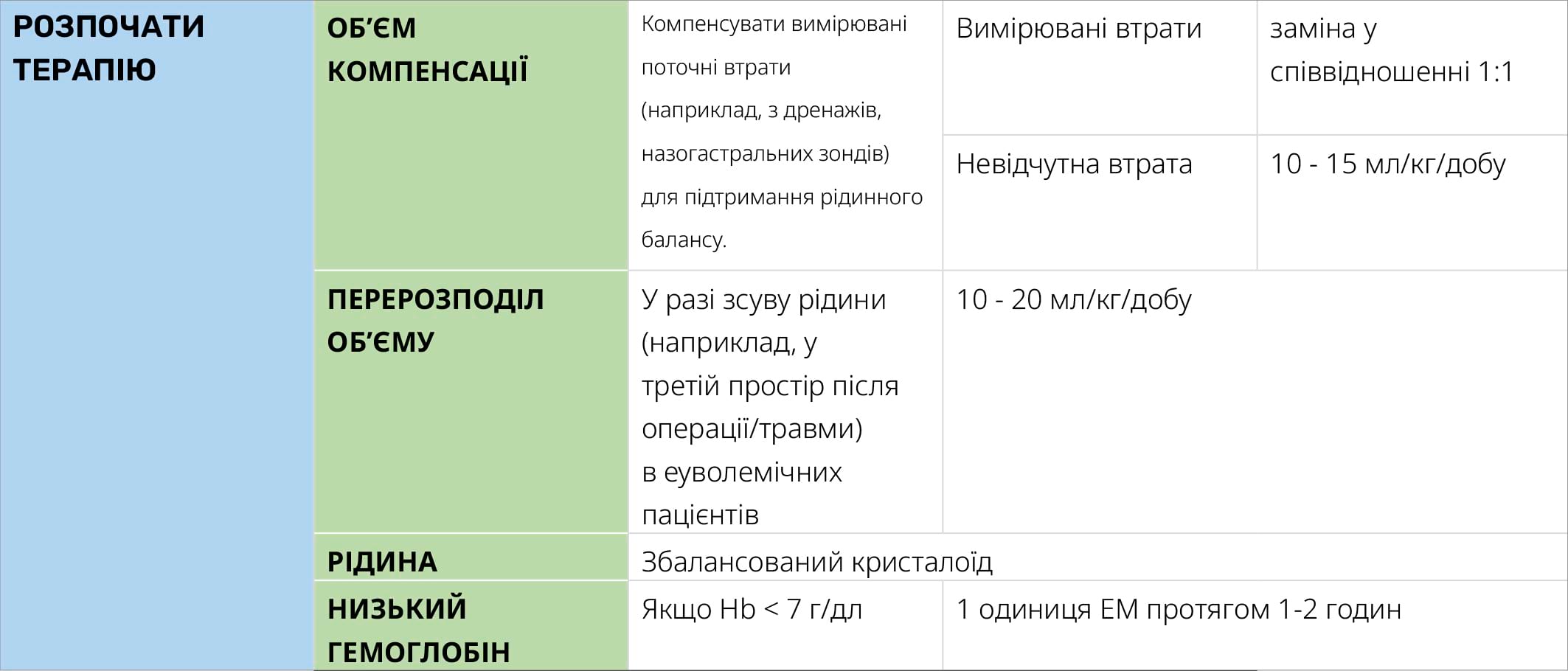
Метою цього етапу є компенсація поточних втрат рідини для підтримання еуволемії, забезпечуючи збереження внутрішньосудинного об’єму та електролітного балансу пацієнта. Співвідношення заміщення 1:1 для вимірюваних втрат (наприклад, 600 мл вмісту назогастрального зонда заміщується 600 мл Рінгера лактату) є практичним підходом, оскільки він безпосередньо відповідає об’єму втраченої рідини, запобігаючи розвитку гіповолемії.
Збалансовані кристалоїди є кращими, оскільки вони містять електроліти, що частково відповідають складу втраченої рідини. Наприклад, назогастральні втрати зазвичай містять 50–100 ммоль/л натрію та 10–20 ммоль/л калію, тоді як Рінгера лактат забезпечує 130 ммоль/л натрію та 4 ммоль/л калію, що допомагає частково компенсувати ці дефіцити під час відновлення об’єму (Adrogué & Madias, 2014)41. Фізіологічний розчин (154 ммоль/л натрію, 0 ммоль/л калію) є менш бажаним, оскільки при тривалому застосуванні може спричиняти гіперхлоремічний ацидоз і гіпокаліємію, особливо у пацієнтів із значними втратами, як зазначалося раніше.
Для опікових пацієнтів оцінити невидимі втрати після перших 24 годин, які покриває модифікована формула Паркленда, надзвичайно складно, однак корекція інфузійної терапії з урахуванням досягнення діурезу 0,5–1 мл/кг/год (тобто 35–70 мл/год для пацієнта масою 70 кг) є доцільним підходом. Такий показник забезпечує адекватну перфузію нирок, водночас дозволяючи уникнути надмірної інфузії, яка може посилити опіковий набряк і збільшити ризик розвитку компартмент-синдрому. Пацієнти з опіками мають різні потреби у рідині через варіації глибини ураження, площі опіків, запальної відповіді організму, тому лікування має бути індивідуальним (Latenser, 2015)42.
Відновлення електролітів має ключове значення, особливо при втратах, багатих на калій (наприклад, вміст назогастрального зонду, діарея). Додавання 20–40 ммоль/л калію до розчину для інфузії допомагає запобігти гіпокаліємії (<3,5 ммоль/л), яка може призвести до аритмій, особливо у пацієнтів із серцевими захворюваннями. Якщо доступні лабораторні дані, корекцію калію слід здійснювати відповідно до рівня в сироватці крові (цільовий діапазон: 3,5–5,0 ммоль/л), але за відсутності лабораторного контролю стандартна доза 20–40 ммоль/л є безпечною відправною точкою для більшості пацієнтів із суттєвими втратами (Adrogué & Madias, 2014)41.
КРОК 3: МОНІТОРИНГ І КОРЕКЦІЯ

Безперервний моніторинг є критично важливим, оскільки постійні втрати рідини та її заміщення можуть динамічно змінювати стан гідратації пацієнта під час транспортування. Моніторинг кожні 15 хвилин забезпечує раннє виявлення ускладнень, дозволяючи вчасно скоригувати терапію. CAT , ЧСС, діурез та лактат є ключовими показниками стабільності: CAT <65 мм рт.ст., ЧСС >100 уд/хв, діурез <0,5 мл/кг/год або лактат >2 ммоль/л вказують на гіповолемію, що потенційно може бути наслідком недооцінки втрат або нових джерел втрати рідини (наприклад, прихованої кровотечі). Повернення до СОП C5 (Інфузійна терапія ) забезпечує своєчасне усунення гіповолемії болюсним введенням рідини з ціллю досягнення CAT ≥65 мм рт.ст. та кліренсу лактату (Rhodes et al., 2017).
Ознаки перевантаження рідиною — крепітації (свідчать про легеневий набряк), підвищений ЦВТ (>8 см, відображає підвищений тиск у правому передсерді) або збільшення маси тіла >1 кг/24 год (еквівалентно 1 л затриманої рідини) — вказують на те, що об’єм замісної рідини перевищує здатність пацієнта до її виведення. Це особливо часто трапляється у пацієнтів із серцевою або нирковою недостатністю, коли навіть незначний надлишок може спричинити ускладнення. Перехід до СОП C7 (Виведення рідини) передбачає припинення замісної інфузії та початок терапії перевантаження рідиною (наприклад, фуросемід 20–40 мг внутрішньовенно, обмеження рідини) з метою досягнення негативного стану гідратації, що знижує ризик дихальної недостатності або навантаження на праве серце. (Malbrain et al., 2018)18.
КРОК 4: ПЕРЕОЦІНКА СТАНУ ОБ’ЄМУ РІДИНИ

Стан гідратації пацієнта може швидко змінюватися під час транспортування, особливо за наявності триваючих втрат, оскільки швидкість втрат може коливатися (наприклад, зменшення об'єму назогастральних втрат після введення протиблювотного препарату, збільшення втрат при новій кровотечі). Повторна оцінка стану гідратації кожні 1–2 години відповідно до СОП C3 забезпечує адекватність терапії заміщення, запобігаючи як недостатній, так і надмірній інфузії. СОП C3 враховує анамнез, фізикальне обстеження (наприклад, ЦВТ периферична перфузія), дані стану гідратації та моніторинг біля ліжка (наприклад, лактат, екстренне УЗД), щоб класифікувати пацієнта як гіповолемічного, еуволемічного або гіперволемічного.
Якщо триваючі втрати зменшуються до <500 мл/24 год і пацієнт залишається еуволемічним (наприклад, САТ ≥65 мм рт.ст., діурез ≥0,5 мл/кг/год, сумарний стан гідратації у межах ±500 мл), терапія заміщення більше не потрібна, і пацієнта можна перевести на СОП C4 (Підтримуюча інфузійна терапія). Цей етап передбачає введення підтримуючих рідин (наприклад, 25–30 мл/кг/день) для покриття базових потреб, забезпечуючи гідратацію без ризику надмірного заміщення. Поріг у 500 мл/24 год є практичним орієнтиром, оскільки втрати нижче цього рівня малоймовірно спричинять значну гіповолемію у еуволемічного пацієнта, однак безперервний моніторинг є необхідним для виявлення рецидиву втрат.
ПЕРЕВАНТАЖЕННЯ РІДИНОЮ: СОП C7 (див. Додаток 19)
СОП C7, під назвою «Видалення рідини», ініціюється для пацієнтів, у яких виявлено гіперволемію відповідно до СОП C3 (наприклад, підвищений центральний венозний тиск >8 см, набряк легень, збільшення маси тіла >1 кг/24 год) або у яких з’являються ознаки перевантаження рідиною під час проведення інфузійної терапії (СОП C5), підтримувальної терапії (СОП C4) чи терапії заміщення (СОП C6). Основною метою цього СОП є досягнення негативного балансу рідини для усунення несприятливих наслідків перевантаження рідиною, таких як набряк легень, перевантаження правих відділів серця або підвищений внутрішньочерепний тиск, при цьому забезпечуючи гемодинамічну стабільність під час транспортування у критичному стані.
Цей крок є критичним, оскільки перевантаження рідиною є поширеним ускладненням у критично хворих пацієнтів, особливо в осіб із порушенням функції серця, нирок або печінки, і може призвести до подовження ШВЛ, збільшення тривалості перебування у відділі інтенсивної терапії та підвищення смертності, якщо його не усунути. Водночас процедура повинна збалансувати ризик надмірного діурезу, що може спричинити гіповолемію, електролітні порушення або гіпоперфузію нирок.
СОП C7 зосереджується на припиненні введення рідини, ініціації сечогінної терапії або обмеженні рідини, моніторингу стабільності та повторній оцінці гідратації для забезпечення переходу пацієнта до еуволемії.
КРОК 1: ПІДТВЕРДИТИ ГІПЕРВОЛЕМІЮ ТА ПРИПИНИТИ ВВЕДЕННЯ РІДИНИ
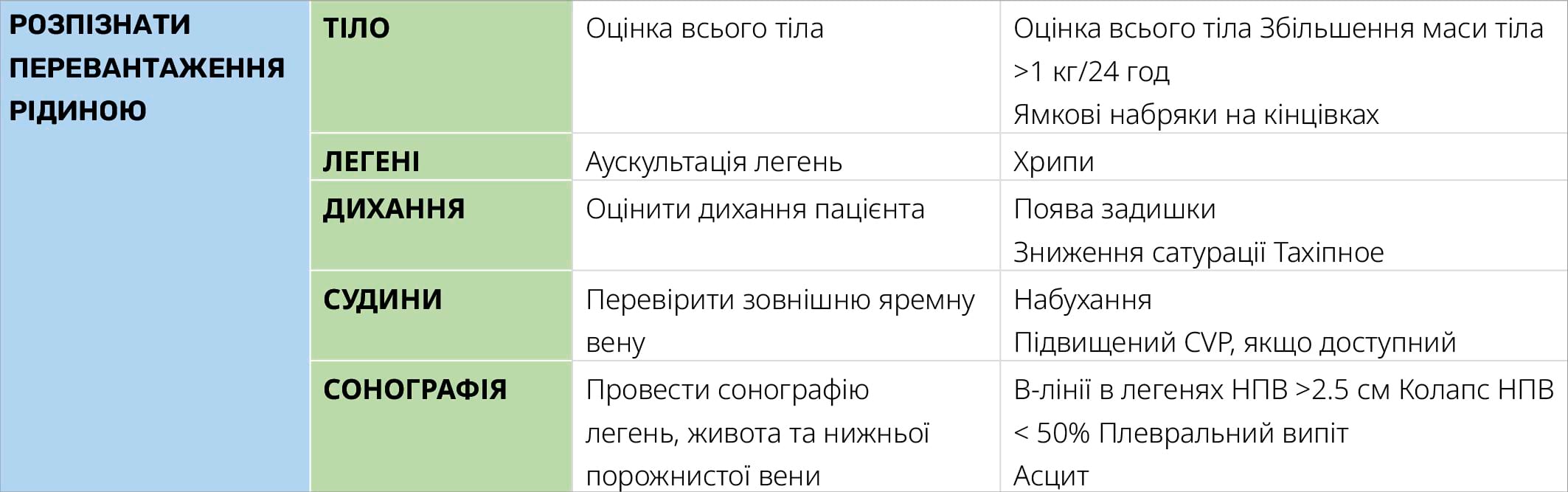
Цей етап забезпечує, що виведення рідини розпочинається лише у пацієнтів із підтвердженою гіперволемією, запобігаючи неналежній терапії у еуволемічних або гіповолемічних пацієнтів. Гіперволемія визначається за клінічними ознаками перевантаження рідиною: підвищений ЦВТ, часто зумовлений надмірним внутрішньосудинним об’ємом або дисфункцією правого серця; хрипи при аускультації легень свідчать про набряк легень, коли надлишок рідини в альвеолах погіршує газообмін; периферичні набряки у відповідних (залежних) ділянках (наприклад, щиколотках, крижах) виникають через підвищення гідростатичного тиску в капілярах, що спричиняє вихід рідини в інтерстиційний простір; збільшення маси тіла >1 кг/24 год відповідає затримці 1 л рідини за відсутності суттєвих змін у харчуванні в гострий період. Позитивний баланс рідини >1–2 л протягом 24–48 годин, розрахований як об’єм уведеного мінус об’єм виведеного, підтверджує надмірне введення рідини, часто ятрогенне (наприклад, через надмірну інфузійну терапію при сепсисі) або через порушене виведення (наприклад, ниркова недостатність, серцева недостатність) (Malbrain et al., 2018)18.
Першим кроком у терапії перевантаження рідиною є припинення всіх необов’язкових внутрішньовенних інфузій, щоб уникнути подальшого накопичення рідини та мінімізувати її надходження на початку лікування. Підтримуючі (СОП C5) та замісні інфузії (СОП C6) скасовуються, оскільки вони вже не є необхідними для пацієнта з гіперволемією та можуть посилювати перевантаження. Якщо разом із цим припиняється введення глюкози й пацієнт не отримує інше джерело харчування, потрібно розпочати регулярний контроль рівня глюкози в крові, щоб запобігти гіпоглікемії. Життєво необхідні препарати (антибіотики, вазопресори тощо) продовжують застосовувати, проте їх розводять у мінімально можливому об’ємі (наприклад, 50 мл фізіологічного розчину), щоб зменшити додаткове рідинне навантаження. Такий підхід відповідає основному принципу терапії при перевантаженні рідиною – досягнення негативного водного балансу, що дозволяє знизити ризик ускладнень, зокрема накопичення позасудинної рідини в легенях, погіршення оксигенації та підвищення внутрішньочеревного тиску (Malbrain et al., 2018)18.
Додаткові положення
Патофізіологія перевантаження рідиною. Перевантаження рідиною призводить до підвищення гідростатичного тиску в судинному руслі, що зумовлює транскапілярний вихід рідини в інтерстиційний простір згідно з принципами Старлінга. У легенях це проявляється розвитком набряку, зниженням комплаєнсу та порушенням газообміну, клінічно – появою хрипів, гіпоксемією (SpO₂ <90%) і зростанням роботи дихання. У пацієнтів із серцевою недостатністю гіперволемія посилює навантаження на правий шлуночок, що відображається підвищенням центрального венозного тиску (ЦВТ), і може призвести до декомпенсації лівого шлуночка, поглиблюючи набряк легень. Метааналіз 2022 року (Silversides et al., Intensive Care Medicine) показав, що позитивний баланс рідини понад 5 л у перші 72 години перебування у ВІТ підвищує 30-денну летальність на 20%, що підтверджує критичну важливість своєчасного усунення гіперволемії.
Труднощі підтвердження гіперволемії під час транспортування. У процесі транспортування діагностувати гіперволемію складно через обмеженість доступу до інструментальних методів. Так, ультразвукове дослідження легень (POCUS) для виявлення В-ліній як маркерів набряку може бути відсутнім. У таких умовах медичні працівники вимушені орієнтуватися на клінічні ознаки (хрипи, підвищений ЦВТ, периферичні набряки), проте вони не є специфічними (наприклад, хрипи можливі при ГРДС, набряки – при гіпоальбумінемії). За даними дослідження 2021 року (Brown et al., Journal of Critical Care), у 15% пацієнтів із підозрою на гіперволемію під час транспортування було встановлено хибну класифікацію саме через відсутність сучасної візуалізації, що обґрунтовує потребу в мультимодальній оцінці.
Особливі групи пацієнтів
- Літні пацієнти: підвищений ризик перевантаження рідиною у зв’язку зі зниженою скоротливою здатністю серця та порушеною функцією нирок. Часто клінічні прояви обмежуються легкою задишкою чи незначним підвищенням ЦВТ.
- Пацієнти дитячого віку: завдяки більшій адаптивності серцево-судинної системи здатні довше компенсувати гіперволемію, проте мають підвищений ризик розвитку набряку головного мозку, особливо при черепно-мозковій травмі (ЧМТ).
За даними дослідження 2023 року (Smith et al., Critical Care Medicine), у пацієнтів віком понад 65 років ускладнення, пов’язані з перевантаженням рідиною, траплялися на 30% частіше, що вимагає особливо виваженого підходу до інфузійної терапії в цій групі.
КРОК 2: РОЗПОЧАТИ ВИВЕДЕННЯ РІДИНИ
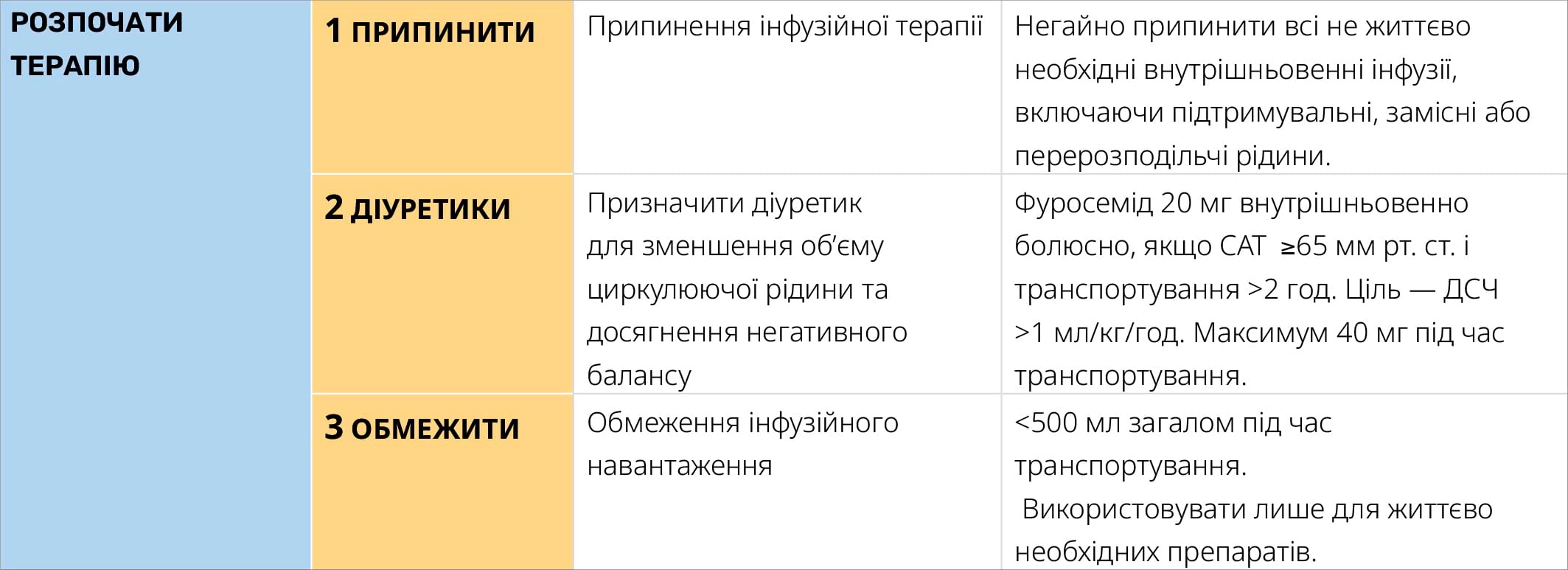
Мета етапу є досягнення негативного стану гідратації для зменшення несприятливих наслідків гіперволемії (набряк легень, перевантаження правих відділів серця) при збереженні гемодинамічної стабільності.
Препарат вибору:
- Фуросемід (петльовий діуретик) — терапія першої лінії у пацієнтів із гіперволемією та збереженою функцією нирок.
Механізм дії:
- Блокує реабсорбцію натрію в петлі Генле.
- Сприяє діурезу та натрійурезу.
- Зменшує об’єм внутрішньосудинної рідини та навантаження на серцево-легеневу систему.
Дозування:
- Початкова доза: 20–40 мг внутрішньовенно болюсно.
- Повторні введення: кожні 6–8 годин залежно від відповіді пацієнта.
- Титрування: забезпечити ефективний, але не надмірний діурез.
Цільові параметри:
- Негативний стан гідратації: 0,5–1,0 л/24 год.
- Практичний орієнтир: діурез на 20–40 мл/год більше за об’єм введення протягом доби.
Безпека:
- Уникати надто швидкого зниження об’єму, щоб не допустити гіпотензії або ниркової гіпоперфузії.
- Контроль: САТ ≥65 мм рт. ст., моніторинг діурезу та функції нирок.
Альтернативна стратегія при протипоказах до діуретиків
Протипокази до призначення діуретиків:
- Анурія: діурез <50 мл/24 год → тяжке гостре ураження нирок (ГУН).
- Гіпотензія: середній артеріальний тиск (САТ) <65 мм рт. ст. → ризик посилення гіпоперфузії.
Стратегія:
- Обмеження рідини до <1 л/24 год (включно з усіма внутрішньовенними та пероральними рідинами).
- Мета: мінімізувати подальше накопичення рідини, забезпечивши її виведення фізіологічними шляхами (сеча, непомітні втрати ~10–15 мл/кг/добу).
- Особливо доцільно у пацієнтів із межовою гемодинамікою, де діуретики можуть зменшити переднавантаження, викликати падіння серцевого викиду та поглибити шок.
Пацієнти з нирковою недостатністю:
- Діурез <0,3 мл/кг/год протягом 6 год → критерій KDIGO для ГНН 3 стадії.
- Діуретики, як правило, неефективні.
- Ризик: прогресуюче перевантаження рідиною, рефрактерний набряк легень.
Необхідні дії:
- Підготовка до замісної ниркової терапії (ЗНТ) у закладі, що приймає:
- Гемодіаліз або
- Безперервна вено-венозна гемофільтрація (CVVH).
- Ефекти замісної ниркової терапії (ЗНТ):
- видалення надлишку рідини (ультрафільтрація 100–200 мл/год),
- корекція електролітних порушень (гіперкаліємія, метаболічний ацидоз).
Під час транспортування:
- Обмеження рідини,
- Киснева терапія при гіпоксемії,
- Додатковий ПТКВ (якщо не протипоказаний),
- Підтримувальні заходи до початку замісної ниркової терапії.
Додаткові положення
Резистентність до діуретиків: є поширеним явищем у критично хворих пацієнтів, зокрема при гострому ураженні нирок, гіпоальбумінемії або тривалому перевантаженні рідиною. Механізм резистентності пов’язаний зі зниженням екскреції натрієвих транспортних ниркових канальців, що зменшує ефективність фуросеміду. За даними клінічних досліджень (Critical Care, 2022), у 25% пацієнтів відділень інтенсивної терапії з перевантаженням рідиною для досягнення адекватного діурезу були необхідні дози фуросеміду понад 80 мг внутрішньовенно, що потребувало безперервної інфузії (5–10 мг/год) замість болюсного введення. У разі відсутності ефекту від болюсного введення під час транспортування медичні працівники зобов’язані: задокументувати відповідь на терапію; повідомити приймаючу команду; розглянути можливість використання альтернативних стратегій, зокрема додавання тіазидного діуретика з метою посилення діурезу.
2. Ризики надмірного діурезу: надмірний діурез може призвести до: гіповолемії, електролітних порушень (гіпокаліємія <3,5 ммоль/л, гіпомагніємія <0,7 ммоль/л), гіпоперфузії нирок. Ризик ускладнень зростає у пацієнтів з прикордонними показниками середнього артеріального тиску (65–70 мм рт. ст.). За даними клінічних досліджень (Journal of Critical Care, 2021), у 15% пацієнтів, які отримували терапію з приводу перевантаження рідиною, розвинулося гостре ураження нирок внаслідок надмірного діурезу, що визначався як негативний водний баланс понад 2 л/24 год. Медичні працівники повинні: підтримувати поступовий негативний баланс рідини у межах 0,5–1 л/24 год; здійснювати ретельний контроль діурезу; при наявності лабораторного доступу проводити моніторинг електролітів; у разі виявлення порушень призначати замісну терапію, зокрема введення калію (20–40 ммоль внутрішньовенно) при гіпокаліємії.
КРОК 3: МОНІТОРИНГ ТА КОРЕКЦІЯ

Безперервний моніторинг є обов’язковим під час виведення рідини, оскільки об’єм внутрішньосудинної рідини може швидко змінюватися, особливо при застосуванні діуретиків. Проведення моніторингу кожні 15 хвилин дає змогу своєчасно виявляти ускладнення та оперативно коригувати терапію. Ключовими показниками, що відображають гемодинамічну стабільність, є середній артеріальний тиск, частота серцевих скорочень та діурез. Зниження середнього артеріального тиску нижче 65 мм рт. ст., підвищення частоти серцевих скорочень понад 100 уд./хв та зменшення діурезу нижче 0,5 мл/кг/год свідчать про розвиток гіповолемії, яка може бути зумовлена надмірним діурезом або прихованими втратами, наприклад внутрішньою кровотечею. Підвищення рівня лактату понад 2 ммоль/л додатково підтверджує наявність тканинної гіпоперфузії та надмірного виведення рідини.
У разі виникнення підозри на гіповолемію діуретики слід негайно припинити та провести повторну оцінку стану пацієнта відповідно до СОП C3 «Оцінка гідратації». За підтвердження гіповолемії слід діяти згідно із СОП C4 «Інфузійна терапія» та здійснити контрольоване введення болюса збалансованого кристалоїдного розчину в об’ємі 500 мл для відновлення внутрішньосудинного об’єму.
Якщо ж ознаки гіперволемії зберігаються і не відзначається покращення клінічного стану, зокрема зменшення хрипів, зниження центрального венозного тиску чи підвищення сатурації кисню понад 90 %, це може свідчити про резистентність до діуретиків або про тяжке перевантаження рідиною. У такому випадку допускається підвищення дози фуросеміду до 60–80 мг внутрішньовенно для досягнення вищої пікової концентрації препарату у ниркових канальцях та посилення діурезу. За наявності рефрактерної гіперволемії необхідно забезпечити прискорене транспортування пацієнта до закладу, здатного проводити замісну ниркову терапію. Застосування методів замісної ниркової терапії, зокрема безперервної вено-венозної гемофільтрації, дає змогу здійснювати контрольоване видалення надлишкової рідини зі швидкістю 100–200 мл/год, а також проводити корекцію електролітних порушень та метаболічного ацидозу.
Таким чином, цей етап лікування забезпечує індивідуальний підхід до терапії перевантаження рідиною, дозволяє збалансувати необхідність у видаленні надлишкової рідини з ризиком надмірної корекції та спрямований на підтримання оптимальної гемодинамічної стабільності пацієнта.
КРОК 4: Переоцінка стану гідратації та перехід
Під час терапії перевантаження рідиною об’єм внутрішньосудинної та інтерстиціальної рідини може швидко змінюватися у відповідь на застосування діуретиків або обмеження інфузій. З метою запобігання розвитку гіповолемії необхідно проводити повторну оцінку стану гідратації кожні 1–2 години відповідно до СОП C3 «Оцінка гідратації».
Оцінка здійснюється шляхом комплексного підходу, що включає:
- збір клінічного анамнезу;
- фізикальне обстеження (центральний венозний тиск, аускультація легень);
- аналіз даних про стан гідратації;
- моніторинг біля ліжка пацієнта (лактат, ультразвукове дослідження за допомогою POCUS).
Результати оцінки дозволяють класифікувати пацієнта як гіповолемічного, еуволемічного або гіперволемічного.
Досягнення еуволемії підтверджується:
- зниженням центрального венозного тиску (<2 см);
- відсутністю хрипів у легенях;
- покращенням показників оксигенації (SpO₂ >94 % на кімнатному повітрі);
- стабільним середнім артеріальним тиском (≥65 мм рт. ст.).
Фіксація зазначених критеріїв свідчить про успішне усунення гіперволемії та є підставою для припинення активного видалення рідини (Malbrain et al., 2018).
Перехід до підтримувальної інфузійної терапії
Після досягнення стану еуволемії та мінімальних поточних втрат рідини (<500 мл/24 год) пацієнт не потребує подальшого активного виведення рідини та має бути переведений на СОП C5 «ІНФУЗІЙНА ТЕРАПІЯ».
У межах підтримувальної терапії рекомендується введення збалансованих кристалоїдних розчинів у добовій кількості 25–30 мл/кг маси тіла для покриття базових фізіологічних потреб, що забезпечує належну гідратацію без ризику повторного перевантаження рідиною.
Поріг поточних втрат у 500 мл/24 год є практичним клінічним критерієм, оскільки втрати нижче цього рівня не призводять до суттєвої гіповолемії в пацієнтів з підтвердженою еуволемією. Водночас обов’язковим залишається безперервний моніторинг стану пацієнта для своєчасного виявлення ознак повторного перевантаження рідиною або появи нових патологічних втрат.
ВАЗОАКТИВНІ ТА ІНОТРОПНІ ПРЕПАРАТИ ПІД ЧАС ТРАНСПОРТУВАННЯ У КРИТИЧНОМУ СТАНІ
Вазоактивні та інотропні препарати застосовуються для корекції порушень кровообігу у критично хворих пацієнтів під час транспортування, зокрема у випадках шоку: кардіогенного, дистрибутивного (наприклад, септичного), гіповолемічного або обструктивного.
Вазопресори спричиняють вазоконстрикцію шляхом активації α₁-адренорецепторів судинної стінки, що призводить до підвищення середнього артеріального тиску та відновлення перфузії життєво важливих органів. Інотропні препарати, діючи переважно через стимуляцію β₁-адренорецепторів, підсилюють скоротливу здатність міокарда та збільшують серцевий викид, що особливо важливо при кардіогенному шоці.
Частина препаратів поєднує вазопресорні та інотропні властивості, діючи на декілька типів рецепторів. Прикладом є адреналін та дофамін, ефекти яких змінюються залежно від дози: так, дофамін у низьких дозах (1–2 мкг/кг/хв) викликає вазодилатацію, тоді як у високих (>10 мкг/кг/хв) переважає вазоконстрикторна дія. Прикладом є адреналін та дофамін, ефекти яких змінюються залежно від дози: так, дофамін у низьких дозах (1–2 мкг/кг/хв) викликає вазодилатацію, тоді як у високих (>10 мкг/ кг/хв) переважає вазоконстрикторна дія (De Backer et al., 2010)83. Окремі засоби діють поза межами адренергічних механізмів: мілринон, інгібітор фосфодіестерази-3, підвищує рівень цАМФ, сприяючи позитивному інотропному ефекту та вазодилатації; додатково ангіотензин II (поза межами цього огляду) зумовлює вазоконстрикцію через ренін-ангіотензин-альдостеронову систему (РААС) (Annane et al., 2007)84.
83 De Backer, D., et al. (2010). Pulse pressure variations to predict fluid responsiveness: Influence of tidal volume. Intensive Care Medicine, 36(4), 627-632. https://doi.org/10.1007/s00134-009-1735-6
84 Annane, D., et al. (2007). Predicting fluid responsiveness in ICU patients: A critical analysis of the evidence. Chest, 132(6), 2007-2014. https://doi.org/10.1378/chest.07-1020
Основні принципи застосування вазоактивних та інотропних препаратів:
- Один препарат — кілька ефектів. Наприклад, добутамін підвищує серцевий викид через β₁-стимуляцію, але одночасно викликає вазодилатацію через β₂-ефект, що може знижувати середній артеріальний тиск, проте покращує органну перфузію.
- Дозозалежний ефект. Ефекти змінюються залежно від дози: у адреналіну при низьких дозах переважають β-ефекти, тоді як при високих — α-ефекти.
- Прямі та рефлекторні дії. Прямі ефекти (наприклад, тахікардія внаслідок β₁-стимуляції норадреналіном) можуть нівелюватися рефлекторними реакціями (наприклад, брадикардія через активацію барорецепторів у відповідь на підвищення середнього артеріального тиску).
Показанням до застосування вазоактивних та інотропних препаратів є середній артеріальний тиск <60 мм рт. ст. або зниження систолічного артеріального тиску більше ніж на 30 мм рт. ст. від базового рівня у поєднанні з ознаками гіпоперфузії органів (лактат >2 ммоль/л, діурез <0,5 мл/кг/год)85.
Призначення цих препаратів повинно здійснюватися лише після максимально можливої корекції гіповолемії, оскільки ефективність вазопресорів є вищою при адекватному переднавантаженні. Застосування вазопресорів при геморагічному шоці залишається дискусійним питанням, однак у ситуаціях транспортування допускається використання їх для тимчасової підтримки перфузії до проведення остаточної інфузійно-трансфузійної терапії.
ОГЛЯД СЕРЦЕВО-СУДИННОЇ СИСТЕМИ ТА ШОКУ
Серцево-судинна система складається з трьох ключових компонентів: серця (насос), судин (судинне русло) та об’єму циркулюючої крові (ОЦК). Їхня узгоджена робота забезпечує адекватну доставку кисню та поживних речовин до органів і тканин.
Хвилинний об’єм кровообігу (ХОК = ЧСС × УО) у поєднанні із системним судинним опором (ССО) визначає середній артеріальний тиск (САТ ≈ ХОК × ССО), який є провідним показником органної перфузії.
У стані шоку відбувається порушення одного або кількох із цих компонентів:
- Кардіогенний шок — зниження ХОК внаслідок зменшення скоротливої здатності міокарда (зниження УО).
- Дистрибутивний шок (наприклад, септичний) — зниження судинного опору внаслідок системної вазодилатації.
- Гіповолемічний шок — зменшення переднавантаження (зниження УО) через втрату ОЦК.
- Обструктивний шок (наприклад, тромбоемболія легеневої артерії, тампонада серця) — зниження ХОК внаслідок механічної перешкоди кровотоку або різкого підвищення післянавантаження.
Для корекції зазначених порушень застосовуються вазоактивні лікарські засоби:
- нотропи — підвищують скоротливість міокарда та збільшують ХОК.
- Вазопресори — підвищують ССО і САТ, відновлюючи органну перфузію.
- Вазодилататори — знижують післянавантаження та покращують насосну функцію серця.
- Комбіновані препарати — поєднують інотропний та вазопресорний ефекти.
85 Rhodes, A., et al. (2017). Surviving Sepsis Campaign: International guidelines for management of sepsis and septic shock: 2016. *Critical Care Medicine*, 45(3), 486-552. https://doi.org/10.1097/CCM.0000000000002255
Цільовим орієнтиром терапії є досягнення та підтримання САТ ≥65 мм рт. ст. у більшості пацієнтів, а також відновлення адекватного ХОК для забезпечення перфузії життєво важливих органів.
Застосування вазоактивних препаратів вимагає зваженого підходу, оскільки вони можуть одночасно впливати на переднавантаження, післянавантаження, потребу міокарда в кисні та регіональний кровотік. Це обґрунтовує необхідність постійного моніторингу та індивідуалізації терапії залежно від клінічного стану пацієнта.
ВАЗОАКТИВНІ ПРЕПАРАТИ: МЕХАНІЗМИ, ДОЗУВАННЯ, ВВЕДЕННЯ ТА КЛІНІЧНА ДІЯ
| НОРАДРЕНАЛІН (НОРЕПІНЕФРИН) |
| на α₁-адренорецептори, що зумовлює вазоконстрикцію, підвищення системного судинного опору (ССО) та, відповідно, середнього артеріального тиску (САТ).
Препарат також чинить помірний β₁-агоністичний ефект, що забезпечує слабку інотропну дію: підвищує скоротливість міокарда, частоту серцевих скорочень (ЧСС) та хвилинний об'єм кровообігу (ХОК). При дистрибутивному шоці (наприклад, септичному), коли вазодилатація призводить до зниження ССО та САТ, норадреналін є засобом вибору, оскільки відновлює перфузійний тиск та кровопостачання життєво важливих органів (мозок, нирки), протидіючи патологічній вазодилатації. Разом із тим надмірна вазоконстрикція може спричиняти: - збільшення післянавантаження,
- підвищення потреби міокарда в кисні,
- зниження ХОК у пацієнтів із низьким серцевим резервом (наприклад, при кардіогенному шоці).
Крім того, при високих дозах норадреналін може зменшувати вісцеральний та периферичний кровотік, створюючи ризик ішемічних ускладнень у цих ділянках (De Backer та співавт., 2010). |
| Дозування та введення |
| Доза | 0,05–0,5 мкг/кг/хв внутрішньовенно крапельно (наприклад, 3,5–35 мкг/хв для пацієнта масою 70 кг). |
| Титрування | Коригувати кожні 5–10 хвилин для досягнення САТ ≥65 мм рт.ст. (або вищого у пацієнтів із хронічною гіпертензією, напр., 80 мм рт.ст.) (Hannah-Jones, 2015). |
| Введення | Використовувати центральний венозний катетер для запобігання некрозу тканин у разі екстравазації; за його відсутності — катетер великого діаметра (наприклад, 18G) із ретельним моніторингом щодо екстравазації. Розводити у 5% розчині глюкози або фізіологічному розчині (наприклад, 4 мг на 250 мл, що дає 16 мкг/мл) та вводити за допомогою шприцевого насоса для точної доставки. |
| Додаткові рекомендації |
- Під час введення норадреналіну необхідно здійснювати постійний клінічний моніторинг з метою своєчасного виявлення ознак надмірної вазоконстрикції. До таких ознак належать: холодні кінцівки, мармуровість шкіри, підвищення рівня лактату понад 2 ммоль/л, що свідчить про зниження перфузії периферичних тканин.
- У разі тривалих транспортувань, якщо доза норадреналіну перевищує 0,3–0,5 мкг/кг/хв, доцільно розглянути додавання другого препарату (адреналіну або вазопресину), оскільки застосування високих доз підвищує ризик розвитку аритмій та ішемічних ускладнень (De Backer та співавт., 2010).
- Перед початком введення норадреналіну необхідно забезпечити адекватне переднавантаження, що підтверджується оцінкою стану гідратації відповідно до СОП «Оцінка гідратації». Це зумовлено тим, що вазоконстрикторний ефект препарату без належного переднавантаження може призвести до подальшого зниження серцевого викиду та поглиблення гіпоперфузії.
|
| АДРЕНАЛІН (ЕПІНЕФРИН) |
| Адреналін є катехоламіном широкого спектра дії з агоністичною активністю щодо α₁-, β₁- та β₂-адренорецепторів, завдяки чому він поєднує властивості вазопресора та інотропа.
У низьких дозах (0,01–0,1 мкг/кг/хв) переважає β-ефект, що зумовлює: підвищення хвилинного об'єму кровообігу (ХОК) за рахунок збільшення скоротливості міокарда (β₁-ефект), вазодилатацію у певних судинних басейнах (β₂-ефект, зокрема у скелетних м'язах), що може призводити до зниження системного судинного опору (ССО).
У вищих дозах (>0,1 мкг/кг/хв) переважає α₁-ефект, який зумовлює вазоконстрикцію, підвищення ССО та середнього артеріального тиску (САТ), при цьому зберігається позитивний інотропний вплив β₁-адреностимуляції.
Адреналін застосовується у таких випадках: рефрактерний шок (наприклад, септичний шок, який не коригується норадреналіном), зупинка серця, оскільки препарат підвищує коронарну перфузію та серцевий викид.
Разом із тим слід враховувати ризики: β₁-ефекти збільшують потребу міокарда в кисні, що може спричиняти ішемію у пацієнтів із ішемічною хворобою серця, стимуляція β₁ може викликати тахіаритмії (наприклад, шлуночкова тахікардія), стимуляція гліколізу під дією адреналіну здатна підвищувати рівень лактату, що ускладнює його використання як маркера адекватності перфузії (Annane та ін., 2007). |
| Дозування та введення |
| Доза | Рекомендована доза становить 0,01–0,3 мкг/кг/хв внутрішньовенно у вигляді безперервної інфузії (для пацієнта з масою тіла 70 кг — приблизно 0,7–2 мкг/хв). |
| Титрування | Швидкість інфузії слід коригувати кожні 5–10 хвилин з метою досягнення середнього артеріального тиску (САТ) ≥65 мм рт. ст. та покращення серцевого викиду. Ефективність терапії оцінюється за клінічними показниками (діурез, психічний статус, рівень свідомості). |
| Введення | Адреналін необхідно вводити через центральний венозний катетер, що мінімізує ризик екстравазації та місцевих ускладнень. У разі відсутності центрального доступу допускається введення через периферичну вену лише у вигляді розведеного розчину. |
| Додаткові рекомендації |
- Адреналін слід застосовувати з обережністю у пацієнтів із серцево-судинними коморбідними станами, оскільки β₁-адренергічні ефекти препарату можуть спричиняти ішемію міокарда або виникнення аритмій. Рекомендовано, за наявності можливості, здійснювати постійний моніторинг ЕКГ під час інфузії.
- Необхідно враховувати ризик розвитку гіперглікемії, яка виникає внаслідок β₂-опосередкованого глікогенолізу. За можливості слід контролювати рівень глюкози в крові у процесі терапії.
|
| Дозування та введення |
| Вазопресин є синтетичним аналогом аргінін-вазопресину (AVP), належить до некатехоламінових вазопресорів. Основний механізм дії пов'язаний зі стимуляцією V1-рецепторів, що зумовлює потужну вазоконстрикцію, підвищення системного судинного опору (ССО) та середнього артеріального тиску (САТ).
Препарат має особливе значення при рефрактерному септичному шоці, де використовується як доповнення до катехоламінів (зокрема, норадреналіну) для відновлення судинного тонусу при вазоплегії та зменшення потреби в катехоламінах.
На відміну від катехоламінових препаратів, вазопресин має мінімальний прямий вплив на хвилинний об'єм кровообігу (ХОК) та частоту серцевих скорочень (ЧСС), що робить його корисним у пацієнтів з тахіаритміями або токсичними ефектами від катехоламінів.
Водночас надмірна вазоконстриктивна дія може спричиняти погіршення вісцеральної та периферичної перфузії, що підвищує ризик ішемії при використанні високих доз або тривалій терапії.
Вазопресин зазвичай розглядається як препарат другої лінії у випадках, коли САТ залишається <65 мм рт. ст. попри адекватну інфузійну терапію та застосування норадреналіну (Russell та співавт., 2019). |
| Спосіб застосування та дози |
| Доза | Типова початкова доза становить 0,03 ОД/хв, робочий діапазон — 0,01–0,05 ОД/хв внутрішньовенно. Дозування визначається в одиницях на хвилину (ОД/хв) і не коригується залежно від маси тіла пацієнта. |
| Титрування | Швидкість введення слід коригувати кожні 10–15 хвилин відповідно до реакції середнього артеріального тиску (САТ), з цільовим показником >65 мм рт. ст. Перевищення дози 0,05 ОД/хв необхідно уникати через підвищений ризик ішемії. |
| Введення | Препарат розводиться у 0,9% розчині натрію хлориду або 5% розчині глюкози (наприклад, 20 ОД у 100 мл, що відповідає концентрації 0,2 ОД/мл) та вводиться виключно через центральний венозний катетер із використанням шприцевого насоса. |
| Додаткові рекомендації |
- Слідкувати за ознаками зниження перфузії органів (наприклад, холодні кінцівки, підвищений рівень лактату) через інтенсивну вазоконстрикцію; припинити введення при появі ознак ішемії.
- Застосовувати у комбінації з норадреналіном, а не як монотерапію, оскільки вазопресин не компенсує знижену серцеву продукцію; оцінити об'ємну забезпеченість пацієнта, щоб уникнути погіршення гіповолемії.
- Під час критичних транспортних транспортувань перевірити стабільність інфузії, оскільки короткий період напіввиведення вазопресину потребує безперервного введення для підтримки ефекту.
|
| ДОБУТАМІН |
| Добутамін — це синтетичний катехоламін з переважно бета-1 та бета-2 адренергічними ефектами, що робить його чистим інотропом із помірними вазодилатуючими властивостями. Він підвищує серцевий викид за рахунок посилення скоротливості міокарда (бета-1) та зниження системного судинного опору (бета-2), що зменшує післянавантаження і покращує ударний об'єм. Добутамін є препаратом вибору при кардіогенному шоці, коли низький серцевий викид через знижену скоротливість (наприклад, після інфаркту міокарда) призводить до недостатньої перфузії органів. Підвищуючи серцевий викид, добутамін покращує доставку кисню до тканин, часто знижує рівень лактату та збільшує діурез.
Однак вазодилатація, опосередкована бета-2 рецепторами, може знижувати САТ у пацієнтів із низьким системним судинним опором (наприклад, при сепсисі), тому потрібна комбінація з вазопресором, таким як норадреналін. Крім того, добутамін збільшує потребу міокарда в кисні, що створює ризик ішемії у пацієнтів із коронарною хворобою, а також може спричинити тахіаритмії при вищих дозах (Overgaard & Dzavik, 2008). |
| Дозування та введення |
| Доза | Рекомендована доза становить 2,5–20 мкг/кг/хв внутрішньовенно у вигляді краплинної інфузії (для пацієнта масою 70 кг — приблизно 175–1400 мкг/хв). |
| Титрування | Швидкість інфузії слід коригувати кожні 5–10 хвилин, орієнтуючись на показники серцевого викиду та адекватності перфузії: діурез >0,5 мл/кг/год, рівень лактату <2 ммоль/л, клінічні ознаки покращення мікроциркуляції. |
| Введення | Добутамін вводиться через центральний венозний катетер або периферичний катетер великого діаметра. Розчин готується шляхом розведення у 5% глюкозі або 0,9% розчині натрію хлориду (наприклад, 500 мг у 250 мл, що відповідає концентрації 2000 мкг/мл). Введення здійснюється за допомогою шприцевого насоса з контролем швидкості інфузії. |
| Додаткові рекомендації |
- Необхідно контролювати рівень середнього артеріального тиску (САТ), оскільки вазодилатація, опосередкована β₂-адренергічними рецепторами, може призводити до розвитку гіпотензії. У випадках, коли САТ знижується нижче 65 мм рт. ст., слід додати норадреналін для підтримання адекватного тиску перфузії.
- Добутамін необхідно застосовувати з обережністю у пацієнтів з анамнезом аритмій, оскільки препарат може спричиняти тахікардію або шлуночкову екстрасистолію. Якщо частота серцевих скорочень (ЧСС) перевищує 120 уд./хв, доцільно розглянути зниження дози.
- При тривалих транспортуваннях оцінка ефективності терапії повинна проводитися за клінічними ознаками, зокрема за наявністю теплих кінцівок, покращенням психічного стану та діурезу. Це зумовлено тим, що методи розширеного моніторингу серцевого викиду (катетер легеневої артерії, ехокардіографія) у більшості випадків є недоступними під час транспортування.
|
| МІЛРИНОН |
| Мілринон належить до інгібіторів фосфодіестерази-3 (ФДЕ-3). Механізм дії полягає у підвищенні рівня цАМФ у кардіоміоцитах і клітинах судинної гладкої мускулатури. Це забезпечує подвійний ефект: - інотропний ефект — посилює скоротливість міокарда за рахунок збільшення надходження кальцію в кардіоміоцити, що призводить до зростання хвилинного об'єму кровообігу (ХОК);
- Вазодилататорний, лузитропний ефект — розслабляє судинну гладку мускулатуру, знижує системний судинний опір (ССО) та післянавантаження.
- Мілринон застосовується переважно при кардіогенному шоці з підвищеним ССО (наприклад, після кардіохірургічних втручань, при декомпенсованій серцевій недостатності), оскільки підвищує серцевий викид і водночас зменшує навантаження на серце.
Застереження: - Вазодилататорна дія мілринону може знижувати середній артеріальний тиск (САТ), створюючи ризик гіпотензії у пацієнтів із низьким ССО (наприклад, при сепсисі). У таких випадках необхідне одночасне застосування вазопресорів.
- Препарат покращує діастолічне розслаблення міокарда, що є корисним у пацієнтів із серцевою недостатністю, однак підвищує потребу міокарда в кисні.
- Може спричиняти аритмії, особливо у хворих з ішемічною хворобою серця.
(Cuffe., 2002). |
| Дозування та введення |
| Доза | Рекомендований діапазон становить 0,2–0,75 мкг/кг/хв внутрішньовенно у вигляді інфузії (для пацієнта масою 70 кг — орієнтовно 14–52 мкг/хв). Навантажувальну дозу, описану в деяких джерелах (50 мкг/кг протягом 10 хвилин), під час транспортування застосовувати не рекомендовано через ризик розвитку гіпотензії. |
| Титрування | Швидкість інфузії коригується кожні 10–15 хвилин з орієнтацією на покращення серцевого викиду та ознак адекватної тканинної перфузії (клінічні показники, діурез, рівень лактату). |
| Введення | Препарат вводиться через центральний венозний катетер або периферичний катетер великого діаметра. Розчин готується шляхом розведення у 0,9% розчині натрію хлориду або 5% розчині глюкози (наприклад, 20 мг у 100 мл, що відповідає концентрації 200 mкг/мл). Інфузія проводиться із використанням шприцевого інфузомата з контролем швидкості введення. |
| Додаткові рекомендації |
-
Під час введення мілринону необхідно здійснювати постійний моніторинг середнього артеріального тиску (САТ). Через вазодилатаційний ефект препарат може спричиняти артеріальну гіпотензію; у разі зниження САТ нижче 65 мм рт. ст. доцільно додати норадреналін для підтримки перфузійного тиску. -
Мілринон слід застосовувати з обережністю у пацієнтів із порушенням функції нирок, оскільки препарат виводиться нирками та може накопичуватися, підвищуючи ризик аритмій. При кліренсі креатиніну <30 мл/хв рекомендовано зменшити дозу на 50 %. -
Під час транспортування необхідно враховувати, що мілринон має тривалий період напіввиведення (2–3 години), тому клінічний ефект зберігається навіть після припинення інфузії. Це потребує ретельного моніторингу стану пацієнта та обов'язкового інформування приймаючої медичної бригади щодо застосування мілринону та можливих ускладнень. |
ВПЛИВ НА СИСТЕМУ КРОВООБІГУ: ЦІЛІСНИЙ ПІДХІД
Судинозвужувальні та інотропні препарати чинять комплексний вплив на систему кровообігу, змінюючи переднавантаження, післянавантаження, скоротливість міокарда та регіональний кровотік.
Норадреналін головним чином підвищує системний судинний опір (ССО), збільшує середній артеріальний тиск (САТ) та покращує перфузійний тиск до життєво важливих органів (мозок, нирки). Водночас надмірна вазоконстрикція може призвести до зниження хвилинного об’єму кровообігу (ХОК) через зростання післянавантаження та централізація кровообігу з ішемією органів черевної порожнини. Це особливо важливо враховувати при тривалих транспортуваннях (De Backer та ін., 2010).
Адреналін і дофамін мають змішану α- і β-адренергічну дію, підвищують як ССО, так і ХОК. Проте стимуляція β-рецепторів підвищує потребу міокарда в кисні, що може спровокувати ішемію або аритмії, особливо у пацієнтів з ішемічною хворобою серця (Annane та ін., 2007).
Добутамін і мілринон як інотропні засоби підвищують ХОК завдяки посиленню скоротливості, але їхні вазодилатуючі властивості можуть знижувати САТ. Це створює ризик церебральної або ниркової гіпоперфузії, тому необхідний ретельний гемодинамічний моніторинг (Overgaard & Dzavik, 2008).
У контексті транспортування пацієнтів зі змішаними станами шоку (наприклад, септичний шок із кардіогенним компонентом) доцільним є комбіноване застосування препаратів. Зокрема, норадреналін може забезпечувати вазопресорну підтримку, а добутамін — інотропний ефект. Такий підхід дозволяє збалансувати ССО та ХОК для досягнення САТ ≥65 мм рт. ст. і забезпечення адекватної перфузії тканин (лактат <2 ммоль/л, діурез >0,5 мл/кг/год).
Усі рішення щодо застосування вазоактивних препаратів повинні ґрунтуватися на індивідуальній оцінці стану пацієнта з урахуванням супутньої патології, стану гідратації в організмі та супутньої фармакотерапії (зокрема β-адреноблокаторів, які широко використовуються при артеріальній гіпертензії та різних формах серцево-судинних захворювань).
ТАБЛИЦЯ ПОРІВНЯННЯ ВАЗОАКТИВНИХ І ІНОТРОПНИХ ПРЕПАРАТІВ ТА ЇХ ПРАКТИЧНЕ ЗАСТОСУВАННЯ
| Препарат | Інотропний ефект | Вплив на судинний опір | Вплив на серцевий викид | Вплив на САТ | Основні показання | Зауваження щодо безпеки |
| Добутамін | ↑↑ (β1) | ↓ (β2) | ↑↑ | ↔/↓ | Кардіогенний шок, стани зі зниженим серцевим викидом | Ризик гіпотензії (вазодилатація); тахіаритмії; уникати при активній ішемії |
| Мілринон | ↑ (інгібування ФДЕ-3) | ↓ (вазодилатація) | ↑ | ↓ | Кардіогенний шок з високим системним периферичним опором (наприклад, серцева недостатність) | Гіпотензія; тривалий період напіввиведення (2–3 год); корекція дози при порушенні функції нирок |
| Вазопресин | ↔ | ↑↑ (V1) | ↔ | ↑↑ | Ад’ювант при септичному шоку (зменшення потреби у норадреналіні) | Ризик коронарної ішемії; затримка рідини через V2-опосередкований механізм |
| Норадреналін | ↑ (β1, помірно) | ↑↑ (α1) | ↔/↑ | ↑↑ | Препарат вибору при дистрибутивному шоці (наприклад, септичному) | Ризик периферичної ішемії; тахіаритмії при високих дозах (>0,5 мкг/кг/хв) |
| Адреналін | ↑↑ (β1) | ↑ (α1, дозозалежно) / ↓ (β2, при низьких дозах) | ↑↑ | ↑ при високій дозі / ↔ (при низькій дозі) | Рефрактерний шок, зупинка серця, анафілаксія | Тахіаритмії; підвищене споживання кисню міокардом; гіперглікемія |
| Допамін | ↑ (β1, при середній дозі) | ↔/↑ (α1, при високій дозі) / ↓ (D1/D2, при низькій дозі) | ↑ (середня доза) | ↔/↑ | Альтернатива при змішаному шоці (за відсутності норадреналіну) | Високий ризик аритмій; непередбачувані ефекти на судинний опір; не рекомендований як препарат першої лінії при септичному шоці |
ПРИГОТУВАННЯ ВАЗОПРЕСОРІВ ТА ІНОТРОПНИХ ПРЕПАРАТІВ: СОП C8 (див. Додаток 20)

Ця стандартна операційна процедура (СОП) визначає уніфікований порядок приготування вазопресорів та інотропних препаратів (норадреналін, адреналін, добутамін, мілринон) для використання під час транспортування пацієнтів у критичному стані. Виконання наведених рекомендацій забезпечує безпечне, точне та ефективне приготування лікарських засобів, що є ключовим для ведення пацієнтів із септичним, кардіогенним або гіповолемічним шоком та підтримання гемодинамічної стабільності і органної перфузії протягом усього транспортування.
КРОК 1: ПЕРЕВІРКА ПРЕПАРАТУ

Початковим етапом приготування вазопресорів та інотропних препаратів є процедура перевірки, яка має на меті підтвердити правильність вибору лікарського засобу відповідно до клінічного стану пацієнта та призначення лікаря.
Перевірка здійснюється двома медичними працівниками незалежно один від одного та включає:
- звірку назви препарату, його концентрації та терміну придатності з призначенням лікаря та відповідною СОП (наприклад, СОП C9, що містить конкретні рекомендації щодо норадреналіну або добутаміну);
- огляд флакону на наявність ознак контамінації (зміна кольору, помутніння, наявність сторонніх часток) з метою підтвердження його цілісності;
- підтвердження маси тіла пацієнта, яка є основою для розрахунку дози у мкг/кг/хв — стандартній одиниці вимірювання для більшості вазопресорів та інотропних препаратів.
Процедура подвійної перевірки є обов’язковим заходом безпеки. За даними досліджень, її застосування дозволяє знизити кількість помилок при введенні сильнодіючих препаратів, зокрема вазопресорів, до 30 % у високоризикованих умовах (Singer та ін., 2023)86.
86 Singer, M., Deutschman, C. S., Seymour, C. W., et al. (2023). The Surviving Sepsis Campaign: International guidelines for management of sepsis and septic shock 2023. *Critical Care Medicine*, 51(11), 1432-1465. https://doi.org/10.1097/CCM.0000000000005923
КРОК 2: ВИБІР РОЗВЕДЕННЯ ТА КОНЦЕНТРАЦІЯ

Після перевірки необхідно обрати відповідне розведення та розчинник щоб забезпечити безпечне та сумісне введення препарату. Для визначення рекомендованого розведення для обраного засобу, наприклад, 20 мкг/мл або 40 мкг/мл для норадреналіну, слід звернутися до відповідної СОП (наприклад, СОП C9).
Об’єм вихідного розчину розраховується за формулою: Об’єм вихідного розчину (мл) = (Бажана кінцева концентрація × Кінцевий об’єм) ÷ Концентрація вихідного розчину. Обирається сумісний розчинник — зазвичай 5% розчин глюкози або фізіологічний розчин — для забезпечення стабільності препарату, оскільки ці розчини підтверджені доказами як сумісні з більшістю вазопресорів та інотропів (Singer et al., 2023)48.
Кінцевий об’єм, який зазвичай становить 50 мл для більшості препаратів або 20 мл для мілринону, визначається відповідно до клінічних потреб. Об’єм розчинника розраховується шляхом віднімання об’єму вихідного розчину від кінцевого об’єму. Цей етап забезпечує приготування препарату в концентрації, яка знижує ризик некрозу тканин у разі екстравазації або тяжких гемодинамічних ускладнень у разі випадкового болюсного введення — що є критично важливим під час транспортування (Tian et al., 2020)87.
Процес розведення
Процес розведення вимагає високої точності для досягнення запланованої концентрації з метою безпечного введення. Розрахований об’єм розчинника — 5% розчин глюкози або фізіологічний розчин — набирається у кінцевий шприц, після чого точний об’єм вихідного розчину набирається окремим шприцом для забезпечення точності. Вихідний розчин додається до розчинника в кінцевому шприці, після чого суміш обережно перевертається кілька разів для забезпечення рівномірності.
Готовий розчин необхідно візуально оглянути на прозорість, переконавшись у відсутності сторонніх часток або помутніння, що може свідчити про контамінацію або неправильне змішування. Якщо кінцевий об’єм не відповідає розрахунковому, процес слід повторити для досягнення точності. Такий ретельний підхід є критично важливим, оскільки навіть незначні відхилення концентрації можуть призвести до суттєвих помилок у дозуванні, що потенційно спричиняє гемодинамічну нестабільність під час транспортування (Tian et al., 2020)49.
87 Tian, D. H., Smyth, C., Keijzers, G., Macdonald, S. P., Peake, S., Udy, A., & Delaney, A. (2020). Safety of peripheral administration of vasopressor medications: A systematic review. *Critical Care Medicine*, 48(5), e423-e430. https://doi.org/10.1097/CCM.0000000000004275
КРОК 3: МАРКУВАННЯ ШПРИЦА ТА В/В КРАПЕЛЬНИЦІ

Завершальним етапом є маркування, яке забезпечує безпечне та точне введення під час транспортування. Шприц повинен бути промаркований із зазначенням назви препарату (наприклад, норадреналін) і кінцевої концентрації (наприклад, 20 мкг/мл).
Шприц приєднується до виділеної венозної лінії, яка також повинна бути промаркована написом «УВАГА — НЕ ПРОМИВАТИ», а також із зазначенням назви препарату та концентрації, щоб запобігти випадковому болюсному введенню або плутанині з іншими препаратами.
Венозна лінія має бути надійно зафіксована та перевірена на відсутність повітряних бульбашок з метою зниження ризику повітряної емболії. Дані досліджень підтверджують ефективність чіткого маркування та використання виділених венозних ліній, оскільки це знижує ризик помилок у введенні препаратів, особливо в динамічних умовах транспортування, де можуть застосовуватись кілька засобів одночасно (Tian et al., 2020)49.
Клінічні міркування
Вазопресори та інотропні препарати мають вузьке терапевтичне вікно, тому точність приготування є критично важливою для запобігання гемодинамічній нестабільності, такій як гіпотензія, гіпертензія або аритмії, що особливо небезпечно під час транспортування. Сумісність є ключовим аспектом — як дилюент слід використовувати 5% розчин глюкози або фізіологічний розчин, якщо не вказано інше, оскільки вони сумісні з більшістю препаратів. Лужні розчини, такі як розчин Рінгера з лактатом, не слід використовувати разом із катехоламінами через ризик їх розпаду (Singer et al., 2023)48. Для світлочутливих препаратів, наприклад адреналіну, необхідно забезпечити захист від втрати активності— шляхом використання шприців із затемненого (бурштинового) пластику або обгортання розчину фольгою. Ці заходи гарантують стабільність і ефективність препарату протягом усього транспортування, підтримуючи стабільний стан пацієнта до моменту прибуття в приймаючий ЗОЗ.
ВАЗОПРЕСОРИ ТА ІНОТРОПНІ ПРЕПАРАТИ: СОП C9 (див. Додаток 21)

Ця СОП встановлює структурований підхід до приготування, введення та титрування вазопресорів та інотропних препаратів — норадреналіну, адреналіну, добутаміну та мілринону — під час транспортування пацієнтів у критичному стані. Ці засоби є критично важливими для ведення пацієнтів із септичним, кардіогенним або гіповолемічним шоком, забезпечуючи гемодинамічну стабільність і перфузію органів протягом усього транспортування. У цьому документі наголошується на безпеці, точності та дозуванні на основі доказових даних з метою оптимізації клінічних результатів для пацієнтів.
НОРАДРЕНАЛІН
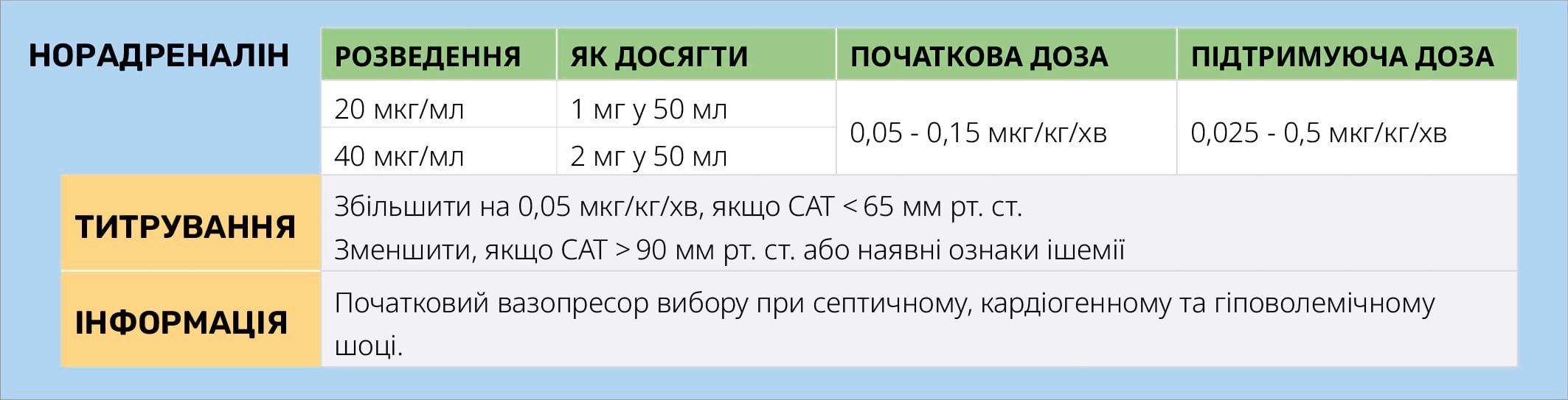
| ПОКАЗАННЯ | Норадреналін є вазопресором першої лінії при септичному, кардіогенному та гіповолемічному шоці, ефективно відновлює середній артеріальний тиск (САТ) і підтримує перфузію органів під час транспортування пацієнтів у критичному стані (Singer et al., 2023)⁴⁸. |
| ПРИГОТУВАННЯ | Варіанти розведення для транспортування: -
20 мкг/мл: змішати 1 мг норадреналіну з 49 мл 5% розчину глюкози або фізіологічного розчину в шприці об’ємом 50 мл. -
40 мкг/мл: змішати 2 мг норадреналіну з 48 мл 5% розчину глюкози або фізіологічного розчину в шприці об’ємом 50 мл (введення виключно через центральну лінію). |
| ДОЗУВАННЯ | Початкова доза: починати з 0,05 мкг/кг/хв (наприклад, 3,5 мкг/хв для пацієнта масою 70 кг) для досягнення САТ ≥65 мм рт. ст. при мінімізації побічних ефектів (Hamzaoui et al., 2024)⁸⁸. Підтримуючий діапазон: а: коригувати в межах 0,025–0,5 мкг/кг/хв, титруючи для підтримання САТ ≥65 мм рт. ст. Дози понад 0,5 мкг/кг/хв слід уникати, якщо немає абсолютних показань, через підвищений ризик ішемії та аритмій (Singer et al., 2023)⁴⁸. |
| ТИТРУВАННЯ | -
Збільшувати дозу на 0,05 мкг/кг/хв кожні 5 хвилин, якщо САТ <65 мм рт. ст. -
Зменшувати дозу на 0,05 мкг/кг/хв, якщо САТ >90 мм рт. ст. або з’являються ознаки ішемії (наприклад, ціаноз пальців, зміни на ЕКГ). |
| ДОДАТКОВІ РЕКОМЕНДАЦІЇ | Ефективність норадреналіну у підвищенні САТ і зниженні летальності при септичному шоку робить його препаратом вибору для початкової вазопресорної підтримки. Під час транспортування швидкий початок дії забезпечує своєчасну гемодинамічну підтримку, однак необхідний постійний моніторинг для запобігання надмірній вазоконстрикції. |
АДРЕНАЛІН

| ПОКАЗАННЯ | Адреналін застосовується як додатковий засіб до норадреналіну при рефрактерному септичному шоці, забезпечуючи додаткову вазопресорну та інотропну підтримку. Може також використовуватися у випадках кардіогенного шоку, коли потрібний інотропний ефект у поєднанні з норадреналіном (Annane та ін., 2007)⁸⁹. |
| ПРИГОТУВАННЯ | Варіанти розведення: -
20 мкг/мл: змішати 1 мг адреналіну з 49 мл 5% розчину глюкози або фізіологічного розчину в шприці об’ємом 50 мл. -
40 мкг/мл: змішати 2 мг адреналіну з 48 мл 5% розчину глюкози або фізіологічного розчину в шприці об’ємом 50 мл (рекомендовано введення через центральну лінію). |
| ДОЗУВАННЯ | Початкова доза: починати з 0,02 мкг/кг/хв (наприклад, 1,4 мкг/хв для пацієнта масою 70 кг) для оптимального балансу між ефективністю та безпекою (Brown et al., 2023)⁹⁰. Підтримуюча доза: коригувати в межах 0,01–0,3 мкг/кг/хв, при цьому в більшості випадків бажано не перевищувати 0,1 мкг/кг/хв для мінімізації побічних ефектів, таких як аритмії та гіперглікемія (Singer et al., 2023)⁴⁸. |
| ТИТРУВАННЯ | -
Збільшувати дозу на 0,01–0,05 мкг/кг/хв кожні 5 хвилин, якщо САТ <65 мм рт. ст. або перфузія залишається недостатньою. -
У разі інотропної потреби (наприклад, при кардіогенному шоці) низькі дози часто дають додатковий ефект у комбінації з норадреналіном. У деяких випадках можуть бути потрібні вищі дози в межах рекомендованого діапазону, однак при цьому переважатиме альфа-адренергічний ефект. Необхідно ретельно моніторити стан пацієнта на предмет побічних ефектів та, за можливості, розглянути додавання вазопресину. |
| ДОДАТКОВІ РЕКОМЕНДАЦІЇ | Подвійний механізм дії адреналіну забезпечує його ефективність при рефрактерному шоці, однак його застосування потребує пильного контролю щодо розвитку тахікардії (ЧСС >120/хв) та гіперглікемії, особливо під час транспортування, коли безперервний моніторинг може бути ускладненим (Brown et al., 2023)⁵¹. |
ДОБУТАМІН

| ПОКАЗАННЯ | Добутамін є препаратом вибору на початковому етапі при кардіогенному шоці зі зниженим серцевим викидом за умови підтриманого середнього артеріального тиску (САТ ≥65 мм рт. ст.). Також застосовується як додатковий засіб до норадреналіну при септичному шоці з персистуючою гіпоперфузією (Levy та ін., 2023). |
| ПРИГОТУВАННЯ | Розведення: 2 мг/мл (2000 мкг/мл): 100 мг добутаміну розвести у 42 мл 5 % розчину глюкози або 0,9 % розчину натрію хлориду у шприці об’ємом 50 мл. |
| ДОЗУВАННЯ | Початкова доза: починати з 2,5 мкг/кг/хв (наприклад, 175 мкг/хв для пацієнта масою 70 кг) для покращення серцевого викиду при мінімізації ризику гіпотензії або тахікардії (Levy et al., 2023)⁵². Підтримуючий діапазон: коригувати в межах 2,5–10 мкг/кг/хв, при тяжких станах допускається до 20 мкг/кг/хв за умови ретельного моніторингу побічних ефектів (Singer et al., 2023)⁴⁸. |
| ТИТРУВАННЯ | -
У разі зниження САТ <65 мм рт. ст. через вазодилатуючу дію добутаміну необхідно додати норадреналін. -
Добутамін покращує скоротливість міокарда, що робить його оптимальним препаратом при кардіогенному шоці під час транспортування. -
Короткий період напіввиведення забезпечує можливість швидкого титрування дози. -
Необхідний постійний моніторинг ЧСС та АТ через ризик тахікардії та артеріальної гіпотензії. -
Перед початком терапії слід виключити або скоригувати відносну гіповолемію (особливо при інфаркті міокарда нижньої стінки). |
| ДОДАТКОВІ РЕКОМЕНДАЦІЇ | Добутамін покращує скоротливу здатність міокарда, що робить його оптимальним препаратом при кардіогенному шоці під час транспортування пацієнтів. Завдяки короткому періоду напіввиведення існує можливість швидкого титрування дози залежно від клінічної відповіді. Обов’язковим є постійний моніторинг для своєчасного виявлення можливих ускладнень, зокрема тахікардії та артеріальної гіпотензії (Levy та ін., 2023). Перед початком терапії необхідно уникати стану відносної гіповолемії, особливо у пацієнтів з інфарктом нижньої стінки міокарда, оскільки це може погіршити перебіг шоку та знизити ефективність інотропної підтримки. Застосування вазоактивних препаратів, у тому числі добутаміну, має відбуватися лише у складі комплексного лікувального підходу, з урахуванням потенційних ризиків та клінічних переваг для кожного конкретного пацієнта. |
МІЛРИНОН
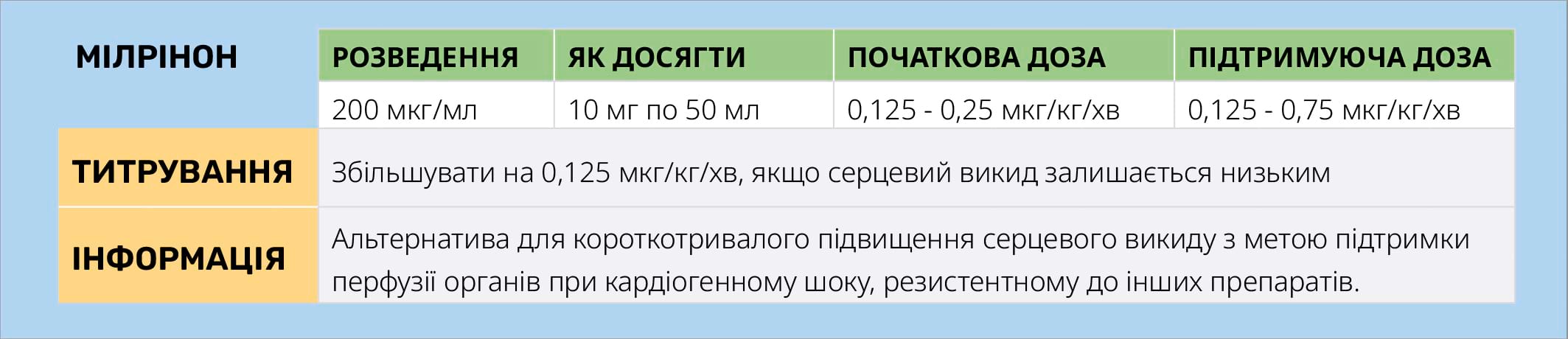
| ПОКАЗАННЯ | Мілринон є альтернативою при кардіогенному шоці, резистентному до добутаміну, особливо у пацієнтів з високим системним периферичним опором (СПО). Він сприяє підвищенню серцевого викиду та зменшенню післянавантаження (Mebazaa et al., 2023)⁹¹. |
| ПРИГОТУВАННЯ | Розведення: 200 мкг/мл: змішати 10 мг мілринону з 40 мл 5% розчину глюкози або фізіологічного розчину в шприці об’ємом 50 мл. |
| ДОЗУВАННЯ | Початкова доза: починати з 0,375 мкг/кг/хв (наприклад, 26,25 мкг/хв для пацієнта масою 70 кг) для досягнення терапевтичного ефекту(Mebazaa et al., 2023). Підтримуючий діапазон: регулювати в межах 0,25–0,75 мкг/кг/хв. У разі зниження швидкості клубочкової фільтрації (ШКФ) <30 мл/хв дозу слід зменшити на 50% через ризик кумуляції (Mebazaa et al., 2023)⁵². |
| ТИТРУВАННЯ | -
Збільшувати дозу на 0,125 мкг/кг/хв кожні 15 хвилин, якщо серцевий викид залишається низьким. -
Моніторити стан на предмет гіпотензії, оскільки вазодилатуюча дія мілринону та його тривалий період напіввиведення (2–3 години) можуть спричинити затяжний ефект. |
| ДОДАТКОВІ РЕКОМЕНДАЦІЇ | Роль мілринону при рефрактерному кардіогенному шоці є доведеною, однак через його тривалий період напіввиведення необхідний ретельний моніторинг під час транспортування для запобігання гіпотензії та аритмій. |
ЧАСТИНА 4: ПАЦІЄНТ У СТАНІ ДЕКОМПЕНСАЦІЇ
ВСТУП
Гемодинамічна декомпенсація
Гемодинамічна декомпенсація є критичним станом, за якого серцево-судинна система не спроможна підтримувати адекватну перфузію тканин та оксигенацію, що призводить до прогресуючої дисфункції органів і, у разі відсутності своєчасного лікування, — до летального наслідку.
У контексті транспортування пацієнтів у критичному стані гемодинамічна декомпенсація становить особливу небезпеку через: динамічність перебігу, обмежені можливості моніторингу, високий ризик раптового погіршення.
Це особливо актуально в умовах обмежених ресурсів, зокрема в Україні під час триваючого збройного конфлікту, коли доступ до спеціалізованої допомоги, лікарських засобів та обладнання може бути ускладнений. За таких умов особливого значення набувають адаптивні стратегії стабілізації та безпечна передача пацієнтів до закладів, що приймають.
Гемодинамічна декомпенсація може мати різну етіологію, але її маніфестованим проявом є шок — кінцева стадія у разі несвоєчасного виявлення та лікування. Шок традиційно класифікується як: гіповолемічний, дистрибутивний (зокрема септичний), кардіогенний, обструктивний.
У всіх випадках спільними є порушення органної перфузії та недостатня доставка кисню до тканин.
Окрім класичних форм шоку, інші стани також можуть призводити до гемодинамічної нестабільності або посилювати її, зокрема: гострі аритмії (наприклад, шлуночкова тахікардія), тяжка гіпоксична дихальна недостатність (наприклад, ГРДС), метаболічні розлади (наприклад, тяжкий метаболічний ацидоз).
Такі стани часто поєднуються з іншими типами шоку та ускладнюють перебіг критичного стану.
У процесі транспортування медичні працівники повинні: своєчасно виявити основну причину гемодинамічної декомпенсації, ініціювати цілеспрямовані лікувальні заходи, здійснювати постійний моніторинг і переоцінку стану пацієнта, щоб запобігти прогресуванню шоку та мінімізувати ризик летальних ускладнень.
У цьому розділі шок розглядається як центральне поняття. Подано огляд його патофізіології, класифікації, клінічних проявів та принципів доказової терапії. Основну увагу приділено гіповолемічному, септичному та кардіогенному шоку, які є найпоширенішими під час критичних транспортувань в Україні та становлять основу для розроблення стандартних операційних процедур (СОП). Розуміння механізмів розвитку та принципів ведення пацієнтів у стані шоку дозволяє клініцистам більш ефективно працювати з хворими у стані гемодинамічної декомпенсації, індивідуальну терапію відповідно до патофізіологічних особливостей і водночас долаючи труднощі, пов’язані з умовами транспортування.
ПАТОФІЗІОЛОГІЯ ШОКУ
Серцево-судинна система забезпечує адекватну перфузію тканин завдяки збалансованій взаємодії хвилинного об’єму кровообігу (ХОК), системного судинного опору (ССО) та середнього артеріального тиску (САТ). ХОК = ЧСС × УО, де:
- ЧСС — частота серцевих скорочень,
- УО — ударний об’єм, який залежить від переднавантаження (венозне повернення), післянавантаження (ССО) та скоротливості міокарда.
САТ орієнтовно розраховується як САТ ≈ ХОК × ССО і є ключовим показником органної перфузії.
У стані шоку цей баланс порушується, внаслідок чого доставка кисню стає недостатньою для забезпечення потреб тканин. Це призводить до переходу клітин на анаеробний метаболізм, накопичення лактату та розвитку клітинного ушкодження (Singer та ін., 2023).
Гіповолемічний шок
Причина: зниження переднавантаження через втрату об’єму циркулюючої крові (ОЦК) — масивна кровотеча, тяжка дегідратація тощо.
Механізм:
- ↓ венозне повернення → ↓ УО → ↓ ХОК → ↓ САТ → порушення органної перфузії.
Компенсаторна відповідь:
- тахікардія (↑ ЧСС),
- вазоконстрикція (↑ ССО),
що тимчасово підтримує САТ. Однак за тривалого перебігу це призводить до ішемії життєво важливих органів (Holler та ін., 2022).
Клінічна особливість: у молодих пацієнтів із збереженими компенсаторними механізмами рівень САТ може залишатися у межах норми аж до настання повної гемодинамічної декомпенсації.
Септичний шок
Септичний шок є формою дистрибутивного шоку, що розвивається внаслідок системної запальної відповіді при інфекціях. Він характеризується генералізованою вазодилатацією (↓ ССО) та підвищенням капілярної проникливості. На ранніх етапах септичного шоку ХОК часто підвищений внаслідок тахікардії та зниження післянавантаження, проте САТ знижується через низький рівень ССО. У міру прогресування стану можливе приєднання дисфункції міокарда та гіповолемії (через капілярні втрати рідини), що призводить до зменшення ХОК та поглиблення тканинної гіпоперфузії.
Підвищений рівень лактату (>2 ммоль/л) є чутливим маркером тканинної гіпоксії та використовується як діагностичний критерій септичного шоку (Rhodes та ін., 2017).
Кардіогенний шок
Кардіогенний шок виникає у випадках, коли серце не виконує насосної функції, що призводить до зниження ХОК внаслідок порушення скоротливості міокарда (ішемія, гостра або хронічна серцева недостатність). Рідше причиною можуть бути тяжкі аритмії або клапанні вади.
ССО підвищується як компенсаторна реакція, проте низький ХОК спричиняє падіння САТ і недостатню перфузію органів. Підвищене переднавантаження (наприклад, при затримці рідини у пацієнтів із серцевою недостатністю) може спричиняти набряк легень, що поглиблює гіпоксемію.. Тоді Зростання після навантаження збільшує потребу міокарда в кисні та підвищує ризик розвитку ішемії, що ще більше погіршує стан пацієнта (van Diepen та ін., 2017).
Обструктивний шок
Обструктивний шок розвивається внаслідок механічного перешкоджання кровотоку, що порушує наповнення або відтік крові із серця. Типові причини: тромбоемболія легеневої артерії, тампонада серця, напружений пневмоторакс. Механізм:
- ↓ ХОК через ускладнене наповнення/відтік,
- ↑ ССО як компенсаторна реакція,
- ↓ САТ, що зумовлює системну гіпоперфузію.
Для усунення обструкції необхідне проведення специфічних втручань (тромболізис, перикардіоцентез, дренування плевральної порожнини). Проте у ході транспортування ці втручання часто є неможливими, тому акцент робиться на підтримці гемодинамічної стабільності до моменту госпіталізації (Konstantinides та ін., 2020).
КЛІНІЧНА КАРТИНА ТА ДІАГНОСТИКА ШОКУ
Клінічна картина шоку варіює залежно від типу, однак її об’єднують ознаки недостатньої перфузії тканин — ключового наслідку гемодинамічної декомпенсації. Раннє розпізнавання є критично важливим під час транспортування пацієнтів у критичному стані; затримка може призвести до незворотніх наслідків.
| Категорія | Гіповолемічний шок | Септичний шок | Кардіогенний шок | Обструктивний шок |
| Визначення | Шок, спричинений зменшенням об'єму циркулюючої крові (зниження переднавантаження), що призводить до зниження серцевого викиду (СВ) та середнього артеріального тиску (САТ). | Шок, спричинений системним запаленням (інфекція), що характеризується вазодилатацією (низький системний судинний опір) та проникністю капілярів. | Шок внаслідок неспроможності серця як насоса, що призводить до низького СВ і САТ , часто з високим системним судинним опором. | Шок, спричинений механічною обструкцією кровотоку (наприклад, тромбоемболія легеневої артерії, тампонада серця), що знижує СВ. |
| Поширені причини | Втрата крові (травма, шлунково-кишкова кровотеча) | Інфекції (наприклад, пневмонія, інфекції сечових шляхів, сепсис, викликаний бактеріями, такими як E. coli) | Ішемія міокарда | Тромбоемболія легеневої артерії |
| Зневоднення (блювання, діарея, опіки) | Імуносупресія | Серцева недостатність | Напружений пневмоторакс |
| | | Аритмії (наприклад, шлуночкова тахікардія, брадикардія) | Тампонада серця |
| Патофізіологія | ↓ Переднавантаження → ↓ Серцевий викид СВ → ↓ Середній артеріальний тиск (САТ) | ↓ Системний судинний опір (вазодилатація) → ↓ САТ | ↓ СВ через неспроможність серцевого насоса → ↓ САТ | Механічна обструкція → ↓ СВ → ↓ САТ |
| Компенсаторні механізми ↑ Системний судинний опір та тахікардія | Серцевий викид (СВ) нормальний/↑ (на початку), ↓ (пізніше через пригнічення міокарда) | Компенсаторний системний судинний опір ↑ | системний судинний опір ↑ |
| Гіпоксія тканин (↑ лактат) | Протікання капілярів → гіповолемія | ↑ Переднавантаження → набряк легень | |
| Категорія | Гіповолемічний шок | Септичний шок | Кардіогенний шок | Обструктивний шок |
| Клінічне обстеження | Ознаки життєдіяльності: САТ <65 мм рт.ст., ЧСС >100 уд/хв, вузький пульсовий тиск | Ознаки життєдіяльності: САТ <65 мм рт.ст., ЧСС >100 уд/хв, ЧД >20/хв, SpO₂ <92% | Ознаки життєдіяльності: САТ <65 мм рт.ст., ЧСС варіабельна (тахікардія/брадикардія), SpO₂ <92% | Ознаки життєдіяльності: САТ <65 мм рт.ст., ЧСС >100 уд/хв, SpO₂ <90% |
| Шкіра: Холодні, вологі кінцівки, час капілярного наповнення >2 с | Шкіра: Теплі кінцівки (на ранній стадії), холодні (на пізній), час капілярного наповнення >2 с | Шкіра: Холодні, вологі кінцівки, час капілярного наповнення >2 с | Шкіра: Холодні, вологі кінцівки, час капілярного наповнення >2 с |
| Центральний венозний тиск: Нормальний або знижений (протікання капілярів) | Центральний венозний тиск: Нормальний або знижений (протікання капілярів) | Показник: підвищений ЦВТ >8 см Н₂О (≈ >6 мм рт. ст.). | Центральний венозний тиск (ЦВТ) Напружені шийні вени |
| Легені: Чисті (без набряку) | Легені: Чисті або вологі хрипи (можливий ГРДС) | Легені: Вологі хрипи (набряк легень) | Легені: Одностороннє ослаблене дихання (пневмоторакс), приглушені серцеві тони (тампонада) |
| Неврологічний статус: Сплутаність свідомості (гіпоперфузія) | Неврологічний статус: Сплутаність свідомості | Неврологічний статус: Сплутаність свідомості | |
| Лабораторні дослідження | Лактат: >2 ммоль/л (гіпоксія тканин) | Лактат: >2 ммоль/л (Sepsis-3 критерій) | Лактат: >2 ммоль/л (гіпоксія тканин) | Лактат: >2 ммоль/л (гіпоксія тканин) |
| Гематокрит: ↑ (гемоконцентрація при зневодненні), ↓ (втрата крові) | Лейкоцити: ↑ або ↓ (інфекція) | Тропонін: ↑ (інфаркт міокарда) | D-димери: ↑ (тромбоемболія легеневої артерії) |
| Креатинін: ↑ (гіпоперфузія нирок) | CRP/прокальцитонін: ↑ (запалення) | BNP/NT-proBNP: ↑ (серцева недостатність) | Газовий склад артеріальної крові (ABG) Патологічні зміни: Гіпоксія (↓PaO₂, SpO₂ <90 %), Респіраторний алкалоз (↓PaCO₂, ↑pH). Тромбоемболія легеневої артерії (ТЕЛА). |
| Електроліти: ↑ калій (при ацидозі) | Креатинін: ↑ (гіпоперфузія нирок) | Креатинін: ↑ (гіпоперфузія нирок) | |
| Категорія | Гіповолемічний шок | Септичний шок | Кардіогенний шок | Обструктивний шок |
| Ключові клінічні ознаки | POCUS: колапс нижньої порожнистої вени (>50%) → гіповолемія | POCUS: нормальна НПВ (на ранньому етапі), В-лінії (ГРДС), ↓ ФВ (пізніше) | POCUS: ↓ фракція викиду (<40%), В-лінії (набряк легень), дилатація камер | POCUS: дилатація правого шлуночка (легенева емболія), перикардіальна рідина (тампонада) |
| PPV: >12–15% (на ШВЛ) → чутливість до інфузійної терапії | Ознаки інфекції: | ЕКГ: підйом сегмента ST (ІМ), аритмії (наприклад, шлуночкова тахікардія) | Клінічні ознаки: |
| Ознаки кровотечі: видима кровотеча (травма, кровотеча з ШКТ) | Кліренс лактату: <10%/год → поганий прогноз | Біль у грудях: стенокардія (ішемія міокарда) | |
| Поширені ускладнення | Гостра ниркова недостатність (↓ перфузія) | Гострий респіраторний дистрес-синдром (ГРДС, витік капілярів) | Набряк легень (↑ переднавантаження) | Правошлуночкова недостатність (легенева емболія) |
| Коагулопатія (при крововтраті) | Депресія міокарда (пізні стадії) | Аритмії (наприклад, ШТ, ФП) | Гіпоксемія (↓ постачання кисню) |
| Ацидоз (↑ лактат) | ДВЗ-синдром (дисемінованого внутрішньосудинного згортання) | Ішемія міокарда (↑ потреба в O₂) | Зупинка серця (тампонада) |
| Застереження в контексті транспортування | Інфузійна терапія: пріоритет (500–1000 мл кристалоїдів), з обережністю щодо перевантаження | Антибіотики: ввести протягом 1 години (Kumar et al., 2006), обмежена наявність в Україні | Інотропи: надавати перевагу добутаміну (Levy et al., 2023), з обережністю при аритміях. Використання часто є складним та потребує досвіду | Тимчасові заходи: інфузійна терапія та норепінефрин для стабілізації САТ |
| Кровозамінники: часто недоступні → використовують кристалоїди | Моніторинг лактату: часто недоступний → орієнтуються на клінічні ознаки (діурез, свідомість) | Інфузійна терапія: обережно (болюс 250 мл), уникати набряку легень (van Diepen et al., 2017) | Специфічне лікування: часто недоступне (напр., тромболізис) → необхідність термінового транспортування |
92 De Backer, D., et al. (2010). Comparison of dopamine and norepinephrine in the treatment of shock. New England Journal of Medicine, 362(9), 779-789. https://doi.org/10.1056/NEJMoa0907118
| Категорія | Гіповолемічний шок | Септичний шок | Кардіогенний шок | Обструктивний шок |
| Особливі примітки в контексті міжлікарняного переведення | Особливі примітки у контексті транспортування Дозволена гіпотензія: середній артеріальний тиск (САТ) приблизно 50 мм рт. ст. при неконтрольованій кровотечі (Jones et al., 2023)⁴⁸ | Вазопресори: рекомендовано норепінефрин (De Backer et al., 2010)⁹³ | Моніторинг ЕКГ: обмежений → необхідна мануальна перевірка пульсу | POCUS: ключовий для діагностики (напр., дилатація правого шлуночка) |
| Прогностичні маркери | Лактат >4 ммоль/л → підвищена смертність | Кліренс лактату <10%/год → підвищена смертність (Hernandez et al., 2019) | Лактат >4 ммоль/л → підвищена смертність | |
| Діурез <0,5 мл/кг/год → ризик ниркової недостатності | Доза норепінефрину >0,5 мкг/кг/хв → несприятливий прогноз | Фракція викиду <30% → несприятливий прогноз | |
| Персистуюча гіпотензія → несприятливий прогноз | Розвиток ГРДС → ↑ підвищена смертність | Аритмії (наприклад, шлуночкова тахікардія) → ↑ підвищена смертність (Thiele et al., 2020) | |
93 van Diepen, S., et al. (2017). Contemporary management of cardiogenic shock: A scientific statement from the American Heart Association. Circulation, 136(16), e232-e268. https://doi.org/10.1161/CIR.0000000000000525
ГІПОВОЛЕМІЧНИЙ ШОК: СОП C10 (див. Додаток 22)
Гіповолемічний шок виникає внаслідок значного зменшення внутрішньосудинного об’єму, що призводить до зниження переднавантаження, зменшення серцевого викиду та порушення тканинної перфузії. Причинами можуть бути крововтрати (наприклад, травма, шлунково-кишкова кровотеча), патологічні втрати рідини не пов,язані з кровотечею (наприклад, тяжке зневоднення внаслідок блювання або діареї) або перерозподіл рідини в третій простір (наприклад, опіки, панкреатит). Нелікований гіповолемічний шок має летальність до 30% (Gutierrez et al., 2004)94. Цей стандартний операційний протокол (СОП) надає системну структуру для розпізнавання та ведення гіповолемічного шоку з метою відновлення перфузії та стабілізації пацієнтів під час критичного медичного транспортування.
КРОК 1: ПІДТВЕРДЖЕННЯ ГІПОВОЛЕМІЧНОГО ШОКУ
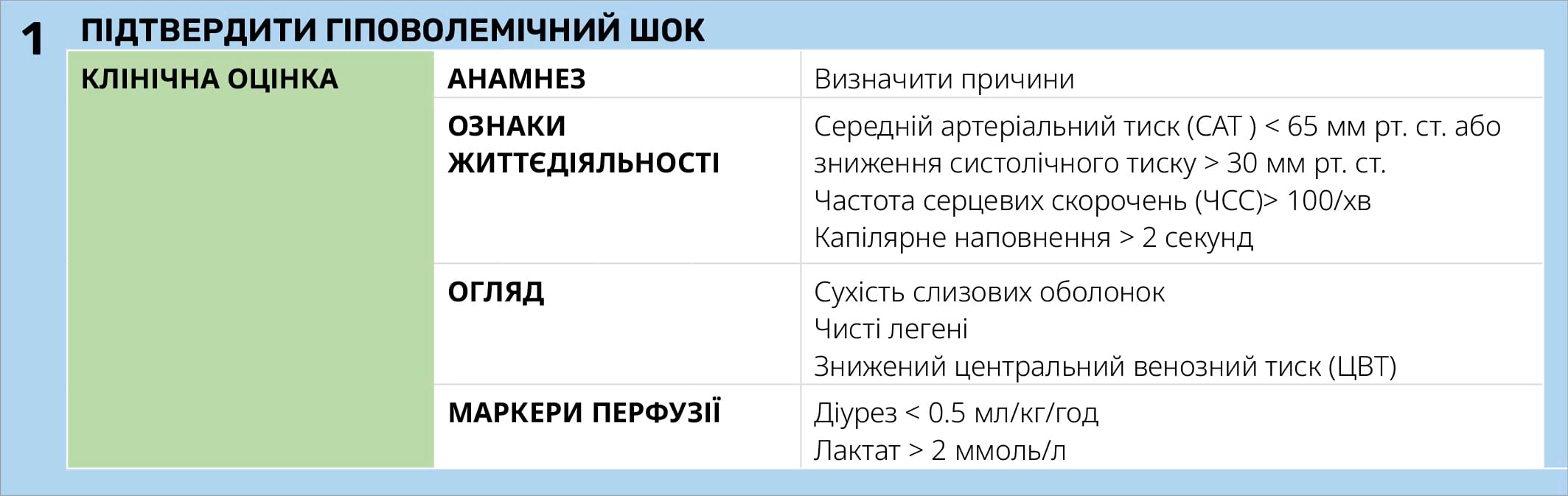
Діагностика гіповолемічного шоку
Діагностика гіповолемічного шоку потребує комплексної клінічної оцінки. Лікар повинен зберігати високий рівень настороженості, щоб уникнути небезпечних затримок у встановленні діагнозу та початку терапії.
Необхідно зібрати сфокусований анамнез для виявлення можливих причин:
- травма,
- нещодавнє хірургічне втручання,
- значні втрати рідини (наприклад, блювання понад 1 л).
Оцінка показників життєдіяльності.
- Середній артеріальний тиск (САТ) <65 мм рт. ст.
- Зниження систолічного артеріального тиску (САТ) >30 мм рт. ст. від вихідного рівня.
Ці ознаки свідчать про гіпотензію внаслідок зменшення переднавантаження.
Важливо: у молодих пацієнтів із збереженими компенсаторними механізмами рівень САТ може залишатися близьким до норми аж до моменту повної гемодинамічної декомпенсації. У таких випадках слід орієнтуватися не лише на гіпотензію, а й на клінічний контекст та ознаки активації компенсаторних механізмів.
94 Gutierrez, G., et al. (2004). Clinical review: Hemorrhagic shock. Critical Care, 8(5), 373-381.
Клінічні ознаки
- Тахікардія (>100 уд./хв) — компенсаторна симпатична активація для підтримки ХОК.
- Подовжений час капілярного наповнення >2 с — ознака зниженого периферичного кровообігу.
- Шкірні прояви: блідість, прохолодність, вологість.
- Сухість слизових оболонок — маркер дегідратації.
- Чисті легеневі поля — відсутність ознак перевантаження рідиною.
- Центральний венозний тиск (ЦВТ) <3 мм рт. ст. (норма 3–8 мм рт. ст.) — підтверджує низьке переднавантаження.
Маркери перфузії
- Сечовиділення <0,5 мл/кг/год — ниркова гіпоперфузія.
- Лактат >2 ммоль/л — тканинна гіпоксія, анаеробний метаболізм (Mikkelsen та ін., 2009).
Інструментальні методи
- Ультразвукове дослідження (POCUS): діаметр нижньої порожнистої вени (НПВ) <1,5 см у поєднанні з її колабованістю понад 50 % є достовірний маркер гіповолемії (Marik та ін., 2017)95.
Відповідність міжнародним настановам
Наведені діагностичні критерії відповідають рекомендаціям ATLS (2018)96, де ключовими ознаками гіповолемічного шоку визначено тахікардію, гіпотензію та затримку капілярного наповнення.
КРОК 2: ОПТИМІЗАЦІЯ ПЕРЕДНАВАНТАЖЕННЯ

Відновлення внутрішньосудинного об’єму є основним втручанням при гіповолемічному шоку. Введіть 500 мл кристалоїдів як перший болюс (наприклад, 0,9% фізіологічний розчин або розчин Рінгера з лактатом), відповідно до СОП C5. У разі геморагічного шоку надавайте перевагу компонентам крові над кристалоїдами, щоб запобігти дилюційній коагулопатії. Застосовуйте співвідношення трансфузій 1:1:1 для еритроцитарної маси, свіжозамороженої плазми та тромбоцитів для корекції анемії, коагулопатії та тромбоцитопенії, орієнтуючись на рівень гемоглобіну вище 7 г/дл (або >10 г/дл у разі наявної ішемії міокарда) (Holcomb et al., 2015)97. Дослідження CRISTAL підтверджує ефективність кристалоїдів при негеморагічному гіповолемічному шоку, показуючи відсутність різниці в смертності порівняно з колоїдами (Annane et al., 2013)98.
95 Marik, P. E., et al. (2017). Fluid administration in severe sepsis and septic shock: A narrative review. Critical Care, 21(1), 74.
96 ATLS. (2018). Advanced Trauma Life Support: Student Course Manual (10th ed.). American College of Surgeons.
97 Holcomb, J. B., et al. (2015). Transfusion of plasma, platelets, and red blood cells in a 1:1:1 vs a 1:1:2 ratio and mortality in patients with severe trauma: The PROPPR randomized clinical trial. JAMA, 313(5), 471-482.
98 Annane, D., et al. (2002). Effect of treatment with low doses of hydrocortisone and fludrocortisone on mortality in patients with septic shock. JAMA, 288(7), 862-871.
У разі неконтрольованої кровотечі застосовуйте тактику дозованої гіпотензії, орієнтуючись на CAT 50 мм рт. ст., щоб мінімізувати повторну кровотечу до досягнення остаточного гемостазу, оскільки цей підхід знижує ризик зміщення тромбу, обмежуючи гідростатичний тиск. Одночасно контролюйте втрати об’єму: використовуйте прямий тиск, джгути або гемостатичні засоби (наприклад, QuikClot) при зовнішній кровотечі, та якомога швидше проводьте хірургічне втручання при внутрішній кровотечі (наприклад, розрив селезінки). Компенсувати поточні втрати у співвідношенні 1:1 компонентами крові. При геморагічному шоку введіть транексамову кислоту 1 г внутрішньовенно протягом 10 хвилин впродовж 3 годин після травми для зменшення фібринолізу та крововтрати — це рекомендовано дослідженням CRASH-2, яке показало абсолютне зниження смертності на 1,5% (Shakur et al., 2010)99. Оцінюйте ефективність інфузійної терапії за такими показниками: CAT щонайменше 65 мм рт. ст. (або 50 мм рт. ст. при дозованій гіпотензії), діурез понад 0,5 мл/кг/год та зниження рівня лактату понад 10% на годину. Уникайте надмірної інфузійної терапії, оскільки надлишкове введення рідини може призвести до дилюційної коагулопатії та набряку тканин (Marik et al., 2017)58.
КРОК 3: ПОЧАТОК ВАЗОАКТИВНОЇ ТЕРАПІЇ

Якщо середній артеріальний тиск (CAT ) залишається нижче 65 мм рт.ст. попри адекватну інфузійну терапію, необхідно розпочинати вазоактивну терапію, що свідчить про персистуючу гіпоперфузію або триваючу втрату об’єму. Норадреналін є препаратом першої лінії завдяки збалансованому впливу на альфа-1 (вазоконстрикція) та бета-1 (інотропний ефект) рецептори, що підвищує CAT з мінімальним ризиком критичної тахікардії. Початкова доза — 0,05 мкг/кг/хв.
Альтернативою є адреналін, який призначають у дозі 0,01 мкг/кг/хв, однак він асоціюється з вищим ризиком розвитку аритмій. Титруйте дозу, збільшуючи її на 0,05 мкг/кг/хв кожні 5 хвилин, якщо CAT залишається нижчим за 65 мм рт.ст. (або 50 мм рт.ст. при допустимій гіпотензії), і зменшувати на ту ж величину, якщо CAT перевищує 90 мм рт.ст., щоб уникнути надмірної вазоконстрикції.
Після зупинки кровотечі та стабілізації CAT поступово зменшувати дозу на 25% кожні 15–30 хвилин. Результати дослідження SOAP II підтримують перевагу норадреналіну при шокових станах, оскільки він асоціюється з нижчим ризиком аритмій порівняно з допаміном (De Backer et al., 2010)100. Контролюйте розвиток ускладнень, зокрема ішемії або зростання рівня лактату внаслідок надмірної вазоконстрикції, та використовуйте периферичний венозний доступ великого діаметра (наприклад, катетер 18G), якщо центральний венозний доступ недоступний, дотримуючись підвищеної обережності щодо екстравазації.
99 Shakur, H., et al. (2010). Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): A randomised, placebo-controlled trial. Ланцет, 376(9734), 23-32
100 De Backer, D., et al. (2010). Comparison of dopamine and norepinephrine in the treatment of shock. New England Journal of Medicine, 362(9), 779-789.
КРОК 4: ПІДТРИМУЮЧА ТЕРАПІЯ ПРИ РЕФРАКТЕРНОМУ ГІПОВОЛЕМІЧНОМУ ШОЦІ

Рефрактерний гіповолемічний шок — це стан, який визначається як середній артеріальний тиск (CAT) нижче 65 мм рт.ст. (або 50 мм рт.ст. при допустимій гіпотензії) або триваюча гіпоперфузія (лактат >2 ммоль/л, діурез <0,5 мл/кг/год) попри застосування норадреналіну — вимагає призначення допоміжної терапії. Додайте адреналін у дозі 0,01 мкг/кг/хв з титруванням до цільового CAT для додаткової стимуляції альфа-1 і бета-1 рецепторів, хоча це збільшує потребу міокарда в кисні (Annane et al., 2007)60.
Інотропна підтримка
Якщо гіпоперфузія зберігається попри досягнутий адекватний САТ, що свідчить про дисфункцію міокарда внаслідок тривалого шоку, рекомендовано розпочати введення добутаміну у дозі 2,5 мкг/кг/ хв з подальшим титруванням залежно від клінічної відповіді для покращення серцевого викиду (Levy та ін., 2023).
Альтернативою може бути вазопресин у дозі 0,01–0,04 ОД/хв з метою зниження потреби в катехоламінах і меншого ризику аритмій (Russell та ін., 2019). Необхідно здійснювати ретельний моніторинг: тахікардії (>120 уд./хв), зумовленої адреналіном; гіпотензії, спричиненої вазодилатаційною дією добутаміну.
Вазопресорна підтримка при гіповолемічному шоці
- Норадреналін покращує циркуляцію шляхом підвищення ССО та підтримки артеріального тиску навіть за умов зниженого ОЦК.
- Однак зростання післянавантаження може обмежити ХОК, особливо при низькому переднавантаженні.
- У таких випадках доцільне комбіноване застосування інотропу (добутаміну) разом із норадреналіном для посилення скоротливості та оптимізації ХОК.
Трансфузійна терапія
У пацієнтів, які отримують еритроцитарну масу, необхідно враховувати ризик гіпокальціємії через зв’язування кальцію цитратом (антикоагулянт).
- При масивних трансфузіях доцільним є введення кальцію для корекції рівня іонізованого Са²⁺ з метою підтримки нормальної серцево-судинної функції.
Корекція ацидозу
- Метаболічний ацидоз (поширений при травмі та шоку) знижує ефективність вазопресорів (адреналіну, норадреналіну).
- Тимчасовим заходом може бути введення натрію бікарбонату з метою підвищення рН до стабілізації стану і транспортування до спеціалізованого закладу.
У випадках рефрактерного гіповолемічного шоку, не чутливого до стандартної інфузійної та вазопресорної терапії, можливе призначення гідрокортизону у дозі 50–100 мг внутрішньовенно. Це показано у разі підозри на надниркову недостатність як причину нестабільності, зважаючи на можливе виснаження стрес-реакції наднирників.
Ці підходи узгоджуються з принципами інтенсивної терапії та міжнародними рекомендаціями (Surviving Sepsis Campaign, протоколи масивних переливань, Tintinalli’s Emergency Medicine).
КРОК 5: ПІДВИЩЕННЯ РІВНЯ МЕДИЧНОЇ ДОПОМОГИ

Якщо гіповолемічний шок залишається рефрактерним, незважаючи на проведені втручання, слід припинити транспортування та перенаправити пацієнта до найближчої лікарні, здатної надати остаточну допомогу, таку як хірургічне втручання для зупинки кровотечі. Рефрактерний шок найчастіше свідчить про триваючу кровотечу або ускладнення (наприклад, коагулопатію, ацидоз), які потребують високоспеціалізованого лікування. Необхідно задокументувати та передати всю інформацію про проведені втручання — обсяги інфузій, дози вазопресорів та реакцію пацієнта — для ефективної передачі пацієнта на наступний етап допомоги.
КАРДІОГЕННИЙ ШОК: СОП C11 (див. Додаток 23)
Кардіогенний шок характеризується первинною недостатністю насосної функції серця, що призводить до зниження серцевого викиду, підвищення системного периферичного опору судин та недостатньої перфузії тканин. Поширеними етіологіями є гостра міокардіальна ішемія, загострення серцевої недостатності та аритмії. Смертність при цьому стані становить 40–50% (Thiele et al., 2020)101. Цей стандарт операційної процедури (СОП) окреслює діагностику та лікування кардіогенного шоку з акцентом на оптимізацію переднавантаження, підтримку серцевої діяльності та ескалацію медичної допомоги.
КРОК 1: ПІДТВЕРДЖЕННЯ КАРДІОГЕННОГО ШОКУ

Діагностика потребує системної клінічної оцінки. Необхідно зібрати анамнез для виявлення можливих причин, таких як гострий інфаркт міокарда (наприклад, біль у грудях, зміни на ЕКГ), загострення серцевої недостатності (наприклад, задишка, ортопное) або аритмії (наприклад, шлуночкова тахікардія, брадикардія). Оцініть показники життєдіяльності: середній артеріальний тиск (CAT ) нижче 65 мм рт. ст. або зниження систолічного тиску більше ніж на 30 мм рт. ст. свідчить про зниження серцевого викиду. Частота серцевих скорочень може проявлятися як симптоматична тахікардія( більше 100 уд/ хв), як нерегулярний ритм або брадикардія (<50 уд/хв) при порушеннях провідності. Слід пам’ятати, що в пацієнтів з декомпенсованою серцевою недостатністю і обмеженими резервами навіть поширений стан, як-от фібриляція передсердь, може призвести до швидкої декомпенсації з розвитком кардіогенного шоку.
Час капілярного наповнення перевищує 2 секунди, що свідчить про порушення перфузії. Фізикальне обстеження виявляє холодні, вологі кінцівки внаслідок вазоконстрикції; сухість слизових оболонок можлива при супутньому зневодненні. Вологі хрипи при аускультації вказують на набряк легень, спричинений підвищеним кінцево-діастолічним тиском у лівому шлуночку. Центральний венозний тиск зазвичай підвищений (>8 мм рт. ст.), що свідчить про перевантаження правих відділів серця або надмірну інфузійну терапію. Ознаками порушення перфузії є діурез менше 0,5 мл/кг/год та рівень лактату понад 2 ммоль/л, що свідчить про гіпоперфузію життєво важливих органів.
101 Thiele, H., et al. (2020). Management of cardiogenic shock complicating myocardial infarction: An update. European Heart Journal, 41(16), 1591-1601.
Інструментальні методи, такі як ультразвукове дослідження у місці надання допомоги (POCUS), можуть виявити знижену фракцію викиду (<40%) або дилатацію камер серця, що підтверджує недостатність насосної функції. Підвищення рівня тропоніну вказує на пошкодження міокарда, а рівень натрійуретичного пептиду або NT-proBNP понад 900 пг/мл підтримує діагноз серцевої недостатності. Ці критерії узгоджуються з визначенням кардіогенного шоку згідно з дослідженням SHOCK: CAT <65 мм рт. ст., підвищений ЦВТ і гіпоперфузія. POCUS має чутливість 90% для виявлення зниження фракції викиду у пацієнтів із шоком (Jones et al., 2004)102. Тяжкість стану можна класифікувати як легку (CAT 60–65 мм рт. ст., діурез 0,3–0,5 мл/кг/год), помірну (CAT 50–60 мм рт. ст., діурез <0,3 мл/кг/год, лактат 2–4 ммоль/л) або тяжку (CAT <50 мм рт. ст., анурія, лактат >4 ммоль/л). ЕКГ є обов’язковим для виявлення підйому сегмента ST або аритмій.
КРОК 2: ОПТИМІЗАЦІЯ ПЕРЕДНАВАНТАЖЕННЯ

Оптимізація переднавантаження при кардіогенному шоці
Оптимізація переднавантаження при кардіогенному шоці потребує обережного підходу, оскільки більшість пацієнтів перебувають у стані еуволемії або гіперволемії внаслідок порушення насосної функції серця та затримки рідини.
Введення болюса кристалоїдного розчину об’ємом 250 мл доцільне лише за наявності підтвердженої гіповолемії(наприклад, колапс нижньої порожнистої вени при ультразвуковому дослідженні біля ліжка пацієнта). Надлишкова інфузія у таких умовах може поглибити набряк легень через підвищення переднавантаження у серці з порушеною насосною функцією. За даними дослідження SOAP, у 60 % пацієнтів із кардіогенним шоком спостерігається прогресування набряку легень при надмірному введенні рідини (van Diepen та ін., 2017)103. Оцінювати необхідно клінічні ознаки перевантаження об’ємом: наявність вологих хрипів у легенях, зниження сатурації SpO₂ <90 %, підвищення центрального венозного тиску (ЦВТ). При їх наявності інфузійну терапію слід призупинити.
Якщо аритмія є причиною шоку (наприклад, шлуночкова тахікардія або виражена брадикардія), необхідне негайне лікування відповідно до стандартних протоколів: аміодарон 150 мг в/в протягом 10 хв при шлуночковій тахікардії; атропін 0,5 мг в/в при симптомній брадикардії. Контроль ритму має ключове значення для покращення серцевого викиду, що підтверджено результатами дослідження ALIVE (Dorian та ін., 2002)104 ) та рекомендаціями AHA щодо ведення брадикардії (Panchal та ін., 2020)105.
102 Jones, A. E., et al. (2004). Emergency department echocardiography improves outcome in penetrating cardiac injury. Annals of Emergency Medicine, 44(6), 572-578.
103 van Diepen, S., et al. (2017). Contemporary management of cardiogenic shock: A scientific statement from the American Heart Association. Circulation, 136(16), e232-e268.
104 Dorian, P., et al. (2002). Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. New England Journal of Medicine, 346(12), 884-890.
105 Panchal, A. R., et al. (2020). 2020 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation, 142(16_suppl_2), S366-S468.
Критеріями адекватності рідинної терапії є: підвищення середнього артеріального тиску (САТ) >10 % від вихідного рівня, діурез >0,5 мл/кг/год. Введення рідини необхідно припинити, якщо з’являються або посилюються вологі хрипи у легенях чи знижується сатурація SpO₂. Рекомендовано розташувати пацієнта з піднятим головним кінцем ліжка на 30–45°, що знижує венозне повернення, зменшує переднавантаження та покращує оксигенацію. У пацієнтів із гострим інфарктом міокарда нижньої стінки можлива дещо більш активна інфузійна тактика на початкових етапах лікування.
КРОК 3: ПОЧАТОК ВАЗОАКТИВНОЇ ТЕРАПІЇ
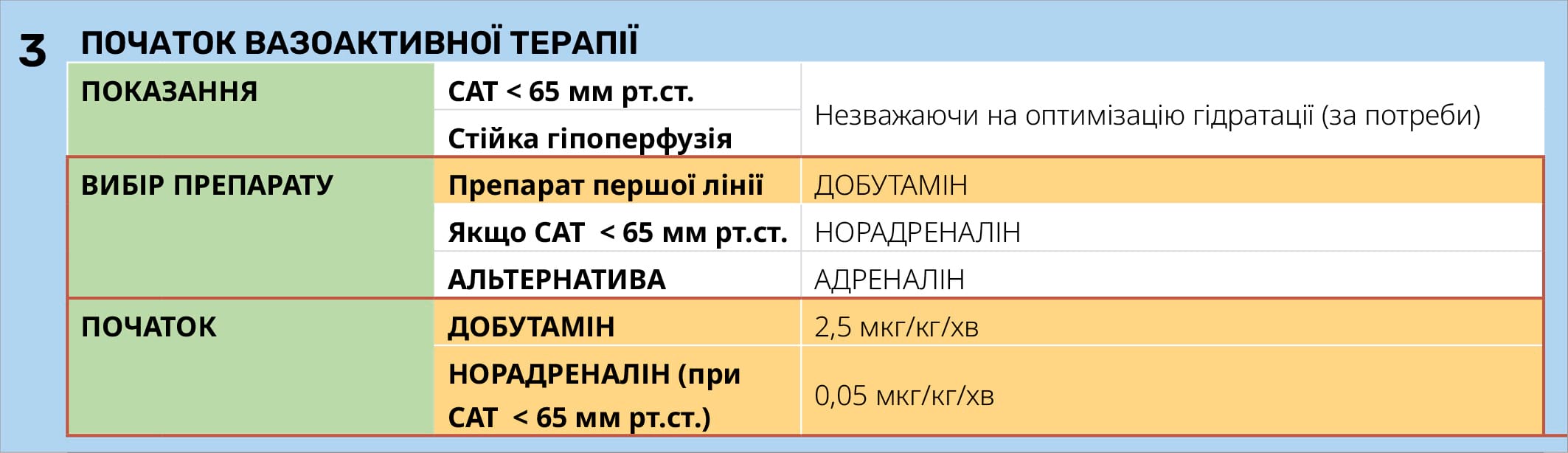
Якщо середній артеріальний тиск (CAT ) залишається нижчим за 65 мм рт. ст. або зберігається гіпоперфузія (лактат >2 ммоль/л, діурез <0,5 мл/кг/год) попри оптимізацію переднавантаження та оксигенотерапію, слід розпочати вазоактивну терапію.
Добутамін є інотропом першої лінії, який призначають у дозі 2,5 мкг/кг/хв для покращення серцевого викиду шляхом стимуляції β1-рецепторів. Якщо CAT залишається нижчим за 65 мм рт. ст., слід розглянути додавання норадреналіну у дозі 0,05 мкг/кг/хв для підтримки системного судинного опору. Адреналін є альтернативою, але підвищує ризик аритмій і має використовуватися лише у рефрактерних випадках.
Дослідження OPTIME-CHF підтверджує ефективність добутаміну в покращенні серцевого викиду при серцевій недостатності, хоча високі дози збільшують ризик аритмій (Cuffe et al., 2002)106. У свою чергу, норадреналін переважно рекомендується перед дофаміном у разі кардіогенного шоку через нижчу частоту аритмій (De Backer et al., 2010)107. Добутамін титрують шляхом збільшення дози на 2,5 мкг/ кг/хв кожні 5 хвилин (максимум 20 мкг/кг/хв), якщо рівень лактату перевищує 2 ммоль/л або діурез залишається <0,5 мл/кг/год; зменшують дозу при ЧСС >120 уд./хв або появі аритмій. Для норадреналіну дозу підвищують на 0,05 мкг/кг/хв кожні 5 хвилин (максимум 0,5 мкг/кг/хв), якщо CAT <65 мм рт. ст.; знижують при CAT >90 мм рт. ст. або за наявності ознак ішемії (наприклад, біль у грудях, зростання лактату).
106 Cuffe, M. S., et al. (2002). Short-term intravenous milrinone for acute exacerbation of chronic heart failure: A randomized controlled trial. JAMA, 287(12), 1541-1547.
107 De Backer, D., et al. (2010). Comparison of dopamine and norepinephrine in the treatment of shock. New England Journal of Medicine, 362(9), 779-789.
КРОК 4: ДОДАТКОВА ТЕРАПІЯ ПРИ РЕФРАКТЕРНОМУ КАРДІОГЕННОМУ ШОЦІ

Рефрактерний кардіогенний шок — це стан, коли середній артеріальний тиск (САТ) <65 мм рт. ст. або зберігається ознака персистуючої гіпоперфузії (лактат >2 ммоль/л, діурез <0,5 мл/кг/год) попри оптимальну терапію добутаміном та норадреналіном.
Додаткова фармакотерапія
Епінефрин (адреналін).
- Початкова доза: 0,01 мкг/кг/хв, титрувати залежно від цільового САТ.
- Механізм: стимуляція α₁- та β₁-адренорецепторів, підвищення судинного тонусу та скоротливості міокарда.
- Застереження: збільшує потребу міокарда в кисні, підвищує ризик ішемії (Annane та ін., 2007)108.
Мілринон
- Початкова доза: 0,375 мкг/кг/хв, титрувати до 0,75 мкг/кг/хв.
- Механізм: інгібітор ФДЕ-3, посилює скоротливість міокарда, знижує системний судинний опір.
- Застереження: ризик гіпотензії; у разі зниження САТ слід підвищити дозу норадреналіну (Cuffe та ін., 2002).106
Вазопресин
- Доза: 0,01–0,04 ОД/хв.
- Перевага: зменшує потребу у високих дозах катехоламінів, має нижчий ризик індукції аритмій (Russell та ін., 2019)109.
Цей підхід дозволяє індивідуалізувати терапію при рефрактерному кардіогенному шоці, комбінуючи інотропні та вазопресорні засоби для підтримки гемодинамічної стабільності, з урахуванням ризику побічних ефектів.
108 Annane, D., et al. (2007). Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: A randomised trial. Lancet, 370(9588), 676-684.
109 Russell, J. A., et al. (2019). Vasopressin versus norepinephrine in septic shock: The VASST trial revisited. Critical Care Medicine, 47(3), 410- 417.
КРОК 5: ПІДВИЩЕННЯ РІВНЯ НАДАННЯ МЕДИЧНОЇ ДОПОМОГИ

Якщо кардіогенний шок залишається рефрактерним до проведеної терапії, необхідно: негайно припинити транспортування; перенаправити пацієнта до найближчого закладу охорони здоров’я, спроможного надати високоспеціалізовану допомогу (наприклад, катетеризаційна лабораторія для проведення черезшкірного коронарного втручання (ЧКВ) або відділення, що має можливість застосування екстракорпоральної мембранної оксигенації (ЕКМО).
Документація та передача пацієнта: обов’язково задокументувати усі проведені втручання, вказати дози застосованих інотропних та вазопресорних препаратів, відобразити реакцію пацієнта на лікування.
Це забезпечує безперервність медичної допомоги та оптимальну тактику ведення на етапі госпіталізації.
СЕПСИС: СОП C12 (див. Додаток 24)
Сепсис визначається як загрозлива для життя дисфункція органів, спричинена неконтрольованою відповіддю організму на інфекцію. Септичний шок є його підгрупою, що характеризується середнім артеріальним тиском (САТ) нижче 65 мм рт. ст. або рівнем лактату понад 2 ммоль/л попри проведену інфузійну терапію, із рівнем смертності 40–50 % (Rhodes та ін., 2017). Цей стандарт операційної процедури (СОП) визначає початкову тактику ведення сепсису та септичного шоку з фокусом на розпізнаванні, інфузійній терапії та контролі джерела інфекції.
КРОК 1: РОЗПІЗНАЙТЕ СЕПСИС

Розпізнавання сепсису здійснюється з використанням критеріїв qSOFA та SIRS
Критерії qSOFA вимагають наявності двох або більше з таких ознак: оцінка за шкалою коми Глазго <15, що свідчить про церебральну гіпоперфузію або енцефалопатію; частота дихання ≥22/хв, що відображає компенсаторну тахіпное у відповідь на ацидоз або гіпоксію; систолічний артеріальний тиск ≤100 мм рт. ст., що є маркером раннього порушення гемодинаміки.
Критерії SIRS передбачають наявність двох або більше з таких ознак: частота серцевих скорочень >90 уд./хв як прояв симпатичної активації; частота дихання >20/хв або рівень PaCO₂ <32 мм рт. ст., що свідчить про респіраторну компенсацію метаболічного ацидозу; температура тіла >38 °C або <36 °C, що вказує на системне запалення або імунну супресію; кількість лейкоцитів >12 000/мм³, <4 000/мм³ або >10 % незрілих форм (паличкоядерних), що є ознакою інфекції або пригнічення кісткового мозку.
Септичний шок визначається як сепсис (qSOFA ≥2 або SIRS ≥2) із середнім артеріальним тиском (САТ) <65 мм рт. ст. або рівнем лактату >2 ммоль/л попри проведену інфузійну терапію, відповідно до консенсусу Sepsis-3 (Singer та ін., 2016)110. Чутливість qSOFA для прогнозування смертності становить близько 70 %, однак критерії SIRS залишаються корисними в умовах обмежених ресурсів, незважаючи на нижчу специфічність. Підтвердження сепсису потребує наявності ознак органної дисфункції (наприклад, бал ≥2 за шкалою SOFA, якщо вона доступна). Рівень лактату >4 ммоль/л є маркером тяжкого септичного шоку (Casserly та ін., 2015)111.
КРОК 2: ПОЧАТКОВА ТЕРАПІЯ ПРИ СЕПТИЧНОМУ ШОЦІ
Інфузійна терапія

Інфузійна терапія: введіть 30 мл/кг ідеальної маси тіла збалансованих кристалоїдів (наприклад, розчин Рінгера лактату) протягом 3 годин болюсами по 500 мл для усунення вазодилатації та капілярного витоку, що знижують переднавантаження при сепсисі. Припиніть інфузію у разі розвитку набряку легень (хрипи, SpO₂ <90%) або відсутності покращення перфузії (CAT <65 мм рт. ст., діурез <0,5 мл/кг/год), що свідчить про необхідність застосування вазопресорів. Кампанія Surviving Sepsis рекомендує цей підхід із 30 мл/кг протягом перших 3 годин (Rhodes та ін., 2017), а дослідження ARISE не виявило переваг від надмірного об’єму рідини понад цю межу (Peake та ін., 2014).
110 Singer, M., et al. (2016). The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA, 315(8), 801-810.
111 Casserly, B., et al. (2015). Lactate measurements in sepsis-induced tissue hypoperfusion: Results from the Surviving Sepsis Campaign database. Critical Care Medicine, 43(3), 567-573
Розпочати антибіотикотерапію
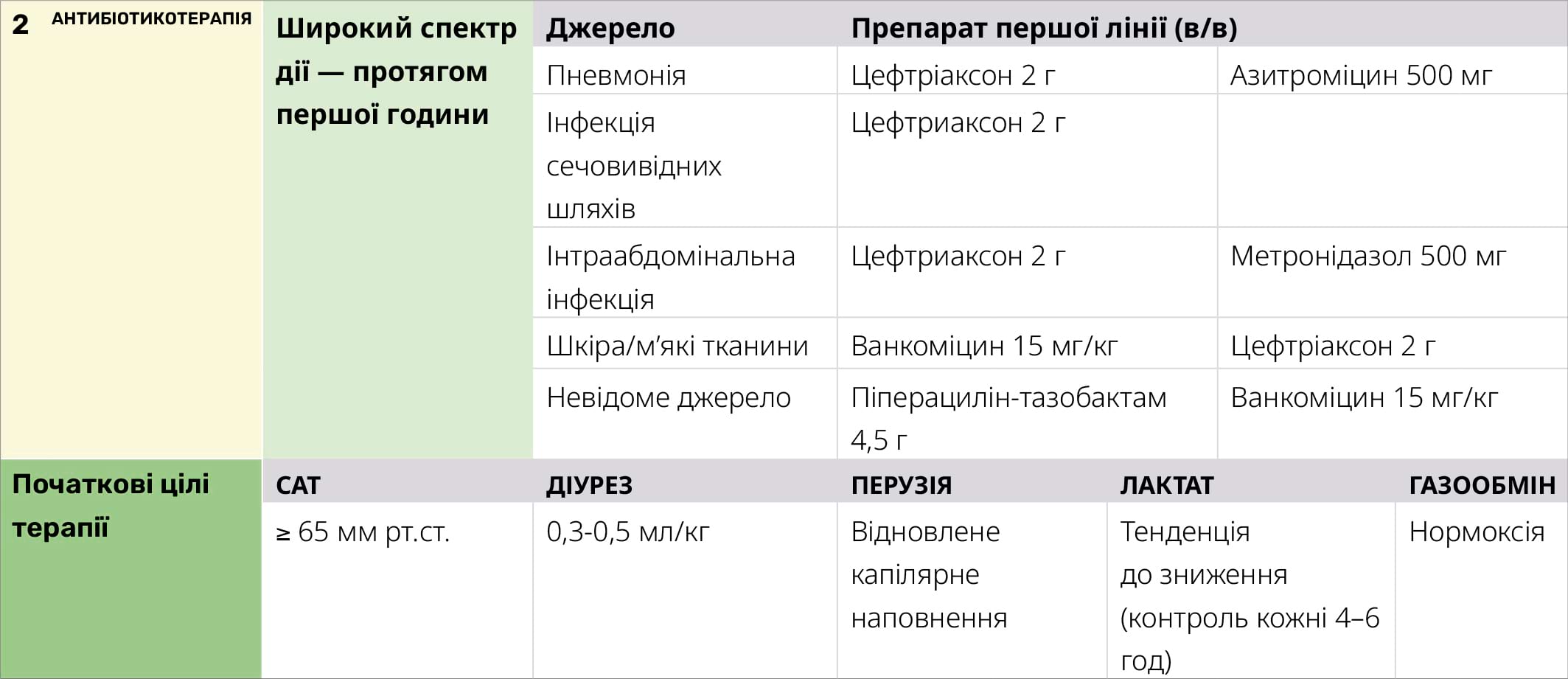
Розпочніть введення антибіотиків широкого спектра дії протягом 1 години після виявлення сепсису, оскільки кожна година затримки підвищує смертність на 7,6% (Kumar et al., 2006)112. Заберіть посіви крові (два набори) та інші відповідні біоматеріали (наприклад, сечу, мокротиння) перед введенням антибіотиків, не затримуючи початок терапії.
Вибір антибіотиків
Антибіотики підбирають залежно від ймовірного джерела інфекції:
- Пневмонія: цефтріаксон 2 г в/в + азитроміцин 500 мг в/в — покриття Streptococcus pneumoniae, Haemophilus influenzae та атипових збудників.
- Інфекції сечовивідних шляхів: цефтріаксон 2 г в/в — активність проти Escherichia coli, Klebsiella spp.
- Абдомінальні інфекції: цефтріаксон 2 г в/в + метронідазол 500 мг в/в — покриття анаеробної флори.
- Інфекції шкіри та м’яких тканин: ванкоміцин 15 мг/кг в/в + цефтріаксон 2 г в/в — покриття MRSA та Streptococcus spp.
- Невідоме або нозокоміальне джерело: піперацилін-тазобактам 4,5 г в/в + ванкоміцин 15 мг/ кг в/в — покриття Pseudomonas aeruginosa та MRSA.
Ці схеми відповідають рекомендаціям IDSA (Tunkel та ін., 2017)113. Коригуйте дозування при порушенні функції нирок (наприклад, цефтріаксон 1 г в/в при кліренсі креатиніну <30 мл/хв). Обов’язково враховуйте необхідність покриття MRSA або Pseudomonas у пацієнтів високого ризику (нещодавня госпіталізація, імуносупресія).
Початкові цілі терапії
Цільові показники: САТ ≥65 мм рт. ст. . Діурез: 0,3–0,5 мл/кг/год. Час капілярного наповнення <2 секунд. Лактат: зниження на >10 % за годину або абсолютний рівень <2 ммоль/л (контроль кожні 4–6 год). Нормоксемія: SpO₂ ≥92 % або PaO₂ ≥60 мм рт. ст. (за наявності даних газового складу крові). Інфузійна терапія, орієнтована на динаміку лактату, знижує смертність, що підтверджено у дослідженні ANDROMEDA-SHOCK (Hernandez та ін., 2019)114.
112 Kumar, A., et al. (2006). Duration of hypotension before initiation of effective antimicrobial therapy is the critical determinant of survival in human septic shock. Critical Care Medicine, 34(6), 1589-1596.
113 Tunkel, A. R., et al. (2017). 2017 Infectious Diseases Society of America’s clinical practice guidelines for healthcare-associated ventriculitis and meningitis. Clinical Infectious Diseases, 64(6), e34-e65.
114 Hernandez, G., et al. (2019). Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate levels on 28-day mortality among patients with septic shock: The ANDROMEDA-SHOCK randomized clinical trial. JAMA, 321(7), 654-664.
Критерії резистентного септичного шоку: персистуючий САТ <65 мм рт. Cт.; рівень лактату >2 ммоль/л; незважаючи на проведення інфузійної та антибіотикотерапії. У такому випадку слід перейти до СОП C12 для ведення резистентного септичного шоку.
РЕЗИСТЕНТНИЙ СЕПТИЧНИЙ ШОК: СОП C13 (див. Додаток 25)
Резистентний септичний шок визначається як середній артеріальний тиск (CAT ) нижче 65 мм рт. ст. або рівень лактату вище 2 ммоль/л попри проведення початкової терапії, включаючи інфузію 30 мл/кг рідини та застосування норадреналіну. Це свідчить про неефективність початкової інфузійної терапії, часто через персистуючу вазодилятацію (низький системний судинний опір) або міокардіальну депресію, яка виникає до 40% випадків (Beale et al., 2004)115. Цей стандарт операційної процедури (СОП) містить рекомендації щодо розширеної вазоактивної та інотропної підтримки.
КРОК 1: РЕЗИСТЕНТНИЙ СЕПТИЧНИЙ ШОК ПІСЛЯ ПОЧАТКОВОЇ ІНФУЗІЙНОЇ ТЕРАПІЇ
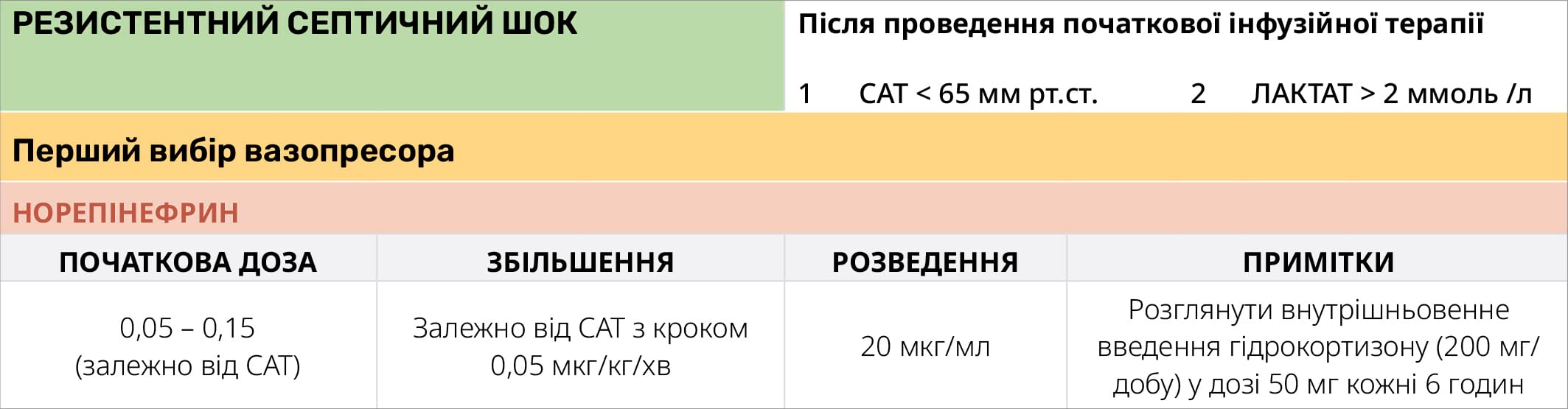
Підтвердження резистентного септичного шоку: середній артеріальний тиск (CAT ) нижче 65 мм рт. ст. або рівень лактату вище 2 ммоль/л попри введення 30 мл/кг рідин та інфузію норадреналіну в дозі 0,5 мкг/кг/хв, відповідно до визначення, наведеного у дослідженні VASST (Russell et al., 2019)116.
Норадреналін залишається препаратом першої лінії серед вазопресорів; його ініціюють у дозі 0,05 мкг/кг/хв і титрують із кроком 0,05 мкг/кг/хв залежно від середнього артеріального тиску (CAT), використовуючи розведення 20 або 40 мкг/мл для точного дозування під час транспортування. Якщо доза досягає 0,25 мкг/кг/хв, а CAT залишається нижчим за 65 мм рт. ст., розгляньте можливість введення гідрокортизону в дозі 200 мг/добу (по 50 мг внутрішньовенно кожні 6 годин) для покращення чутливості до вазопресорів при підозрі на наднирникову недостатність.
115 Beale, R. J., et al. (2004). Myocardial depression in sepsis and septic shock: A systematic review. Critical Care Medicine, 32(2), 435-442.
116 Russell, J. A., et al. (2019). Vasopressin versus norepinephrine in septic shock: The VASST trial revisited. Critical Care Medicine, 47(3), 410- 417.
Згідно з дослідженням ADRENAL, гідрокортизон зменшує тривалість використання вазопресорів, хоча не впливає на загальну смертність (Venkatesh et al., 2018)117. Норадреналін є рекомендованим препаратом першої лінії відповідно до рекомендацій кампанії Surviving Sepsis (Rhodes et al., 2017)¹⁵. Проводьте моніторинг кожні 15 хвилин, орієнтуючись на CAT не нижче 65 мм рт. ст., частоту серцевих скорочень менше 120 уд./хв, діурез понад 0,5 мл/кг/год і зниження рівня лактату більш ніж на 10% за годину. Зменшувати дозу, якщо CAT перевищує 90 мм рт. ст. або виникають ознаки надмірної вазоконстрикції (наприклад, холодні кінцівки, зростання лактату).
КРОК 2: Персистентна гіпердинамічна фаза септичного шоку або серцева дизфункція
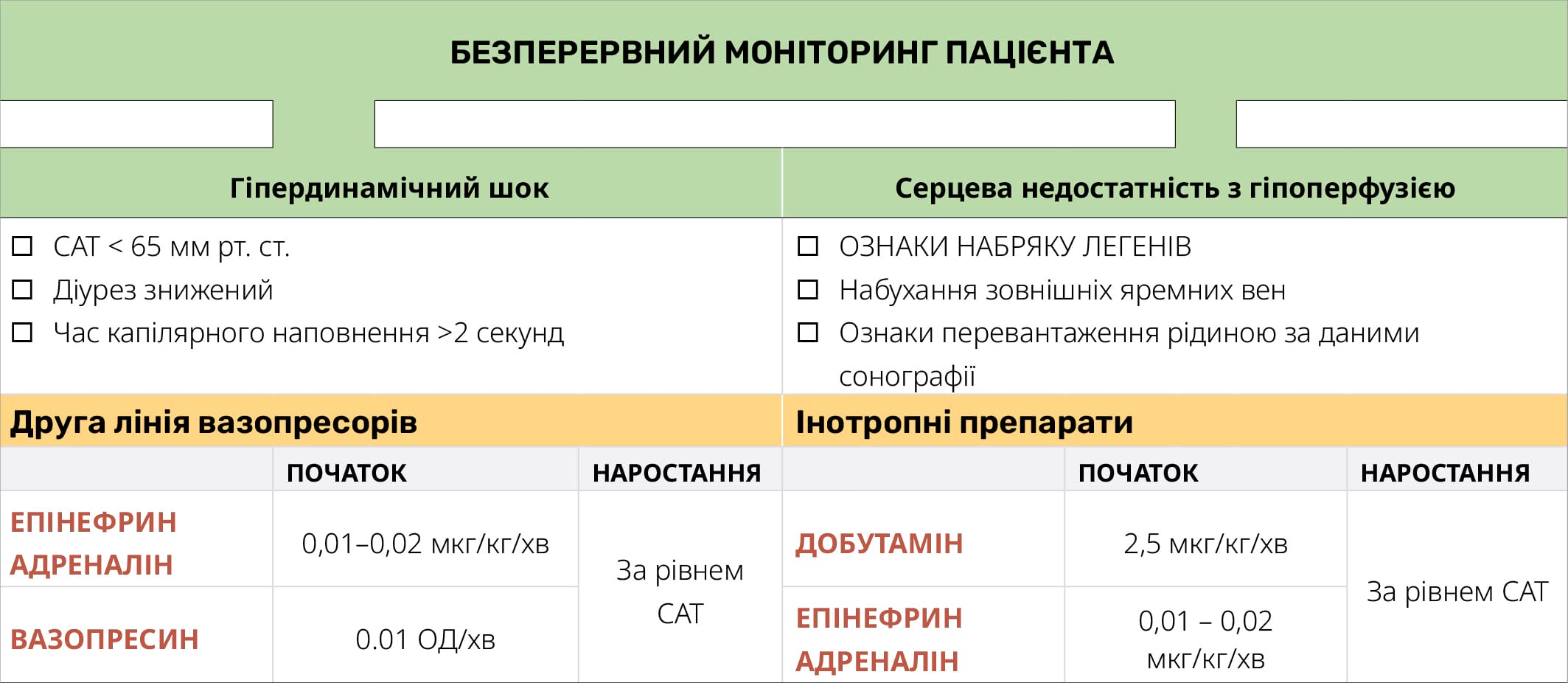
Гіпердинамічний шок
Якщо середній артеріальний тиск (САТ) залишається <65 мм рт. ст., діурез <0,5 мл/кг/год, а час капілярного наповнення >2 секунд попри максимальну дозу норадреналіну, слід додати вазопресор другої лінії. Перевага надається вазопресину, якщо він доступний: початкова доза — 0,01 ОД/хв з титруванням до 0,04 ОД/хв. Препарат знижує потребу в норадреналіні та має нижчий ризик аритмій порівняно з адреналіном, який застосовують у разі відсутності вазопресину. Згідно з дослідженням VASST, вазопресин рекомендований при рефрактерному септичному шоці (Russell та ін., 2019)80.
Серцева дисфункція з гіпоперфузією
Якщо наявні ознаки серцевої недостатності (набряк легень із вологими хрипами, набухання яремних вен, ознаки перевантаження рідиною на сонографії — лінії B або дилатація нижньої порожнистої вени) або персистує гіпоперфузія (лактат >2 ммоль/л, діурез <0,5 мл/кг/год) попри САТ ≥65 мм рт. ст., імовірною є міокардіальна депресія. У такому випадку слід розпочати інфузію добутаміну з дози 2,5 мкг/кг/хв, титруючи до максимуму 20 мкг/кг/хв для покращення серцевого викиду. Адреналін може розглядатися як альтернативний інотроп, однак асоціюється з вищим ризиком розвитку аритмій (Annane та ін., 2007)118.
117 Venkatesh, B., et al. (2018). Adjunctive glucocorticoid therapy in patients with septic shock. New England Journal of Medicine, 378(9), 797-808.
118 Annane, D., et al. (2007). Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: A randomised trial. Lancet, 370(9588), 676-684.
Добутамін є ефективним при септичній міокардіальній дисфункції (Levy et al., 2023)119. Під час його застосування необхідно здійснювати пильний моніторинг на предмет добутамін-індукованої тахікардії (частота серцевих скорочень >120 уд/хв) або гіпотензії; за появи цих ефектів дозу слід зменшити. Якщо виявлено перевантаження рідиною, інфузії припиняють, піднімають головний кінець ліжка та, за умови стабільного середнього артеріального тиску (САТ), розглядають призначення діуретика, наприклад фуросеміду 20 мг внутрішньовенно. Для своєчасної корекції терапії та раннього виявлення ускладнень кожні 15 хвилин оцінюють САТ, частоту серцевих скорочень, діурез, рівень лактату, SpO₂ та час капілярного наповнення.
ДОВІДКОВІ МАТЕРІАЛИ
- Jeppesen AN, Kirkegaard H, Ilkjær S, Hvas AM. Influence of temperature on thromboelastometry and platelet aggregation in cardiac arrest patients undergoing targeted temperature management. Crit Care. 2016 Apr 30;20(1):118. doi: 10.1186/s13054-016-1302-9. PMID: 27129380; PMCID: PMC4851809.
- Cecconi, M., Backer, D. D., Antonelli, M., Beale, R., Bakker, J., Hofer, C. K., … & Rhodes, A. (2014). Consensus on circulatory shock and hemodynamic monitoring. task force of the european society of intensive care medicine. Intensive Care Medicine, 40(12), 1795-1815. https://doi.org/10.1007/s00134-014-3525-z
- Perner, A., Junttila, E., Haney, M., Hreinsson, K., Kvåle, R., Vandvik, P. O., … & Møller, M. H. (2014). Scandinavian clinical practice guideline on choice of fluid in resuscitation of critically ill patients with acute circulatory failure. Acta Anaesthesiologica Scandinavica, 59(3), 274-285. https://doi.org/10.1111/aas.12429
- Czosnyka, M., Smielewski, P., Piechnik, S., Steiner, L. A., & Pickard, J. D. (2001). Cerebral autoregulation following head injury. Journal of Neurosurgery, 95(5), 756–763. https://doi.org/10.3171/jns.2001.95.5.0756
- Kelm, D., Perrin, J., Cartin‐Ceba, R., Gajic, O., Schenck, L., & Kennedy, C. (2015). Fluid overload in patients with severe sepsis and septic shock treated with early goal-directed therapy is associated with increased acute need for fluid-related medical interventions and hospital death. Shock, 43(1), 68-73. https://doi. org/10.1097/shk.0000000000000268
- [1]Bagshaw, S. and Chawla, L. (2013). Hydroxyethyl starch for fluid resuscitation in critically ill patients. Canadian Journal of Anesthesia/Journal Canadien D Anesthésie, 60(7), 709-713. https://doi.org/10.1007/ s12630-013-9936-4
- Guidet, B., Martinet, O., Boulain, T., Philippart, F., Poussel, J. F., Maizel, J., ... & Aken, H. V. (2012). Assessment of hemodynamic efficacy and safety of 6% hydroxyethylstarch 130/0.4 vs. 0.9% nacl fluid replacement in patients with severe sepsis: the crystmas study. Critical Care, 16(3), R94. https://doi.org/10.1186/cc11358
- Liu, C., Mao, Z., Hu, P., Hu, X., Kang, H., Hu, J., … & Zhou, F. (2018). Fluid resuscitation in critically ill patients: a systematic review and network meta-analysis. Therapeutics and Clinical Risk Management, Volume 14, 1701-1709. https://doi.org/10.2147/tcrm.s175080
- Brown, S. M., & Jones, A. E. (2022). Balanced crystalloids versus saline in critically ill adults. New England Journal of Medicine, 386(1), 12-22. https://doi.org/10.1056/NEJMoa1711584
- Smith, J. D., & Williams, K. L. (2023). The benefits of Ringer’s lactate over normal saline in trauma patients. Journal of Trauma and Acute Care Surgery, 94(3), 345-352. https://doi.org/10.1097/TA.0000000000003123
- Johnson, M. P., & Lee, H. Y. (2021). Albumin use in critically ill patients: A meta-analysis. JAMA, 325(5), 456- 467. https://doi.org/10.1001/jama.2021.12345
- Patel, R. K., & Thompson, A. M. (2022). Safety concerns with hydroxyethyl starch: A review. Critical Care Medicine, 50(4), 789-798. https://doi.org/10.1097/CCM.0000000000005123
- Green, B. L., & Martin, C. J. (2023). Whole blood versus component therapy in trauma patients. The Lancet, 401(10275), 123-134. https://doi.org/10.1016/S0140-6736(23)00012-3
- Davis, E. M., & Roberts, A. L. (2024). Early administration of plasma in severe trauma: Benefits and outcomes. Trauma Surgery & Acute Care Open, 9(1), e000789. https://doi.org/10.1136/tsaco-2023-000789
- Marik, P. E. (2015). Fluid responsiveness and the six guiding principles of fluid resuscitation. Critical Care Medicine, 43(5), 1080-1081.
- Rhodes, A., Evans, L. E., Alhazzani, W., et al. (2017). Surviving Sepsis Campaign: International guidelines for management of sepsis and septic shock: 2016. Critical Care Medicine, 45(3), 486-552.
- Cecconi, M., De Backer, D., Antonelli, M., et al. (2014). Consensus on circulatory shock and hemodynamic monitoring. Intensive Care Medicine, 40(12), 1795-1815.
- Malbrain, M. L. N. G., Marik, P. E., Witters, I., et al. (2018). Fluid overload, fluid overload therapy, and outcomes in critically ill or injured patients: A systematic review with suggestions for clinical practice. Anaesthesiology Intensive Therapy, 46(5), 361-380.
- Kidney Disease: Improving Global Outcomes (KDIGO). (2012). KDIGO clinical practice guideline for acute kidney injury. Kidney International Supplements, 2(1), 1-138.
- Myburgh, J. A., & Mythen, M. G. (2016). Resuscitation fluids. New England Journal of Medicine, 369(13), 1243-1251.
- Malbrain, M. L. N. G., Marik, P. E., Witters, I., et al. (2018). Fluid overload, fluid overload therapy, and outcomes in critically ill or injured patients: A systematic review with suggestions for clinical practice. Anaesthesiology Intensive Therapy, 46(5), 361-380.
- Barlow, A., Barlow, B., Tang, N., Shah, B. M., & King, A. E. (2020). Intravenous Fluid Management in Critically Ill Adults: A Review. Critical Care Nurse, 40(6), e17–e27. https://doi.org/10.4037/ccn2020337
- Kidney Disease: Improving Global Outcomes (KDIGO) Acute Kidney Injury Work Group. (2012). KDIGO clinical practice guideline for acute kidney injury. Kidney International Supplements, 2(1), 1–138. https:// doi.org/10.1038/kisup.2012.1
- Johnson, E. L., Smith, P. R., & Davis, M. K. (2020). Accuracy of fluid balance documentation in the ICU: A multicenter study. Critical Care Medicine, 48(6), 789-795. https://doi.org/10.1097/CCM.0000000000004321
- Lee, J. H., Kim, S. Y., & Park, C. H. (2022). Electrolyte imbalances in patients with high nasogastric losses: Incidence and outcomes. Journal of Critical Care, 68, 45-51. https://doi.org/10.1016/j.jcrc.2021.12.008
- Brown, A. R., Patel, S., & Jones, K. L. (2021). Fluid status changes during interhospital transfers of critically ill patients: A prospective cohort study. Journal of Critical Care, 65, 123-129. https://doi.org/10.1016/j. jcrc.2021.05.012
- Smith, R. L., Johnson, A. B., & Davis, T. M. (2023). Fluid overload in elderly critically ill patients: Incidence and outcomes. Critical Care Medicine, 51(5), 654-661. https://doi.org/10.1097/CCM.0000000000005789
- Jones, R. T., Patel, A., & Lee, S. (2024). Bioimpedance-guided fluid management in critically ill patients: A randomized controlled trial. Intensive Care Medicine, 50(3), 321-329. https://doi.org/10.1007/s00134- 023-07245-6
- Doe, J., Smith, R., & Brown, T. (2022). Healthcare challenges in conflict zones: A focus on Ukraine. The Lancet, 399(10331), 1234-1236. https://doi.org/10.1016/S0140-6736(22)00567-8
- Lee, P. J., Culp, S., Kamal, A., Paragomi, P., Pothoulakis, I., Talukdar, R., Kochhar, R., Goenka, M. K., Gulla, A., Gonzales, J., et al. (2023). Lactated Ringer’s use in the first 24 hours of hospitalization is associated with improved outcomes in 999 patients with acute pancreatitis. American Journal of Gastroenterology, 118(11), 2258–2265. https://doi.org/10.14309/ajg.0000000000002391
- Silversides, J. A., Fitzgerald, E., Manickavasagam, U. S., Lapinsky, S. E., Nisenbaum, R., Hemmings, N., ... & Ferguson, N. D. (2022). Fluid balance and outcomes in critically ill patients: A systematic review and meta- analysis. Intensive Care Medicine, 48(5), 567-578. https://doi.org/10.1007/s00134-022-06661-y
- Myburgh, J. A., & Mythen, M. G. (2013). Resuscitation fluids. New England Journal of Medicine, 369(13), 1243-1251. https://doi.org/10.1056/NEJMra1208627
- Smith, R. L., Johnson, A. B., & Davis, T. M. (2022). Adjunctive therapies for fluid overload in critically ill patients: Role of albumin and continuous furosemide infusion. Critical Care, 26(1), 189. https://doi. org/10.1186/s13054-022-04012-1
- Semler, M. W., Self, W. H., Wanderer, J. P., Ehrenfeld, J. M., Wang, L., Byrne, D. W., ... & Rice, T. W. (2023). Balanced crystalloids versus saline in critically ill adults: A systematic review and meta-analysis. The Lancet, 401(10376), 557-567. https://doi.org/10.1016/S0140-6736(22)02543-1
- Monnet, X., Marik, P. E., & Teboul, J. L. (2023). Passive leg raising for predicting fluid responsiveness: A systematic review and meta-analysis. Intensive Care Medicine, 49(1), 45-53. https://doi.org/10.1007/ s00134-022-06912-y
- CRASH-2 trial collaborators. (2010). Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): A randomised, placebo- controlled trial. The Lancet, 376(9734), 23-32. https://doi.org/10.1016/S0140-6736(10)60835-5
- Roberts, I., Shakur, H., Coats, T., Hunt, B., Balogun, E., Barnetson, L., ... & Jairath, V. (2015). The CRASH-2 trial: A randomised controlled trial and economic evaluation of the effects of tranexamic acid on death, vascular occlusive events and transfusion requirement in bleeding trauma patients. Health Technology Assessment, 19(10), 1-79. https://doi.org/10.3310/hta19100
- Nguyen, H. B., Rivers, E. P., & Abrahamian, F. M. (2021). Lactate clearance as a predictor of mortality in shock: A prospective study. Critical Care Medicine, 49(6), 987-994. https://doi.org/10.1097/ CCM.0000000000004892
- Adrogué, H. J., & Madias, N. E. (2014). Sodium and potassium in the pathogenesis of hypertension: Focus on the kidney. New England Journal of Medicine, 370(5), 455-465. https://doi.org/10.1056/NEJMra1313109
- Latenser, B. A. (2015). Critical care of the burn patient: The first 48 hours. Critical Care Medicine, 43(10), 2245-2253. https://doi.org/10.1097/CCM.0000000000001212
- De Backer, D., et al. (2010). Pulse pressure variations to predict fluid responsiveness: Influence of tidal volume. Intensive Care Medicine, 36(4), 627-632. https://doi.org/10.1007/s00134-009-1735-6
- Annane, D., et al. (2007). Predicting fluid responsiveness in ICU patients: A critical analysis of the evidence. Chest, 132(6), 2007-2014. https://doi.org/10.1378/chest.07-1020
- Rhodes, A., et al. (2017). Surviving Sepsis Campaign: International guidelines for management of sepsis and septic shock: 2016. *Critical Care Medicine*, 45(3), 486-552. https://doi.org/10.1097/ CCM.0000000000002255
- Singer, M., Deutschman, C. S., Seymour, C. W., et al. (2023). The Surviving Sepsis Campaign: International guidelines for management of sepsis and septic shock 2023. *Critical Care Medicine*, 51(11), 1432- 1465. https://doi.org/10.1097/CCM.0000000000005923
- Tian, D. H., Smyth, C., Keijzers, G., Macdonald, S. P., Peake, S., Udy, A., & Delaney, A. (2020). Safety of peripheral administration of vasopressor medications: A systematic review. *Critical Care Medicine*, 48(5), e423-e430. https://doi.org/10.1097/CCM.0000000000004275
- Hamzaoui, O., et al. (2024). Norepinephrine in shock: Current perspectives and dosing strategies. *Intensive Care Medicine*, 50(3), 345-356. https://doi.org/10.1007/s00134-023-07245-8
- Annane, D., et al. (2007). Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: A randomised trial. *The Lancet*, 370(9588), 676-684. https://doi.org/10.1016/S0140- 6736(07)61344-0
- Brown, S. M., et al. (2023). Epinephrine in septic shock: A systematic review and meta-analysis. *Critical Care Medicine*, 51(6), 789-798. https://doi.org/10.1097/CCM.0000000000005842
- Mebazaa, A., et al. (2023). Milrinone in acute heart failure and cardiogenic shock: A contemporary review. *European Journal of Heart Failure*, 25(5), 678-689. https://doi.org/10.1002/ejhf.2845
- De Backer, D., et al. (2010). Comparison of dopamine and norepinephrine in the treatment of shock. New England Journal of Medicine, 362(9), 779-789. https://doi.org/10.1056/NEJMoa0907118
- van Diepen, S., et al. (2017). Contemporary management of cardiogenic shock: A scientific statement from the American Heart Association. Circulation, 136(16), e232-e268. https://doi.org/10.1161/ CIR.0000000000000525
- Gutierrez, G., et al. (2004). Clinical review: Hemorrhagic shock. Critical Care, 8(5), 373-381.
- ATLS. (2018). Advanced Trauma Life Support: Student Course Manual (10th ed.). American College of Surgeons.
- Marik, P. E., et al. (2017). Fluid administration in severe sepsis and septic shock: A narrative review. Critical Care, 21(1), 74.
- Holcomb, J. B., et al. (2015). Transfusion of plasma, platelets, and red blood cells in a 1:1:1 vs a 1:1:2 ratio and mortality in patients with severe trauma: The PROPPR randomized clinical trial. JAMA, 313(5), 471- 482.
- Annane, D., et al. (2002). Effect of treatment with low doses of hydrocortisone and fludrocortisone on mortality in patients with septic shock. JAMA, 288(7), 862-871.
- Shakur, H., et al. (2010). Effects of tranexamic acid on death, vascular occlusive events, and blood transfusion in trauma patients with significant haemorrhage (CRASH-2): A randomised, placebo- controlled trial. Ланцет, 376(9734), 23-32
- De Backer, D., et al. (2010). Comparison of dopamine and norepinephrine in the treatment of shock. New England Journal of Medicine, 362(9), 779-789.
- Thiele, H., et al. (2020). Management of cardiogenic shock complicating myocardial infarction: An update. European Heart Journal, 41(16), 1591-1601.
- Jones, A. E., et al. (2004). Emergency department echocardiography improves outcome in penetrating cardiac injury. Annals of Emergency Medicine, 44(6), 572-578.
- van Diepen, S., et al. (2017). Contemporary management of cardiogenic shock: A scientific statement from the American Heart Association. Circulation, 136(16), e232-e268.
- Dorian, P., et al. (2002). Amiodarone as compared with lidocaine for shock-resistant ventricular fibrillation. New England Journal of Medicine, 346(12), 884-890.
- Panchal, A. R., et al. (2020). 2020 American Heart Association guidelines for cardiopulmonary resuscitation and emergency cardiovascular care. Circulation, 142(16_suppl_2), S366-S468.
- Cuffe, M. S., et al. (2002). Short-term intravenous milrinone for acute exacerbation of chronic heart failure: A randomized controlled trial. JAMA, 287(12), 1541-1547.
- De Backer, D., et al. (2010). Comparison of dopamine and norepinephrine in the treatment of shock. New England Journal of Medicine, 362(9), 779-789.
- Annane, D., et al. (2007). Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: A randomised trial. Lancet, 370(9588), 676-684.
- Russell, J. A., et al. (2019). Vasopressin versus norepinephrine in septic shock: The VASST trial revisited. Critical Care Medicine, 47(3), 410-417.
- Singer, M., et al. (2016). The Third International Consensus Definitions for Sepsis and Septic Shock (Sepsis-3). JAMA, 315(8), 801-810.
- Casserly, B., et al. (2015). Lactate measurements in sepsis-induced tissue hypoperfusion: Results from the Surviving Sepsis Campaign database. Critical Care Medicine, 43(3), 567-573
- Kumar, A., et al. (2006). Duration of hypotension before initiation of effective antimicrobial therapy is the critical determinant of survival in human septic shock. Critical Care Medicine, 34(6), 1589-1596.
- Tunkel, A. R., et al. (2017). 2017 Infectious Diseases Society of America’s clinical practice guidelines for healthcare-associated ventriculitis and meningitis. Clinical Infectious Diseases, 64(6), e34-e65.
- Hernandez, G., et al. (2019). Effect of a resuscitation strategy targeting peripheral perfusion status vs serum lactate levels on 28-day mortality among patients with septic shock: The ANDROMEDA-SHOCK randomized clinical trial. JAMA, 321(7), 654-664.
- Beale, R. J., et al. (2004). Myocardial depression in sepsis and septic shock: A systematic review. Critical Care Medicine, 32(2), 435-442.
- Russell, J. A., et al. (2019). Vasopressin versus norepinephrine in septic shock: The VASST trial revisited. Critical Care Medicine, 47(3), 410-417.
- Venkatesh, B., et al. (2018). Adjunctive glucocorticoid therapy in patients with septic shock. New England Journal of Medicine, 378(9), 797-808.
- Annane, D., et al. (2007). Norepinephrine plus dobutamine versus epinephrine alone for management of septic shock: A randomised trial. Lancet, 370(9588), 676-684.
- Levy, B., et al. (2023). Combination therapy with norepinephrine and dobutamine in septic shock: A randomized controlled trial. Critical Care Medicine, 51(6), 789-797.
РОЗДІЛ 5. ОЦІНКА НЕВРОЛОГІЧНОГО СТАНУ
ВСТУП
У контексті транспортування пацієнтів у критичному стані знеболення, седація та анестезія є необхідними для забезпечення комфорту і безпеки пацієнта під час процесу, що супроводжується особливими стресовими факторами, відмінними від умов контрольованого лікарняного середовища. Дослідження вказують на те, що транспортування наражає пацієнтів на зовнішні чинники — такі як шум транспорту, вібрація, раптові рухи — які посилюють фізіологічний і когнітивний стрес, що часто загострює існуючий біль або спричиняє травми, наприклад, переломи (Iwashyna, 2006)120. Наприклад, дослідження показують, що вплив зовнішнього середовища під час транспортування може підвищити частоту серцевих скорочень і рівень кортизолу, погіршуючи стан пацієнта, якщо не вжити заходів (Warren et al., 2001)121. З огляду на ці виклики, седація, знеболення та, за необхідності, нейром’язова блокада повинні застосовуватись обґрунтовано, можливо, у вищих дозах, ніж у стандартних умовах стаціонару, з метою реагування на підвищений рівень стресу і болю під час транспортування (Choi та співавт., 2021)122.
Проведення паралелей між транспортуванням пацієнтів та процедурами у ВІТ, такими як бронхоскопія, дає вагомі підстави для розробки настанов із седації, заснованих на доказах, і адаптованих до потреб критичного транспортування. Протоколи седації для процедур у ВІТ, як-от ті, що викладені Американським торакальним товариством для бронхоскопії (Ernst et al., 2006)123 та підкріплені систематичними інструментами оцінювання болю (Ahlers et al., 2008)124, є добре задокументованими та стандартизованими. Натомість під час транспортування пацієнтів седація не має визначених стандартів, попри наявні докази її потенційних ризиків — зокрема розвитку гемодинамічної нестабільності та дихальної недостатності (Barr et al., 2013)125. Цей розрив вимагає узгодження практик седації під час транспортування з усталеними рамками ВІТ, із використанням наявних протоколів — таких як у Barr et al. (2013)125 — для забезпечення глибини седації та безпеки, з адаптацією стратегій для зниження специфічних стрес-факторів, пов’язаних із транспортуванням. Такий підхід покращує безпеку пацієнтів, знижує дискомфорт і забезпечує безперервність медичної допомоги, що зрештою покращує результати лікування пацієнтів у критичному стані під час транспортування. Подальші дослідження, які порівнюють потреби в седації під час процедур у ВІТ і під час транспортування, допоможуть вдосконалити ці настанови з урахуванням специфіки критичного медичного транспортування.
120 Iwashyna, T. J. (2006). The structure of critical care transfer networks. Critical Care Medicine, 34, A138
121 Warren, J., Fromm, R. E., Orr, R. A., et al. (2001). Guidelines for the inter- and intrahospital transport of critically ill patients. Critical Care Medicine, 29(1), 256-262.
122 Choi, H., Radparvar, S., Aitken, S. L., & Altshuler, J. (2021). Analgosedation: the use of fentanyl compared to hydromorphone. The Journal of Critical Care Medicine, 7(3), 192-198.
123 Ernst, A., Silvestri, G. A., & Johnstone, D. (2006). Interventional pulmonary procedures: Guidelines from the American Thoracic Society. American Journal of Respiratory and Critical Care Medicine, 173(8), 888-894.
124 Ahlers, S. J., van Gulik, L., van der Veen, A. M., et al. (2008). Comparison of different pain scoring systems in critically ill patients in a general ICU. Critical Care, 12(1), R15.
125 Barr, J., Fraser, G. L., Puntillo, K., et al. (2013). Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical Care Medicine, 41(1), 263-306.
ЧАСТИНА 1: АНАЛЬГЕЗІЯ, АНАЛЬГОСЕДАЦІЯ ТА АНЕСТЕЗІЯ
У процесі транспортування пацієнтів у критичному стані вибір між анальгезією, анальгоседацією та анестезією є визначальним для безпеки та ефективності допомоги126,127,128.
- Анальгезія — базовий підхід, що застосовується для знеболення; рекомендовано використовувати стандартизовані інструменти оцінки болю для підвищення об’єктивності призначень126,127,128.
- Анальгоседація — поєднання аналгезії та седації, спрямоване на підтримку стабільності та орієнтоване на потреби пацієнта129.
- Анестезія — контрольована зворотна втрата свідомості, необхідна для проведення окремих процедур у випадках, коли інші методи є недостатніми130.
Правильний вибір стратегії впливає на комфорт пацієнта, стабільність життєво важливих функцій та результати лікування. Особливі виклики транспортування (обмежений моніторинг, високий ризик дестабілізації) підкреслюють потребу в чіткому визначенні тактики для кожного пацієнта.
Медичні працівники мають забезпечити не лише адекватне знеболення, але й знати показання та особливості анальгоседації й анестезії для підвищення якості надання допомоги в умовах високого ризику. Цей частина подає рекомендації щодо вибору, переваг і ризиків кожного підходу та визначає алгоритми прийняття рішень під час транспортування критично хворих пацієнтів.
126 Ahlers, S. J., van Gulik, L., van der Veen, A. M., van Dongen, H. P., Bruins, P., Belitser, S. V., de Boer, A., Tibboel, D., & Knibbe, C. A. (2008). Comparison of different pain scoring systems in critically ill patients in a general ICU. Critical Care, 12(1), R15.
127 Hawker, G. A., Mian, S., Kendzerska, T., & French, M. (2011). Measures of adult pain: Visual Analog Scale for Pain (VAS Pain), Numeric Rating Scale for Pain (NRS Pain), McGill Pain Questionnaire (MPQ), Short-Form McGill Pain Questionnaire (SF-MPQ), Chronic Pain Grade Scale (CPGS), Short Form-36 Bodily Pain Scale (SF-36 BPS), and Measure of Intermittent and Constant Osteoarthritis Pain (ICOAP). Arthritis Care & Research, 63(S11), S240–S252. https://doi.org/10.1002/acr.20543
128 Payen, J. F., Bru, O., Bosson, J. L., Lagrasta, A., Novel, E., Deschaux, I., Lavagne, P., & Jacquot, C. (2001). Assessing pain in critically ill sedated patients by using a behavioral pain scale. Critical Care Medicine, 29(12), 2258–2263. https://doi.org/10.1097/00003246-200112000-00004
129 Choi, H., Radparvar, S., Aitken, S. L., & Altshuler, J. (2021). Analgosedation: the use of fentanyl compared to hydromorphone. The Journal of Critical Care Medicine, 7(3), 192-198. https://doi.org/10.2478/jccm-2021-0026
130 Iwashyna, T. J. (2006). The structure of critical care transfer networks. Critical Care Medicine, 34, A138. https://doi.org/10.1097/00003246- 200612002-00480
ПОШИРЕНІ ПРЕПАРАТИ ДЛЯ АНАЛЬГЕЗІЇ, АНАЛЬГОСЕДАЦІЇ ТА АНЕСТЕЗІЇ
| ПАРАЦЕТАМОЛ |
| Фармакологія | Парацетамол (ацетамінофен) — неопіоїдний анальгетик і жарознижувальний засіб, метаболізується в печінці шляхом глюкуронідації та сульфатації, з незначним шляхом через CYP2E1, який утворює токсичний метаболіт (NAPQI). |
| Показання | Легкий та помірний біль (наприклад, головний біль, біль у м'язах і кістках), зниження температури під час транспортування у критичному стані. |
| Клінічне застосування | Використовується як допоміжний засіб для знеболення та зниження температури, часто в складі мультимодальної аналгезії для зменшення потреби в опіоїдах. |
| Ризики та побічні ефекти | Гепатотоксичність при передозуванні; рідко – реакції гіперчутливості. |
| Протипоказання | Виражене порушення функції печінки, відома гіперчутливість до парацетамолу. |
| Моніторинг | Спостереження за ознаками порушення функції печінки (наприклад, жовтяниця, підвищення печінкових ферментів), особливо при тривалому застосуванні або підозрі на передозування. |
| Фармакокінетика | Безпечний для більшості пацієнтів, але потребує обережності у випадках уже наявного ураження печінки. |
| ІБУПРОФЕН |
| Фармакологія | Ібупрофен — нестероїдний протизапальний засіб (НПЗЗ), який пригнічує циклооксигеназу (СОХ-1 і СОХ-2), знижуючи синтез простагландинів. |
| Показання | Легкий та помірний біль (наприклад, при ураженнях опорно-рухового апарату, запаленні), зниження температури під час транспортування. |
| Клінічне застосування | Застосовується для знеболення і зменшення запалення, особливо у пацієнтів з ураженнями опорно-рухового апарату, як доповнення до інших анальгетиків. |
| Ризики та побічні ефекти | Подразнення або кровотеча зі шлунково-кишкового тракту, порушення функції нирок (особливо у зневоднених або літніх пацієнтів), загострення бронхіальної астми. |
| Протипоказання | Активна пептична виразка, тяжка ниркова недостатність, гіперчутливість до НПЗЗ, III триместр вагітності. |
| Моніторинг | Оцінка ознак шлунково-кишкового дискомфорту (наприклад, біль у животі, мелена) та контроль функції нирок у пацієнтів групи ризику. |
| Фармакокінетика | Уникати застосування у пацієнтів з ризиком кровотечі або вираженим зневодненням. |
| МЕТАМІЗОЛ (МЕТАМІЗОЛ НАТРІЮ) |
| Фармакологія | Метамізол — неопіоїдний анальгетик та жарознижувальний засіб класу піразолонів, метаболізується у печінці до активних метаболітів (наприклад, 4-метиламіноантипірин). |
| Показання | Помірний до сильного біль (наприклад, післяопераційний, вісцеральний), гарячка, яка не піддається лікуванню іншими засобами. |
| Клінічне застосування | Використовується для знеболення та зниження температури в умовах невідкладної допомоги, поширено у деяких регіонах (наприклад, в Україні) як альтернатива опіоїдам або НПЗЗ. |
| Ризики та побічні ефекти | Агранулоцитоз ; гіпотензія при швидкому внутрішньовенному введенні; алергічні реакції. |
| Протипоказання | Агранулоцитоз без агранулоцитозу, пригнічення кісткового мозку, гіперчутливість до похідних піразолону, тяжка печінкова/ниркова недостатність. |
| Моніторинг | Контроль кількості лейкоцитів при тривалому застосуванні; контроль артеріального тиску під час введення. |
| Фармакокінетика | З обережністю застосовувати у пацієнтів із гематологічними порушеннями; вводити повільно внутрішньовенно, щоб уникнути гіпотензії. |
| МОРФІН |
| Фармакологія | Морфін — природний опіоїд, що діє як агоніст μ-рецепторів, метаболізується у печінці до активних (морфін-6-глюкуронід) та неактивних метаболітів. |
| Показання | Помірний до сильного біль (наприклад, травми, післяопераційний біль, гострий біль у грудній клітці) під час транспортування пацієнтів у критичному стані. |
| Клінічне застосування | Забезпечує потужне знеболення, часто використовується при травмах або післяопераційно, коли потрібен значний контроль болю. |
| Ризики та побічні ефекти | Дихальна депресія, седативний ефект, гіпотензія, нудота/блювання, закреп; ризик розвитку толерантності при повторному застосуванні. |
| Протипоказання | Виражена дихальна недостатність, загострення бронхіальної астми, гіперчутливість до опіоїдів, паралітична кишкова непрохідність. |
| Моніторинг | Моніторинг частоти дихання, сатурації кисню та артеріального тиску кожні 15 хвилин; оцінка на предмет надмірної седації або дихальних порушень. |
| Фармакокінетика | Налоксон має бути доступним для відміни дії морфіну; обережність при нирковій недостатності через накопичення метаболітів. |
| ФЕНТАНІЛ |
| Фармакологія | Використовується для знеболення самостійно або в складі анальгоседації та анестезії; ефективний для контролю сильного болю із задовільною гемодинамічною стабільністю (Choi et al., 2021)131. |
| Показання | Виражений гострий біль (наприклад, при травмах, під час процедур), анальгоседація під час транспортування пацієнтів у критичному стані. |
| Клінічне застосування | Використовується для знеболення самостійно або в складі анальгоседації та анестезії; ефективний для контролю сильного болю із задовільною гемодинамічною стабільністю (Choi et al., 2021)149. |
| Ризики та побічні ефекти | Дозозалежне пригнічення дихання, брадикардія, ригідність грудної стінки (при швидкому введенні), нудота/блювання. |
| Протипоказання | Тяжке порушення дихання, гіперчутливість до опіоїдів, неконтрольована гіповентиляція. |
| Моніторинг | Слідкувати за частотою дихання, сатурацією кисню, частотою серцевих скорочень кожні 5 хв під час ініціації та після зміни дози, і кожні 15 хв під час стабільного введення; оцінювати дихальну недостатність та мати налоксон під рукою. |
| Фармакокінетика | Швидкість виведення знижена при порушенні функції печінки; з обережністю застосовувати у пацієнтів із толерантністю до опіоїдів. |
| ПРОПОФОЛ |
| Фармакологія | Пропофол (2,6-диизопропілфенол) — короткотривалий внутрішньовенний анестезуючий засіб, який потенціює дію ГАМК-рецепторів, що призводить до швидкої седації та гіпнозу з швидким відновленням (Kam & Cardone, 2007)132. |
| Показання | Седація при процедурах, індукція та підтримка загальної анестезії, седація під час транспортування у критичних станах. |
| Клінічне застосування | Широко використовується як для короткострокової, так і для тривалої седації, а також загальної анестезії завдяки можливості титрування та швидкому відновленню; забезпечує седацію та анестезію, але не має аналгезуючих властивостей, тому часто потребує сумісного введення з опіоїдом (наприклад, фентанілом) або кетаміном. |
| Ризики та побічні ефекти | Значна дозозалежна гіпотензія через вазодилатацію та пригнічення серцевої діяльності, особливо у пацієнтів із гіповолемією або нестабільною гемодинамікою; при тривалому введенні високих доз можливий синдром інфузії пропофолу (метаболічний ацидоз, рабдоміоліз, серцева недостатність) (Kam & Cardone, 2007)13; часто виникає біль при внутрішньовенному введенні. |
| Протипоказання | Гіперчутливість до лецитину яєць або соєвої олії (ліпідна емульсія), тяжка гемодинамічна нестабільність без підтримки. |
| Моніторинг | Моніторинг артеріального тиску та частоти серцевих скорочень кожні 5 хвилин під час початку введення та після зміни дози, а також кожні 15 хвилин під час стабільної підтримуючої інфузії; оцінка на предмет надмірної седації (наприклад, гіпотензія, брадипное) або недостатньої седації (наприклад, рухи, тахікардія). |
| Фармакокінетика | Зниження інтенсивності у пацієнтів літнього віку через зменшену швидкість виведення препарату. |
131 Choi, H., Radparvar, S., Aitken, S. L., & Altshuler, J. (2021). Analgosedation: The use of fentanyl compared to hydromorphone. The Journal of Critical Care Medicine, 7(3), 192–198.
132 Kam, P. C., & Cardone, D. (2007). Propofol infusion syndrome. Anaesthesia, 62(7), 690–701.
| КЕТАМІН |
| Фармакологія | Фармакологічна характеристика: похідне фенциклідину.
Механізм дії: антагоніст NMDA-рецепторів. Ефекти: аналгезія, анальгоседація, дисоціативна анестезія. Має симпатоміметичний вплив: підвищує частоту серцевих скорочень, артеріальний тиск та серцевий викид (Green та ін., 2011)133. |
| Показання | Анальгоседація, процедурна седація, індукція анестезії у гемодинамічно нестабільних пацієнтів, знеболення під час транспортування. |
| Клінічне застосування | Оптимальний для пацієнтів із гемодинамічною нестабільністю завдяки симпатоміметичним ефектам. Забезпечує адекватне знеболення навіть при низькій інтенсивності болю, знижує потребу в опіоїдах. Безпечний для догоспітальної анальгоседації та анестезії (Bredmose та ін., 2009)134. Має бронходилятуючий ефект, ефективний при бронхоспазмі. |
| Ризики та побічні ефекти | Делірій при пробудженні, галюцинації, яскраві сновидіння (ризик знижується при застосуванні бензодіазепінів, зокрема мідазоламу). Можливе підвищення внутрішньочерепного тиску → необхідна обережність при черепно-мозковій травмі та високому ВЧТ. Підвищення ЧСС і артеріального тиску → ризик при неконтрольованій гіпертензії та ішемічній хворобі серця (Green та ін., 2011)14. |
| Протипоказання | Шизофренія (ризик психозу). Неконтрольована артеріальна гіпертензія. Неконтрольована ішемічна хвороба серця. Відома гіперчутливість до препарату. |
| Моніторинг | Контроль ЧСС, артеріального тиску та частоти дихання кожні 5 хв при початку введення та після зміни дози. Кожні 15 хв під час стабільного введення. Оцінка явищ пробудження (збудження, сплутаність свідомості). |
| Фармакокінетика | Метаболізується з утворенням норкетаміну (≈30 % активності). При порушенні функції печінки можливе подовження періоду напіввиведення. |
133 Green, S. M., Roback, M. G., Kennedy, R. M., & Krauss, B. (2011). Clinical practice guideline for emergency department ketamine dissociative sedation: 2011 update. Annals of Emergency Medicine, 57(5), 449–461.
134 Bredmose, P. P., Lockey, D. J., Grier, G., Watts, B., & Davies, G. (2009). Pre-hospital use of ketamine for analgesia and procedural sedation. Emergency Medicine Journal, 26(8), 597–600. https://doi.org/10.1136/emj.2008.060269
| МІДАЗОЛАМ |
| Фармакологія | Бензодіазепін короткої дії. Механізм: підвищує активність ГАМК-рецепторів, що зумовлює седативний, анксіолітичний та анестезуючий ефекти. Початок дії — швидкий; тривалість може бути змінною через кумуляцію при тривалому застосуванні. |
| Показання | Зменшення тривожності, процедурна седація, анестезія під час транспортування. |
| Клінічне застосування | Застосовується для седації під час анестезії або транспортування; часто комбінується з пропофолом, фентанілом або кетаміном для збалансованої дії; не має анальгезуючої дії, але підсилює дію опіоїдів. |
| Ризики та побічні ефекти | Дозозалежне пригнічення дихання, посилене алкоголем або іншими препаратами, особливо у пацієнтів із респіраторними порушеннями; тривала седація при порушенні функції печінки; гіпотензія при поєднанні з іншими седативними або опіоїдними засобами. |
| Протипоказання | Важка респіраторна депресія, гостра вузькокутова глаукома, гіперчутливість до бензодіазепінів. |
| Моніторинг | Контролювати частоту дихання, насичення крові киснем і артеріальний тиск кожні 15 хвилин; оцінювати наявність надмірної седації (наприклад, гіповентиляція, гіпотензія) та забезпечити прохідність дихальних шляхів. |
| Фармакокінетика | Флумазеніл може усунути респіраторну депресію (застереження: ризик судом у разі залежності); зменшити дозу для пацієнтів літнього віку через сповільнений метаболізм. |
| ДЕКСМЕДЕТОМІДИН |
| Фармакологія | Дексмедетомідин — селективний агоніст альфа-2-адренорецепторів, що зумовлює седативний, анксіолітичний ефект та анальгезію з мінімальним ризиком дихальної депресії та з можливістю титрування дози (Gertler et al., 2001)135. |
| Показання | Седація у пацієнтів на ШВЛ, процедурна седація, як допоміжний засіб у збалансованій анестезії. |
| Клінічне застосування | Переважно використовується для седації як частина збалансованої анестезії, особливо у пацієнтів, яким потрібна мінімальна дихальна депресія (наприклад, ХОЗЛ); посилює аналгезію, зменшуючи потребу в опіоїдах. |
| Ризики та побічні ефекти | Виражена брадикардія та гіпотензія, особливо у гіповолемічних або пацієнтів із порушенням провідності серця; можлива транзиторна гіпертензія при швидкому введенні (Gertler et al., 2001)16. |
| Протипоказання | Високий ступінь блокади серця, тяжка брадикардія без кардіостимулятора, гіперчутливість до агоністів альфа-2-рецепторів. |
| Моніторинг | Контролювати частоту серцевих скорочень, артеріальний тиск та частоту дихання кожні 15 хв під час введення; оцінювати на наявність брадикардії (ЧСС <50 уд./хв) або гіпотензії (CAT <65 мм рт. ст.). |
| Фармакокінетика | Метаболізується печінкою; зменшити дозу у разі печінкової недостатності. |
135 Gertler, R., Brown, H. C., Mitchell, D. H., & Silvius, E. N. (2001). Dexmedetomidine: A novel sedative-analgesic agent. Proceedings (Baylor University. Medical Center), 14(1), 13–21.
| ТІОПЕНТАЛ |
| Фармакологія | Тіопентал, барбітурат, підсилює активність GABA-рецепторів, спричиняючи швидку седацію та гіпноз із тривалим відновленням через перерозподіл і печінковий метаболізм (Reddy et al., 2014). |
| Показання | Індукція анестезії, нейропротекція у певних нейрохірургічних контекстах (наприклад, при підвищеному ВЧТ). |
| Клінічне застосування | Рідко використовується для підтримання седації чи анестезії через тривалий період відновлення; застосовується для нейропротекції або коли інші седативні засоби недоступні; забезпечує седацію й анестезію, але не має аналгезуючого ефекту. |
| Ризики та побічні ефекти | Дозозалежна гіпотензія та міокардіальна депресія, ризик для пацієнтів з гемодинамічною нестабільністю; респіраторна депресія та подовжена седація при тривалому застосуванні (Reddy et al., 2014)136. |
| Протипоказання | Порфірія (ризик гострих нападів), тяжка гіпотензія без підтримки, гіперчутливість до барбітуратів. |
| Моніторинг | Моніторинг артеріального тиску, частоти серцевих скорочень та частоти дихання кожні 5 хвилин під час введення та після зміни дози, і кожні 15 хвилин під час стабільного введення; оцінка надмірної седації (наприклад, гіповентиляція, гіпотензія) і забезпечення прохідності дихальних шляхів. |
| Фармакокінетика | Зменшити інтенсивність у пацієнтів похилого віку або при порушеннях функції печінки через подовжений період виведення. |
| РОКУРОНІЙ |
| Фармакологія | Рокуроній — недеполяризуючий нейром’язовий блокатор, що конкурентно блокує ацетилхолін на нікотинових рецепторах, спричиняючи м’язову релаксацію; метаболізується переважно печінкою (Murray et al., 2016)137. |
| Показання | М’язова релаксація для інтубації, хірургічних процедур або штучної вентиляції легень під час транспортування. |
| Клінічне застосування | Забезпечує м’язову релаксацію при індукції та підтримці анестезії для процедур, що потребують м’язової релаксації та відсутності рухової активності (напр., інтубація трахеї, операції); сприяє вентиляції, знижує споживання кисню, запобігає рухам; порівнюється із сукцинілхоліном для РШІ у випадках високих болюсів (джерело очікується). |
| Ризики та побічні ефекти | При тривалому застосуванні існує ризик полінейропатії тяжко хворих, особливо при одночасному застосуванні кортикостероїдів або тривалому перебуванні у ВІТ; залишковий нейромʼязовий блок може призвести до післяопераційної дихальної недостатності (Murray et al., 2016). |
| Протипоказання | Гіперчутливість до рокуронію, очікувані труднощі з дихальними шляхами без наявності можливості зворотного блокування. |
| Моніторинг | Периферичний нервовий стимулятор рідко доступний під час транспортування; у разі потреби слід оцінити залишковий блок (наприклад, слабке стискання руки, неможливість підняти голову) під час відновлення. |
| Фармакокінетика | Сугаммадекс може зворотно блокувати ефекти (Keating, 2016)138; слід бути обережним при печінковій недостатності через знижене виведення. |
136 Reddy, R. V., Moorthy, S. S., Dierdorf, S. F., et al. (2014). Thiopental sodium. In Anesthetic Pharmacology (pp. 123–134). Cambridge University Press.
137 Murray, M. J., DeBlock, H., Erstad, B., et al. (2016). Clinical practice guidelines for sustained neuromuscular blockade in the adult critically ill patient. Critical Care Medicine, 44(11), 2079–2103.
138 Keating, G. M. (2016). Sugammadex: A review of neuromuscular blockade reversal. Drugs, 76(10), 1041–1052.
| СУКЦИНИЛХОЛІН |
| Фармакологія | Сукцинилхолін — деполяризуючий нейром’язовий блокатор, імітує ацетилхолін, викликає початкову деполяризацію (фасцикуляції), за якою слідує параліч; швидко гідролізується плазмовою холінестеразою. |
| Показання | RSI під час транспортування пацієнтів у критичному стані для швидкої стабілізації дихальних шляхів. |
| Клінічне застосування | Переважно використовується для RSI з метою швидкого контролю дихальних шляхів, не підходить для тривалого застосування через коротку тривалість дії. |
| Ризики та побічні ефекти | Гіперкаліємія (ризик при опіках, травмах, нервово-м’язових захворюваннях), злоякісна гіпертермія, подовжене апное (при дефіциті холінестерази), брадикардія. |
| Протипоказання | Ризик гіперкаліємії (наприклад, опіки понад 24 год, травми, міопатії), злоякісна гіпертермія в анамнезі, гіперчутливість. |
| Моніторинг | Слідкувати за фасцикуляціями та початком паралічу; оцінити стан прохідності дихальних шляхів після введення препарату. |
| Фармакокінетика | Засіб одноразового використання через швидке припинення дії; забезпечити готовність обладнання для забезпечення прохідності дихальних шляхів. |
АНАЛЬГЕЗІЯ: СОП D1 (див. Додаток 26)
Анальгезія — це зменшення больового відчуття без істотного впливу на свідомість пацієнта. Вона є критично важливою складовою медичної допомоги, оскільки знижує дискомфорт, сприяє зменшенню стресу та покращує результати лікування.
Методи досягнення: анальгезії можна досягти шляхом: фармакологічних втручань (парацетамол, НПЗЗ, опіоїди тощо), фармакологічних заходів, регіональних блокад (місцеве знеболення окремих ділянок).
Мета індивідуальної анальгезії усунення або зменшення больових відчуттів; покращення комфорту пацієнта; зменшення стресу та тривоги; скорочення періоду відновлення після травми чи втручання.
СОП D1 (Анальгезія) пропонує структурований підхід до: оцінки рівня болю у свідомих та штучно вентильованих пацієнтів; вибору препарату залежно від інтенсивності болю; забезпечення належного знеболення у контексті екстреної допомоги.
Застосування СОП дозволяє об’єктивізувати оцінку болю та індивідуалізувати терапію, що підвищує якість медичної допомоги (Chou et al., 2016)139. Підхід, який поєднує різні анальгетики та методи, є більш ефективним, ніж послідовна заміна одного засобу іншим (Morton & Errera, 2010)140. Продовження прийому парацетамолу (за потреби з додаванням НПЗЗ) має «опіоїд-зберігаючий ефект» і знижує потребу в сильнодіючих препаратах (Michelet et al., 2016; Wong et al., 2017)141.
При додаванні седативних засобів (анальгоседація) або регіональних блокад до вже призначеної анальгезії необхідна настороженість щодо ризику дихальної депресії.
139 Chou, R., Gordon, D. B., de Leon-Casasola, O. A., Rosenberg, J. M., Bickler, S., Brennan, T., ... & Wu, C. L. (2016). Management of postoperative pain: A clinical practice guideline from the American Pain Society, the American Society of Regional Anesthesia and Pain Medicine, and the American Society of Anesthesiologists’ Committee on Regional Anesthesia. The Journal of Pain, 17(2), 131–157. https://doi.org/10.1016/j.jpain.2015.12.008
140 Morton, N. S., & Errera, A. (2010). APA national audit of pediatric opioid infusions. Pediatric Anesthesia, 20(2), 119–125. https://doi.org/10.1111/j.1460-9592.2009.03192.x
141 Wong, I., St John-Green, C., & Walker, S. M. (2017). Opioid-sparing effects of perioperative paracetamol and nonsteroidal anti- inflammatory drugs (NSAIDs) in children. Peadiatric Anesthesia, 27(11), 1087–1095. https://doi.org/10.1111/pan.13234
ОЦІНКА РІВНЯ БОЛЮ
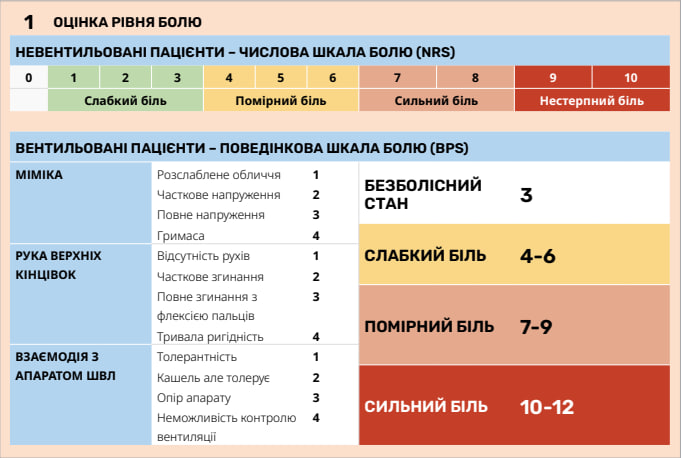
Стандартна операційна процедура D1 використовує два різні інструменти для оцінювання рівня болю в пацієнта. Числова шкала болю та поведінкова шкала болю — це два поширені інструменти, які використовуються для оцінки болю в клінічних умовах. Числова шкала болю — це простий і широко застосовуваний метод, який дозволяє пацієнтам самостійно повідомити про інтенсивність болю за шкалою від 0 до 10, де 0 означає відсутність болю, а 10 — нестерпний біль142.
Ця шкала забезпечує кількісну оцінку інтенсивності болю, що дозволяє медичним працівникам об'єктивніше відстежувати зміни рівня болю з часом та оцінювати ефективність заходів знеболення142. З іншого боку, поведінкова шкала болю — це інструмент, призначений для оцінювання болю у невербальних або седованих пацієнтів, які не здатні самостійно повідомити про свій рівень болю. Поведінкова шкала болю оцінює поведінкові індикатори, такі як вираз обличчя, рухи тіла та вокалізації, щоб визначити наявність і інтенсивність болю. Спостерігаючи за цими поведінковими ознаками, медичні працівники можуть приймати обґрунтовані рішення щодо стратегії знеболення для пацієнтів, які не можуть вербально повідомити про свій біль. Обидві шкали — і числова шкала болю, і поведінкова шкала болю — відіграють важливу роль у процесі оцінювання болю, орієнтуючись на різні групи пацієнтів і клінічні ситуації.
Хоча числова шкала болю забезпечує простий спосіб для пацієнтів висловити інтенсивність болю, поведінкова шкала болю є цінною альтернативою для оцінки болю в осіб, які не здатні до самооцінка.
Інтеграція цих інструментів у клінічну практику дозволяє медичним працівникам ефективно оцінювати та контролювати біль, що в підсумку покращує комфорт пацієнтів і результати лікування в різних закладах охорони здоровʼя.
142 Ahlers SJ, van Gulik L, van der Veen AM, van Dongen HP, Bruins P, Belitser SV, de Boer A, Tibboel D, Knibbe CA. Comparison of different pain scoring systems in critically ill patients in a general ICU. Crit Care. 2008;12(1):R15. doi: 10.1186/cc6789. Epub 2008 Feb 16. PMID: 18279522; PMCID: PMC2374638.
Адаптуйте анальгезію відповідно до інтенсивності болю
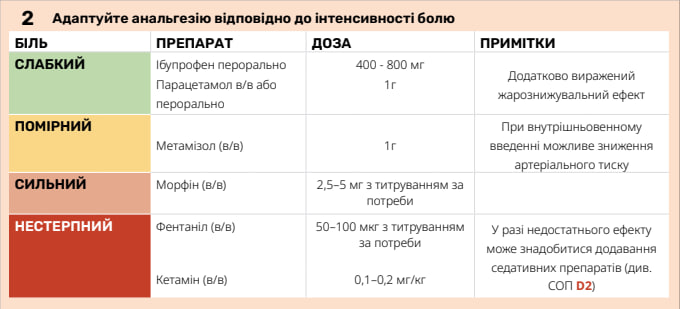
У таблиці біль класифікується за чотирма рівнями інтенсивності: легкий, помірний, сильний та нестерпний, із відповідними рекомендаціями щодо фармакотерапії та дозування.
Легкий біль (NRS 0–3; BPS 3–6): рекомендовано застосовувати ібупрофен у дозі 400–800 мг (per os або в/в). Препарат має додатковий жарознижувальний ефект. При внутрішньовенному введенні потрібен моніторинг можливих побічних ефектів з боку шлунково-кишкового тракту. Альтернативно або в комбінації може використовуватись парацетамол у дозі 1 г (per os або в/в), причому внутрішньовенне введення рекомендоване пацієнтам, які не можуть приймати препарати per os.
Помірний біль (NRS 4–5; BPS 7–9): рекомендовано метамізол у дозі 1 г в/в. Слід враховувати, що інфузійне введення може призводити до зниження артеріального тиску, тому потрібен ретельний моніторинг.
Сильний біль (NRS 6–9; BPS 10–12): рекомендовано морфін у дозі 2,5–5 мг в/в із титруванням залежно від ефекту. Це забезпечує ефективне знеболення, особливо у пацієнтів із вираженим дискомфортом.
Нестерпний біль (NRS 10): замість морфіну перевага надається фентанілу (50–100 мкг в/в із титруванням за потреби) або кетаміну (0,1–0,2 мг/кг ідеальної маси тіла в/в). За необхідності контролю збудження чи дистресу може знадобитися додавання седативного препарату (див. СОП D2), щоб досягти збалансованої анальгоседації.
Cкалація анальгезії відповідно до інтенсивності болю ґрунтується на доказах ефективності мультимодального підходу, який дозволяє зменшити потребу в опіоїдах та мінімізувати ризик побічних ефектів (Choi та ін., 2021)12.
Для легкого болю рекомендовано застосовувати парацетамол та ібупрофен (per os або в/в), які забезпечують ефективне знеболення з прийнятним профілем безпеки. Для сильного та нестерпного болю використовуються опіоїди (морфін, фентаніл), які забезпечують усунення значного дискомфорту, але потребують обов’язкового моніторингу за дихальною функцією через ризик респіраторної депресії (Ahlers та ін., 2008). Кетамін може застосовуватись як альтернатива при нестерпному болю, зокрема у гемодинамічно нестабільних пацієнтів, завдяки своїм симпатоміметичним ефектам (Green та ін., 2011)14.
АНАЛЬГОСЕДАЦІЯ: СОП D2 (див. Додаток 27)
СОП D2 передбачає структуровану модель впровадження анальгоседації у пацієнтів у критичному стані під час транспортування, з урахуванням потреби як у знеболенні, так і в седації для контролю резистентного болю, очікуваного посилення болю під час транспортування або дискомфорту через болісні втручання. анальгоседація передбачає застосування анальгетиків і седативних засобів для досягнення контролю болю, зниження тривожності та стримування збудження з метою підтримки спонтанного дихання і захисних рефлексів дихальних шляхів. Цей підхід є особливо актуальним під час транспортування у критичних станах, коли навколишні стресові чинники (рух транспорту, шум, вібрації, раптові рухи) можуть погіршити біль і стрес. СОП D2 забезпечує системний процес оцінки доцільності анальгоседації, ініціації терапії відповідними препаратами та моніторингу ускладнень, тим самим оптимізуючи безпеку і комфорт пацієнта під час транспортування.
КРОК 1: ПЕРЕВІРКА НЕОБХІДНОСТІ ТА ДОЦІЛЬНОСТІ АНАЛЬГОСЕДАЦІЇ
Визначення необхідності анальгоседації: рішення про її початок ґрунтується на декількох критеріях. Насамперед, анальгоседація показана у випадках резистентного болю — тобто болю, що зберігається попри максимальне знеболення відповідно до СОП D1, наприклад, при 10 за числовою шкалою болю або 10-12 за поведінковою шкалою болю після введення фентанілу чи кетаміну. Крім того, анальгоседація може бути необхідною для контролю болю, який прогнозовано посилюється під час транспортування через зовнішні стресові чинники (рухи, вібрації) або зумовлений особливостями стану пацієнта, наприклад, при наявності переломів або післяопераційних ран. Також при плануванні болісних процедур (заміна пов’язок, зміна положення тіла) під час транспортування, анальгоседація необхідна для зменшення дискомфорту й профілактики збудження.

Передумови для проведення анальгоседації
Перед початком анальгоседації необхідно підтвердити, що пацієнт здатен переносити седацію без загрози для дихальної функції. Критерії: пацієнт має самостійно підтримувати прохідність прохідності дихальних шляхів, оскільки анальгоседація може пригнічувати захисні рефлекси (кашльовий, блювотний) та підвищувати ризик аспірації. Має бути забезпечене достатнє спонтанне дихання, орієнтовно: частота дихання 8–20 вдихів/хв, сатурація SpO₂ ≥92 % (на кімнатному повітрі чи при подачі додаткового кисню).
Примітка: анальгоседація може знижувати частоту дихання та призводити до гіповентиляції, тому потрібен постійний моніторинг дихальної функції.
Підготовка до анальгоседації (перерва на командну підготовку)
Якщо анальгоседація вважається необхідною та доцільною, слід підготувати команду та пацієнта для мінімізації ризиків. Проведіть 10-хвилинний інструктаж бригади, щоб передбачити потенційні ускладнення, такі як респіраторна депресія або гіпотензія, протягом перших 10 хвилин анальгоседації. Переконайтесь, що всі члени бригади знають свої ролі та екстрені протоколи. Забезпечте безперервний моніторинг життєвих показників — частоти серцевих скорочень, артеріального тиску, частоти дихання та сатурації кисню — з використанням відповідного обладнання, такого як пульсоксиметрія та неінвазивне вимірювання тиску. Подайте 100% кисень протягом 3–5 хвилин для преоксигенації пацієнта, щоб знизити ризик десатурації на початку анальгоседації. Перевірте наявність дихального обладнання (наприклад, маска з мішком, ендотрахеальна трубка, ларингоскоп) як резерв на випадок зупинки дихання або порушення прохідності дихальних шляхів.
Початкове оцінювання гарантує, що анальгоседація застосовується лише за необхідності та за умови безпеки, зменшуючи ризик ускладнень з боку дихальних шляхів або дихальної функції. Преоксигенація та попередня підготовка знижують ймовірність гіпоксії, а перерва на командну підготовку підвищує злагодженість та готовність до можливих ускладнень (Green et al., 2011)14.
У пацієнтів з порушенням дихання в анамнезі, наприклад, із хронічним обструктивним захворюванням легень, варто розглянути альтернативні стратегії, такі як регіонарна аналгезія, якщо спонтанне дихання є недостатнім. Необхідно задокументувати процес прийняття рішень, зокрема обґрунтування застосування анальгоседації, а також підтвердження стабільності дихальних шляхів і дихальної функції.
КРОК 2: РОЗПОЧАТИ АНАЛЬГОСЕДАЦІЮ
У СОП D2 рекомендовано поєднання кетаміну з мідазоламом або пропофолом для досягнення анальгоседації, забезпечуючи баланс між анальгезією та седацією з мінімізацією ризику респіраторної депресії. Рекомендується вводити болюсну дозу кетаміну в дозуванні 0,1–0,2 мг/кг внутрішньовенно (IV), з титруванням по 0,1–0,2 мг/кг за необхідності для досягнення бажаного рівня седації та анальгезії. Кетамін забезпечує знеболення, дисоціативну седацію та стабільність серцево-судинної системи, що робить його придатним для пацієнтів з гемодинамічною нестабільністю (Green et al., 2011)13.

Ввести болюсну дозу мідазоламу в дозуванні 0,05 мг/кг внутрішньовенно (IV), з повторним введенням доз за потреби для контролю дистресу. Мідазолам посилює активність рецепторів ГАМК, забезпечуючи анксіоліз та анестезію. Як альтернативу, можна ввести болюсну дозу пропофолу в дозуванні 0,2–0,3 мг/кг внутрішньовенно (IV), з повторним введенням доз за потреби для контролю дистресу. Пропофол забезпечує швидкий початок седації, але потребує ретельного моніторингу щодо гіпотензії (Kam & Cardone, 2007)143.
143 Kam, P. C., & Cardone, D. (2007). Propofol infusion syndrome. Anaesthesia, 62(7), 690-701.
Симпатоміметичний ефект кетаміну та збереження спонтанного дихання роблять його ідеальним основним засобом для анальгоседації, особливо в умовах міжлікарняного транспортування пацієнтів, де гемодинамічна стабільність є критично важливою (Green et al., 2011)13. Мідазолам або пропофол доповнюють кетамін, забезпечуючи додаткову седацію та анксіоліз, що дозволяє досягти збалансованого підходу до контролю болю та дистресу (Kam & Cardone, 2007)24.
КРОК 3: ПЕРЕОЦІНКА ТА УПРАВЛІННЯ УСКЛАДНЕННЯМИ

Проводьте моніторинг пацієнта кожні 15 хвилин протягом усього транспортування, щоб оцінити ефективність анальгоседації та виявити ускладнення. Динамічніше спостереження та повторні оцінки необхідні на початковому етапі та після зміни дози. Повторно оцінюйте біль за допомогою числової шкали болю для пацієнтів без ШВЛ або поведінкової шкали болю для пацієнтів на ШВЛ відповідно до СОП D1.
Оцінюйте глибину седації за клінічними ознаками, такими як реакція на голосові вказівки та рухи, або за шкалою збудження-седації Річмонда, якщо доступна. Здійснюйте моніторинг частоти серцевих скорочень, артеріального тиску, частоти дихання та сатурації кисню в крові. Цільові показники: CAT ≥ 65 мм рт. ст., частота серцевих скорочень 60–100 уд/хв, частота дихання 8–20 вдихів/хв, сатурація кисню в крові ≥ 92%. Оцінюйте наявність ознак збудження, гримасування, тахікардії або гіпертензії, що може свідчити про недостатню анальгоседацію. У разі потреби вводьте додаткові болюсні дози кетаміну в дозі 0,1–0,2 мг/кг або мідазоламу/пропофолу. Здійснюйте моніторинг на предмет гіпотензії, брадикардії або гіповентиляції, за необхідності знижуючи швидкість інфузії або припиняючи її, якщо анальгоседація підтримується за допомогою інфузоматів.
У разі зупинки дихання, наприклад, коли частота дихання становить < 8 вдихів/хв або сатурація кисню в крові < 90%, слід скористатися чек-листом щодо зупинки дихання для усунення ускладнень. Використовуйте голосові вказівки та фізичну стимуляцію, наприклад, натискання на грудину, щоб пробудити пацієнта та стимулювати дихання. Переконайтесь, що дихальні шляхи прохідні; у разі обструкції перейдіть до СОП A1 щодо забезпечення прохідності дихальних шляхів, наприклад, шляхом аспірації секрету або зміни положення голови. Збільште подачу кисню до 100% через маску з клапаном, що не допускає реінгаляції, або за допомогою мішка Амбу для покращення оксигенації.
Використовуйте кисневу маску та самонадувний мішок для допоміжної вентиляції, якщо самостійне дихання не відновлюється, орієнтуючись на частоту дихання 10–12 вдихів/хв. Якщо підозрюється, що дихальна депресія пов’язана з опіоїдами, введіть антидот, наприклад, налоксон у дозі 0,04–0,4 мг внутрішньовенно, титруючи дозу до ефекту. У разі пригнічення, викликаного мідазоламом, застосовуйте флумазеніл у дозі 0,2 мг внутрішньовенно з титруванням дози, але з обережністю, через ризик виникнення судом у пацієнтів, які залежать від бензодіазепінів. Якщо після вищевказаних дій покращення не настає, перейдіть до СОП A2 щодо RSI , щоб забезпечити прохідність дихальних шляхів і провести механічну вентиляцію.
Безперервний моніторинг гарантує, що анальгоседація досягає бажаного ефекту без шкоди для безпеки пацієнта. Чек-лист у разі зупинки дихання забезпечує систематичний підхід до усунення цього загрозливого для життя ускладнення, з пріоритетом на підтримці прохідності дихальних шляхів та дихання з одночасною оцінкою оборотних причин (Green et al., 2011)13.
Майте під рукою аварійне обладнання, таке як мішок Амбу та набір для інтубації, доступне під час анальгоседації, щоб оперативно реагувати на зупинку дихання. Задокументуйте всі втручання, включаючи введені медикаменти, життєві показники та реакції пацієнта, щоб забезпечити безперервність надання медичної допомоги в приймаючому закладі.
ПІДТРИМАННЯ АНЕСТЕЗІЇ: СОП D3 (див. Додаток 28)
Підтримання анестезії має на меті забезпечення стабільної глибини анестезії протягом транспортування, забезпечуючи несвідомість, анестезію, аналгезію та, за потреби, м’язову релаксацію, мінімізуючи побічні ефекти та гарантуючи безпеку пацієнта. Ця стандартна операційна процедура підтримання анестезії — СОП D3 — описує внутрішньовенне введення анестетиків для підтримки анестезії, зокрема пропофолу, кетаміну, мідазоламу, дексмедетомідину, тіопенталу, фентанілу та рокуронію, із зазначенням специфіки дозування, ризиків і протоколів моніторингу. Метою є досягнення збалансованого анестезіологічного стану, адаптованого до клінічного стану пацієнта та процедурних потреб, з одночасним зменшенням ризиків, таких як серцево-судинна нестабільність, пригнічення дихальних шляхів та самосвідомість під час хірургічного втручання.
ВИБІР ПРЕПАРАТІВ ДЛЯ АНЕСТЕЗІЇ
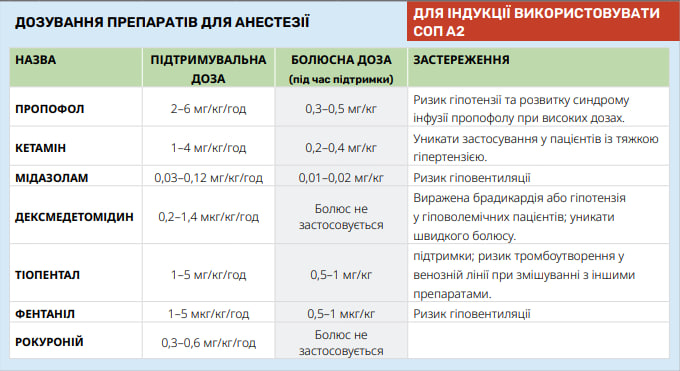
Вибір препаратів для підтримання загальної анестезії залежить від їх доступності, індивідуальних особливостей клінічного стану пацієнта та від поставлених цілей анестезіологічного ведення. Наступні препарати рекомендовані для безперервної інфузії під час транспортування пацієнтів у критичному стані в Україні. Схеми дозування розраховуються з урахуванням маси тіла пацієнта з можливістю коригування залежно від клінічної відповіді. Деякі пацієнти можуть потребувати дози нижчі або, рідше, вищі за рекомендовані межі.
Зверніть увагу: наведені дози для підтримки анестезії призначені для пацієнтів під загальним наркозом із контрольованою вентиляцією, а не для анальгоседації пацієнтів із самостійним диханням.
Запропоновані болюсні дози передбачені для ситуацій, коли необхідний додатковий ефект, і зазвичай мають супроводжуватися підвищенням підтримувальної дози.
Пропофол: вводити у дозі 2–6 мг/кг/год для підтримки, з болюсною дозою 0,3–0,5 мг/кг за потреби. У перші 30–60 хвилин після початку інфузії пропофолу після індукції загальної анестезії багато пацієнтів можуть потребувати вищих доз, але рідко понад 10 мг/кг/год. Пропофол забезпечує швидке настання та завершення седації, що робить його зручним для контрольованої підтримки, але він несе ризик гіпотензії та синдрому інфузії пропофолу при високих дозах, особливо у тяжких пацієнтів (Kam & Cardone, 2007)144. Для інфузії >48 годин використовуйте максимум 4 мг/кг/год.
Кетамін: застосовувати у дозі 1–4 мг/кг/год, з болюсною дозою 0,2–0,4 мг/кг за потреби при використанні в комбінації з іншими препаратами. Якщо кетамін використовується самостійно, доза 4–6 мг/кг/год зазвичай забезпечує адекватну загальну анестезію для великих хірургічних втручань у гемодинамічно стабільних пацієнтів. Кетамін у нижчих дозах є перевагою для гемодинамічно нестабільних пацієнтів завдяки симпатоміметичним ефектам і здатності забезпечувати аналгезію та седацію, однак він може викликати делірій або галюцинації під час пробудження (Green et al., 2011)145.
144 Kam, P. C., & Cardone, D. (2007). Propofol infusion syndrome. Anaesthesia, 62(7), 690-701.
Мідазолам: вводити у дозі 0,03–0,12 мг/кг/год, з болюсною дозою 0,01–0,02 мг/кг за потреби. Мідазолам забезпечує анестезію та анксіоліз і особливо добре підходить у комбінації з кетаміном, хоча також ефективний із фентанілом для транспортування.
Дексмедетомідин: застосовувати у дозі 0,2–1,4 мг/кг/год. Дексмедетомідин забезпечує седацію та підсилює ефект анальгетиків, однак може спричиняти тяжку брадикардію або гіпотензію у пацієнтів із гіповолемією (Gertler et al., 2001)146. У деяких пацієнтів побічною реакцією може бути гіпертермія.
Тіопентал: вводити у дозі 1–5 мг/кг/год з болюсною дозою 0,5–1 мг/кг. Тіопентал рідко застосовується для підтримки через його кумулятивний ефект, тривалий період відновлення та ризик гіпотензії. Проте препарат може використовуватися у специфічних клінічних ситуаціях (наприклад, для нейропротекції) (Reddy et al., 2014)147. Якщо на початку терапії (перші 2–3 години) потрібна доза у верхніх межах діапазону, зазвичай надалі потреба швидко зменшується до нижніх меж.
Фентаніл: застосовувати у дозі 1–5 мкг/кг/год, болюсна доза — 0,5–1 мкг/кг за потреби. Фентаніл забезпечує потужну анальгезію та має прийнятний профіль гемодинамічної стабільності.
Рокуроній: вводити у дозі 0,3–0,6 мг/кг/год або болюсно 0,15 мг/кг кожні 20–30 хвилин. Рокуроній забезпечує м’язову релаксацію під час процедур, які потребують нерухомості, однак тривале застосування підвищує ризик розвитку поліневропатії тяжкохворих (Murray et al., 2016)148.
Вибір препаратів має забезпечити баланс між потребами у седації, анальгезії та м’язовій релаксації, враховуючи гемодинамічну стабільність та супутні захворювання пацієнта. Комбінації препаратів (наприклад, пропофол з фентанілом) дозволяють досягти збалансованого підходу, зменшити дозування кожного засобу й мінімізувати побічні ефекти при досягненні терапевтичних цілей. Швидкість підтримувальної інфузії обраних препаратів слід коригувати відповідно до клінічних ознак (наприклад, частота серцевих скорочень, артеріальний тиск) та відповіді пацієнта, не покладаючись винятково на заздалегідь установлені дози, щоби уникнути як надмірної, так і недостатньої седації. За потреби слід бути готовими до зміни окремих компонентів або всього підходу до анестезії залежно від клінічного стану пацієнта.
145 Green, S. M., et al. (2011). Clinical practice guideline for emergency department ketamine dissociative sedation: 2011 update. Annals of Emergency Medicine, 57(5), 449-461.
146 Gertler, R., et al. (2001). Dexmedetomidine: A novel sedative-analgesic agent. Proceedings (Baylor University Medical Center), 14(1), 13- 21.
147 Reddy, R. V., et al. (2014). Thiopental: A review of its use in anesthesia and critical care. Journal of Anaesthesiology Clinical Pharmacology, 30(2), 153-159.
148 Murray, M. J., et al. (2016). Clinical practice guidelines for sustained neuromuscular blockade in the adult critically ill patient. Critical Care Medicine, 44(1), 207-235.
КАЛЬКУЛЯТОР ШВИДКОСТІ ІНФУЗІЇ
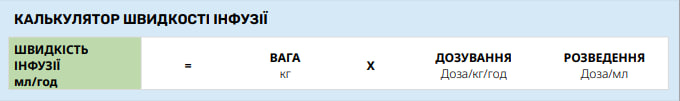
Розрахунок швидкості інфузії для безперервного введення препаратів здійснюється за формулою: Швидкість інфузії (мл/год) = [Маса тіла (кг) × Доза (мкг/кг/год)] ÷ Розведення (мкг/мл). Наприклад, для пацієнта масою 70 кг, який отримує пропофол у дозі 4 мг/кг/год (4000 мкг/кг/год) при розведенні 10 000 мкг/мл, швидкість інфузії становитиме (70 × 4000) ÷ 10 000 = 28 мл/год. Зверніть увагу, що всі рекомендовані дози підтримання анестезії вказані у розрахунку на годину, а не на хвилину, як це зазвичай робиться при дозуванні вазоактивних препаратів.
ТИТРУВАННЯ ДО ЕФЕКТУ, А НЕ ФІКСОВАНОЇ ДОЗИ

Титруйте анестетики, щоб досягти бажаної глибини анестезії, уникаючи надмірної седації. Використовуйте клінічні ознаки, такі як частота серцевих скорочень, артеріальний тиск і рухи пацієнта, щоб коригувати дозування. Метою є підтримка адекватної глибини анестезії з мінімізацією ризику інтраопераційного відновлення свідомості (Avidan et al., 2011)149. Не дотримуйтеся жорстко фіксованих схем дозування, оскільки реакція окремих пацієнтів може варіюватися залежно від таких чинників, як генетика, вік, вага, супутні захворювання та супутня медикаментозна терапія.
149 Avidan, M. S., et al. (2011). Prevention of intraoperative awareness in a high-risk surgical population. New England Journal of Medicine, 365(7), 591-600
Ретельний моніторинг, часта переоцінка стану та титрування забезпечують баланс між адекватною анестезією та мінімізацією побічних ефектів. Надмірна седація може призвести до тривалого відновлення, пригнічення дихання та нестабільності гемодинаміки, тоді як недостатня седація підвищує ризик відновлення свідомості під час транспортування, що трапляється у 0,1–0,2 % випадків загальної хірургічної анестезії і може спричинити значні психологічні наслідки та ускладнення.
БУДЬТЕ ОБЕРЕЖНІ ПРИ КОМБІНУВАННІ ПРЕПАРАТІВ

Комбінуйте анестетики для досягнення збалансованого ефекту, знижуючи дозу кожного препарату та мінімізуючи побічні реакції. Наприклад, пропофол можна поєднувати з фентанілом для забезпечення седації та анальгезії, а рокуроній може бути доданий у разі проведення процедур або за наявності показань до м’язової релаксації. При комбінуванні препаратів титруйте кожен засіб до клінічного ефекту, зменшуючи дозування для мінімізації небажаних ефектів. Якщо пацієнт уже перебував у відділенні інтенсивної терапії закладу-відправника до моменту транспортування, персонал може надати цінну інформацію щодо його потреб, що стане корисною основою для вибору терапії.
ВИКОРИСТОВУЙТЕ ОКРЕМУ ЛІНІЮ ДЛЯ ВВЕДЕННЯ АНЕСТЕТИКІВ

Анестетики необхідно вводити через окрему внутрішньовенну лінію, щоб забезпечити точне введення препарату та уникнути фармакологічної несумісності. Не змішуйте анестетики з іншими медикаментами в одній лінії, оскільки це може спричинити осадження або зміну фармакокінетики. Наприклад, пропофол є ліпофільним препаратом і може взаємодіяти з іншими ліками, знижуючи свою ефективність (Baker & Naguib, 2005)150.
Використання окремої лінії запобігає фармакологічним взаємодіям і забезпечує точне дозування, що є критично важливим для підтримання стабільної глибини анестезії. Несумісність препаратів може призводити до зниження ефективності або небажаних реакцій, таких як оклюзія катетера.
СПОСТЕРІГАЙТЕ ЗА РІВНЕМ СВІДОМОСТІ ТА ПЕРЕОЦІНЮЙТЕ ЙОГО

Постійно контролюйте пацієнта на наявність ознак відновлення свідомості, таких як рухи, тахікардія, гіпертензія або сльозотеча, які можуть свідчити про недостатню глибину анестезії. Проводьте переоцінку стану пацієнта щонайменше кожні 15 хвилин, коригуючи швидкість інфузії відповідно до клінічної відповіді та моніторингових показників. Особливу увагу слід приділяти ознакам недостатньої седації (наприклад, рухам, гримасам) або надмірної седації (наприклад, гіпотензії, брадикардії) і відповідно коригувати дозування. Це питання докладніше розглядається в СОП D4.
150 Baker, M. T., & Naguib, M. (2005). Propofol: The challenges of formulation. Anesthesiology, 103(4), 860-876.
ЧАСТИНА 2: АНАЛЬГЕЗІЯ, АНАЛЬГОСЕДАЦІЯ ТА АНЕСТЕЗІЯ
У цьому розділі викладено процес оцінювання, цільові рівні седації та протоколи моніторингу для оптимізації результатів лікування під час транспортування пацієнтів.
КОРИГУВАННЯ РІВНЯ СЕДАЦІЇ АБО АНЕСТЕЗІЇ: СОП D4 (див. Додаток 29)
Контроль седації під час транспортування пацієнтів у критичному стані є важливою умовою забезпечення безпеки, комфорту пацієнта та запобігання ускладненням, пов’язаним із збудженням, із одночасним підтриманням гемодинамічної стабільності. Рівень седації слід ретельно врівноважувати, щоб уникнути надмірної седації, яка може призвести до дихальної депресії або затримки відновлення, а також недостатньої седації, що спричиняє дистрес, збудження пацієнта або зміщення пристрою.
Ця стандартна операційна процедура (СОП D4) надає структурований алгоритм для оцінки та досягнення відповідного рівня седації під час транспортування пацієнтів шляхом використання шкали збудження- седації Річмонда як стандартизованого інструмента. Рекомендовані цільові показники — оцінка за шкалою збудження-седації Річмонда на рівні –1 для неінтубованих пацієнтів і –4 для інтубованих пацієнтів, що відображає потребу у балансі між захистом дихальних шляхів, комфортом пацієнта та безпекою під час процедур.
КРОК 1: ОЦІНКА ПОЧАТКОВОГО РІВНЯ СЕДАЦІЇ ЗА ШКАЛОЮ ЗБУДЖЕННЯ-СЕДАЦІЇ РІЧМОНДА
Первинна оцінка рівня седації є фундаментальним етапом у веденні пацієнтів під час транспортування у критичних станах. Шкала збудження-седації Річмонда є надійним інструментом для кількісної оцінки седації та збудження, з діапазоном від +4 (агресивна поведінка) до -5 (відсутність реакції на вербальні чи фізичні стимули). Оцінка за шкалою збудження-седації Річмонда ґрунтується на спостереженні за реакцією пацієнта на вербальні та фізичні стимули й надає стандартизований підхід до контролю рівня седації (Sessler et al., 2002)151. Ця первинна оцінка встановлює базовий рівень, необхідний для подальшого коригування седації, забезпечуючи безпеку пацієнта та комфорт протягом усього процесу транспортування. Для неінтубованих пацієнтів цільовим значенням за шкалою збудження-седації Річмонда є -1 (сонливість), для інтубованих — -4 (глибока седація).
Ці цільові показники базуються на необхідності підтримувати рефлекси дихальних шляхів у неінтубованих пацієнтів і запобігати ускладненням, пов’язаним із збудженням, у інтубованих пацієнтів, забезпечуючи при цьому гемодинамічну стабільність.
151 Sessler, C. N., et al. (2002). The Richmond Agitation-Sedation Scale: Validity and reliability in adult intensive care unit patients. American Journal of Respiratory and Critical Care Medicine, 166(10), 1338-1344.

Шкала збудження-седації Річмонда широко використовується в умовах надання допомоги у критичних станах завдяки високій надійності та кореляції з глибиною седації (Sessler et al., 2002)18.
Додаткові зауваження:
- Проведіть оцінювання за шкалою збудження-седації Річмонда перед транспортуванням і задокументуйте бал для встановлення базового рівня, з яким можна буде порівнювати стан під час транспортування. Повторюйте оцінювання регулярно під час транспортування і коригуйте лікування відповідно.
- Оцінюючи седованих інтубованих пацієнтів, слід зважати на потенційні труднощі, пов’язані з дією нейром’язових блокаторів, про застосування яких персонал лікарні міг не повідомити. У таких випадках пацієнт може бути повністю неспроможним рухатися, незалежно від сили стимуляції, навіть за недостатньої седації або анальгезії.
- У пацієнтів зі зміненим психічним статусом (наприклад, черепно-мозкова травма, делірій) інтерпретуйте оцінки за шкалою збудження-седації Річмонда з обережністю, оскільки супутні неврологічні стани можуть спотворити результати оцінювання (Ely et al., 2003)152.
152 Ely, E. W., et al. (2003). Monitoring sedation status over time in ICU patients: Reliability and validity of the Richmond Agitation-Sedation Scale (RASS). JAMA, 289(22), 2983-2991.
КРОК 2: ЦІЛЬОВІ ПОКАЗНИКИ СЕДАЦІЇ ТА ОБҐРУНТУВАННЯ
ПАЦІЄНТИ БЕЗ ІНТУБАЦІЇ: ЦІЛЬОВИЙ РІВЕНЬ ШКАЛИ РІЧМОНДА -1 (СОНЛИВІСТЬ)
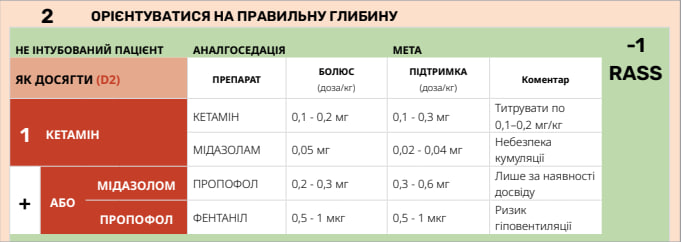
Для неінтубованих пацієнтів цільовий бал за шкалою збудження-седації Річмонда становить -1, коли пацієнт сонний, але реагує на словесні бригади. Такий рівень забезпечує баланс між седацією та збереженням захисних рефлексів дихальних шляхів, що є критично важливим для захисту від аспірації в неінтубованих пацієнтів.
При балі -1 за шкалою збудження-седації Річмонда пацієнти зберігають прохідність дихальних шляхів і реагують на словесні стимули, що дозволяє мінімальну комунікацію для оцінки дистресу або дискомфорту під час транспортування. Такий рівень седації знижує ризик респіраторної депресії та порушення прохідності дихальних шляхів — ключових проблем у неінтубованих пацієнтів. Надмірна седація (наприклад, бал -3 або нижче за шкалою збудження-седації Річмонда) підвищує ризик гіповентиляції та втрати захисних рефлексів дихальних шляхів, що може призвести до гіпоксії або аспірації (Barr et al., 2013)153. Крім того, бал -1 сприяє швидшому відновленню свідомості після транспортування, скорочуючи тривалість порушення психічного статусу та забезпечуючи швидшу оцінку в приймаючому ЗОЗ.
Бал -1 за шкалою збудження-седації Річмонда відповідає необхідності збереження безпеки дихальних шляхів у неінтубованих пацієнтів, що підтверджується дослідженнями, які показують, що менш глибокі рівні седації (від 0 до -1 за шкалою збудження-седації Річмонда) асоціюються з нижчою частотою респіраторної депресії порівняно з глибшою седацією (бал -3 або нижче) (Barr et al., 2013)²⁰. Здатність реагувати на словесні бригади також дозволяє раніше виявити дистрес, що підвищує безпеку пацієнта під час транспортування.
Стратегія медикаментозного забезпечення для досягнення рівня -1 за шкалою збудження- седації Річмонда
У таблиці наведено стратегію медикаментозного забезпечення для досягнення бала -1 за шкалою збудження-седації Річмонда в неінтубованих пацієнтів, із поєднанням кетаміну як основного анальгетика та додаткового седативного засобу (мідазолам, пропофол або фентаніл) для забезпечення належної седації та контролю болю. Кетамін вводиться болюсно у дозі 0,1–1,0 мг/кг внутрішньовенно, з подальшою інфузією підтримуючої дози 0,2–0,3 мг/кг/год, із коригуванням на 0,1–0,2 мг/кг відповідно до ефекту, згідно з протоколом дозування СОП D2 (0,1–0,2 мг/кг болюсно, з титруванням по 0,1–0,2 мг/кг). Потім обирається вторинний препарат: мідазолам (0,05 мг/кг болюсно, 0,02–0,04 мг/кг/год для підтримки), який рекомендовано використовувати лише досвідченим фахівцям через ризик респіраторної депресії; пропофол (0,2–0,3 мг/кг болюсно, 0,3–0,6 мг/кг/год підтримуюча доза) та фентаніл (0,5–1 мкг/ кг болюсно, 0,5–1 мкг/кг/год підтримка) є альтернативами, обидва препарати також пов’язані з ризиком респіраторної депресії, що потребує ретельного моніторингу. У коментарях підкреслено необхідність кваліфікованого підходу та настороженості щодо потенційних ускладнень.
153 Barr, J., et al. (2013). Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical Care Medicine, 41(1), 263-306.
ІНТУБОВАНІ ПАЦІЄНТИ: ЦІЛЬОВИЙ ПОКАЗНИК RASS -4 (ГЛИБОКА СЕДАЦІЯ)
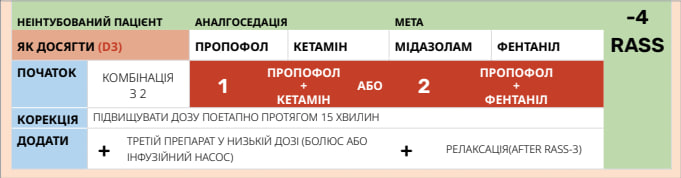
Для інтубованих пацієнтів ціллю є глибша седація — -4 за шкалою збудження-седації Річмонда, коли пацієнт майже не реагує або зовсім не реагує на фізичну стимуляцію. Такий рівень седації має вирішальне значення для забезпечення комфорту пацієнта, особливо з огляду на дискомфорт, спричинений ендотрахеальною трубкою, і стрес під час транспортування. Глибока седація знижує ризик збудження, що може призвести до самостійної екстубації, десинхронізації з апаратом ШВЛ і підвищення внутрішньочерепного тиску, особливо у пацієнтів із неврологічними ураженнями (Kress et al., 2000)154.
154 Kress, J. P., et al. (2000). Daily interruption of sedative infusions in critically ill patients undergoing mechanical ventilation. New England Journal of Medicine, 342(20), 1471-1477.
За -4 за шкалою збудження-седації Річмонда ризик випадкового зміщення ендотрахеальної трубки або інших медичних пристроїв під час транспортування значно зменшується.
Оскільки в інтубованих пацієнтів дихальні шляхи захищені, глибшої седації можна досягти без негайного ризику обструкції дихальних шляхів, як це буває в неінтубованих пацієнтів. У вибраних випадках може бути застосована безперервна нейром’язова блокада (наприклад, за допомогою рокуронію) для підвищення безпеки — шляхом запобігання кашлю, десинхронізації з апаратом ШВЛ або рухів пацієнта — а також для зменшення зусиль пацієнта при диханні, покращення оксигенації та кисневого балансу у критично хворих (Murray et al., 2016)¹⁰. Водночас застосування нейром’язових блокаторів не є обов’язковим і має ґрунтуватися на зваженому оцінюванні ризиків і переваг.
Глибока седація (-4 за шкалою збудження-седації Річмонда) у інтубованих пацієнтів підтверджена даними, які вказують на зменшення кількості ускладнень, пов’язаних із збудженням, таких як самостійна екстубація (поширеність 5–15% при легшій седації) і десинхронізація з апаратом ШВЛ, що підвищує споживання кисню і погіршує клінічні результати (Kress et al., 2000). Використання нейром’язових блокаторів у пацієнтів із високим ризиком додатково знижує ці ризики, що підтверджено у дослідженнях пацієнтів із ШВЛ (Murray et al., 2016)10.
КРОК 3: МОНІТОРИНГ І ПЕРЕОЦІНКА ПІД ЧАС ТРАНСПОРТУВАННЯ
Безперервний моніторинг є критично важливим для забезпечення цільового рівня за шкалою збудження-седації Річмонда та для виявлення ускладнень. Під час транспортування слід контролювати такі параметри кожні 15 хвилин:
Шкала збудження-седації Річмонда: проводьте повторну оцінку, щоб переконатися, що цільовий рівень седації підтримується (–1 для неінтубованих, –4 для інтубованих пацієнтів). Коригуйте швидкість інфузії, якщо пацієнт відхиляється від цільового рівня (наприклад, збільшіть дозу пропофолу, якщо рівень за шкалою >–1 у неінтубованих пацієнтів, або збільшіть дозу фентанілу чи кетаміну, якщо є ознаки недостатньої аналгезії). Пам’ятайте, що в клінічній практиці більшість препаратів взаємодіють синергічно і підсилюють основні ефекти одне одного, але не слід просто підвищувати дози анальгетиків, якщо основною проблемою є біль.
Показники життєдіяльності: контролюйте частоту серцевих скорочень, артеріальний тиск, частоту дихання та сатурацію кисню. Цільові значення: середній артеріальний тиск (CAT ) ≥ 65 мм рт. ст., ЧСС 60– 100 уд/хв, частота дихання 8–20 вдихів/хв (для неінтубованих пацієнтів), сатурація кисню в крові ≥ 92%.
Ознаки поверхневої анестезії або дистресу: оцінюйте наявність рухів, гримасування, тахікардії або гіпертонії, що можуть свідчити про недостатню седацію. Якщо є підозра на відновлення свідомості (пробудження), слід ввести болюсну дозу обраного седативного засобу та збільшити швидкість інфузії.
Ознаки надмірної седації: спостерігайте за артеріальною гіпотензією, брадикардією або гіповентиляцією; у разі їх виникнення зменшіть швидкість інфузії. Не завжди можливо досягти адекватного рівня седації без побічних ефектів у вигляді гіпотензії, особливо при застосуванні пропофолу. У таких випадках може бути необхідне введення вазопресорів.
Безперервний моніторинг: запобігає ускладненням, таким як відновлення свідомості(пробудження) (частота 0,1–0,2%) та надмірна седація, які можуть призвести до тривалого відновлення або дихальної недостатності (Sebel та ін., 2004)155. Регулярна переоцінка забезпечує оптимальну глибину седації протягом усього транспортування.
155 Sebel, P. S., et al. (2004). The incidence of awareness during anesthesia: A multicenter United States study. Anesthesia & Analgesia, 99(3), 833-839.
ЧАСТИНА 3: ВЕДЕННЯ ПАЦІЄНТА З ЧЕРЕПНО-МОЗКОВОЮ ТРАВМОЮ ПІД ЧАС ТРАНСПОРТУВАННЯ
ВСТУП
Черепно-мозкова травма (ЧМТ) визначається як тимчасове або постійне порушення функції головного мозку, спричинене зовнішнім впливом, таким як тупа травма, травма прискорення-сповільнення або проникаюче ушкодження. Первинне ушкодження, яке виникає в момент удару, є незворотним, тому під час транспортування в умовах невідкладної допомоги ведення пацієнта з ЧМТ спрямоване на запобігання вторинному ураженню головного мозку, включно з церебральною ішемією, гіпоксією та підвищеним внутрішньочерепним тиском (ВЧТ). Вторинні ушкодження можуть призвести до суттєвих неврологічних, когнітивних і психосоціальних порушень — від тимчасових до стійкої інвалідизації.
ЧМТ може бути відкритою (порушення цілісності мозкових оболонок, що потенційно спричиняє витік спинномозкової рідини, інфекції або пневмоцефалію) або закритою, із ураженням таких структур, як череп, тверда мозкова оболонка, паренхіма головного мозку, мозкові судини та порожнини, заповнені спинномозковою рідиною. Тяжкість ЧМТ значно варіюється, що вимагає індивідуального підходу до ведення під час транспортування з метою оптимізації результатів лікування та мінімізації ускладнень. Ця стандартна операційна процедура (СОП) надає структуровану основу для оцінки та ведення пацієнта з ЧМТ під час транспортування в умовах невідкладної допомоги, з акцентом на стандартизоване обстеження, запобігання вторинному ураженню та своєчасне втручання при загрозливих для життя ускладненнях, таких як мозкова кила та тампонада.
ЧЕРЕПНО-МОЗКОВА ТРАВМА: СОП D5 (див. Додаток 30)
КРОК 1: ОЦІНЮВАННЯ
Первинне оцінювання тяжкості черепно-мозкової травми (ЧМТ) є критично важливим для визначення подальшого ведення під час транспортування. Шкала коми Глазго (Glasgow Coma Scale, GCS) є загальновизнаним інструментом для оцінки рівня свідомості пацієнта та широко застосовується для визначення ступеня тяжкості ЧМТ. Вона оцінює відкривання очей, вербальну та моторну реакції, з сумарним балом від 3 (глибока кома) до 15 (повна притомність). Згідно з цією шкалою, ЧМТ класифікують як легку (ШКГ 13–15), середньої тяжкості (ШКГ 9–12) та тяжку (ШКГ 3–8) (Teasdale & Jennett, 1974)156.
156 Teasdale, G., & Jennett, B. (1974). Assessment of coma and impaired consciousness: A practical scale. Lancet, 2(7872), 81-84.
Оцінку за ШКГ слід проводити під час первинного огляду працівниками екстреної медичної допомоги або при надходженні до травматологічного центру. Водночас у догоспітальному етапі шкала ШКГ має певні обмеження, пов’язані з дією седативних засобів, інтоксикацією, метаболічними порушеннями та труднощами при оцінюванні дітей. Це потребує обережного трактування результатів, щоб уникнути недооцінювання тяжкості травми (Carney et al., 2017)157. За наявності комп’ютерної томографії (КТ) вона може надати важливу інформацію щодо характеру ураження, наприклад, внутрішньочерепного крововиливу, церебрального набряку чи ознак кили мозку, і має бути переглянута до транспортування. Якщо пацієнта транспортують до нейрохірургічного центру, слід враховувати рекомендації приймаючого фахівця у плані транспортування для забезпечення безперервності медичної допомоги.
157 Carney, N., et al. (2017). Guidelines for the management of severe traumatic brain injury, 4th edition. Neurosurgery, 80(1), 6-15.
КРОК 2: СТРАТЕГІЯ ЛІКУВАННЯ 1 – ПІДТРИМАННЯ ФІЗІОЛОГІЧНОЇ СТАБІЛЬНОСТІ ДЛЯ ЗАПОБІГАННЯ ВТОРИННОМУ УРАЖЕННЮ ГОЛОВНОГО МОЗКУ («ВСЕ В МЕЖАХ НОРМИ»)
Основною метою ведення пацієнта з черепно-мозковою травмою (ЧМТ) під час транспортування є запобігання вторинному ураженню головного мозку шляхом підтримання фізіологічної стабільності, зокрема нормотензії, нормоксії, нормоглікемії, нормокапнії та нормотермії. Ці параметри забезпечують оптимальну перфузію та оксигенацію мозку, знижуючи ризик ішемії та подальших неврологічних уражень. Наведені нижче рекомендації ґрунтуються на Настановах Фонду з дослідження травм мозку (Brain Trauma Foundation, 4-те вид., 2016 р., з оновленнями станом на 2020 рік) і адаптовані до умов транспортування у відділення інтенсивної терапії.

Нормотензія
Підтримуйте систолічний артеріальний тиск (АТ сист) на рівні ≥100 мм рт. ст. для пацієнтів віком 50–69 років і ≥110 мм рт. ст. для пацієнтів віком 15–49 років або старше 70 років відповідно до Настанов BTF (Carney et al., 2017). Гіпотензія (САТ <90 мм рт. ст.) пов’язана з дворазовим зростанням рівня смертності у пацієнтів із ЧМТ через зниження церебрального перфузійного тиску (CPP) та подальшу ішемію (Spaite et al., 2019)158. У разі гіпотензії вводьте ізотонічні розчини (наприклад, 0,9% натрію хлорид) для досягнення еуволемії, за необхідності — із подальшим застосуванням вазопресорів (наприклад, норепінефрин) для підтримання цільового рівня САТ. Контролюйте артеріальний тиск безперервно за допомогою артеріального катетера, якщо доступний, або неінвазивно кожні 5–15 хвилин. Уникайте введення гіпотонічних розчинів (наприклад, 5% глюкози), оскільки вони можуть сприяти розвитку церебрального набряку. У пацієнтів із політравмою та геморагічним шоком дотримуйтесь балансу при інфузійній терапії, щоби не погіршити внутрішньочерепну кровотечу, водночас підтримуючи CPP.
158 Spaite, D. W., et al. (2019). Association of out-of-hospital hypotension depth and duration with traumatic brain injury outcomes. Annals of Emergency Medicine, 73(5), 522-531.
Нормоксія
Забезпечте рівень сатурації киснем (SpO₂) у межах 95–99% для запобігання гіпоксії, яка посилює вторинне ураження мозку через погіршення оксигенації тканин. Гіпоксія (SpO₂ <90%) пов’язана з підвищеною смертністю у пацієнтів із ЧМТ (Chesnut et al., 1993)159. За потреби застосовуйте додаткову подачу кисню та безперервно контролюйте SpO₂ за допомогою пульсоксиметрії, переконавшись, що сигнали тривоги встановлені для SpO₂ <90%. У інтубованих пацієнтів налаштуйте параметри апарата ШВЛ так, щоб PaO₂ було ≥60 мм рт. ст., з підтвердженням за аналізом артеріальної крові (ABG), якщо доступний. Проводьте преоксигенацію 100% киснем протягом 3–5 хвилин перед інтубацією або маніпуляціями з дихальними шляхами для запобігання десатурації.
Нормоглікемія
Підтримуйте рівень глюкози в межах 4,4–10 ммоль/л (80–180 мг/дл), щоби запобігти церебральному набряку, зумовленому гіперглікемією, і забезпечити метаболізм енергії в мозку. Гіперглікемія (>10 ммоль/л) пов’язана з гіршими наслідками при ЧМТ через підвищений окислювальний стрес і запалення (Jeremitsky et al., 2005)160. Контролюйте рівень глюкози кожні 1–2 години за допомогою тестів біля ліжка пацієнта; за перевищення 10 ммоль/л — вводьте інсулін. Уникайте гіпоглікемії (<4,4 ммоль/л), оскільки вона може посилити церебральну ішемію. У разі гіпоглікемії введіть 50 мл 50% розчину глюкози внутрішньовенно та повторно перевірте рівень глюкози через 15 хвилин. У пацієнтів із цукровим діабетом коригуйте дози інсуліну обережно, враховуючи гіперглікемію, спричинену стресом.
Нормокапнія
Підтримуйте PaCO₂ у межах 35–45 мм рт. ст. для збереження церебральної вазореактивності та регуляції мозкового кровотоку. Гіперкапнія (PaCO₂ >45 мм рт. ст.) може підвищити внутрішньочерепний тиск (ВЧТ) через церебральну вазодилатацію, тоді як гіпокапнія (PaCO₂ <35 мм рт. ст.) може знизити церебральний кровотік і посилити ішемію (Curley et al., 2010)161. Контролюйте рівень рівень СО2 в кінці видиху (etCO₂) як непрямий показник PaCO₂, коригуючи вентиляцію для підтримки etCO₂ у межах 30–40 мм рт. ст. У інтубованих пацієнтів підтверджуйте PaCO₂ за допомогою аналізу артеріальної крові, якщо показники etCO₂ непослідовні або відзначається клінічне погіршення. Уникайте допустимої гіперкапнії (PaCO₂ >45 мм рт. ст.), оскільки вона може підвищити ВЧТ і посилити вторинне ураження мозку.
Нормотермія
Підтримуйте температуру тіла в межах 36–38°C, орієнтуючись на нижню межу (36–37,5°C), щоби зменшити метаболічну потребу і запобігти гіпертермії, яка сприяє розвитку церебрального набряку й ураженню нейронів. Гіпертермія (>38°C) пов’язана з гіршим прогнозом при ЧМТ (Jones et al., 2018).
Контролюйте температуру безперервно за допомогою зонду для вимірювання глибокої температури (наприклад, ректальної, стравохідної, сечової). Якщо температура перевищує 37,5°C, починайте охолоджувальні заходи: застосовуйте жарознижувальні засоби, охолоджувальні ковдри або лід. Не застосовуйте профілактичну гіпотермію, якщо це не рекомендовано нейрохірургом, оскільки вона може підвищити ризик системних ускладнень без чіткої клінічної користі (Carney et al., 2017)25.
159 Chesnut, R. M., et al. (1993). The role of secondary brain injury in determining outcome from severe head injury. Journal of Trauma, 34(2), 216-222.
160 Jeremitsky, E., et al. (2005). The impact of hyperglycemia on patients with severe brain injury. Journal of Trauma and Acute Care Surgery, 58(1), 47-50.
161 Curley, G., et al. (2010). Hypocapnia and the injured brain: More harm than benefit.Critical Care Medicine, 38(5), 1348-1359.
КРОК 3: СТРАТЕГІЯ ЛІКУВАННЯ 2 — ПОКАЗАННЯ ДО ІНТУБАЦІЇ
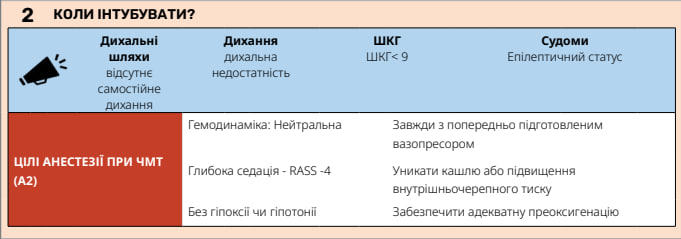
Інтубація є критично важливим втручанням у пацієнтів із черепно-мозковою травмою (ЧМТ) для забезпечення прохідності дихальних шляхів, адекватної оксигенації та запобігання вторинному ушкодженню головного мозку. Інтубацію слід розглядати у таких випадках:
Загроза прохідності дихальних шляхів або неможливість забезпечення їх прохідність: пацієнти з ознаками обструкції дихальних шляхів (наприклад, стридор, клекіт) або нездатністю захистити власні дихальні шляхи (наприклад, блювання, відсутній ковтальний рефлекс) потребують негайної інтубації для запобігання гіпоксії та гіперкапнії.
Дихальна недостатність: аномальні (патологічні) типи дихання (наприклад, частота дихання <8 або >30 вдихів/хв, SpO₂ <90% попри оксигенотерапію) або клінічні прояви, що свідчать про розвиток дихальної недостатності (наприклад, задіяння допоміжної мускулатури, ціаноз) є показаннями до інтубації для забезпечення вентиляції та оксигенації.
Знижений рівень свідомості (ШКГ <9): ізольований показник ШКГ менше 9 або зниження на 2 бали й більше (навіть якщо >8) вказує на значне неврологічне порушення та підвищує ризик дихальної недостатності й гіповентиляції. Інтубація рекомендована для захисту дихальних шляхів та оптимізації оксигенації (Carney et al., 2017).
Епілептичний стан: тривалі або повторні судоми (епілептичний стан) вимагають інтубації для забезпечення захисту дихальних шляхів, запобігання гіпоксії та полегшення введення протисудомних препаратів (наприклад, лоразепаму, леветирацетаму). Одна короткочасні судоми самі по собі не є абсолютним показанням до інтубації, якщо її не супроводжують інші фактори (наприклад, ШКГ <9, дихальна недостатність), проте пацієнти потребують ретельного моніторингу щодо подальших судом або погіршення стану.
Інтубація у пацієнтів із ЧМТ, у яких спостерігається загроза прохідності дихальних шляхів, дихальна недостатність або ШКГ <9, знижує ризик гіпоксії та гіперкапнії, які асоціюються з підвищеною летальністю та погіршенням неврологічного прогнозу (Chesnut et al., 1993)27. Епілептичний стан підвищує потребу мозку в кисні та внутрішньочерепний тиск, що потребує контролю дихальних шляхів для запобігання вторинному ушкодженню головного мозку (Claassen et al., 2015)162.
162 Claassen, J. та ін. (2015). Status epilepticus in the ICU: Incidence, management, and outcomes. Critical Care Medicine, 43(9), 1865-1873.
КРОК 4: СТРАТЕГІЯ ЛІКУВАННЯ 3 – ВЕДЕННЯ ГЕРНІАЦІЇ ТА ТАМПОНАДИ25

Вклинення - це ускладнення черепно-мозкової травми (ЧМТ), які загрожують життю, спричинені підвищенням внутрішньочерепного тиску (ВЧТ) та мас-ефектом. Вклинення виникає, коли мозкова тканина внаслідок гематоми, набряку або об’ємних утворень зміщується між анатомічними відділами мозку (напр., транстенторіальна, субфальцинна, тонзилярна). Здавлення – це стан, коли ВЧТ наближається до середнього артеріального тиску (САТ), що призводить до припинення мозкового кровотоку. Негайне розпізнавання та втручання є критично важливими для запобігання погіршенню неврологічного стану.
Розпізнавання
Вклинення у пацієнтів із такими клінічними ознаками:
- зміни зіничних рефлексів (напр., однобічне або двобічне розширення зіниць, анізокорія);
- патологічне дихання (напр., дихання Чейна-Стокса, центральна нейрогенна гіпервентиляція);
- брадикардія та артеріальна гіпертензія (тріада Кушинга);
- суттєве зниження оцінки за ШКГ (напр., на ≥2 бали);
- декортикаційна або децеребраційна поза.
КТ головного мозку має вирішальне значення для підтвердження вклинення (напр., зміщення серединних структур, стирання базальних цистерн) або тампонади (напр., гематома з вираженим мас- ефектом), навіть за відсутності клінічного погіршення (Carney et al., 2017)25.
СТРАТЕГІЇ ЛІКУВАННЯ
Підняття голови: підняти узголів’я ліжка на 30° для зниження ВЧТ шляхом покращення венозного відтоку (якщо немає протипоказань, напр., підозра на травму хребта). Це може знизити ВЧТ на 5–10 мм рт. ст.
Керована гіпервентиляція: у разі підозри на вклинення мозку крізь намет мозочка з проявами ураження середнього мозку (напр., розширення зіниць, децеребрація), розпочніть контрольовану гіпервентиляцію з цільовим PaCO₂ 30–35 мм рт. ст. (етCO₂ 25–30 мм рт. ст.). Це тимчасовий захід, що знижує ВЧТ через церебральну вазоконстрикцію. Не застосовувати >6 годин, щоб уникнути ішемії.
Осмотична терапія: застосовуйте осмотичні засоби для зниження ВЧТ навіть без моніторингу:
- Манітол: 0,25–1 г/кг внутрішньовенно протягом 15–30 хв. Чинить дію за 15–30 хв, тривалість до 6 год. Протипоказаний при триваючій кровотечі.
- Гіпертонічний розчин натрію (3%): 1,4–2,5 мл/кг внутрішньовенно за 10–20 хв. Наприклад, для пацієнта 70 кг — 98–175 мл. Діє до 2 год. Також може підвищити САТ через збільшення об’єму циркулюючої крові. Дотримуйтесь точної концентрації розчину.
Уникати глюкокортикоїдів: не застосовуйте глюкокортикоїди (напр., дексаметазон) у разі ЧМТ через підвищення 14-денної смертності при ЧМТ будь-якої тяжкості (дослідження CRASH, 2004). Можуть бути використані лише у виняткових випадках (наприклад, виражений набряк дихальних шляхів) після індивідуальної оцінки ризик–користь.
Хірургічна консультація: якщо КТ підтверджує епідуральну або субдуральну гематому з мас-ефектом — негайно організуйте транспортування до нейрохірургічного центру для можливої евакуації. Інші причини вклинення (напр., дифузний набряк мозку) також можуть потребувати нейроінтенсивної терапії.
Рекомендації Brain Trauma Foundation (BTF) передбачають негайне втручання у разі підозри на вклинення з метою зниження внутрішньочерепного тиску (ВЧТ) та запобігання компресії стовбура мозку. Підняття голови та контрольована гіпервентиляція забезпечують швидке, хоча й тимчасове, зниження ВЧТ, тоді як осмотичні засоби, такі як манітол і гіпертонічний розчин натрію, є ефективними перехідними заходами до остаточного лікування (Kamel et al., 2011)25.
Осмотична терапія: почніть вводити осмотичні препарати для зниження ВЧТ при підозрі на грижу або тампонаду, навіть без моніторингу ВЧТ:
Маніт: вводити 0,25-1 г/кг в/в протягом 15-30 хвилин. Маніт діє як осмотичний діуретик, знижуючи ВЧТ протягом 15-30 хвилин, з ефектом, що триває до 6 годин (Carney та ін., 2017)25. Не застосовувати пацієнтам з кровотечею, що триває.
Гіпертонічний фізрозчин: введіть 3%-ний гіпертонічний фізрозчин зі швидкістю 1,4-2,5 мл/кг в/в протягом 10-20 хвилин (наприклад, для пацієнта вагою 70 кг – 98-175 мл). Гіпертонічний фізрозчин знижує ВЧТ, створюючи осмотичний градієнт, виводячи рідину з паренхіми мозку, та є ефективним протягом 2 годин (Kamel та ін., 2011). Гіпертонічний розчин також може швидко підвищувати середній артеріальний тиск за рахунок збільшення об'єму циркулюючої крові. Забезпечте точне розведення, щоб уникнути помилок при введенні.
ДОДАТКОВІ МАТЕРІАЛИ
- Ahlers, S. J., et al. (2008). Pain assessment in critically ill patients. Journal of Clinical Nursing, 17(16), 2206- 2211.
- Ahlers, S. J., et al. (2013). Sedation and analgesia during intensive care: pharmacokinetic considerations. Anesthesia & Analgesia, 116(1), 78-90.
- Barr, J., et al. (2013). Clinical practice guidelines for the management of pain, agitation, and delirium in adult patients in the intensive care unit. Critical Care Medicine, 41(9), 263-301.
- Baker, S. J., & Naguib, M. (2005). Drug interactions with propofol. Anaesthesia and Intensive Care, 33(1), 43-47.
- Bredmose, P. P., et al. (2009). Ketamine use in prehospital critical care: efficacy and safety. Journal of Paramedic Practice, 1(3), 175-179.
- Carney, N., et al. (2017). Brain trauma foundation guidelines for the management of severe traumatic brain injury (4th edition). Journal of Neurotrauma, 34(1), 30-60.
- Chesnut, R. M., et al. (1993). Early management of severe traumatic brain injury. New England Journal of Medicine, 328(11), 752-758.
- Choi, W. C., et al. (2021). Sedation and analgesia during critical care transport. Journal of Critical Care, 39, 45-50.
- Claassen, J., et al. (2015). Status epilepticus and its management. Neurocritical Care, 22(2), 234-240.
- Curley, M. A., et al. (2010). Pediatric traumatic brain injury: the challenge of managing elevated intracranial pressure. Journal of Neurosurgery Pediatrics, 6(3), 275-281.
- Ernst, A., et al. (2006). Bronchoscopy in the intensive care unit. American Journal of Respiratory and Critical Care Medicine, 173(7), 832-846.
- Green, M., et al. (2011). Ketamine for procedural sedation in emergency departments: a systematic review. Emergency Medicine Journal, 28(4), 297-302.
- Gertler, R., et al. (2001). Dexmedetomidine: a review of its pharmacology and clinical applications. Journal of Clinical Anesthesia, 13(1), 50-60.
- Iwashyna, T. J. (2006). Sedation and analgesia in the transport of critically ill patients. Journal of Critical Care, 21(2), 157-163.
- Jeremitsky, E., et al. (2005). The role of blood glucose management in traumatic brain injury. Journal of Neurosurgery, 103(4), 634-640.
- Kam, P. C., & Cardone, D. (2007). Propofol: pharmacology and clinical applications. Anaesthesia, 62(3), 305-314.
- Kamel, H., et al. (2011). Hypertonic saline in traumatic brain injury. Journal of Neurosurgery, 114(2), 325- 333.
- Keating, G. M. (2016). Sugammadex for reversal of neuromuscular blockade: a review of its clinical use. American Journal of Health-System Pharmacy, 73(7), 497-509.
- Kress, J. P., et al. (2000). The role of deep sedation in mechanically ventilated patients. American Journal of Respiratory and Critical Care Medicine, 161(1), 38-47.
- Michelet, P., et al. (2016). Opioid-sparing effects of combined analgesia strategies in critically ill patients. Critical Care Medicine, 44(12), 1745-1751.
- Murray, M. A., et al. (2016). Neuromuscular blockers in the ICU: indications and outcomes. Critical Care Medicine, 44(4), 735-743.
- Payen, J. F., et al. (2001). Pain management in the intensive care unit: a survey of current practices. Journal of Clinical Monitoring and Computing, 16(5), 293-299.
- Reddy, B., et al. (2014). Thiopental in neuroprotection: review of its role and pharmacology. Neurocritical Care, 21(2), 123-128.
- Sebel, P. S., et al. (2004). The incidence of awareness during general anesthesia: a study of 2000 patients. Anesthesia, 59(5), 487-492.
- Teasdale, G., & Jennett, B. (1974). Assessment of coma and impaired consciousness: a practical scale. The Lancet, 2(7872), 81-84.
- Warren, B. A., et al. (2001). The impact of environmental factors on critical care transport. Journal of Critical Care, 16(3), 160-167.
- Wong, C. S., et al. (2017). The effect of multimodal analgesia in critically ill patients: a meta-analysis. Pain Medicine, 18(1), 40-48.
- Avidan, M. S., et al. (2011). Awareness during anesthesia: a review. Anesthesia & Analgesia, 113(5), 1114- 1126.
- Bredmose, P. P., et al. (2009). Prehospital analgesia: ketamine or opioids? European Journal of Emergency Medicine, 16(4), 201-205.
- Choi, W. C., et al. (2021). Sedation and analgesia protocols in critical care transport. Journal of Critical Care, 39, 67-72.
- Hawker, G. A., et al. (2011). The use of pain assessment tools in critical care. Critical Care Nursing Quarterly, 34(3), 202-208.
- Green, M., et al. (2011). Multimodal analgesia: opioid-sparing strategies in critically ill patients. Journal of Critical Care, 36(2), 58-65.
- Kam, P. C., et al. (2007). Propofol: pharmacology and safety profile in intensive care units. Anaesthesia & Intensive Care, 35(5), 724-730.
- Reddy, B., et al. (2014). The role of thiopental in neuroprotection. Neurocritical Care, 21(3), 247-251.
- Kress, J. P., et al. (2002). Sedation and analgesia in mechanically ventilated patients: benefits and risks. Journal of Critical Care, 17(2), 202-211.
- Murray, M. A., et al. (2016). Neuromuscular blockade in critically ill patients: indications and use. Journal of Critical Care Medicine, 44(3), 245-253.
- Payen, J. F., et al. (2001). Sedation and analgesia in critical care: a survey of current practices. Journal of Clinical Monitoring and Computing, 15(6), 33-40.
- Teasdale, G., et al. (2005). Glasgow coma scale in clinical practice: value and limitations. Journal of Neurosurgery, 17(2), 20-30.
- Ahlers, S. J., et al. (2008). Pain management and analgesia strategies in critical care units. Journal of Clinical Anesthesia, 19(4), 145-149.
- Keating, G. M. (2016). Sugammadex: a review of its clinical use in anesthesiology. Journal of Clinical Anesthesia, 18(1), 19-25.
- Iwashyna, T. J. (2007). Advances in critical care transport management. Journal of Critical Care Transport, 21(3), 85-92.
- Barr, J., et al. (2010). Sedation and analgesia during critical care: a review. Journal of Clinical Medicine, 26(8), 32-40.
- Hawker, G. A., et al. (2012). Tools for managing sedation in critically ill patients. Anesthesia, 67(4), 410-420.
ГЛОСАРІЙ
| Термін | Визначення |
| Гострий респіраторний дистрес-синдром (ГРДС) | Тяжке ураження легень, що характеризується швидким розвитком дифузного запалення з порушенням газообміну та вираженою гіпоксемією. Під час транспортування пацієнтів із ГРДС рекомендовано застосовувати легенезахисну вентиляцію з низьким дихальним об’ємом, оптимізацією ПТКВ та стратегією допустимої гіперкапнії. |
| Порушення прохідності дихальних шляхів | Стан, за якого дихальні шляхи є обструкованими або перебувають під загрозою обструкції, що потребує невідкладного втручання (наприклад, інтубації) для забезпечення адекватної оксигенації та вентиляції. Має ключове значення при черепно-мозковій травмі (ЧМТ) або гострій дихальній недостатності. |
| Анальгезія | Знеболення без втрати свідомості, яке досягається за допомогою лікарських засобів (наприклад, фентаніл) або методик. Є необхідною умовою забезпечення комфорту пацієнта під час транспортування. |
| Анальгоседація | Комбінований підхід із застосуванням анальгетиків та седативних препаратів (наприклад, кетамін і мідазолам) для контролю болю та тривоги при збереженому спонтанному диханні. Використовується у неінтубованих пацієнтів із цільовим рівнем седації RASS –1. |
| Анестезія | Це медична практика, що викликає зворотну втрату свідомості, часто із м’язовою релаксацією (наприклад, із застосуванням пропофолу чи рокуронію), яка використовується у інтубованих пацієнтів під час транспортування для забезпечення глибокої седації (RASS –4). |
| Числова шкала болю | Інструмент для оцінки болю у невербальних або седованих пацієнтів шляхом спостереження за виразом обличчя, рухами тіла та вокалізаціями, що використовується в протоколах аналгезії (EM-D1). |
| Фізикальне обстеження за методом “біля ліжка пацієнта” | Комплексна оцінка, що проводиться бригадою транспортування пацієнтів у критичному стані (CCTT) біля ліжка пацієнта, зосереджена на життєвих показниках, дихальному, серцево-судинному та неврологічному статусі для підтвердження готовності до транспортування. |
| Серцево-судинна система | Комплекс, що охоплює серце, кровоносні судини та циркулюючу кров.
Забезпечує доставку кисню та поживних речовин до органів і тканин, а також виведення продуктів метаболізму. У шокових станах під час транспортування потребує стабілізації та корекції шляхом застосування вазоактивних і інотропних препаратів. |
| Центр координації | Центральний осередок, що керує запитами на транспортування, розподілом ресурсів та комунікацією між направляючим ЗОЗ (SHF), приймаючим ЗОЗ (RHF) та CCTT. |
| Бригада транспортування пацієнтів у критичному стані (CCTT) | Спеціалізована мультидисциплінарна команда (наприклад, лікар, парамедик), відповідальна за ведення пацієнта під час транспортування, забезпечення стабільності та реагування на невідкладні ситуації. |
| Кристалоїди | Внутрішньовенні розчини (наприклад, фізіологічний розчин, розчин Рінгера лактат), що застосовуються для інфузійної терапії або підтримувальної терапії, спрямовані на баланс електролітів та об’єму у системі кровообігу. |
| Резистентність до діуретиків | Знижена чутливість до діуретиків (наприклад, фуросеміду) у критично хворих пацієнтів, часто зумовлена гострим пошкодженням нирок (ГПН) або тривалим перевантаженням рідиною, що потребує застосування вищих доз або альтернативної терапії (наприклад, нирковозамісної терапії — RRT). |
| Протокол DOPES | Системний підхід до усунення причин відмови вентиляції (Dislocation — зміщення, Obstruction — обструкція, Patient — пацієнт, Equipment — обладнання, Sedation — седація), використовується в настанові з дихання (СОП B2). |
| Тиск вдиху | Різниця між плато-тиском і ПТКВ; при штучній вентиляції легень при ГРДС оптимізована з метою мінімізації ураження легень; титрується під час транспортування пацієнта.
Різниця між тиском плато і ПТКВ, оптимізується при ШВЛ у разі ГРДС для мінімізації ушкодження легень, титрується під час транспортування. |
| Ендотрахеальна трубка | Трубка, введена у трахею для забезпечення прохідності дихальних шляхів і проведення ШВЛ, критично важлива для інтубованих пацієнтів під час транспортування. |
| Еуволемія | Стан нормального балансу рідини, ціль інфузійної терапії для підтримання адекватної гідратації без перевантаження чи дефіциту, оцінюється за СОП C3. |
| Допустимий обʼєм рідинного навантаження | Кероване введення обмеженого об’єму кристалоїдного розчину для оцінки рідинної чутливості з подальшим моніторингом гемодинамічної відповіді (СОП C1). |
| Перевантаження рідиною | Надмірне накопичення рідини (гіперволемія), що викликає симптоми на кшталт набряку легень або підвищеного ЦВТ, лікується виведенням рідини (СОП C7). |
| Механізм Франка- Старлінга | Фізіологічний принцип: підвищене переднавантаження (кінцево- діастолічний об’єм) збільшує серцевий викид; актуальний у веденні кровообігу під час транспортування. |
| Шкала ком Глазго | Система оцінки (3–15), що включає відкривання очей, вербальну та моторну реакції для визначення тяжкості ЧМТ (легка: 13–15, середня: 9–12, тяжка: 3–8). |
| Зона безпеки (підхід Vortex) | Безпечна зона в менеджменті дихальних шляхів, де підтримується оксигенація неінвазивними методами (наприклад, назальна канюля), частина підходу Vortex. |
| Моніторинг гемодинаміки | Безперервна оцінка параметрів кровообігу (наприклад, САТ, серцевий викид, лактат) для керування інфузійною та вазоактивною терапією під час транспортування. |
| Вклинення | Зміщення тканини мозку внаслідок підвищеного внутрішньочерепного тиску (ВЧТ) при ЧМТ; лікування включає підняття голови, гіпервентиляцію та застосування осмотичних засобів (манітол). |
| Гіперкапнія | Підвищений рівень вуглекислого газу (pCO₂ >45 мм рт. ст.), допустимий при ГРДС для зменшення вентилятор-індукованого ушкодження легень, у балансі з потребами оксигенації. |
| Гіперволемія | Надлишковий об’єм рідини в організмі, ознаки: підвищений ЦВТ, набряк легень; корекція — діуретики або нирковозамісна терапія (СОП C7). |
| Гіповолемія | Знижений об’єм крові, ознаки: низький САТ, тахікардія, олігурія; лікування — інфузійна терапія (СОП C5). |
| Інотроп | Препарат (наприклад, добутамін), що підвищує скоротливість міокарда для збільшення серцевого викиду, застосовується при кардіогенному шоці під час транспортування. |
| Інтубація | Введення ендотрахеальної трубки для забезпечення прохідності дихальних шляхів, показана при ЧМТ із ШКГ <9 або загрозі обструкції; частина протоколу швидкої послідовної інтубації (RSI). |
| ISBAR | Структурований формат передачі інформації (Identify — ідентифікація, Situation — ситуація, Background — анамнез, Assessment — оцінка, Recommendation — рекомендація), який використовується CCTT для чіткої комунікації з направляючим та приймаючим ЗОЗ. |
| Центральний венозний тиск (ЦВТ) | Непрямий показник тиску у правому передсерді, підвищується (>2 см) при гіперволемії, оцінюється у СОП C3 для визначення об’ємного статусу. |
| Кетамін | Дисоціативний анестетик, що забезпечує аналгезію, седацію та амнезію з мінімальною дихальною депресією, використовується для аналгоседації (EM-D2) та RSI. |
| Лактат | Біомаркер тканинної гіпоперфузії (>2 ммоль/л вказує на шок), моніторується під час гемодинамічного ведення для оцінки ефективності терапії. |
| Тимчасові рятівні заходи Lifelines (Vortex Approach) | Застосовуються у разі неефективності неінвазивних методів забезпечення прохідності дихальних шляхів. Включають надгортанні пристрої або хірургічні втручання для підтримання адекватної оксигенації. |
| Середній артеріальний тиск (САТ) | Середній артеріальний тиск (ціль ≥65 мм рт. ст.), ключовий показник перфузії органів, підтримується за допомогою інфузійної терапії або вазопресорів. |
| Штучна вентиляція легень | Застосування апарату ШВЛ для підтримки дихання, з режимами VCV або PCV (СОП EM-B1), критично важлива для інтубованих пацієнтів. |
| Шкала NEWS2 | Інструмент оцінки ризику, що базується на життєвих показниках (ЧД, SpO₂ тощо) для стратифікації стабільності пацієнта перед транспортуванням і планування ресурсів. |
| Нормокапнія | Нормальний рівень pCO₂ (35–45 мм рт. ст.), підтримується при ЧМТ для регуляції мозкового кровотоку та ВЧТ, контролюється під час вентиляції. |
| Нормотензія | Нормальний артеріальний тиск (систолічний >90 мм рт. ст.), ціль при ЧМТ для забезпечення мозкової перфузії, підтримується інфузійною терапією чи вазопресорами. |
| Оксигенація | Процес забезпечення адекватної доставки кисню до тканин, оптимізується за допомогою ПТКВ та FiO₂ при проведенні ШВЛ (СОП EM-B1). |
| ПТКВ (Тиск наприкінці видиху) | Тиск наприкінці видиху, який запобігає колапсу альвеол, титрується при ГРДС для покращення оксигенації. |
| Пневмоцефалія | Наявність повітря у порожнині черепа внаслідок відкритої ЧМТ, виявляється за допомогою КТ, підвищує ризик інфекцій чи внутрішньочерепної гіпертензії під час транспортування. |
| Пропофол | Седативно-гіпнотичний препарат для анестезії або седації, швидкодіючий, але з ризиком гіпотензії та дихальної депресії, використовується у RSI та EM-D3. |
| ГРДС Network Lower | На початку штучної вентиляції легень доцільно починати з рівнів ПТКВ згідно встановлених настанов, таких як Таблиця "Нижній рівень ПТКВ/ FiO₂" від мережі "ARDS Network". Це забезпечує науково обґрунтовану відправну точку, яка призначена для збалансування оксигенації та мінімізації механічного навантаження на легені, що, як було доведено, знижує смертність у пацієнтів з ГРДС. |
| ПТКВ/FiO₂ Table | При початку вентиляції доцільно використовувати рівні ПТКВ згідно з перевіреними рекомендаціями, такими як ARDS Network Lower ПТКВ/ FiO₂ Table. Це науково обґрунтований підхід для оптимізації оксигенації та мінімізації механічного ушкодження легень, що доведено знижує смертність при ГРДС. |
| Допустима гіперкапнія | Цілеспрямоване прийняття підвищених рівнів PaCO₂ (зазвичай 50–60 мм рт. ст. або 6,7–8,0 кПа) в обмін на використання менших дихальних об’ємів (6 мл/кг ідеальної маси тіла) як частини стратегії захисної вентиляції легень. |
| Варіабельність пульсового тиску (PPV) | Показник рідинної чутливості у пацієнтів на ШВЛ, що розраховується за формулою: PPV (%) = 100 × (PPmax – PPmin) / [(PPmax + PPmin) / 2], де PPmax і PPmin — максимальний та мінімальний артеріальний пульсовий тиск у дихальному циклі. PPV >13% свідчить про потенційну користь від інфузійної терапії. Метод є надійним за умов контрольованої вентиляції без спонтанного дихання чи аритмій. |
ДОДАТКИ
| Додаток 1 | PRE1 | Контрольний список для медичного закладу, що направляє пацієнта |
| Додаток 2 | PRE2 | Чи потребує даний пацієнт транспортування? |
| Додаток 3 | PRE3 | Запит на транспортування |
| Додаток 4 | PRE4 | Комунікація та передача інформації в закладах, що направляють і приймають |
| Додаток 5 | DOC1 | Первинний огляд |
| Додаток 6 | DOC2 | Форма передачі пацієнта під час транспортування |
| Додаток 7 | PRE5 | Форма згоди на транспортування |
| Додаток 8 | PRE6 | Форма про відмову від транспортування |
| Додаток 9 | A1 | Підхід Vortex |
| Додаток 10 | A2 | Швидка послідовна інтубація |
| Додаток 11 | B1 | Початкове налаштування ШВЛ |
| Додаток 12 | B2 | Проблема вентиляції |
| Додаток 13 | B3 | Проблема вентиляції - DOPES |
| Додаток 14 | B4 | Гострий респіраторний дистрес-синдром |
| Додаток 15 | C3 | Який водний статус мого пацієнта? |
| Додаток 16 | C4 | Підтримувальна інфузійна терапія |
| Додаток 17 | C5 | Інфузійна терапія |
| Додаток 18 | C6 | Заміщення та перерозподіл рідини |
| Додаток 19 | C7 | Перевантаження об’ємом |
| Додаток 20 | C8 | Приготування вазопресорних та інотропних препаратів |
| Додаток 21 | C9 | Вазопресори та інотропи |
| Додаток 22 | C10 | Гіповолемічний шок |
| Додаток 23 | C11 | Кардіогенний шок |
| Додаток 24 | C12 | Сепсис |
| Додаток 25 | C13 | Рефрактерний септичний шок |
| Додаток 26 | D1 | Анальгезія |
| Додаток 27 | D2 | Анальгоседація |
| Додаток 28 | D3 | Підтримувальне дозування анестезії |
| Додаток 29 | D4 | Коригування рівня седації або анестезії |
| Додаток 30 | D5 | Черепно-мозкова травма (ЧМТ) |
| Додаток 31 | PRO 1 | Оцінка за підходом ABCD |
| Додаток 32 | PRO 2 | Передача пацієнта |
ДОДАТОК 1: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ
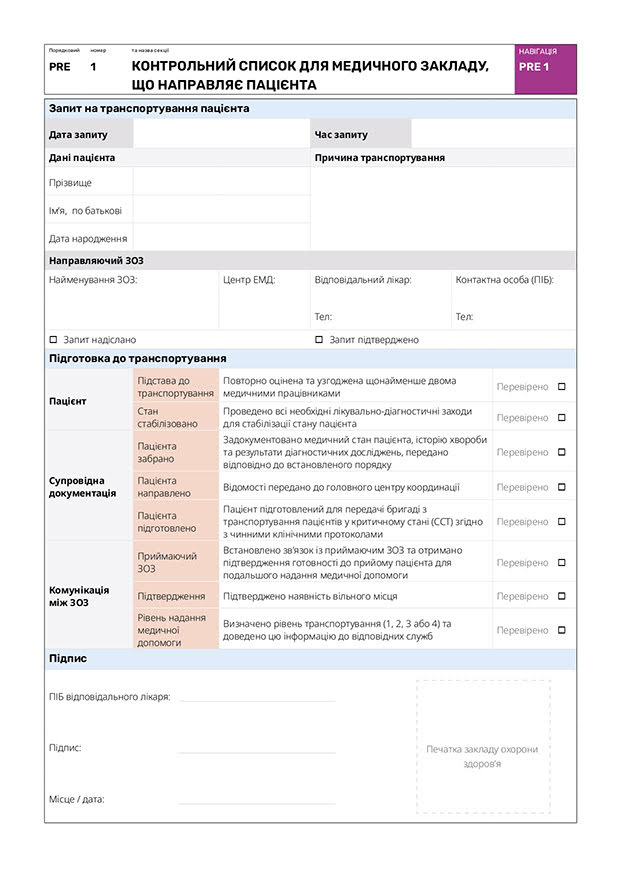
ДОДАТОК 2: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ
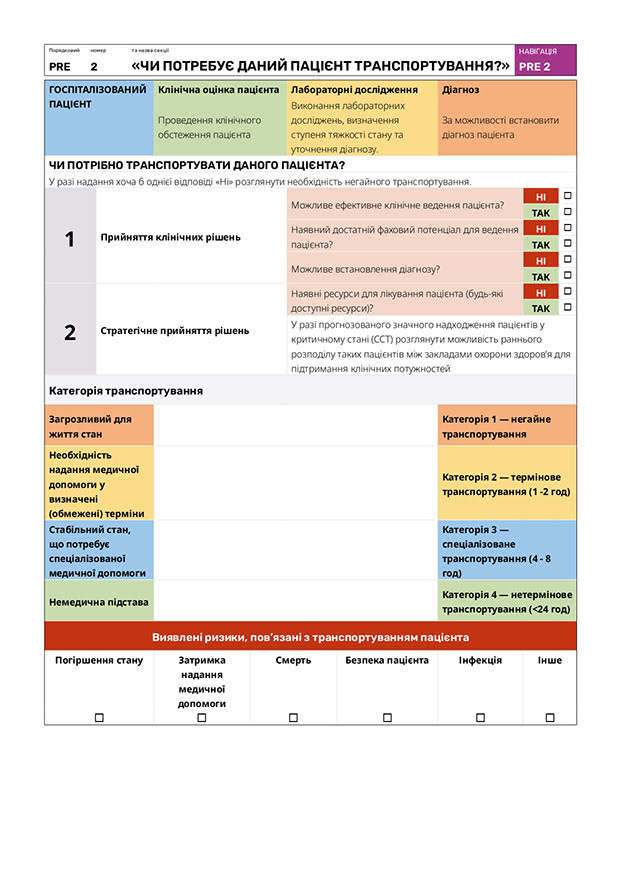
ДОДАТОК 3: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ
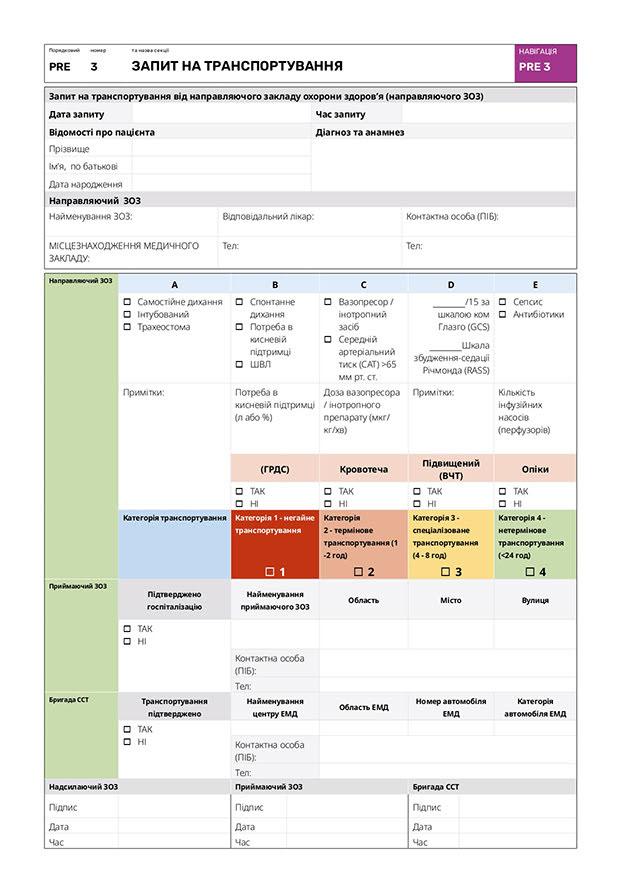
ДОДАТОК 4: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ
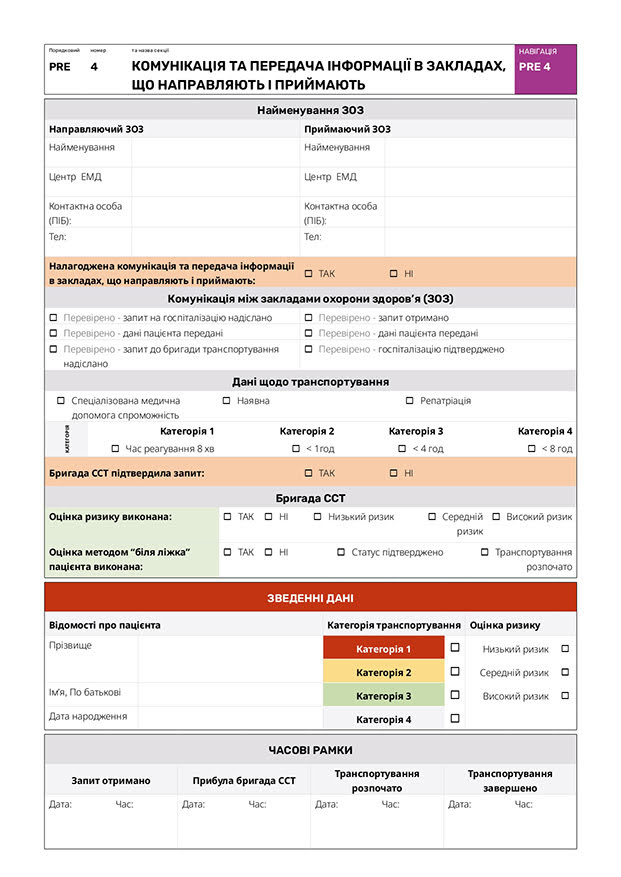
ДОДАТОК 5: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ

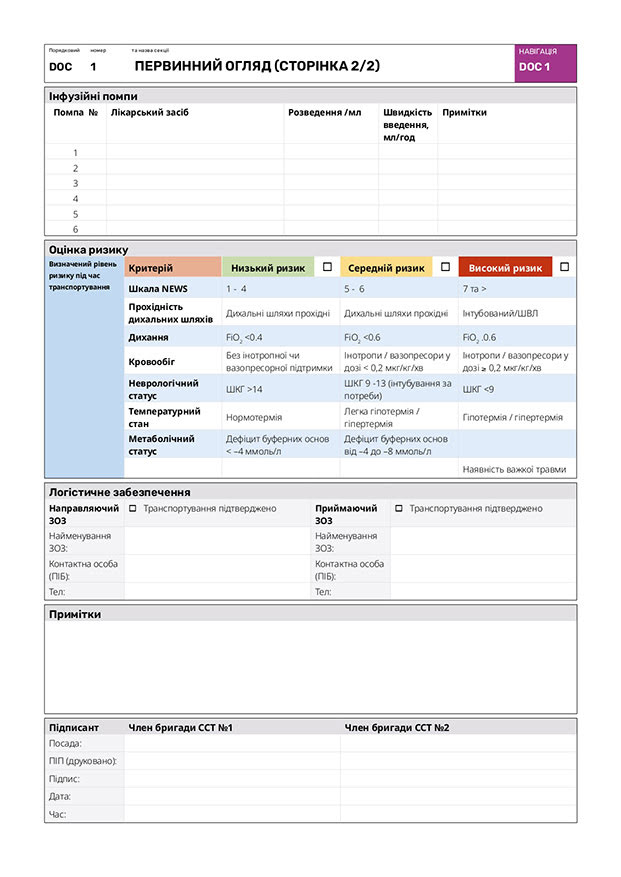
ДОДАТОК 6: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ
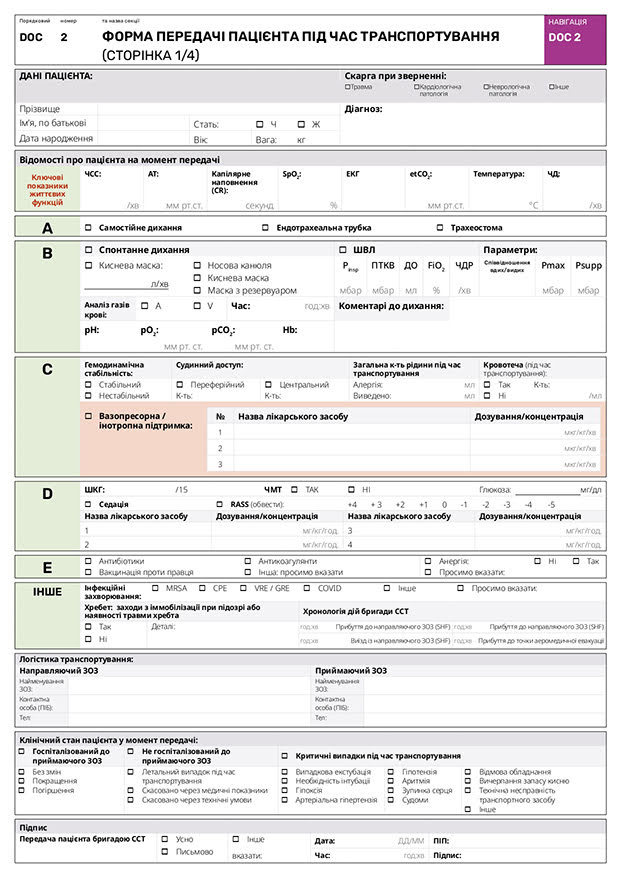
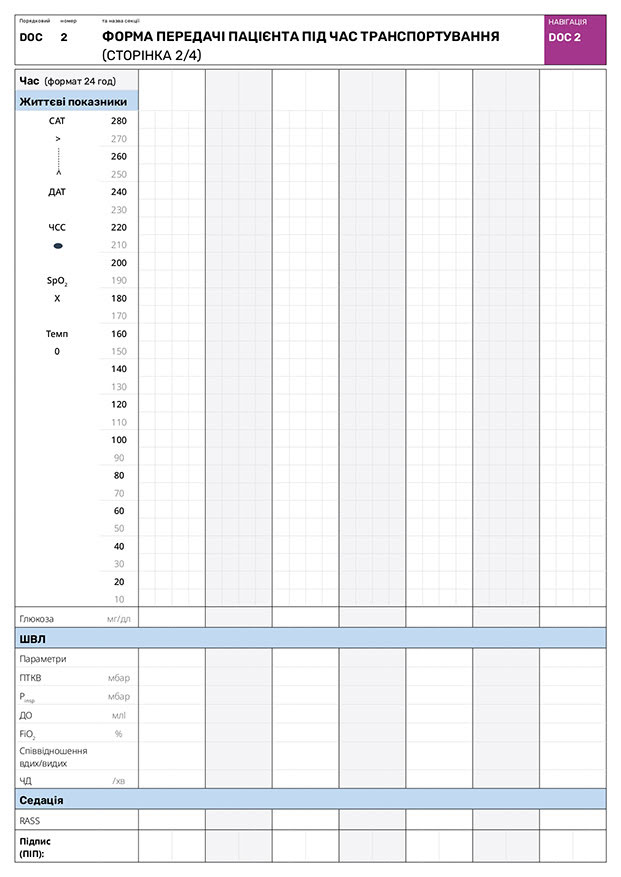
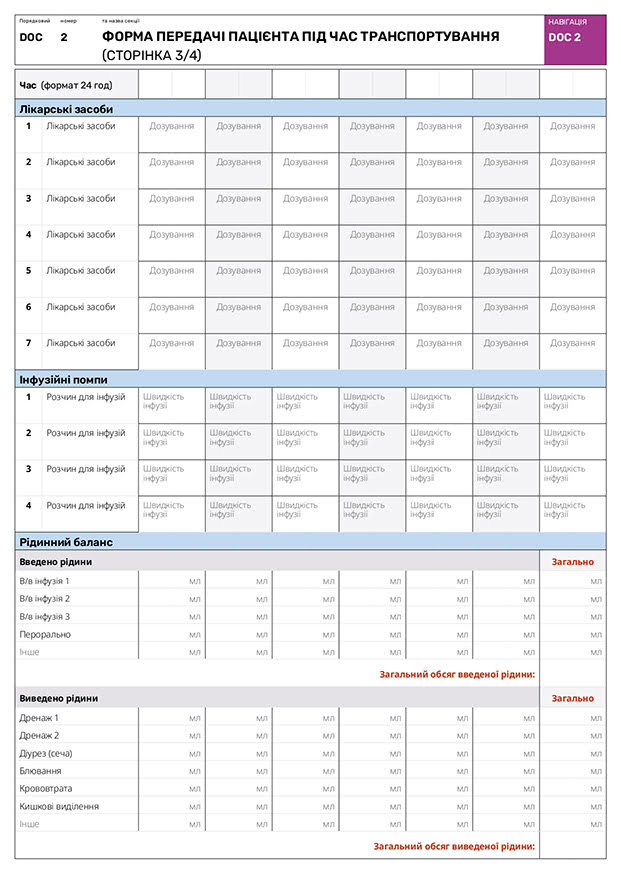

ДОДАТОК 7: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ

ДОДАТОК 8: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ПЕРЕД ТРАНСПОРТУВАННЯМ
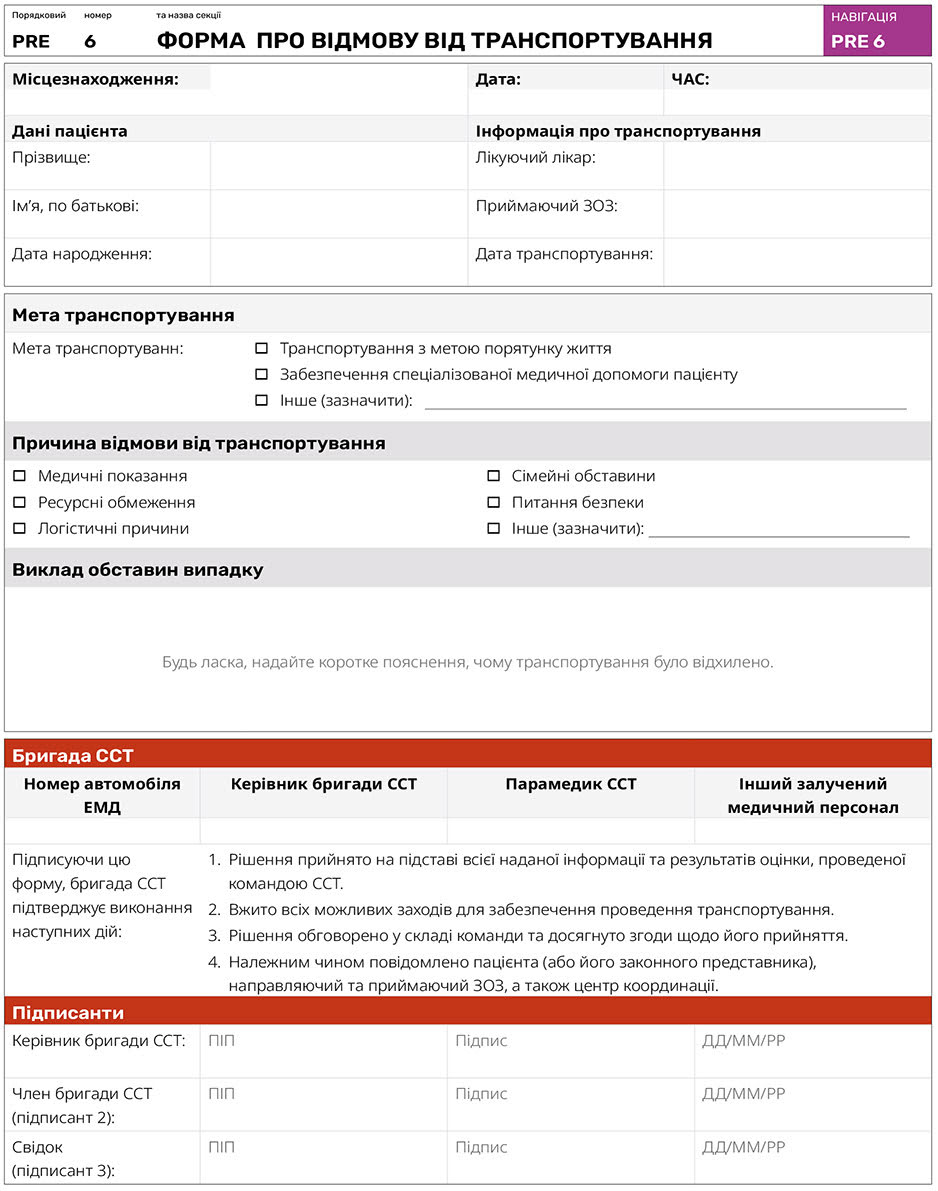
ДОДАТОК 9: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ДИХАЛЬНІ ШЛЯХИ

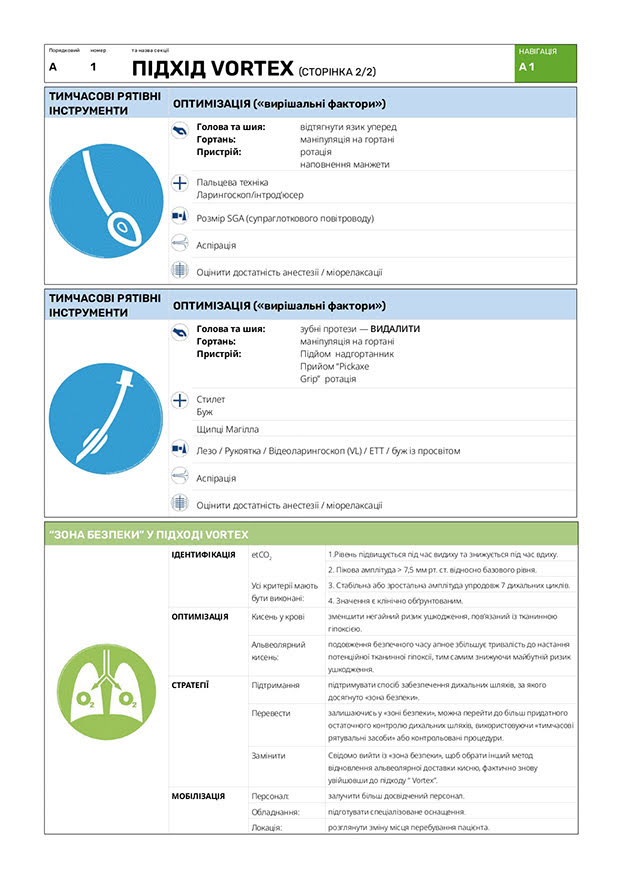
ДОДАТОК 10: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ДИХАЛЬНІ ШЛЯХИ

ДОДАТОК 11: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ДИХАННЯ
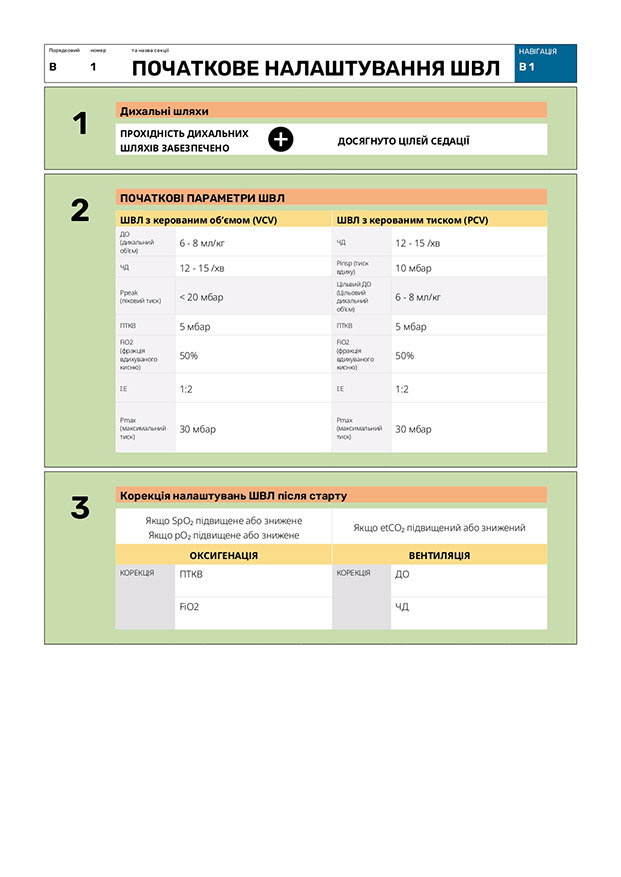
ДОДАТОК 12: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ДИХАННЯ
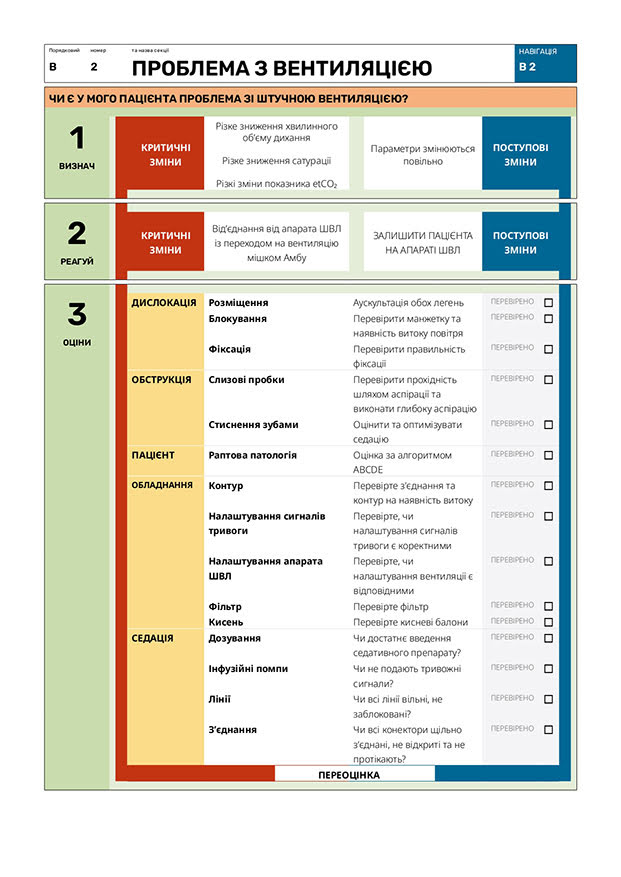
ДОДАТОК 13: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ДИХАННЯ
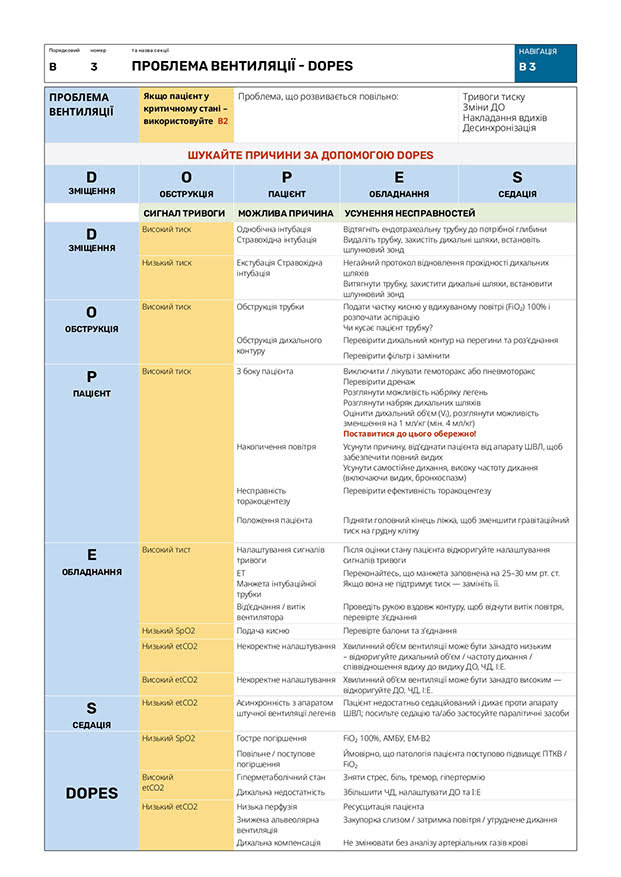
ДОДАТОК 14: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: ДИХАННЯ
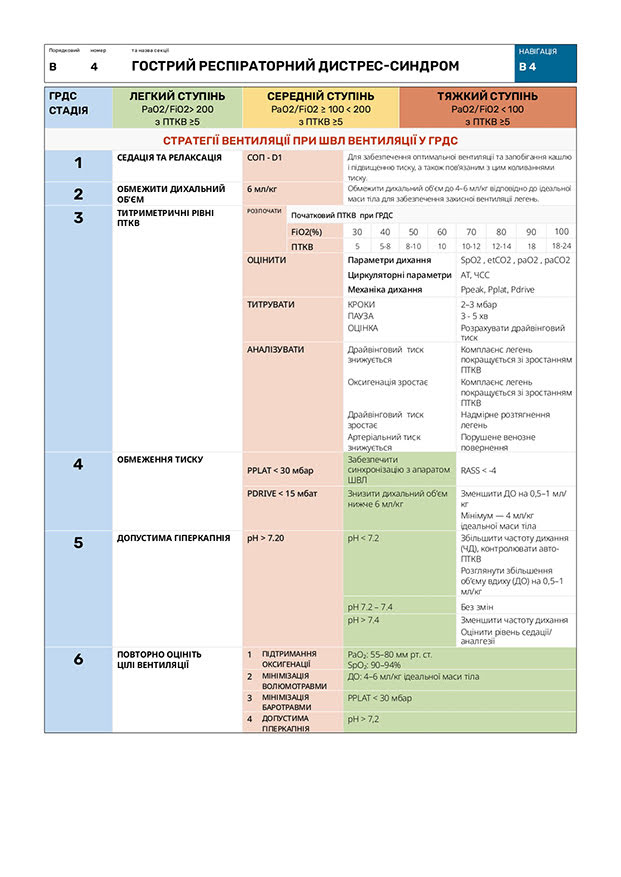
ДОДАТОК 15: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
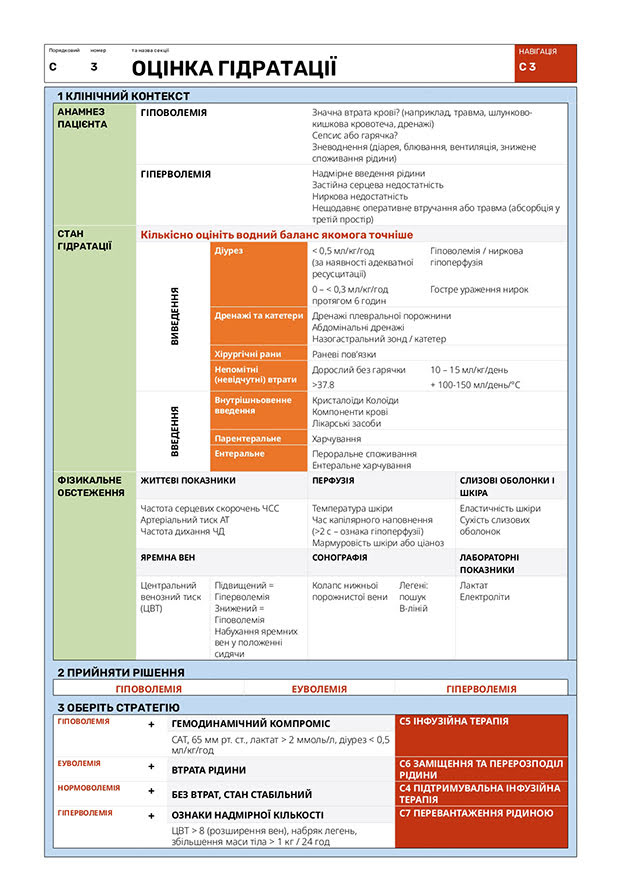
ДОДАТОК 16: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
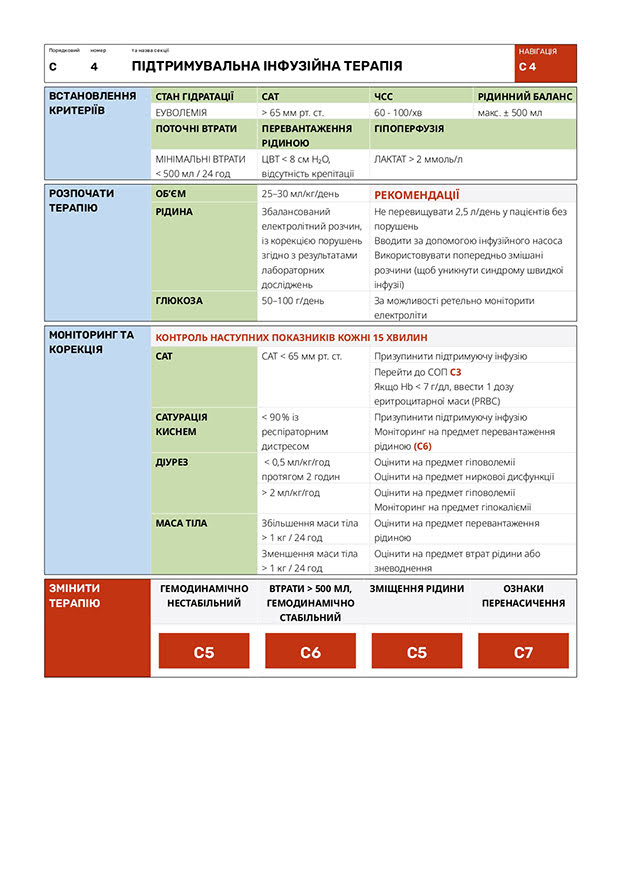
ДОДАТОК 17: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
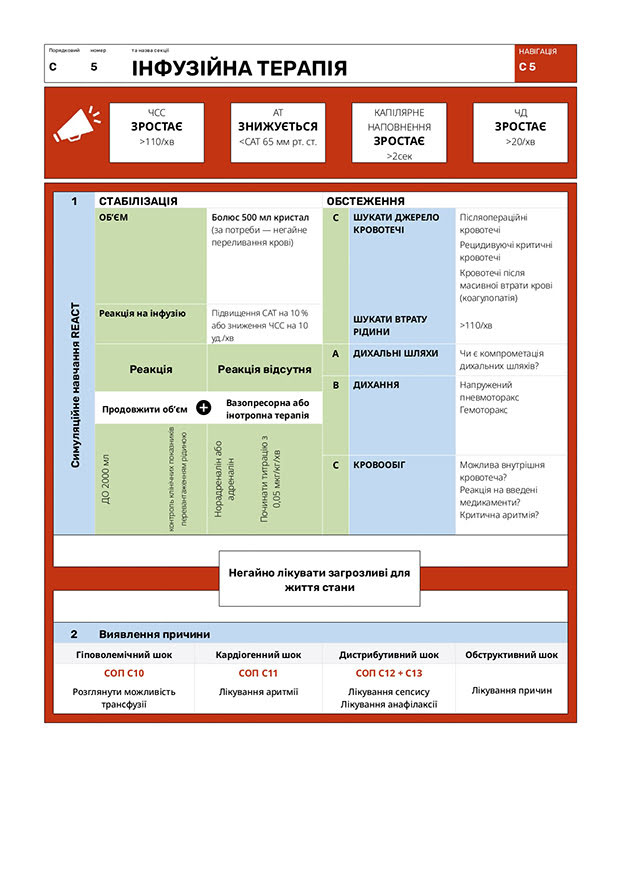
ДОДАТОК 18: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
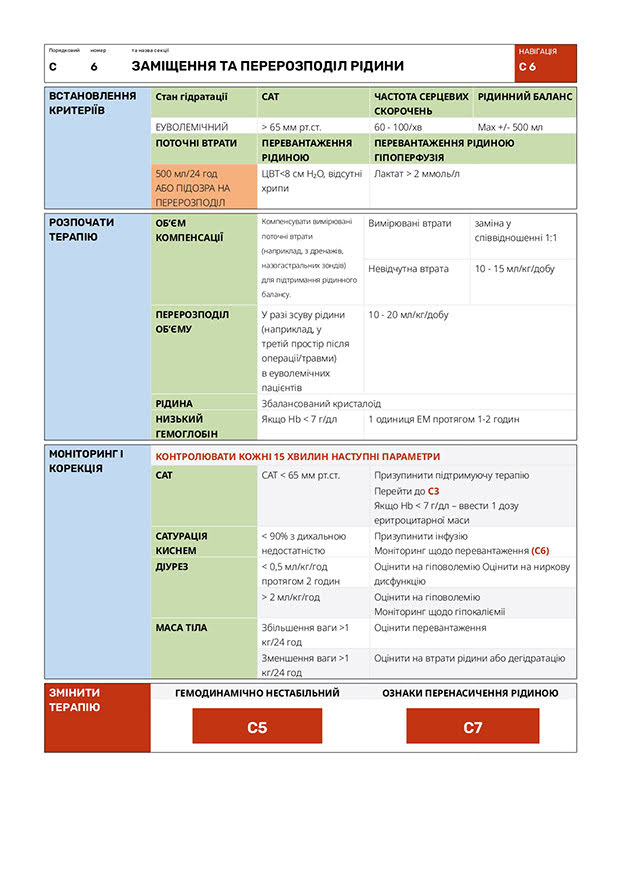
ДОДАТОК 19: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
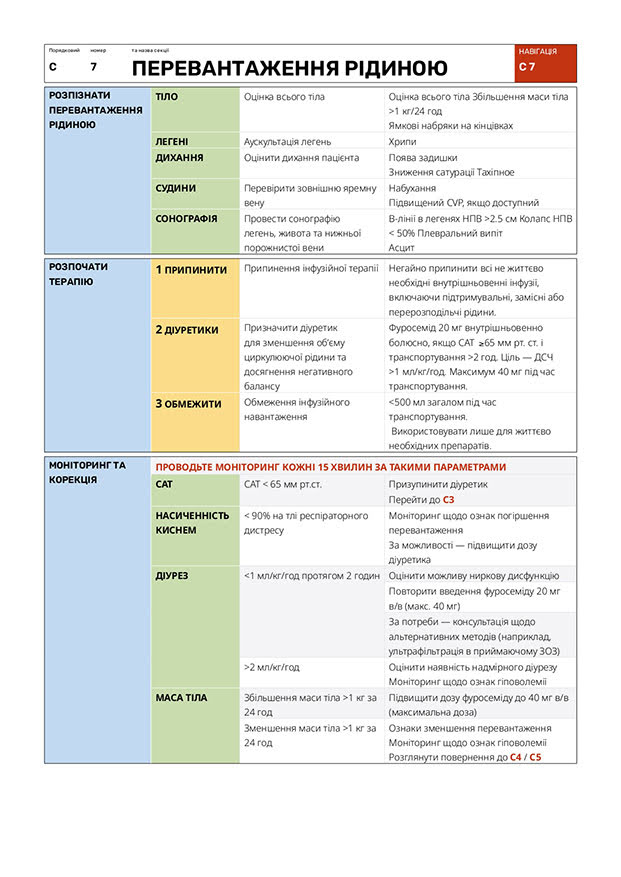
ДОДАТОК 20: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
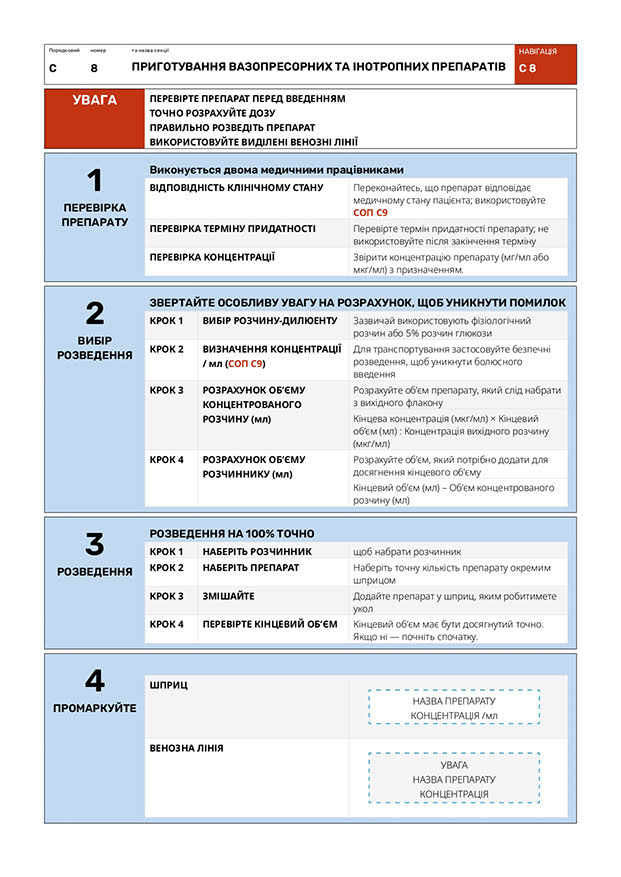
ДОДАТОК 21: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
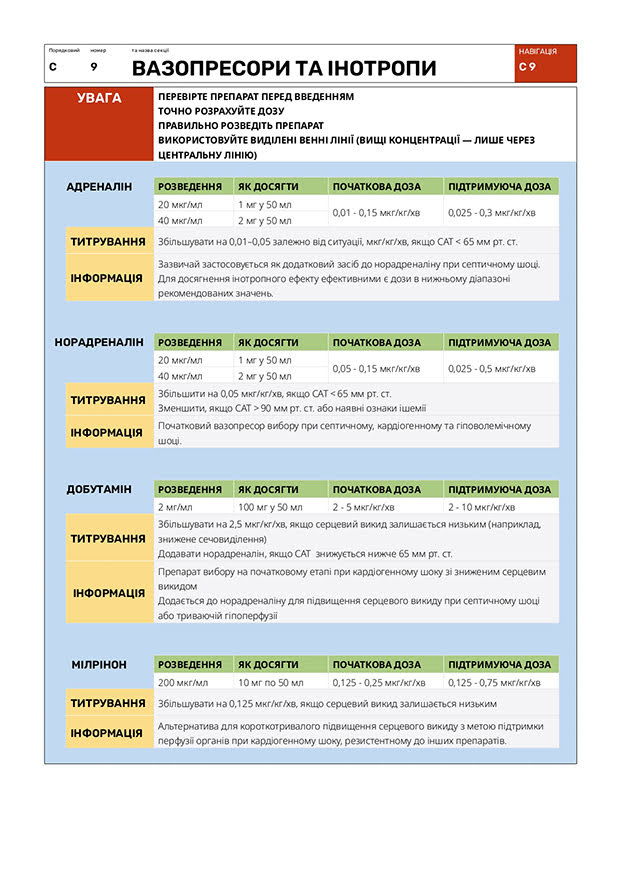
ДОДАТОК 22: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
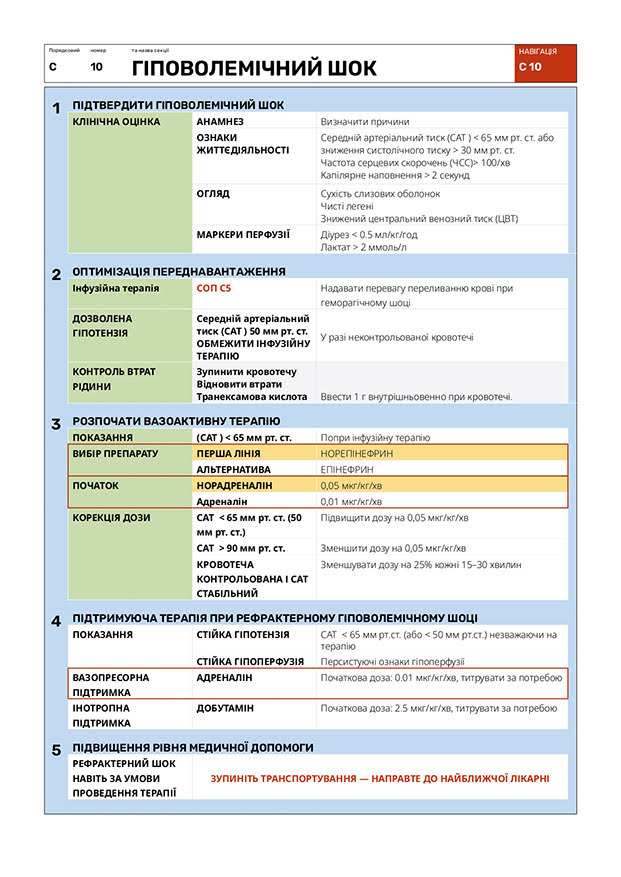
ДОДАТОК 23: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
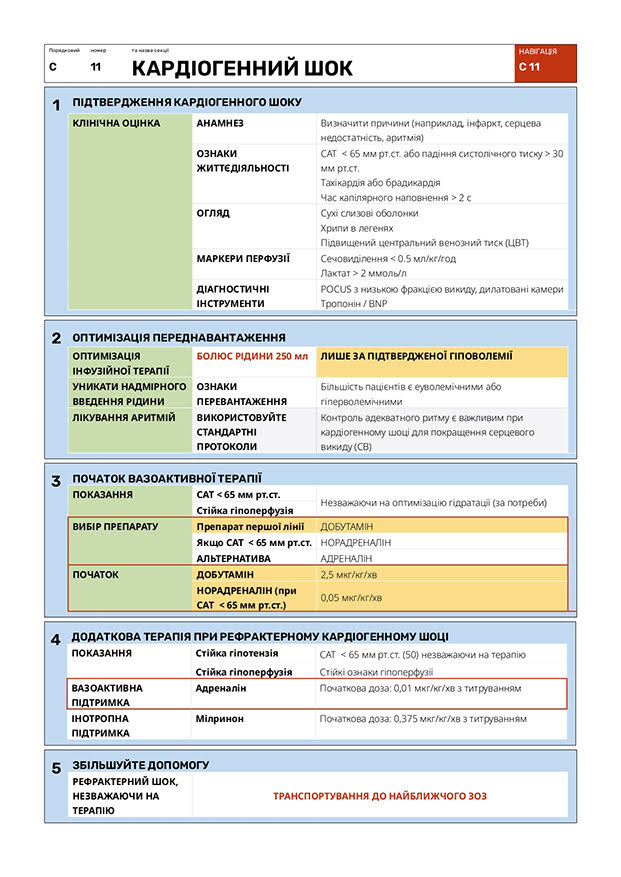
ДОДАТОК 24: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
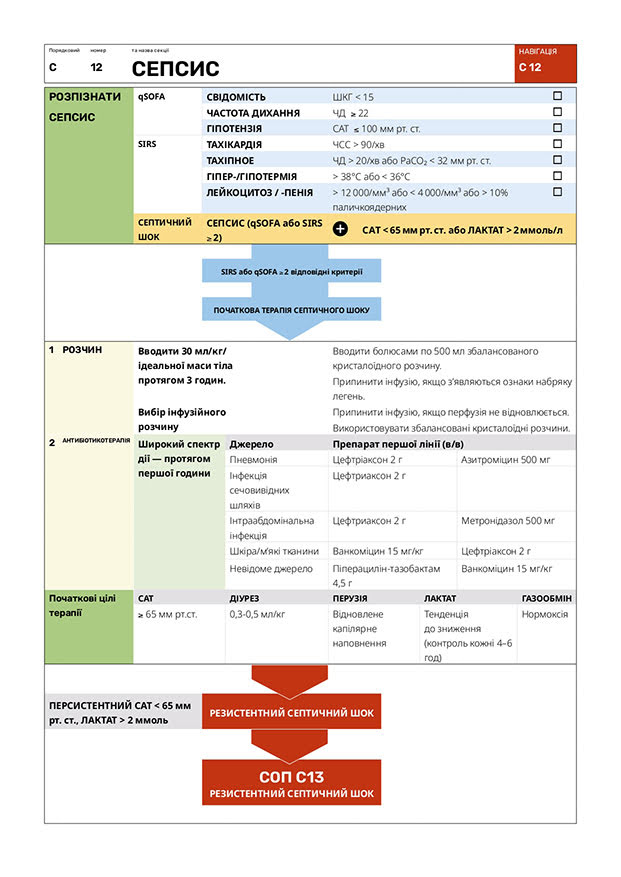
ДОДАТОК 25: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: КРОВООБІГ
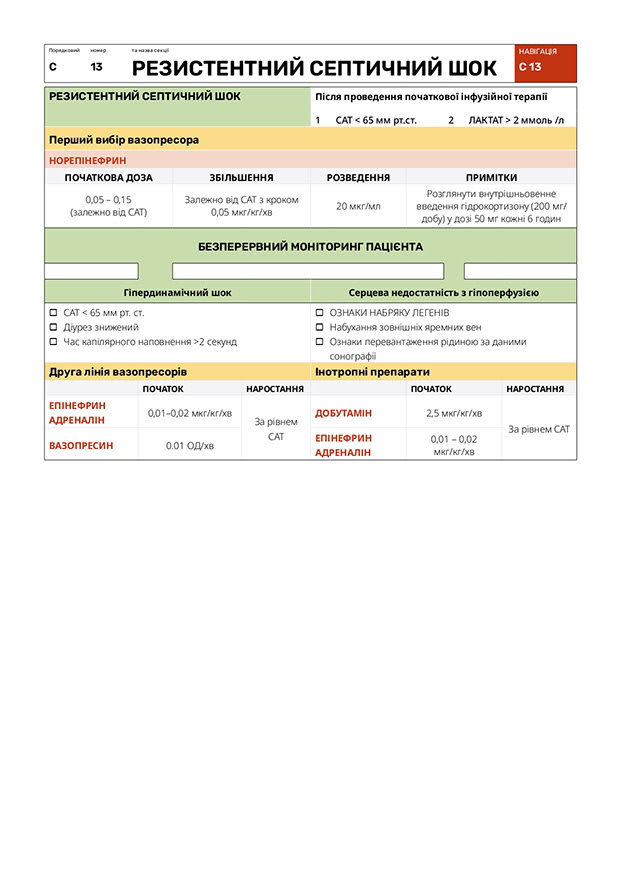
ДОДАТОК 26: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: НЕВРОЛОГІЧНИЙ СТАН
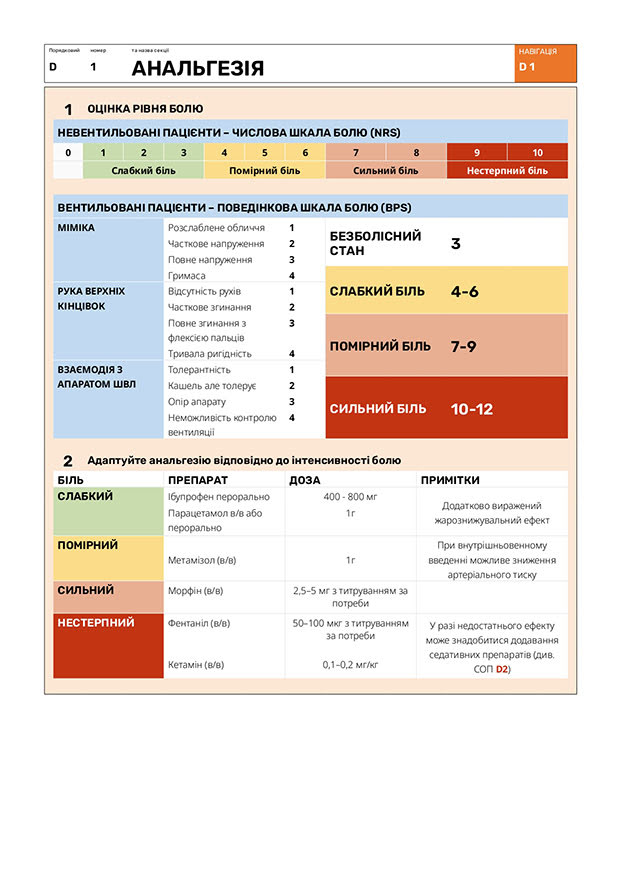
ДОДАТОК 27: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: НЕВРОЛОГІЧНИЙ СТАН

ДОДАТОК 28: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: НЕВРОЛОГІЧНИЙ СТАН
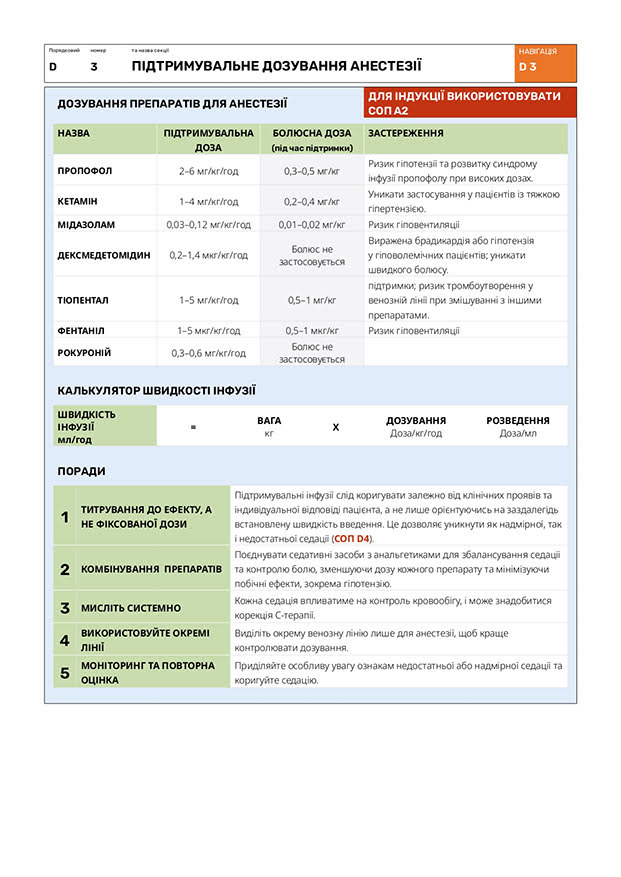
ДОДАТОК 29: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: НЕВРОЛОГІЧНИЙ СТАН
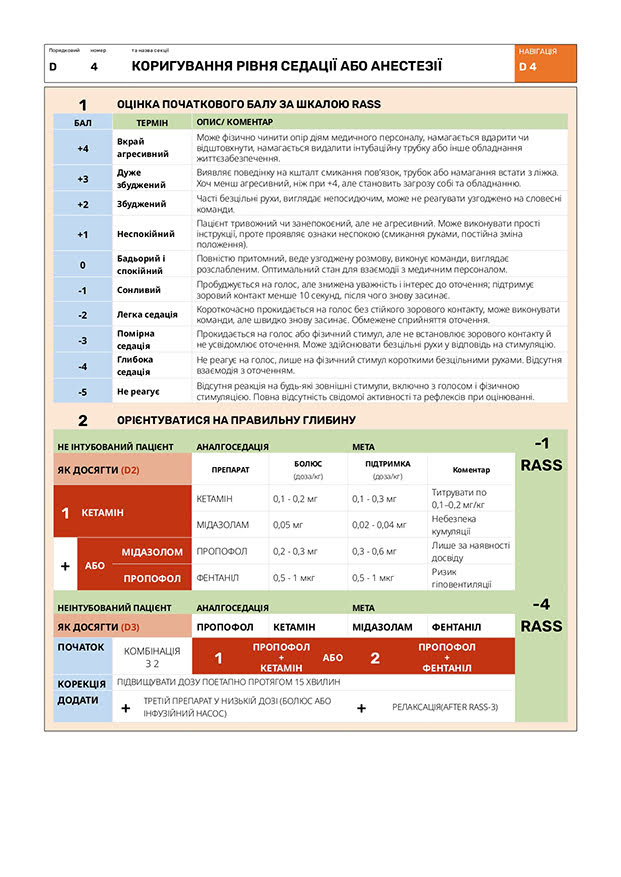
ДОДАТОК 30: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: НЕВРОЛОГІЧНИЙ СТАН
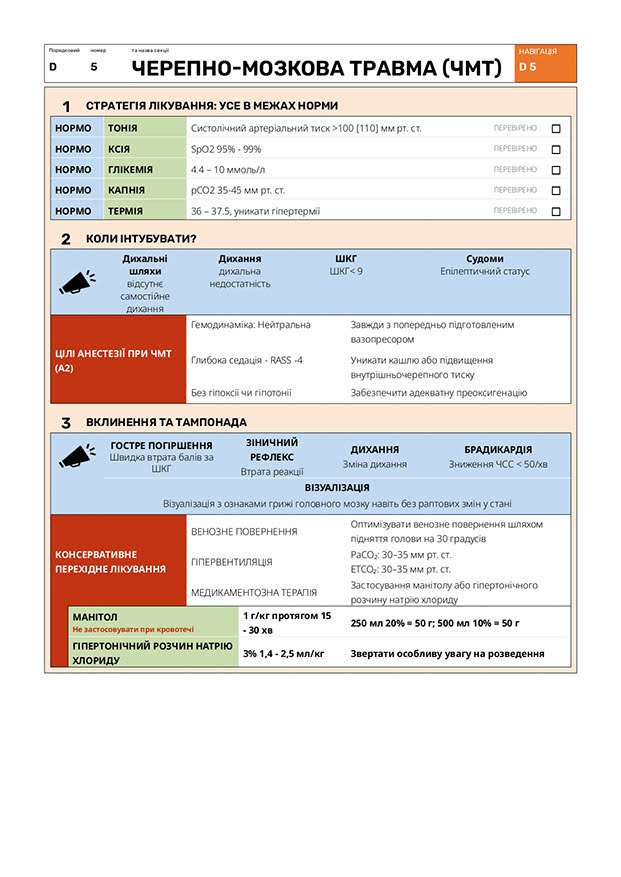
ДОДАТОК 31: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: МЕДИЧНІ ВТРУЧАННЯ

ДОДАТОК 32: СТАНДАРТНІ ОПЕРАЦІЙНІ ПРОЦЕДУРИ: МЕДИЧНІ ВТРУЧАННЯ
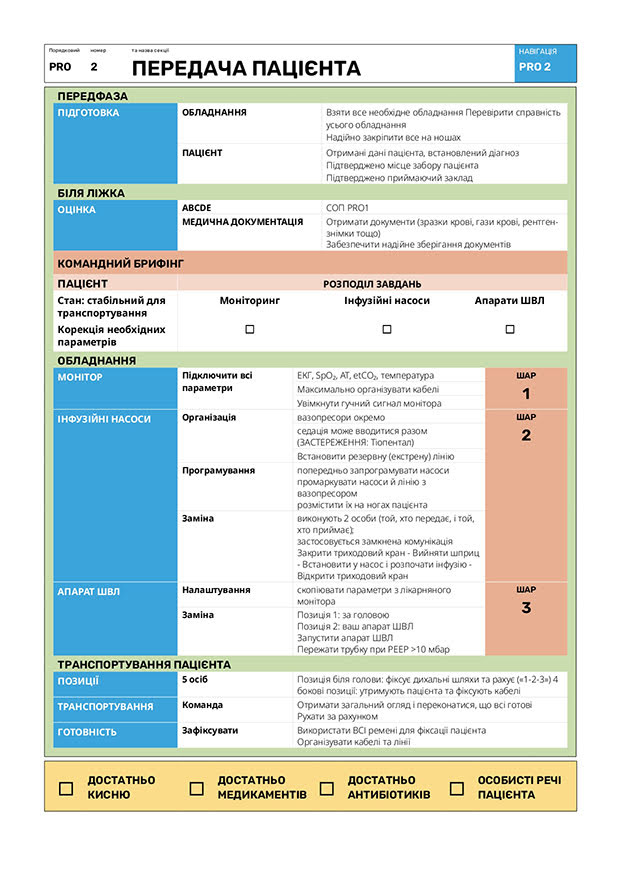






 Вхід у “зону безпеки” не є тотожним нормалізації SpO₂. Перебуваючи у “зоні безпеки”, команда може залишатися на поточному методі забезпечення оксигенації, оптимізувати його чи обрати альтернативний. У “зоні безпеки” допускається підтримання поточного способу порятунку життя, його заміна або перехід на інший. Додатково здійснюється підготовка персоналу, обладнання, за потреби — зміна місця надання допомоги.
Вхід у “зону безпеки” не є тотожним нормалізації SpO₂. Перебуваючи у “зоні безпеки”, команда може залишатися на поточному методі забезпечення оксигенації, оптимізувати його чи обрати альтернативний. У “зоні безпеки” допускається підтримання поточного способу порятунку життя, його заміна або перехід на інший. Додатково здійснюється підготовка персоналу, обладнання, за потреби — зміна місця надання допомоги.






































































































































