Вихідна інформація
Укуси змій, які нещодавно були віднесені до категорії “забутих” тропічних хвороб (Neglected tropical diseases) та є глобальним пріоритетом охорони здоров'я згідно з Всесвітньою організацією охорони здоров'я (ВООЗ), щорічно призводять до розвитку близько 2,5 млн отруєнь, 138 000 смертей та більш ніж 500 000 випадків постійної втрати працездатності в усьому світі.1-10 Отруєння внаслідок укусів змій, павуків та скорпіонів є поширеними екзогенними та професійними чинниками ризику для військовослужбовців у цілому світі.11-46 Наслідки отруєнь варіюють від легких місцевих реакцій до постійної втрати працездатності або навіть смерті. Прогноз щодо стану пацієнта значною мірою визначається часом введення протиотрути та рівнем підготовки залучених медичних працівників.
Після укусу починається змагання лікаря і пацієнта з часом; метою є нейтралізація активних компонентів отрути до появи серйозних наслідків для організму. Некроз, викликаний цитотоксичними отрутами, є незворотнім, проте його розвитку можна запобігти шляхом раннього введення протиотрути, або ж зупинити його поширення та появу подальших пошкоджень у випадках пізнього введення протиотрути.1,7,47,48 Гемотоксичні отрути можуть викликати розвиток коагулопатії в межах години після потрапляння в організм, що супроводжуватиметься швидким розвитком місцевих та системних зовнішніх і внутрішніх кровотеч. Нейротоксичні отрути можуть діяти швидко та призводити до смерті. Африка є одним із небагатьох місць на Землі, де мешкають такі змії, як чорна мамба, отрута котрих здатна вбити людину протягом однієї години після укусу. Більшість пацієнтів, укушених чорною мамбою, яким не була швидко введена протиотрута, помирають протягом 2–6 годин внаслідок зупинки дихання.1,49 При потраплянні в організм нейротоксичної отрути під час укусу швидке введення протиотрути (ще до появи слабкості дихальних м’язів) може зупинити прогресування низхідного паралічу та розвитку серйозних системних проявів.1,50,51 Кожна втрачена година від моменту укусу до введення протиотрути асоційована з різким зростанням смертності, а також розвитком хронічних ускладнень або пожиттєвих наслідків, таких як ампутації, залишкові деформації, посттравматичний стресовий розлад (ПТСР), сліпота, пошкодження нирок, інфекції та часткова або повна втрата функції ураженої кінцівки.4,7,8,52–58
Дані настанови надають інформацію про допомогу постраждалим у випадку укушень отруйними зміями для кожного з Командувань Збройних сил США.
Загальні принципи лікування укусів змій
Не намагайтесь ідентифікувати змію. Не слід спеціально витрачати на це час, адже даний процес є ненадійним. НЕ НАМАГАЙТЕСЯ зловити або вбити змію; лікування базується на клінічних ознаках, через що немає потреби у визначенні виду плазуна.
Виділено 3 основні клінічні синдроми, що виникають внаслідок укусу змій, кожен з яких включає 3 головні ознаки/симптоми. Усі небезпечні змії, що здатні отруїти або вбити людину, спричинятимуть появу принаймні однієї ознаки/симптому щонайменше одного із 3-х основних синдромів (нейротоксичного, гемотоксичного та цитотоксичного). Перебування у певному регіоні визначатиме використання специфічної протиотрути, проте основні клінічні тріади залишаються незмінними, незалежно від географії.
Малюнок 1. Клінічні тріади, характерні для укусів змій.
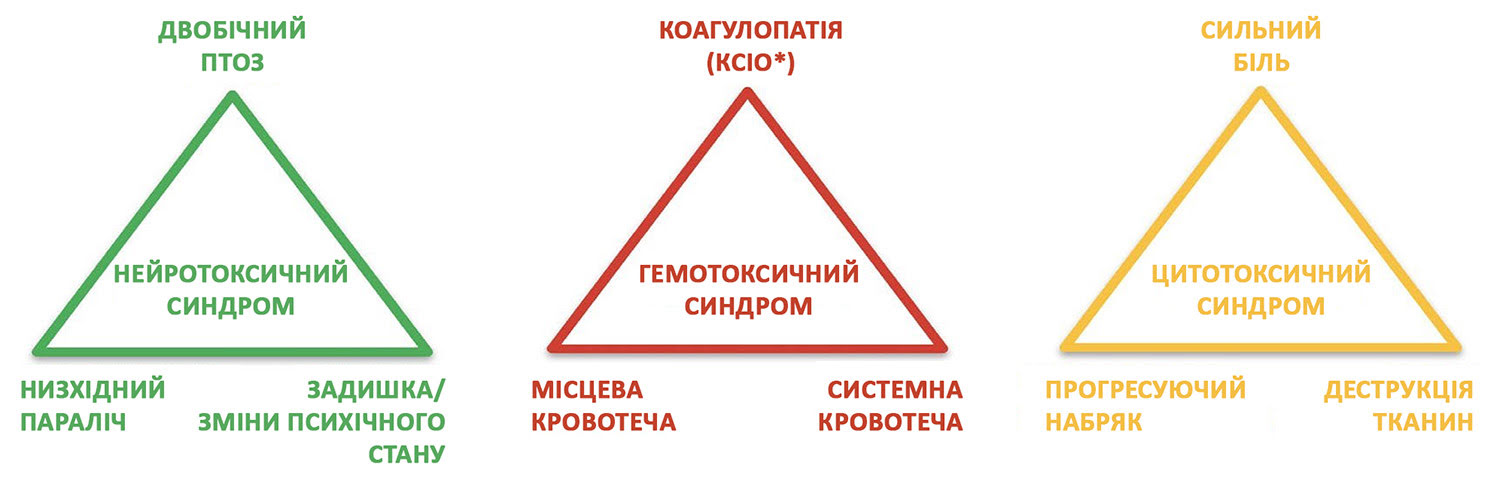
* КСІО - Коагулопатія споживання, індукована отрутою (VICC - Venom-induced consumption coagulopathy)
Укуси змій та використання протиотрути - перлини клінічної мудрості
- Не всі змії отруйні, і не всі укуси змій призводять до розвитку отруєння!
Більшість змій не становлять небезпеки для людини, і лише ~600 із понад 3500 видів змій у всьому світі вважаються потенційно небезпечними. Однак, останні часто наближаються до людських осель у пошуках їжі, води чи притулку; випадки отруєнь внаслідок укусів змій дуже поширені у країнах, що розвиваються. - Приблизно 25% укусів небезпечних отруйних змій є нешкідливими - «сухими укусами», під час яких отрута в рану не вводиться!
- Це означає, що навіть за наявної інформації про укус вашого пацієнта змією, яка належить до небезпечного виду, постраждалий не завжди потребуватиме лікування протиотрутою. Хоча точний відсоток залежить від виду, в середньому 25% укусів отруйних змій вважаються «сухими». Вони призначені для відлякування плазунами потенційної загрози, яка є надто великою, аби її з’їсти, без витрачання отрути. Утворення отрути метаболічно витратне, тому, за можливості, змії будуть намагатися зберегти її для потенційної здобичі.
- Феномен «сухого укусу» пояснює, чому багато людей вважають, що неефективні або потенційно шкідливі втручання, такі як використання відсмоктувачів отрути або чорних каменів, діють: виглядає, ніби такі пацієнти дивовижним чином одужали завдяки проведеному лікуванню, проте насправді вони ніколи й не хворіли!
- Лікування укусу змії завжди має визначатися на основі клінічної картини, а також розвитку характерних ознак і симптомів у пацієнта, а не видом змії, яка його вкусила!
- Пам’ятайте, що багато укусів змій часто виникають внаслідок атаки неотруйних плазунів, і що приблизно 1/4 людей, укушених небезпечними видами, швидше за все, будуть почуватися добре через феномен «сухого укусу». Багато небезпечних видів змій зовнішньо виглядають як неотруйні, і навпаки (явище мімікрії). Не намагайтеся визначити вид змії, якщо ви не є герпетологом. Ідентифікація виду не змінить лікування пацієнта!
- Не проводьте лікування пацієнтів просто на підставі того, що вони були вкушені небезпечним видом змії.
- Завжди лікуйте пацієнтів, яких вкусила змія, базуючись на наявних ознаках і симптомах. Постраждалий, який приносить вам мертву змію-мамбу, але не має жодних ознак чи симптомів отруєння, не потребує введення протиотрути (крім випадків розвитку прогресуючих ознак та симптомів від дії отрути). І навпаки, пацієнт, який не пам’ятає факту укусу змії або вважає, що дана змія була неотруйною, потребуватиме спеціального лікування у випадку подальшого розвитку прогресуючого набряку, системної кровотечі або інших ознак трьох клінічних тріад, які виникають внаслідок укусів змій.
- Абсолютних протипоказань щодо застосування протиотрути у пацієнтів із симптомами отруєння внаслідок укусу змії немає. Ризик розвитку стійкого порушення функцій організму внаслідок отрути, яка не була нейтралізована, є набагато вищим, ніж ризик виникнення анафілаксії внаслідок дії високоякісної сучасної протиотрути.
- Раннє введення протиотрути є золотим стандартом лікування укусів змій та найбільш ефективним способом зниження ризику смерті або постійної втрати працездатності серед пацієнтів.
- Раннє введення протиотрути в польових умовах поблизу або безпосередньо на місці отримання укусу може припинити розвиток отруєння до моменту появи будь-яких серйозних системних ознак чи симптомів.
- Не звертайте уваги на пакування та інструкцію від виробника - дійте відповідно до вказівок, викладених у цих клінічних настановах.
- Дозування та спосіб введення рекомендованих протиотрут, представлені у даних настановах, можуть суттєво відрізнятися залежно від препаратів; шукайте відповідну до наявної у вас протиотрути інструкцію, вміщену далі в документі.
- Протиотруту можна вводити шляхом внутрішньовенної (ВВ) або внутрішньокісткової (ВК) ін’єкції чи інфузії.54,59 Кращим варіантом є ВВ введення препарату, проте прийнятною альтернативою може бути і ВК шлях, при якому ефективність дії лікарського засобу не змінюється.
- НЕ ВВОДЬТЕ протиотруту шляхом внутрішньом’язової (ВМ) чи підшкірної (ПШ) ін’єкції, навіть якщо даний шлях зазначений на упаковці. Концентрація в крові протиотрути, введеної ВМ або ПШ, ніколи не буде більшою, ніж швидко отримана концентрація при ВВ введенні.
- Перед введенням повного об’єму протиотрути НЕ ВВОДЬТЕ її пробні дози для перевірки гіперчутливості. Такі дози не мають прогностичного значення у виявленні пацієнтів із гіперчутливістю та є лише витратою часу і протиотрути.60–63
- Доза протиотрути не залежить від ваги постраждалого, тому доза для дорослих і дітей однакова.
- Необхідна доза протиотрути пропорційна дозі отрути, введеної пацієнту. Кількість отрути, що потрапила до організму пацієнта, відповідає тяжкості синдрому(ів) отруєння.
- Додаткову дозу протиотрути слід вводити стільки разів, скільки потрібно, доки не буде досягнуто контролю над отруєнням.
- Під час фази активного лікування занепокоєння щодо передозування протиотрутою слід відкласти; найгіршим сценарієм тут буде розвиток алергічної реакції. У випадку появи у пацієнта реакції на великі дози препарату, вона, швидше за все, проявиться через 1–3 тижні у вигляді так званої сироваткової хвороби (гарячка, висип, артралгії тощо). У випадку виникнення даних скарг пацієнта можна лікувати антигістамінними препаратами або стероїдами. Сироваткова хвороба може погано переноситись, але вона не несе загрози для життя.
- Складіть графік та відслідковуйте показники через певні проміжки часу, спостерігаючи за динамікою стану. Проведення періодичного оцінювання та документування даних є надзвичайно важливим, оскільки зменшення/розрішення певних клінічних симптомів буде індикатором того, що на даний час введена достатня доза протиотрути. Мінімальні дані, що завжди мають бути занотовані:
- Час і дата укусу змії
- Час, що минув від моменту укусу до надходження постраждалого (запишіть у вигляді хвилин, годин, днів тощо)
- Час введення першої дози протиотрути (визначається як “Година 0/Hour 0”, записується як “Год0/H0”)
- Завжди виконуйте повну повторну оцінку стану постраждалого після укусу змії через 2, 4, 6, 12 і 24 годин (Год2, Год4, Год6, Год12, Год24) після введення першої дози протиотрути. Таким чином ви визначите динаміку клінічних проявів синдромів укусу змії з плином часу.
- Укуси змій є клінічно динамічними екстреними ситуаціями, перебіг яких може різко змінюватися аж до моменту досягнення повного контролю за станом постраждалого.
Спочатку в пацієнтів можуть спостерігатися прояви одного синдрому, а пізніше з’являтися ознаки та симптоми іншого (наприклад, у постраждалого з локальним болем і легким набряком на Год0 може розвинутися місцева кровотеча або птоз на Год4). Завжди проводьте пошук ознак та симптомів усіх трьох тріад під час повторної оцінки стану пораненого. За потреби змінюйте тактику лікування відповідно до змін клінічної картини.
Універсальний підхід до лікування пацієнта, укушеного змією
Початкові пріоритети
- Прохідність дихальних шляхів, дихання, кровообіг та швидке введення протиотрути є пріоритетами під час стабілізації стану та лікування постраждалого від укусу змії.
- Оцініть стан постраждалого за алгоритмом “ABC”; перш ніж продовжити огляд, визначте та усуньте усі загрозливі для життя стани.
- Зверніться до Протоколу лікування гострої судинної недостатності (колапсу) для отримання конкретних інструкцій щодо стабілізації стану та лікування пацієнтів, у яких стрімко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та/або діарея протягом перших 30 хвилин після укусу змії.
- Проводьте лікування можливих вторинних патологічних станів (таких як анафілаксія або гіповолемічний шок) відповідно до стандартних клінічних протоколів.
- Перш ніж продовжити, забезпечте ВВ або ВК доступ на кінцівці, де немає укусів.
- НЕ НАКЛАДАЙТЕ компресійні бандажі або турнікети, оскільки вони можуть посилити місцеве пошкодження тканин та підвищити ризик постійної втрати працездатності.64–66
Якщо попередньо було накладено турнікет, не знімайте його до моменту повної готовності до проведення лікування та ресусцитації пацієнта, оскільки існує можливість розвитку швидкої декомпенсації.67,68 Знімайте турнікет поступово (послабте на кілька секунд – затягніть – спостерігайте – повторіть) впродовж 20-30 хв.; у випадку появи симптомів отруєння введіть протиотруту та зачекайте щонайменше 30 хвилин, перш ніж продовжити зняття турнікета. В ідеальних умовах турнікет має залишатися на кінцівці до появи доступу до протиотрути, проте тривалий час евакуації без введення препарату може призвести до потреби ранішого зняття турнікета (з метою попередження втрати кінцівки). Зверніться до Настанов Об'єднаної системи лікування травм з Допомоги пораненим в умовах бойових дій (Joint Trauma System Tactical Combat Casualty Care (TCCC) Guidelines) щодо питань конверсії турнікета в цих умовах. - Якщо і коли дозволяють умови, зведіть до мінімуму рухову активність пацієнта та виконайте нетуге знерухомлення укушеної кінцівки з метою зменшення обсягу рухів без стиснення тканин.
- У випадку відсутності протиотрути на місці події оберіть той варіант евакуації, яким відбудеться безпечне транспортування пораненого до місця знаходження препарату у найшвидший термін. У деяких випадках це навіть може бути варіант, коли постраждалий самостійно піде до місця надання допомоги.
- Утримуйте укушену кінцівку в зручному положенні піднятою вище рівня серця за наявності відповідних умов під час транспортування.
- Після того, як пацієнт прибув до лікарні та був укладений на ліжко, надайте кінцівці з укусом якомога вище положення (за наявних умов та можливості з боку пацієнта намагайтесь досягти положення під кутом мінімум 60º в положенні хворого лежачи), щоб зменшити онкотичний тиск на набряклі тканини.
- Огляньте щодо специфічних ознак і симптомів зміїного отруєння. Дивіться Таблицю 1 та зверніться до відповідних критеріїв стосовно початкового та повторного введення протиотрути, а також ознайомлення з додатковою інформацією.
Цілеспрямована оцінка та обстеження
Зберіть анамнез та проведіть фізикальне обстеження, зосереджуючись на виявленні ознак і симптомів нейротоксичного, гемотоксичного та цитотоксичного синдромів внаслідок укусу змії.
- Визначте, як давно відбувся укус. За допомогою перманентного маркера обведіть місце ураження на тілі пораненого та зазначте конкретний час появи укусу.
- Не покладайтеся на сліди від зубів змії, щоб оцінити можливість укусу чи отруєння. Змії можуть залишати на тілі постраждалого проколи, численні рвані рани або взагалі не лишити явних слідів від зубів.
- Проведіть швидке обстеження щодо наявності болю, набряку або руйнування тканин (цитотоксичний синдром). За допомогою перманентного маркера окремо позначте межі болючості (пунктирна лінія) і набряку (суцільна лінія), а також запишіть час оцінювання біля кожної з ліній.
- Виконайте швидке обстеження щодо наявності місцевої або системної кровотечі (гемотоксичний синдром)
- Огляньте уражену кінцівку на предмет тривалої місцевої кровотечі (> 30 хв) з місця укушеної рани (якщо її видно) або з ділянок інших пошкоджень.1,70–72
- Огляньте ясна молярів та інші слизові оболонки на наявність ознак системної кровотечі.1,69,70
- Виконайте швидке обстеження щодо наявності ознак нервово-м'язової слабкості (нейротоксичний синдром)
- Оцініть слабкість дихальних м’язів за допомогою тесту рахунку на одному подиху.72 Періодично повторюйте дане обстеження, щоб визначити тенденцію до покращення або погіршення дихальної функції протягом часу.
- Тест рахунку на одному подиху (single breath count - SBC) не потребує обладнання та легко виконується в непристосованих умовах:
Попросіть пацієнта зробити глибокий вдих і якомога довше рахувати вголос, не змінюючи при цьому свій звичайний тембр та не роблячи додатковий вдих. Продемонструйте виконання тесту пацієнтові, після чого попросіть його повторити завдання та запишіть найбільше число, до якого дорахував пацієнт. - Тест SBC тісно корелює зі спірометричними показниками.
- Нормальний показник тесту становить приблизно 50, а значення < 20 вказують на необхідність проведення штучної вентиляції легень.
- Якщо є можливість, замість тесту рахунку на одному подиху може бути використана спірометрія, під час якої можна оцінити параметри негативного тиску на вдиху (NIF) та/або форсовану життєву ємність легень (ФЖЄЛ, FVC). Проведіть загальну оцінку та зверніть особливу увагу на наступне:
- Ознаки та симптоми низхідного млявого паралічу: птоз, диплопія, слабкість м’язів-згиначів шиї, бульбарний синдром тощо.1,54,73
- Ознаки та симптоми парасимпатичного/холінергічного кризу: мнемоніка SLUDGE - Слиновиділення (S-Salivation), сльозотеча (L-Lacrimation), сечовипускання (U-Urination), дефекація (D-Defecation), шлунково-кишкові розлади (G-GI distress), блювання (Е-Emesis).
- Виконайте та/або перевірте дані клінічних лабораторних досліджень, що наведені нижче (за наявності).
Нестабільні пацієнти
Протокол лікування гострої судинної недостатності (колапсу)
Протягом 30 хв після укусу в пацієнта швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта шляхом ВМ або ВВ введення адреналіну та рідин відповідно до протоколів лікування анафілаксії.
- Заінтубуйте постраждалого у випадку набряку дихальних шляхів, що не реагує на адреналін швидко.
- Слідом за адреналіном негайно застосуйте високу дозу відповідної для даного регіону протиотрути шляхом швидкого ВВ або ВК введення під час ресусцитації.
- Для боротьби з гіпотензією до моменту початку дії протиотрути проводьте підтримку рівня артеріального тиску за допомогою ВВ або ВК введення рідин та адреналіну.
Для отримання додаткової інформації зверніться до розділу «Гостра судинна недостатність (колапс)».
Лабораторні дослідження
До розширених лабораторних досліджень відносяться:
- Загальний аналіз крові (ЗАК)
- Рівень гемоглобіну (Hb) або гематокриту (HCT) - коли проведення ЗАК недоступне, але є можливість визначити Hb або HCT
- Протромбіновий час (ПЧ/англ.-PT), частковий тромбопластиновий час (АЧТЧ/англ.-PTT) і міжнародне нормалізоване співвідношення (МНВ/INR)
- Фібриноген
- Комплексна метаболічна панель (англ.-CMP)
- Креатинфосфокіназа (КФК/англ.-CK)
Простий коагуляційний тест для проведення у непристосованих умовах: у випадку відсутності розширених лабораторних можливостей використайте тест на визначення згортання цільної крові (Whole Blood Clotting Test, WBCT), як описано в Додатку А, для діагностики та моніторингу коагулопатій.
Особливості при транспортуванні
- У випадку евакуації пацієнта з польових умов або переміщення між етапами медичної допомоги переконайтесь, що приймаючий заклад має достатній запас відповідних для даного регіону протиотрут (перелічених у даних Настановах), щоб забезпечити належне лікування від укусів усіх видів місцевих небезпечних змій.
ПРИМІТКА: Евакуація не є альтернативою введенню протиотрути. Пацієнт, який має необхідність в евакуації внаслідок укусу змії, потребуватиме введення протиотрути. Чим раніше це буде виконано, тим більше буде шансів у постраждалого на повне одужання без розвитку стійкої втрати працездатності. НЕ ВІДКЛАДАЙТЕ введення протиотрути пацієнту з укусом змії в польових умовах.
- За наявності клінічних доказів отруєння та проведення лікування в умовах медичного закладу завжди призначайте суворий ліжковий режим з постійним моніторингом життєвих показників. У випадку відсутності початкових клінічних ознак отруєння помістіть хворого під нагляд на 24 год. Якщо лікування відбувається в польових умовах, постійно спостерігайте за станом пацієнта щодо появи ознак прогресування отруєння, покращення чи погіршення.
- Слід очікувати на появу симптомів отруєння протягом перших 24 год; якщо після 24 год у пацієнта повністю відсутні симптоми, то він, найбільш ймовірно, отримав “сухий” укус і може бути виписаний з медичного закладу. Див. Критерії виписки.
Початкове лікування за допомогою протиотрути
Рекомендації щодо дозування, підготовки та введення протиотрути відрізняються залежно від препарату. У ці Настанови з клінічної практики включені дані про спектр охоплення, початкове дозування, підготовку та введення протиотрут. Перед застосуванням протиотрути ознайомтеся із вказівками щодо відповідного препарату.
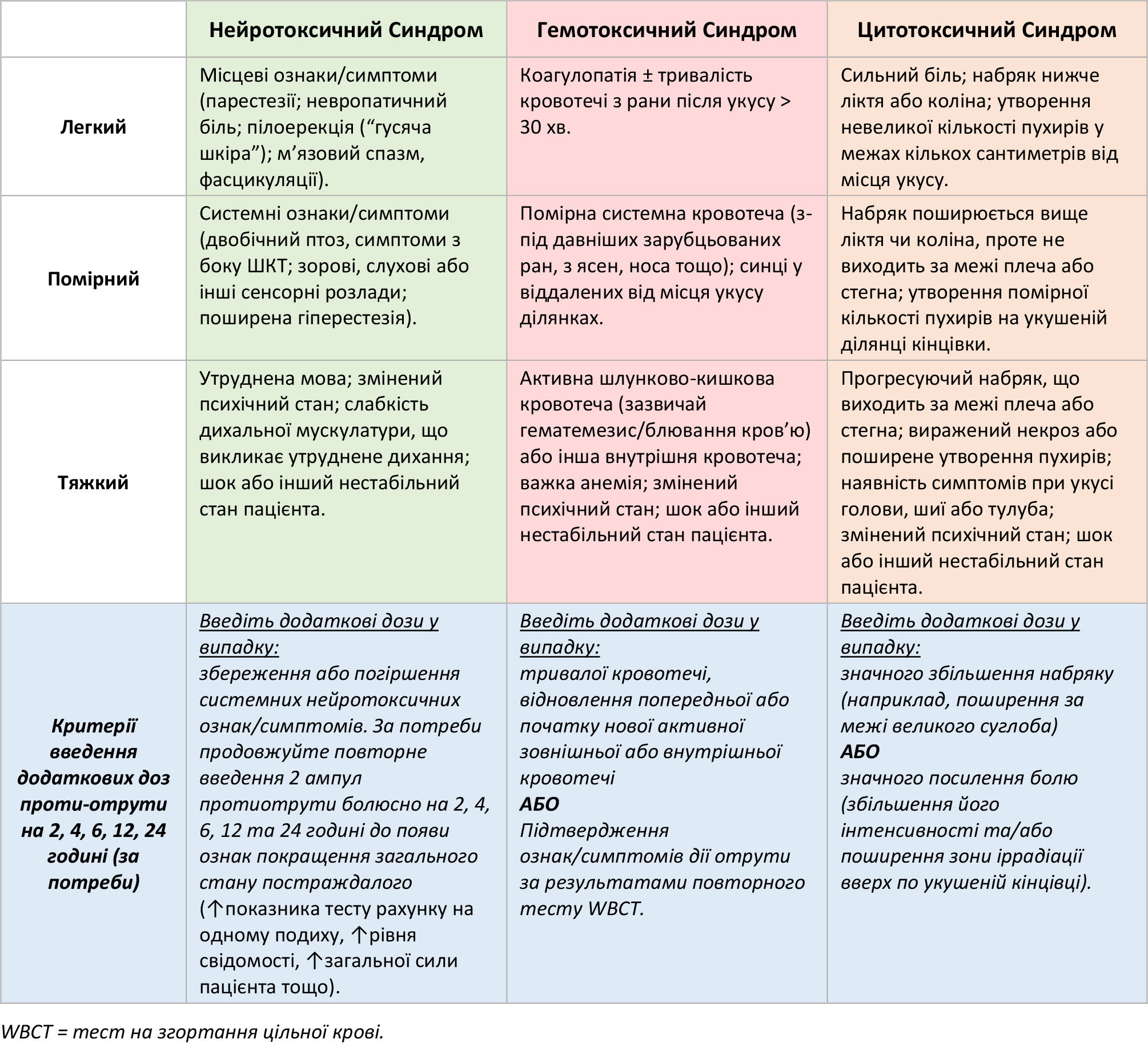
Таблиця 1. Спрощені універсальні критерії діагностики та лікування укусів змій у всьому світі
Таблиця 2. Усі Командування Збройних сил США - Протиотрути першої лінії
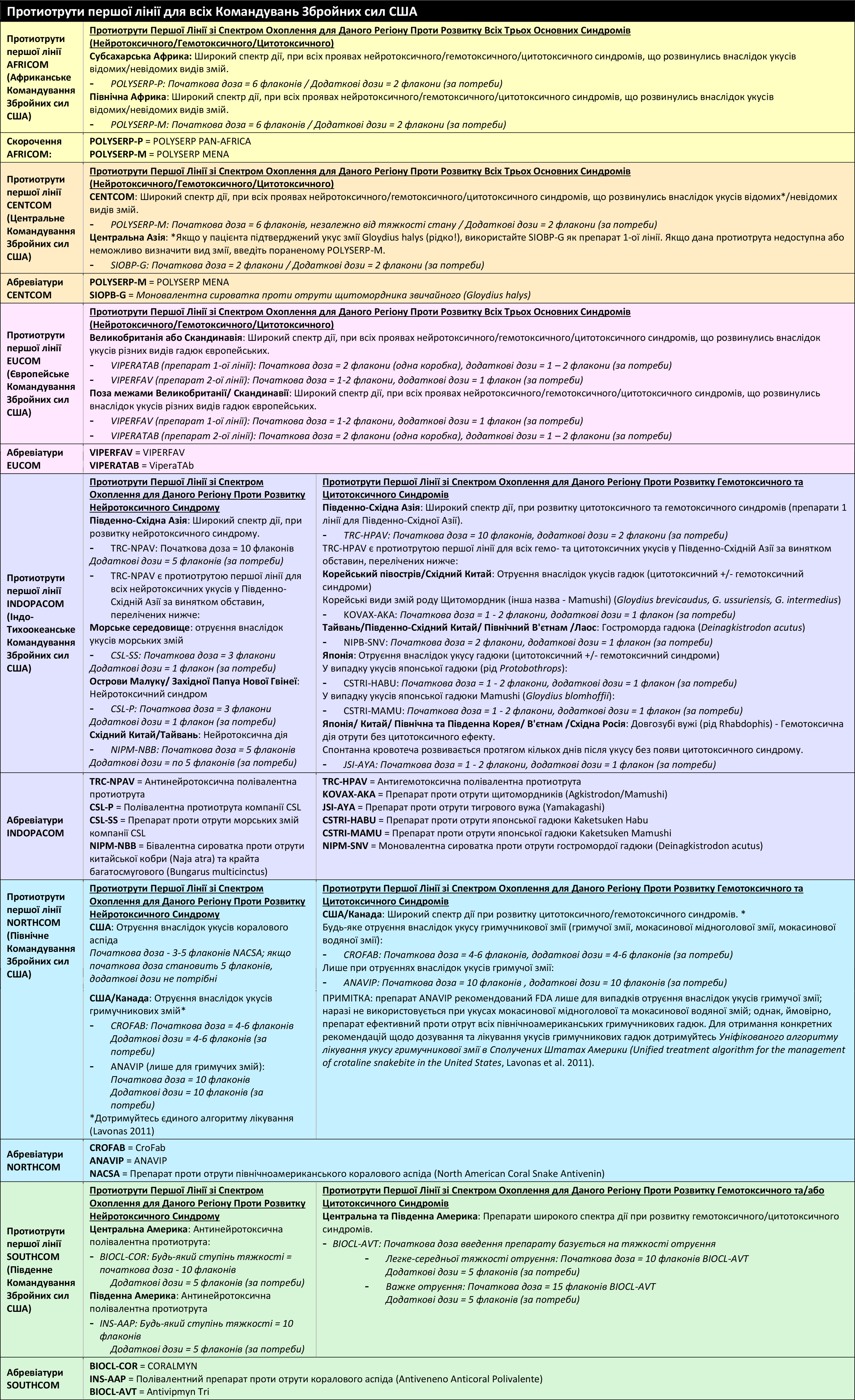
- Наявності одного або кількох критеріїв для кожної категорії у Таблиці 1 (універсальне лікування) зазвичай достатньо для визначення певного синдрому, тяжкості отруєння та початку лікування. Пацієнти зі «змішаними синдромами» (наявність ознак та симптомів > 1 синдрому) отримують ті самі початкові дози протиотрути, що й пацієнти з ізольованим синдромом.
Для визначення необхідної протиотрути та її початкової дози зверніться до опису специфічного лікування укусів змій для кожного окремого регіону Командування Збройних сил США (COCOM) (відповідні розділи розміщені далі в цьому документі). Кожен розділ COCOM містить інструкції щодо підготовки, дозування та введення усіх протиотрут. - У деяких випадках перед введенням протиотрути рекомендоване попереднє введення невеликої дози адреналіну підшкірно. Це допомагає зменшити ризик розвитку побічної реакції на терапію протиотрутою. Зверніться до відповідних настанов щодо попереднього введення адреналіну з метою попередження розвитку ранніх побічних реакцій.
- Більшість важких ранніх реакцій на дію протиотрути виникають протягом перших 5-60 хв після введення препарату. Уважно спостерігайте за станом пацієнта біля його ліжка протягом щонайменше однієї години після введення кожної дози протиотрути.
Для отримання конкретних вказівок зверніться до спеціальних настанов щодо лікування легких, помірних і важких реакцій на введення протиотрути.
Додаткове лікування та підтримуюча терапія
Підтримуюча терапія та подальше ведення пацієнтів
Проводьте підтримуючу терапію та вирішуйте вторинні проблеми, пов’язані з отруєнням, наступним чином:
- У всіх пацієнтів з нейротоксичним отруєнням передбачайте необхідність раннього забезпечення прохідності дихальних шляхів шляхом інтубації трахеї та тривалої ШВЛ, особливо у пацієнтів із пізнім зверненням, загрозою дихальної недостатності чи відсутністю відповіді на введену протиотруту.
- При нейротоксичному укусі змії, який спричинив холінергічний криз, розгляньте ВВ або ВК застосування 0,5 мг атропіну, титруючи препарат згідно з даними аускультації до зникнення бронхіальної гіперсекреції та гіперсалівації, що становлять ризик для дихальних шляхів і дихання.
Повторюйте введення початкової дози кожні 5 хвилин до усунення вологих і сухих хрипів та бронхоспазму. Дози атропіну для дітей розраховують на основі маси тіла - 0,01 мг/кг, до 0,25 мг. - При нейротоксичних укусах змій на Середньому Сході, у Північній Африці та Центральній Азії без холінергічного кризу, але із птозом і слабкістю дихальних м’язів, розгляньте введення пробної дози 0,5 мг атропіну з наступним введенням ВВ або ВК 1,0 мг неостигміну для тимчасового усунення нервово-м’язової слабкості та відтермінування необхідності інтубації. Дози для дітей розраховують на основі маси тіла - 0,01 мг/кг до максимальної дози 0,25 мг атропіну з 0,5 мг неостигміну. 54,74–77
Не всі пацієнти відповідають на лікування, проте в тих, які відповідають, спостерігається тимчасове покращення (реверсія птозу, збільшення сили дихальних м’язів тощо). Якщо відповіді на неостигмін немає, не повторюйте пробу. Якщо реакція позитивна, повторюйте кожні 1-4 години за необхідності (максимальна доза за 24 години = 10 мг для дорослих/ 5 мг для дітей), доки протиотрута остаточно не усуне параліч.
- При гемотоксичних отруєннях всі внутрішні та зовнішні активні кровотечі повинні зупинитися протягом 30-60 хвилин після введення необхідної дози протиотрути. Якщо пацієнт перебуває в стані геморагічного шоку, можна розглянути можливість переливання еритроцитарної маси або цільної крові.17,69,70,78-82 Тромбоцити, свіжозаморожена плазма, кріопреципітат, транексамова кислота та інші засоби не є ефективними в цих випадках через механізм дії отрут.
- При знеболенні слід надавати перевагу кетаміну та фентанілу. Вивільнення гістаміну внаслідок застосування морфіну може нагадувати алергічну реакцію чи посилити гіпотензію.
- Важливо утримувати кінцівку в високо піднятому положенні (ідеальний варіант – більше 60º), коли це можливо, щоб обмежити застійний набряк.
- НЕ проколюйте та НЕ аспіруйте вміст пухирів, пухирців чи бул, якщо вони не спричиняють значного дискомфорту або немає загрози їх неконтрольованого розриву. Якщо є підозра на абсцес, лікуйте згідно з існуючими протоколами.
- НЕ проводьте фасціотомію при укусах змій. Компартмент-синдром при укусах змій зустрічається рідко. Навіть при підтвердженому підвищеному тиску всередині фасціального простору, пацієнти, яким вводили протиотруту без фасціотомії, мали кращі результати лікування (коротший час одужання та нижчий рівень тривалої захворюваності), ніж ті, кому робили фасціотомію.83-86 Введення необхідної кількості протиотрути повинне усунути основну причину, яка призводить до підвищеного внутрішньофасціального тиску.
- НЕ призначайте антибіотики, якщо немає ознак і симптомів інфекції. Інфікування контактним шляхом рідко трапляється при укусах змій, якщо надається своєчасне та належне лікування.54
Подальший моніторинг пацієнтів і потреба в додатковому застосуванні протиотрути
- Уважно спостерігайте за пацієнтом щодо ознак прогресування отруєння в перші години лікування, доки не буде досягнуто контролю над симптомами.
Послідовні оцінювання щодо наявності ознак і симптомів нейротоксичного, гемотоксичного та цитотоксичного синдромів слід проводити на 2, 4, 6, 12, 24 годині (Год2, Год4, Год6, Год12, Год24). - Протягом перших 24 годин протиотруту можна вводити на годинах 0, 2, 4, 6, 12 та 24 відповідно до конкретних критеріїв для лікування протиотрутою, перелічених у розділі «Критерії введення протиотрути та застосування повторних доз»
- Якщо при настанні наступного часового інтервалу ознаки та симптоми, які належать до критеріїв застосування протиотрути, не вдалося усунути, вводьте додаткові дози протиотрути далі за графіком (на годинах 2, 4, 6, 12 та 24), доки не буде досягнуто контролю. Див. перелік COCOM щодо детальних інструкцій з дозування для кожного препарату.
- Якщо симптоми з’являються знову чи зберігаються більше 24 годин після введення першої дози протиотрути, слід обговорити додаткові інтервали лікування зі спеціалістом.
- Якщо були введені 10 або більше флаконів однієї протиотрути без будь-яких ознак покращення, розгляньте можливість переходу до протиотрути 2-ї лінії, якщо це можливо, оскільки перша протиотрута може не охоплювати деяких видів змій. Якщо з’явилися ознаки покращення, продовжуйте застосування даної протиотрути.
- Якщо пацієнт не має симптомів, але коагулопатія і далі зберігається через 24 години після введення першої дози протиотрути, введіть ще одну дозу протиотрути та повторюйте лабораторні дослідження кожні 24 години до нормалізації показників.
- Необхідно проводити постійний моніторинг ефективності застосованої протиотрути. Іноді в набряклих ділянках тканин можуть утворюватися так звані “кишені” з отрутою, яка потрапить в кров після покращення кровообігу. Це явище має назву рецидивуючого отруєння і найчастіше трапляється протягом перших 24-48 годин після сильного укусу зі значним набряком та утворенням пухирів.78,87-93
- Постійний клінічний моніторинг включає щогодинну перевірку життєвих показників, діурезу, а також детальну оцінку нових або погіршення наявних ознак нейротоксичного, гемотоксичного чи цитотоксичного отруєння.
- Серійні лабораторні дослідження, включаючи загальний аналіз крові, комплексну метаболічну панель, протромбіновий час/активований частковий тромбопластиновий час/міжнародне нормалізоване відношення, креатинфосфокіназу, рівень фібриногену (або тест на згортання цільної крові (WBCT) за відсутності розширених аналізів), можна повторювати кожні 2 години, доки зберігаються ознаки отруєння.
- Після появи ознак клінічного покращення/розрішення симптомів частота моніторингу може бути зменшена до одного разу на 6 годин.
- Якщо ознаки рецидивуючого отруєння виявлено більш, ніж через 24 години після введення першої дози протиотрути, проводиться наступне лікування:
- Безсимптомний пацієнт з коагулопатією та відсутністю інших змін:
Введіть дозу протиотрути та повторюйте лабораторні аналізи кожні 24 години до нормалізації показників. - Симптоматичний пацієнт із появою чи посиленням болю, набряку, кровотечі, нейротоксичності або інших ознак активного отруєння:
Вводьте додаткову дозу протиотрути кожні 2 години до повного зникнення гострих симптомів.
Рекомендації щодо виписки
- Після розрішення всіх ознак і симптомів пацієнту слід залишатися у стаціонарі щонайменше 24 години, а перед випискою потрібно виконати наступні кроки:
- Повторіть аналіз крові, щоб переконатися у відсутності коагулопатії.
- У разі необхідності введіть бустерну дозу протиправцевого анатоксину.
- Проінструктуйте пацієнтів про необхідність повернення в лікарню при появі будь-яких нових чи тривожних ознак або симптомів.
- Сироваткова хвороба характеризується грипоподібними симптомами ± висипом, який зазвичай розвивається через 1-3 тижні після введення протиотрути. Вона рідко зустрічається при застосуванні високоочищених сучасних протиотрут, але може виникати частіше при застосуванні деяких протиотрут другої чи третьої лінії, перерахованих у цих настановах.94-97
Сироваткова хвороба може погано переноситись пацієнтом, але не є небезпечною. Лікується симптоматично чи за допомогою курсу пероральних стероїдів.94,95,97–99
Критерії введення протиотрути та застосування повторних доз
Цитотоксичність
Наявність значного болю в місці укусу АБО прогресуючого набряку АБО ознак руйнування тканин (синці, пухирі, некроз) є показанням для застосування протиотрути.1,47,48,79,100-105 При наявності будь-якого з цих критеріїв (або інших системних ознак і симптомів) слід негайно розпочати лікування та не зволікати з прийняттям рішення про введення протиотрути, поки не настали незворотні пошкодження. Зауважте, що прогресування набряку в будь-якому інтервалі лікування є показанням для введення додаткової дози протиотрути; однак, набряк може зберігатися без помітного зменшення протягом декількох днів, а сильний набряк може повністю зникнути тільки через 1-2 тижні чи довший час. Отже, критерієм лікування є ПОСИЛЕННЯ набряку; персистуючий набряк без прогресування НЕ є критерієм лікування. Значне посилення болю або його поширення проксимальніше (вгору по кінцівці), є ще одним показанням до застосування протиотрути.
Нейротоксичність
Поява, збереження або повторне виникнення системних нейротоксичних ознак отруєння (задишка, слабкість м’язів-згиначів шиї, бульбарна м’язова слабкість [м'язи глотки, язика, надгортанника, губ, м'якого піднебіння, голосових зв'язок], зниження рівня свідомості, ↓ функції дихальних м’язів тощо) у будь-який з інтервалів лікування протиотрутою завжди є показанням для початкового чи повторного застосування протиотрути.1,50,107-109 Проводьте моніторинг функції дихання за допомогою визначення негативної сили вдиху (NIF) чи форсованої життєвої ємності легень (ФЖЄЛ), тесту SBC, капнографії, спірометрії, пікфлоуметрії тощо.1,54,72 У пацієнтів, які не досягли пізніх стадій дихальної недостатності/зупинки дихання, перші ознаки відновлення після паралічу можуть з’явитися протягом 30-60 хвилин після введення потрібної дози протиотрути. Заінтубованим пацієнтам знадобиться декілька годин після введення протиотрути, перш ніж настане покращення. Зазвичай, це відбувається протягом 1-3 годин, однак у деяких пацієнтів може тривати 6-12 годин або навіть довше. Існують численні задокументовані випадки, коли пацієнти, яким не вводили протиотруту, потребували тривалої штучної вентиляції легень від декількох днів до 13 тижнів, перш ніж наставало одужання. Протиотрута, зазвичай, або зупиняє прогресування симптомів, або значно скорочує тривалість паралічу.
Кровотеча
Виникнення, продовження чи відновлення будь-якої активної місцевої або системної кровотечі в будь-який зі стандартних інтервалів для оцінки (0, 2, 4, 6, 12, 24 години) завжди є показанням для початкового чи повторного застосування протиотрути, незалежно від часу згортання цільної крові на той момент.1,70,78,106,109–111 Усі зовнішні та внутрішні кровотечі припиняться після введення належної дози протиотрути і повної нейтралізації отрути, яка активно циркулює в організмі.
Тест на згортання цільної крові (WBCT)/коагулограма
Показники коагулограми, зазвичай, нормалізуються протягом 2-6 годин після введення ефективної дози протиотрути, але в деяких випадках для повної нормалізації лабораторних показників може знадобитися більше часу.78,112-120 Процедура проведення та інтерпретація тесту на згортання цільної крові (WBCT) описані в Додатку А: Тест на згортання цільної крові (WBCT) при коагулопатіях споживання, індукованих зміїною отрутою (КСІО/VICC).
Існує три ситуації, коли відхилення від норми WBCT або інших лабораторних показників коагуляції (наприклад, фібриногену, протромбінового часу/активованого часткового тромбопластинового часу/міжнародного нормалізованого відношення тощо) повинні лікуватися протиотрутою:
- Початкова оцінка на годині 0 (Год0): коагулопатія після укусу змії є показанням для введення протиотрути. Якщо результати тесту на згортання не відповідають нормі, але пацієнт не має відповідних симптомів, повторіть тест, використовуючи нову скляну пробірку, щоб підтвердити результат перед застосуванням протиотрути.78,111,113,114,121
- Год2, Год4, Год6, Год12, Год24: попередньо нормальний тест на згортання, який змінюється на патологічний за наявності будь-яких нових симптомів, відповідає критеріям для введення додаткової дози протиотрути. Це також стосується випадків, коли патологічний WBCT нормалізувався через кілька годин після застосування протиотрути, але потім знову став патологічним (рецидивуюче отруєння).78
- Коагулопатія залишається на Год24: якщо WBCT або інші тести згортання крові залишаються патологічними на 24 годині, введіть додаткову дозу протиотрути й повторюйте введення кожні 24 години, доки коагулопатія не зникне.
Гостра судинна недостатність (колапс)
У рідкісних випадках стан пацієнта може різко погіршитися протягом перших 5-30 хвилин після укусу. Це проявляється глибокою гіпотензією, тахікардією, ангіоневротичним набряком, зниженням рівня свідомості тощо.1,122-130 Таких пацієнтів слід одночасно лікувати від тяжкої анафілаксії та тяжкого отруєння зміїною отрутою. Анафілаксія лікується агресивно, відповідно до протоколів. Для лікування отруєння зміїною отрутою швидко ВВ струминно введіть високу початкову дозу протиотрути (щонайменше 6 флаконів), а також забезпечте прохідність дихальних шляхів, інфузію рідин та інші заходи за необхідності.122,123,125,131,132 Більшість пацієнтів з гіпотензією чи ангіоневротичним набряком чутливі до адреналіну, проте якщо після ВМ введення адреналіну відповідь відсутня, для досягнення ефекту може знадобитися ВВ інфузія препарату.122
Як запобігти розвитку ранніх побічних реакцій на введення протиотрути
Адреналін – це єдиний профілактичний засіб (претерапія), який довів ефективне зниження частоти виникнення ранніх побічних реакцій, таких як анафілаксія.60,98,133-136
- НЕ проводьте попереднє лікування стероїдами чи антигістамінними препаратами.
- НЕ вводьте тестові дози протиотрути для перевірки на гіперчутливість.60-63
Відносні протипоказання до претерапії адреналіном: вік > 70 років, артеріальна гіпертензія, ішемічна хвороба серця, інсульт в анамнезі, підтверджений внутрішньочерепний крововилив або підозра на нього. Абсолютні протипоказання відсутні.
- Претерапія адреналіном перед введенням протиотрути не показана за замовчуванням для всіх протиотрут і рекомендована лише за таких обставин:
- Нестабільний стан постраждалого від укусу змії з ознаками шоку.
- Атопія (астма, екзема тощо), гіперчутливість до альбуміну кінської сироватки в анамнезі або тяжкі реакції на протиотруту в анамнезі.
- Необхідність використання певних протиотрут другої чи третьої лінії (через високу частоту виникнення серйозних ранніх побічних реакцій, пов’язаних із цими препаратами).
- Стандартний протокол претерапії адреналіном:
- Доза для дорослих становить 0,25 мг 0,1% (1:1000) розчину адреналіну; вводиться шляхом підшкірної ін’єкції за кілька хвилин до введення протиотрути.
- Дози для дітей розраховують залежно від маси тіла - 0,01 мг/кг, максимальна доза – 0,25 мг.60,134,135,137,138
- Пацієнтам з ознаками шоку адреналін слід вводити ВМ у бічну поверхню стегна.
Як проводити лікування побічних реакцій на введення протиотрути легкого, середнього і тяжкого ступеня
Реакції легкого та середнього ступеня тяжкості під час інфузії
- Припиніть інфузію, проведіть симптоматичне лікування реакцій легкого та помірного ступеня (наприклад, нудоти, блювання, кропив’янки, свербежу, ознобу, гарячки тощо) за допомогою протиблювотних засобів, антигістамінних препаратів, стероїдів тощо.
- Повторно оцініть стан пацієнта після зникнення проявів реакції; якщо симптоми-критерії лікування протиотрутою цитотоксичного, гемотоксичного чи нейротоксичного синдромів не усунуті повністю, відновіть інфузію з меншою швидкістю, впродовж не менше 30 хвилин.
- Якщо протиотрута вводилася струминно, розведіть решту дози в 100-500 мл 0,9% розчину NaCl та вводьте ВВ краплинно протягом 30 хвилин.
Розвиток реакції тяжкого ступеня (анафілаксії) під час інфузії
- Припиніть інфузію та проводьте лікування відповідно до протоколу лікування анафілаксії.
- Повторно оцініть стан пацієнта після зникнення проявів реакції; якщо симптоми-критерії лікування протиотрутою цитотоксичного, гемотоксичного чи нейротоксичного синдромів не усунуті повністю, відновіть інфузію з меншою швидкістю, впродовж не менше 30 хвилин.
- Якщо протиотрута вводилася струминно, розведіть решту дози в 100-500 мл 0,9% розчину NaCl та вводьте ВВ краплинно протягом 30 хвилин.
- При виникненні реакції припиніть інфузію та проконсультуйтесь із спеціалістом (за допомогою телемедичних засобів) щодо подальшого ведення пацієнта.
Протокол лікування анафілаксії
Примітка: Якщо не відбувається швидкого зменшення набряку дихальних шляхів після введення адреналіну, виконайте інтубацію трахеї
Якщо анафілаксія виникла після введення протиотрути, проводьте лікування згідно з наступним протоколом:
- Перша лінія при лікуванні анафілаксії – швидке введення 0,1% (1:1000) розчину адреналіну (початкова доза для дорослих = 0,5 мг ВМ у бічну поверхню стегна для швидкого всмоктування). За необхідності повторюйте ВМ введення адреналіну до стабілізації стану пацієнта та/або розпочніть ВВ або ВК інфузію відповідно до стандартних протоколів, якщо відсутня реакція на ВМ введення.
Адреналін слід завжди вводити до застосування антигістамінних препаратів або стероїдів, щоб протидіяти безпосереднім загрозам життю, пов’язаним із бронхоспазмом і вазодилатацією. - Після введення адреналіну:
- Введіть 125 мг метилпреднізолону ВВ
- Введіть 50 мг димедролу чи прометазину
- Розгляньте додаткове застосування антагоністів Н2-гістамінових рецепторів, наприклад, ранітидину.
Якщо анафілаксія виникла під час введення протиотрути, припиніть введення і проведіть лікування реакції, а потім відновіть введення протиотрути, як описано нижче.15,61,95,99,128,129,140–146
Пізні реакції на введення протиотрути (сироваткова хвороба)
- Сироваткова хвороба характеризується грипоподібними симптомами ± висипом, який, зазвичай, розвивається через 1-3 тижні після введення протиотрути.
- Сироваткова хвороба може погано переноситись пацієнтом, але не є небезпечною.
- Лікування симптоматичне – антигістамінними препаратами, парацетамолом або курсом пероральних стероїдів, якщо пацієнти відчувають значний дискомфорт.94,95,97–99
Особливі ситуації
Якщо протиотрута недоступна
- Протиотрута – це золотий стандарт лікування симптоматичних отруєнь внаслідок укусів змій. Раннє лікування є найкращою стратегією для запобігання смерті, ампутації кінцівки або іншої значної інвалідизації. У випадку недоступності протиотрути слід спрямувати всі зусилля, щоб якнайшвидше транспортувати пацієнта туди, де вона є (або навпаки) для запобігання незворотнім ушкодженням органів і тканин.
- Планування бойового завдання повинне включати пошук і закупівлю відповідної регіонально специфічної протиотрути, рекомендованої цими настановами для вашої географічної зони. Якщо ви вже перебуваєте на бойовому завданні і не забезпечені протиотрутою, слід дістати/закупити відповідну протиотруту, рекомендовану в цих настановах, через надійні канали забезпечення, оскільки в місцевих аптеках Африки та країн, що розвиваються, часто можна зустріти підроблені або неякісні протиотрути.
- Щодо ведення пацієнта до моменту отримання протиотрути - дотримуйтеся чек-листа, пропускаючи кроки, пов’язані з введенням протиотрути, допоки вона не стане доступною.
Конкретні рекомендації див. у розділі “Підтримуюча терапія”.
Військові службові собаки/Собаки багатоцільового призначення
Всі протиотрути можна вводити військовим службовим та багатоцільовим собакам відповідно до критеріїв лікування та початкових доз, наведених у даних настановах; інше лікування повинне ґрунтуватися на Настановах з клінічної практики для військових службових собак.
Пізнє звернення та затримки у лікуванні
Не існує часових обмежень для застосування протиотрути при симптоматичному укусі змії. Раннє застосування протиотрути протягом перших хвилин або годин після укусу є найкращим методом запобігання захворюваності та смертності, однак протиотрута залишається ефективним засобом для вирішення зворотних проблем, зокрема коагулопатії, і попередження подальшого незворотного пошкодження тканин навіть у пацієнтів, які звернулися через багато годин або днів після укусу змії.56,69,78,145,147
Застарілі заходи, які не слід проводити
- ЗАБОРОНЕНО висікати рану, відсмоктувати отруту, застосовувати електрокоагуляцію, припікати чи наносити хімічні речовини на місце укусу.
- НЕ НАКЛАДАЙТЕ тиснучі або тугі пов’язки, турнікети чи інші засоби, які знижують кровообіг у кінцівці!
- НЕ ВИКОРИСТОВУЙТЕ екстрактори отрути чи інші комерційні засоби першої допомоги при укусах змій.148-152
- НЕ ВВОДЬТЕ пробні дози протиотрути для перевірки на гіперчутливість, оскільки це неефективно і призводить до марних витрат часу та протиотрути.60-63
- НЕ ЗАСТОСОВУЙТЕ антигістамінні препарати та стероїди для профілактики анафілаксії чи інших ранніх побічних реакцій на протиотруту, оскільки вони неефективні в якості премедикації.133,134
Потрапляння отрути плюючої кобри в очі (отруйна офтальмія)
Плюючі кобри мають видозмінені ікла, які дозволяють їм випорскувати струмінь отрути в очі хижака чи істоти, яку кобра сприймає в якості загрози.153-155 Отрута розлітається, ніби дріб при пострілі; змія цілиться у відблиск сонячного світла на оці жертви. Отрута не становить шкоди, допоки вона не потрапить в очі (миттєво викликаючи печіння, сльозотечу, затуманення зору тощо) або в кров, наприклад, при укусі, контакті з відкритою раною на шкірі або в ротовій порожнині чи через шлунково-кишковий тракт (наприклад, якщо випити склянку отрути, маючи виразку шлунка). Якщо значна кількість отрути потрапляє в кров через відкриту рану і викликає типові симптоми укусу, її лікують протиотрутою, як і будь-яке інше отруєння. Якщо отрута потрапила лише в очі і немає ознак системного отруєння, протиотрута не показана, а лікування таке ж, як і при потраплянні будь-якої хімічної речовини в очі – рясне промивання. Плююча кобра вводить отруту і шляхом укусу, тому важливо перевірити пацієнта на відсутність укусів після контакту з такими зміями.
Ознаки та симптоми
До перших ознак і симптомів отруйної офтальмії належать локальний біль високої інтенсивності, набряк та/або посмикування повік, сльозотеча та слизові білі виділення.156 Основна загроза – пошкодження епітелію рогівки, яке може призвести до сліпоти внаслідок приєднання вторинної інфекції чи рубцювання при відсутності належної допомоги.7,25,54,156-158 Лікування отруйної офтальмії відносно просте та схоже на допомогу при потраплянні в очі розчину шкідливої хімічної речовини.
Перша допомога
Переконайтеся, що в пацієнта з отруйною офтальмією немає укусу змії. Негайно промийте око великою кількістю води, 0,9% NaCl або неагресивної рідини, наприклад, молока, якщо нічого іншого немає поруч. Зніміть одяг та виконайте деконтамінацію пацієнта з голови до ніг водою з милом, щоб запобігти повторному впливу засохлої отрути.54
Основне лікування
Застосовуйте очні краплі з місцевим анестетиком (тетракаїном), щоб полегшити ретельне промивання та огляд ураженого ока. Ретельно промийте очі водою або 0,9% NaCl впродовж ≥ 15 хв.156
Нанесіть флюоресцеїн (для забарвлення) та огляньте очі за допомогою щілинної лампи чи офтальмоскопа для виявлення пошкоджень рогівки. При наявності ушкодження застосуйте антибактеріальні очні краплі (наприклад, з тетрацикліном або хлорамфеніколом) чи мазі, а також мідріатики. Щодня проводьте повторну оцінку за допомогою щілинної лампи. При відсутності ушкодження рогівки зважте переваги та ризики застосування антибактеріальних очних крапель.
Додаткові методи лікування, які слід розглянути
Повідомляється, що очні краплі з адреналіном (1:1000) або фенілефрином (10%) негайно усувають відчуття печіння, викликане отрутою.54,156
Протипоказані методи лікування
Місцеве чи системне застосування протиотрути не показане при потраплянні зміїної отрути в очі.54,156,159 У таких пацієнтів також протипоказане застосування топічних стероїдів.
Регіональні особливості лікування укусів змій
У цих настановах представлено широкий спектр різних протиотрут для лікування укусів змій у зонах відповідальності Африканського (AFRICOM), Центрального (CENTCOM), Індо-Тихоокеанського (INDOPACOM), Європейського (EUCOM), Північного (NORTHCOM) та Південного (SOUTHCOM) Командувань Збройних сил США. Спектр дії, початкова доза, підготовка та спосіб застосування відрізняються для різних препаратів, тому для кожного з них наведено детальну інформацію. Спрощені алгоритми вибору та дозування кожної протиотрути також включені до відповідного за регіоном розділу.
За можливості, рекомендовано використовувати протиотруту широкого спектра дії, стабільну в польових умовах. Це дасть змогу проводити діагностику та посиндромне лікування безпосередньо на місці отримання укусу, без необхідності ідентифікації виду змії. Посилання на відповідну літературу з питань безпеки, ефективності та дозування для кожного препарату наведені в розділі «Література».
Визначте протиотруту першої лінії для вашої географічної зони перед тим, як відправлятися на бойове завдання, використовуючи цей розділ. Після цього поверніться до розділу, де описаний універсальний підхід до оцінки, діагностики та лікування зміїних укусів вище в Настановах, для отримання детальних інструкцій і поетапного підходу до лікування укусів змій протягом усього періоду надання допомоги. Нижче наведені скорочені рекомендації із застосування протиотрути для кожного регіонального командування Збройних сил США.
Категорії медично значущих видів змій
Всесвітня організація охорони здоров’я (ВООЗ) класифікує отруйних змій відповідно до ризику, який вони становлять, відносячи кожен вид до Категорії 1 або Категорії 2, як описано нижче. У рекомендаціях ВООЗ зазначено, що «види, віднесені до Категорії 1 в межах країни, території чи району, повинні розглядатися як найбільш пріоритетні для виробництва протиотрут, оскільки наявні дані свідчать про те, що саме вони є причиною найбільшого тягаря хвороб у даному конкретному середовищі».160
Категорія 1 за ВООЗ: Отруйні змії, які мають найбільше медичне значення
Визначаються як «високоотруйні змії, які є поширеними або широко розповсюдженими та завдають численних укусів, що призводить до високого рівня захворюваності, інвалідності чи смертності».
Категорія 2 за ВООЗ: Отруйні змії другорядного медичного значення
Визначаються як «високоотруйні змії, здатні спричинити захворюваність, інвалідність або смерть, щодо яких можуть бути відсутні точні епідеміологічні чи клінічні дані; та/або які рідше зустрічаються (через їхні цикли активності, поведінку, вподобання щодо середовища проживання чи поширення в районах, віддалених від великих людських поселень).»
Примітка: ВВ або ВК краплинне введення протиотрути порівняно з болюсним введенням:
Більшість протиотрут першої лінії в цих настановах рекомендовано: а) вводити, використовуючи 100, 250 або 500 мл ізотонічного розчину шляхом ВВ або ВК інфузії протягом 10 хвилин або б) вводити безпосередньо шляхом ВВ болюсу для того, щоб пацієнт якнайшвидше отримав повну дозу протиотрути, а також для нейтралізації отрути до того, як відбудеться подальше ушкодження. Однак, якщо це неможливо, можна розвести протиотруту в пакеті з ізотонічним розчином будь-якого об’єму, який у вас є, і ввести протягом 10-30 хвилин.
Контакти
Для екстрених телемедичних консультацій зателефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
AFRICOM
Африканське Командування Збройних Сил США
Настанови з лікування
У цій зоні відповідальності (ЗВ) доступні безпечні та ефективні, стабільні в польових умовах протиотрути широкого спектра дії при всіх трьох синдромах отруєння зміїною отрутою; для лікування ідентифікація виду змії не потрібна. Лікування укусів змій для AFRICOM рекомендовано проводити на тому місці, де відбувся укус, через тривалий час евакуації, високу частоту укусів змій і високий ризик смерті чи стійкої інвалідності, який спричиняють багато отруйних змій у цій ЗВ при недоступності раннього лікування протиотрутою.
Лікування побічних реакцій
- У разі виникнення реакції легкого чи помірного ступеня зменшіть швидкість інфузії та проведіть симптоматичне лікування антигістамінними препаратами, стероїдами та/або протиблювотними препаратами за необхідності. Щоб отримати конкретні інструкції, див. розділ про лікування побічних реакцій.
- У разі виникнення тяжкої реакції, наприклад, анафілаксії, припиніть інфузію та проведіть лікування згідно з протоколом лікування анафілаксії, наведеним у даних настановах. Повторно оцініть стан пацієнта після зникнення проявів реакції та відновіть інфузію з нижчою швидкістю, якщо не усунутий повністю будь-який зі специфічних симптомів-критеріїв для застосування протиотрути, наведених в інших розділах настанов.
Протокол лікування гострої судинної недостатності (колапсу)
У пацієнта протягом 30 хвилин після укусу швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта за допомогою ВМ або ВВ введення адреналіну та розчинів для інфузії відповідно до протоколів лікування анафілаксії.
- Виконайте інтубацію трахеї при набряку дихальних шляхів, якщо відсутня швидка реакція на застосування адреналіну.
- Після введення адреналіну негайно ВВ або ВК болюсно введіть високу дозу відповідної регіональної протиотрути, продовжуючи заходи ресусцитації.
- Підтримуйте артеріальний тиск за допомогою ВВ або ВК введення розчинів та адреналіну, доки гемодинаміка не стабілізується завдяки дії протиотрути.
Для отримання додаткової інформації див. розділ «Гостра судинна недостатність (колапс)».
Контакти
Для екстрених телемедичних консультацій телефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
Таблиця 3. AFRICOM: протиотрути першої лінії
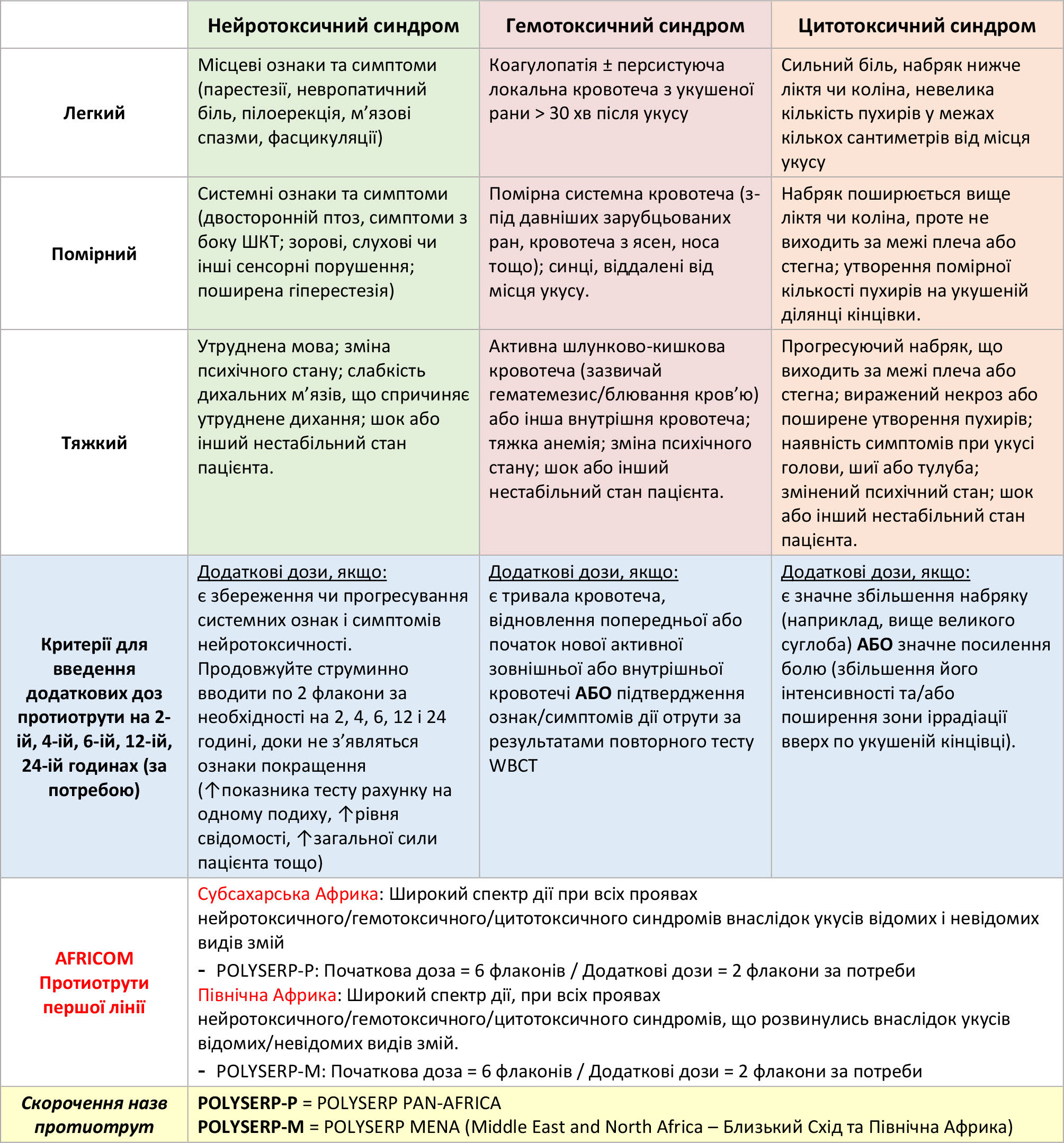
Малюнок 2. Алгоритм введення протиотрути: зона відповідальності AFRICOM
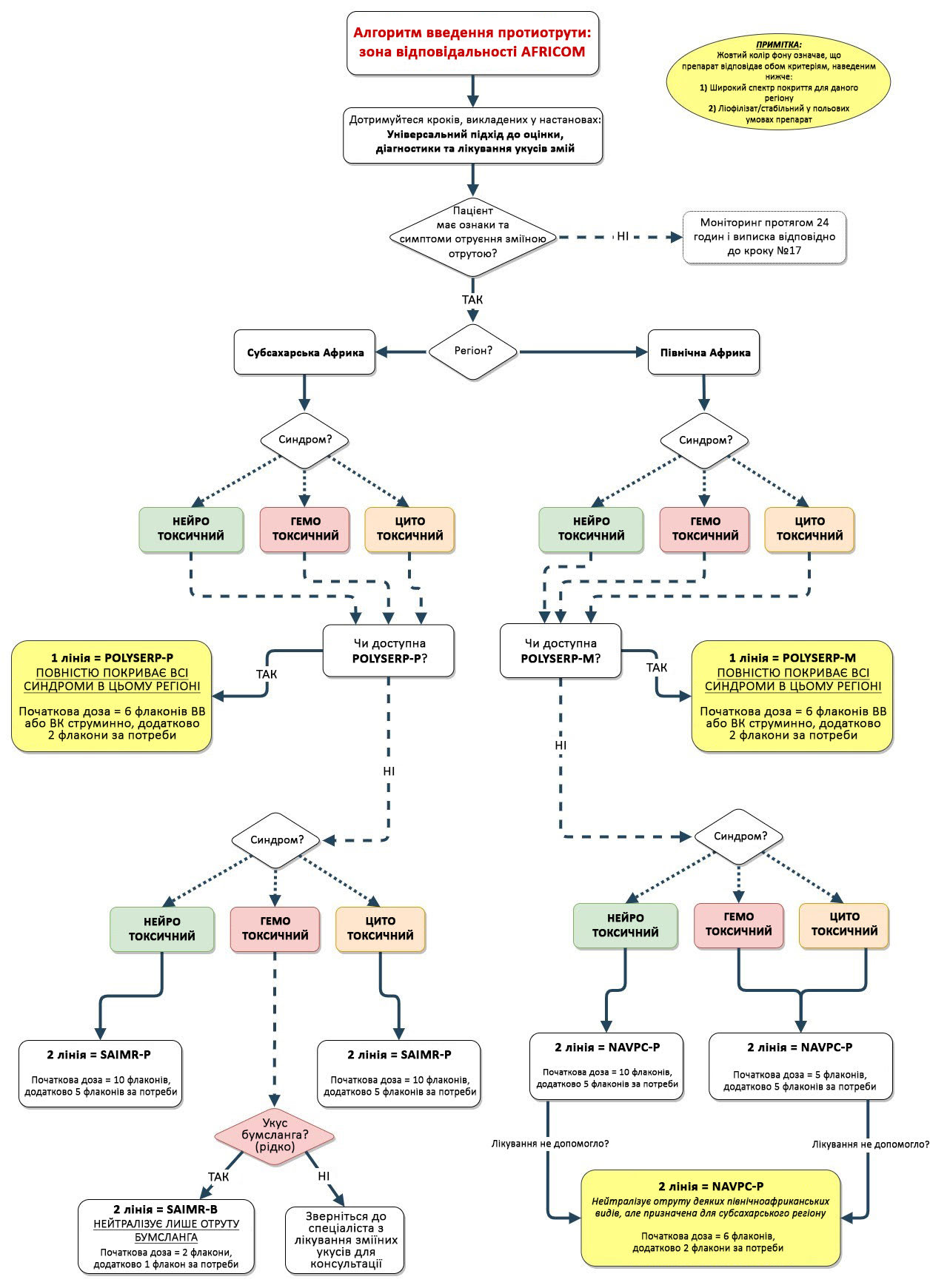
Протиотрута першої лінії (AFRICOM - Субсахарська Африка): POLYSERP-P
POLYSERP/Inosan, Іспанія – POLYSERP PAN-AFRICA полівалентна (POLYSERP-P) (Ліофілізат/Не потребує охолодження)1,106,161-164:
- Стабільна в польових умовах. Широкий спектр дії для 24+ видів змій при цито-/гемо-/нейротоксичному синдромах.
- Варіант лікування одним курсом всіх нейротоксичних, гемотоксичних, цитотоксичних отруєнь зміїною отрутою в Субсахарській Африці, коли вид змії невідомий або входить до числа 24 видів змій, при укусах яких цей препарат безпосередньо показаний. Єдина полівалентна протиотрута, яка нейтралізує отруту бумслангів, а також єдина протиотрута при укусах земляними гадюками. Прямо чи опосередковано охоплює всіх змій 1 та 2 категорій за ВООЗ у цьому регіоні, для яких наразі існує протиотрута.
- Початкова доза = 6 флаконів для всіх синдромів, додаткові дози = 2 флакони за необхідності.
Протиотрута третьої лінії (AFRICOM – Північна Африка): POLYSERP-P
POLYSERP/Inosan, Іспанія – POLYSERP PAN-AFRICA полівалентна (POLYSERP-P) (Ліофілізат/Не потребує охолодження)1,106,161-164:
Показана при всіх нейротоксичних, гемотоксичних або цитотоксичних отруєннях зміїною отрутою в Північній Африці, якщо після застосування 10 флаконів POLYSERP-M та/або NAVPC-P немає ознак покращення. Прямо чи опосередковано охоплює деяких змій 1 і 2 категорій за ВООЗ у Північній Африці.
Можливість застосування в непристосованих умовах: Рекомендована для застосування в умовах бойових дій і спеціально розроблена з урахуванням можливостей наземних медиків, які працюють у зоні бойових дій у цих районах. Оновлена версія протиотрути Inoserp PanAfrica створена спеціально для непристосованих умов і тактичної медицини. Ліофілізована, не потребує охолодження, стабільна при температурі > 37ºС протягом щонайменше 180 днів без втрати ефективності. Широкий спектр покриття та просте дозування дозволяють застосовувати препарат у польових умовах при будь-яких симптомах внаслідок укусу змій невідомого виду в цьому регіоні. Сили спеціальних операцій і звичайні підрозділи, що розгортаються в непристосованих оперативних умовах та в районах із критично небезпечними отруйними видами змій, повинні мати при собі по 8 флаконів на кожного медика. Рекомендовано також мати запас протиотрути у всіх медичних закладах AFRICOM 2-го та 3-го рівня на випадок, якщо після прибуття знадобиться додаткова доза протиотрути, а також для поповнення запасів польових медиків, які використали отриману протиотруту.
Побічні реакції: Висока ефективність при всіх основних синдромах і дуже низька частота побічних реакцій (0,2% за даними сучасних публікацій).
Показання для застосування: Полівалентна протиотрута широкого спектра дії, призначена безпосередньо для лікування нейротоксичного, гемотоксичного та цитотоксичного синдромів отруєння зміїною отрутою внаслідок укусів 24 різних африканських видів змій з родин Elapidae, Viperidae, Colubridae та Atractaspididae.
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Dendroaspis angusticeps, D. jamesoni, D. polylepis, D. viridis; Naja anchieta, N. annulifera, N. haje, N. senegalensis; Naja melanoleuca
- ЦИТОТОКСИЧНИЙ та/або ГЕМОТОКСИЧНИЙ ЕФЕКТ: Atractaspis irregularis; Bitis arietans, B. gabonica, B. nasicornis, B. rhinoceros; Cerastes cerastes; Dispholidus typus; Echis leucogaster, E. ocellatus, E. pyramidum; Naja katiensis, N. mossambica, N. nigricollis, N. nubiae, N. pallida
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- Нейротоксичний синдром: початкова доза = 6 флаконів
- Гемотоксичний синдром: початкова доза = 6 флаконів
- Цитотоксичний синдром: початкова доза = 6 флаконів
Додаткові дози: Можливе додаткове застосування по 2 флакони POLYSERP-P на 2-й, 4-й, 6-й, 12-й та 24-й годинах, якщо це необхідно.
Підготовка та введення: Розчиняйте по 2 флакони POLYSERP-P в одному шприці об’ємом 10 мл. Введіть ізотонічний розчин у перший флакон, змішайте, втягніть назад у шприц та введіть у другий флакон, щоб отримати дозу 2 флаконів у 1 шприці (загальна доза: 6 флаконів = 3 шприци). Один за одним вводьте вміст шприців з отриманим розчином повільно й безперервно ВВ або ВК струминно (болюсно), приблизно по 2 хв на кожен шприц. У разі виникнення побічної реакції припиніть введення, проведіть лікування реакції, повторно оцініть на наявність відповіді згідно з критеріями лікування. Решту дози розчиніть у пакеті зі 100 мл ізотонічного розчину та вводьте повільно ВВ або ВК краплинно протягом 30 хв, якщо необхідно.
Для зручності рекомендоване струминне (болюсне) введення, проте POLYSERP-P також можна вводити ВВ або ВК краплинно. Розчиніть ліофілізат у пакеті з 50 мл або 100 мл ізотонічного розчину, введіть весь вміст пакета за 5-10 хв.
Протиотрута першої лінії (AFRICOM - Північна Африка): POLYSERP-M
POLYSERP/Inosan, Іспанія - POLYSERP MENA Полівалентна (POLYSERP-M) (Ліофілізат/Не потребує охолодження) 156-172:
- Стабільна в польових умовах. Широкий спектр дії проти 27+ видів змій при цито-/гемо-/нейротоксичному синдромах.
- Варіант лікування одним курсом всіх нейротоксичних, гемотоксичних, цитотоксичних отруєнь зміїною отрутою в Північній Африці (Алжир, Єгипет, Лівія, Марокко, Туніс, Західна Сахара), коли вид змії або невідомий, або входить до числа 27 видів змій, при укусах яких цей препарат безпосередньо показаний. Прямо чи опосередковано охоплює всіх змій 1 та 2 категорій за ВООЗ у цьому регіоні, для яких наразі існує протиотрута.
- Початкова доза = 6 флаконів для всіх синдромів, додаткові дози = 2 флакони за необхідності.
Можливість застосування в непристосованих умовах: Рекомендована для застосування в умовах бойових дій і спеціально розроблена з урахуванням можливостей наземних медиків, які працюють у зоні бойових дій у цих районах. Оновлена версія препарату Inoserp MENA створена спеціально для непристосованих умов і тактичної медицини. Ліофілізована, не потребує охолодження, стабільна при температурі > 37ºС протягом щонайменше 180 днів без втрати ефективності. Широкий спектр покриття та просте дозування дозволяють застосовувати препарат у польових умовах при будь-яких симптомах внаслідок укусу змій невідомого виду в цьому регіоні. Сили спеціальних операцій і звичайні підрозділи, що розгортаються в непристосованих оперативних умовах та в районах із критично небезпечними отруйними видами змій, повинні мати при собі по 8 флаконів на кожного медика. Рекомендовано також мати запас протиотрути у всіх медичних закладах AFRICOM 2-го та 3-го рівня на випадок, якщо після прибуття знадобиться додаткова доза протиотрути, а також для поповнення запасів польових медиків, які використали отриману протиотруту.
Побічні реакції: Висока ефективність при всіх основних синдромах та низька частота серйозних побічних реакцій (приблизно 1% за даними сучасних публікацій).
Показання: Універсальна полівалентна протиотрута широкого спектру дії, рекомендована для лікування нейротоксичного, гемотоксичного та цитотоксичного синдромів отруєння, спричинених 27 різними видами близькосхідних, північноафриканських та центральноазійських змій з родин Elapidae та Viperidae. Це препарат першої лінії при отруєннях внаслідок укусу змій у цьому регіоні, коли вид отруйної змії невідомий, або належить до тих, для яких препарат безпосередньо призначений.
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Naja haje, N. oxiana; Walterinnesia aegyptia
- ЦИТОТОКСИЧНИЙ та/або ГЕМОТОКСИЧНИЙ ЕФЕКТ: Bitis arietans; Cerastes cerastes, C. vipera, C. gasperettii; Daboia palestinae, D. mauritanica, D. deserti; Echis. carinatus sochureki, E. coloratus, E. khosatskii, E. leucogaster, E. megalocephalus, E. omanensis, E. pyramidum; Macrovipera lebetina obtusa, M. l. transmediterranea, M. l. turanica; Montivipera bornmuelleri, M. raddei kurdistanica; Naja nubiae, N. pallida; Pseudocerastes persicus persicus, P. fieldi; Vipera latastei
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ: початкова доза = 6 флаконів
- ГЕМОТОКСИЧНИЙ: початкова доза = 6 флаконів
- ЦИТОТОКСИЧНИЙ: початкова доза = 6 флаконів
Додаткове дозування: Додаткові дози по 2 флакони препарату POLYSERP-М можна вводити через 2, 4, 6, 12 та 24 години, якщо необхідно.
Підготовка та введення: Розчиняйте по 2 флакони POLYSERP-P в одному шприці об’ємом 10 мл. Введіть ізотонічний розчин у перший флакон, змішайте, втягніть назад у шприц та введіть у другий флакон, щоб загалом отримати дозу 2 флаконів у 1 шприці (загальна доза: 6 флаконів = 3 шприци). Один за одним вводьте вміст шприців з отриманим розчином повільно й безперервно ВВ або ВК струминно (болюсно), приблизно по 2 хв на кожен шприц. У разі виникнення побічної реакції припиніть введення, проведіть лікування реакції, повторно оцініть на наявність відповіді згідно з критеріями лікування. Решту дози розчиніть у пакеті зі 100 мл ізотонічного розчину та вводьте повільно ВВ або ВК краплинно протягом 30 хв, якщо необхідно.
Для зручності рекомендується струминне (болюсне) введення, але препарат POLYSERP-М можна також вводити шляхом ВВ або ВК інфузії. Розведіть у 50 мл або 100 мл фізіологічного розчину і введіть весь розчин протягом 5 - 10 хв.
Протиотрута другої лінії (AFRICOM - Субсахарська Африка): SAIMR-P
Південноафриканські виробники вакцин, Південна Африка - SAVP SAIMR Полівалентна зміїна протиотрута (SAIMR-P) (Рідка /Потребує охолодження) 50,173-181:
- Нестабільна в польових умовах. Широкий спектр дії проти 10+ видів змій; має лише антинейротоксичний та антицитотоксичний ефект.
- Показана при невідомих нейротоксичних та/або цитотоксичних отруєннях у країнах Субсахарської Африки або для пацієнтів без ознак покращення стану після застосування 10 флаконів POLYSERP-P. Неефективна для лікування гемотоксичних отруєнь. Південна Африка: Прямо чи опосередковано охоплює всі види змій 1-ої та 2-ої категорій за ВООЗ, для яких наразі існує протиотрута. Східна/Центральна/Західна Африка: Нейтралізує отруту багатьох цитотоксичних і нейротоксичних змій у Західній, Центральній та Східній Африці, але має значні недоліки щодо захисту від усіх гемотоксичних видів змій 1-ої та 2-ої категорій за ВООЗ.
- Початкова доза = 10 флаконів, лише для нейротоксичних/цитотоксичних отруєнь, додаткові дози = 5 флаконів.
Можливість застосування в непристосованих умовах: Не рекомендується для використання у бойових умовах. Потребує дотримання “холодового ланцюга”. Рекомендовано зберігати невелику кількість на стратегічно розташованих об'єктах другого і третього етапів допомоги в зоні відповідальності AFRICOM.
Побічні реакції: Висока ефективність, але дуже висока частота виникнення анафілаксії (від 25% до 75%), що було задокументовано в численних публікаціях.
Показання до застосування: Цей полівалентний препарат можна використовувати для лікування нейротоксичних та цитотоксичних отруєнь внаслідок укусів 10 різних видів африканських змій. Препарат успішно застосовувався для знешкодження отрути інших видів африканських змій шляхом параспецифічної нейтралізації, але дослідження в цій галузі обмежені, а більшість даних отримано з повідомлень про поодинокі випадки. Для 10 видів змій, перелічених нижче, є офіційні показання щодо лікування, рекомендовані виробником:
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Dendroaspis polylepis, D. angusticeps, D. jamesoni, Naja melanoleuca, N. nivea, N. annulifera
- ЦИТОТОКСИЧНИЙ ЕФЕКТ: Bitis arietans, B. gabonica, Naja mossambica, Hemachatus haemachatus
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ - початкова доза = 10 флаконів
- Не призначається при гемотоксичному синдромі
- ЦИТОТОКСИЧНИЙ - початкова доза = 10 флаконів
Додаткове дозування: Додаткові дози по 5 флаконів SAIMR-P можна вводити через 2, 4, 6, 12 та 24 години, якщо необхідно.
Претерапія: Рекомендована для цієї протиотрути. Введіть 0,25 мг адреналіну підшкірно (ПШ) перед початком введення протиотрути, щоб зменшити ризик розвитку небезпечної реакції. Дозування адреналіну для дітей визначається на основі маси тіла (0,01 мг/кг).
Підготовка та введення: Всю дозу протиотрути розвести в 250 - 500 мл ізотонічного розчину і ввести шляхом внутрішньовенної інфузії протягом 10 - 30 хвилин.
Протиотрута другої лінії, укус бумсланга (AFRICOM - Субсахарська Африка): SAIMR-B
Південноафриканські виробники вакцин, Південна Африка - SAVP SAIMR Протибумслангова моновалентна (SAIMR-B) (Рідка /Потребує охолодження) 173-181:
- Нестабільна в польових умовах. Не має широкого спектра дії. Захист від одного виду змій.
- Підтверджений або підозрюваний укус бумсланга без ознак покращення стану після введення 10 флаконів препарату POLYSERP-P. Моновалентна, можна використовувати лише для лікування отруєння внаслідок укусу бумсланга (змія категорії 2 за ВООЗ). Не забезпечує захисту від інших видів змій 1 або 2 категорії за ВООЗ.
- Початкова доза = 2 флакони, тільки у випадку укусу бумсланга, додаткові дози = 1 флакон, за потребою
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Потребує дотримання “холодового ланцюга”. Рекомендовано зберігати невелику кількість на стратегічно розташованих об'єктах другого та третього етапів допомоги у країнах Субсахарської Африки.
Побічні реакції: Клінічні випробування не проводилися, але препарат є ефективним, судячи з поодиноких повідомлень та звітів про клінічні випадки. Передбачається помірно-високий ризик розвитку анафілаксії (згідно з обмеженою кількістю повідомлень про випадки анафілаксії у пацієнтів, які отримували лікування протиотрутою SAIMR-B).
Показання до застосування: Ця моновалентна протиотрута ефективна лише при укусі бумсланга.
- Гемотоксичний ефект: Dispholidus typus
Початкове дозування відповідно до синдрому:
- Не призначається при нейротоксичному синдромі
- Гемотоксичний синдром з підтвердженим або підозрюваним укусом бумсланга (типовими є виникнення коагулопатії та кровотеча через 1-3 дні після укусу; без значного болю, набряку або ушкодження тканин)
- Початкова доза = 2 флакони SAIMR-B
- POLYSERP-P повинен бути препаратом першої лінії у цьому випадку (якщо він доступний), через менший ризик виникнення алергічних реакцій.
- Не рекомендується при гемотоксичних отруєннях внаслідок укусів інших змій, крім бумсланга
- Не призначається при цитотоксичному синдромі
Додаткове дозування: Додаткові дози - по 1 флакону SAIMR-B - можна повторювати, за необхідності, через 2, 4, 6, 12 і 24 години до зупинки всіх активних кровотеч або через 6, 12 і 24 години при коагулопатії без кровотечі.
Претерапія: РЕКОМЕНДОВАНА для цієї протиотрути. Введіть 0,25 мг адреналіну ПШ до початку введення протиотрути, щоб зменшити ризик виникнення гострої реакції. Дози для дітей розраховуються на основі маси тіла у дозі – від 0,01 мг/кг (до 0,25 мг).
Підготовка та введення: Усю дозу антиотрути розвести в одному пакеті ізотонічного розчину об'ємом 250 - 500 мл і ввести шляхом внутрішньовенної інфузії за 10 - 30 хвилин.
Протиотрута другої лінії (AFRICOM - Північна Африка): NAVPC-C
Національний центр з виробництва протиотрут та вакцин, Саудівська Аравія - Полівалентна зміїна протиотрута (NAVPC-P) (Рідка/Потребує охолодження)182-186:
Отруєння внаслідок укусу невідомої змії з нейротоксичним, гемотоксичним або цитотоксичним синдромами без ознак покращення стану після введення 10 флаконів препарату POLYSERP-M. Прямо чи опосередковано охоплює деяких змій категорії 1 та 2 за ВООЗ у цьому регіоні, для яких наразі існує протиотрута.
- Нестабільна в польових умовах. Широкий спектр дії для 6+ видів змій при цито-/гемо-/нейротоксичному синдромах.
- Отруєння внаслідок укусу невідомої змії з нейротоксичним, гемотоксичним або цитотоксичним синдромами без ознак покращення стану після введення 10 флаконів препарату POLYSERP-М. Прямо чи опосередковано поширюється на деяких змій категорії 1 і 2 за ВООЗ у цьому регіоні, для яких наразі існує протиотрута.
- Початкова доза при нейротоксичних отруєннях = 10 флаконів. Початкова доза при гемо-/цитотоксичних отруєннях = 5 флаконів. Всі додаткові дози = 5 флаконів.
Можливість застосування в непристосованих умовах: НЕ РЕКОМЕНДОВАНА для використання у бойових умовах. Потребує охолодження; має помірно-високий ризик виникнення побічних реакцій. Існують кращі альтернативи. У разі придбання препарат слід зберігати на об'єктах другого та третього етапів допомоги на Аравійському півострові.
Побічні реакції: Наразі недостатньо доказових даних для визначення ризику виникнення побічних реакцій.
Показання до застосування: Цей полівалентний препарат можна використовувати для лікування нейротоксичних та цитотоксичних отруєнь 6 різними видами змій Близького Сходу, Північної Африки та Центральної Азії. Потенційно здатний нейтралізувати отруту інших видів через параспецифічну нейтралізацію, але це не досліджувалося.187-192 Для шести видів змій, перелічених нижче, є офіційні показання щодо лікування, рекомендовані виробником:
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Walterinnesia aegyptia, Naja haje
- ГЕМОТОКСИЧНИЙ та/або ЦИТОТОКСИЧНИЙ ЕФЕКТ: Bitis arietans, Echis coloratus, Echis carinatus, Cerastes cerastes
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ - початкова доза = 10 флаконів
- ГЕМОТОКСИЧНИЙ - початкова доза = 5 флаконів
- ЦИТОТОКСИЧНИЙ - початкова доза = 5 флаконів
Додаткове дозування: Додаткові дози по 5 флаконів NAVPC-C можна вводити через 2, 4, 6, 12 та 24 години, якщо необхідно.
Претерапія: Рекомендована для цієї протиотрути через недостатню кількість доказових даних для визначення ризику виникнення ранніх побічних реакцій. Введіть 0,25 мг адреналіну ПШ до початку введення протиотрути, щоб зменшити розвитку небезпечної реакції. Дозування адреналіну для дітей визначається на основі маси тіла (0,01 мг/кг, до 0,25 мг).
Підготовка та введення: Усю дозу протиотрути розвести в 250 - 500 мл ізотонічного розчину і ввести шляхом внутрішньовенної інфузії за 10 - 30 хв.
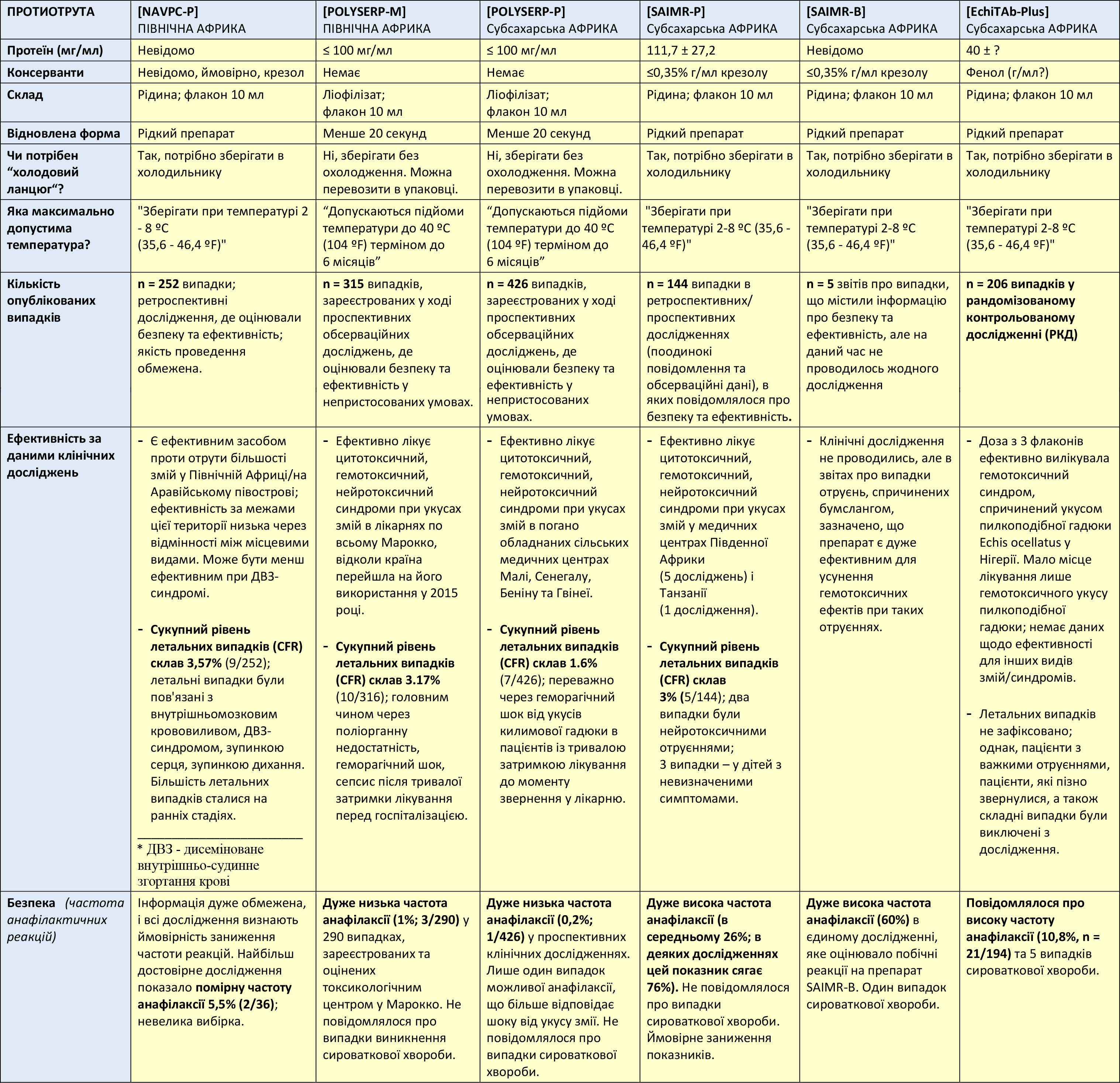
Порівняння складу протиотрут, доступних у зоні AFRICOM
Склад, зберігання, стабільність, безпека та ефективність шести протиотрут, доступних у зоні відповідальності AFRICOM. EchiTAb-Plus включено для довідки, але не рекомендовано через обмежене видове покриття, погану доступність та високу частоту анафілактичних реакцій.
Примітка: Особливі показання наведені в інструкції для медичного застосування.
Таблиця 4a. Порівняння складу протиотрут у зоні AFRICOM
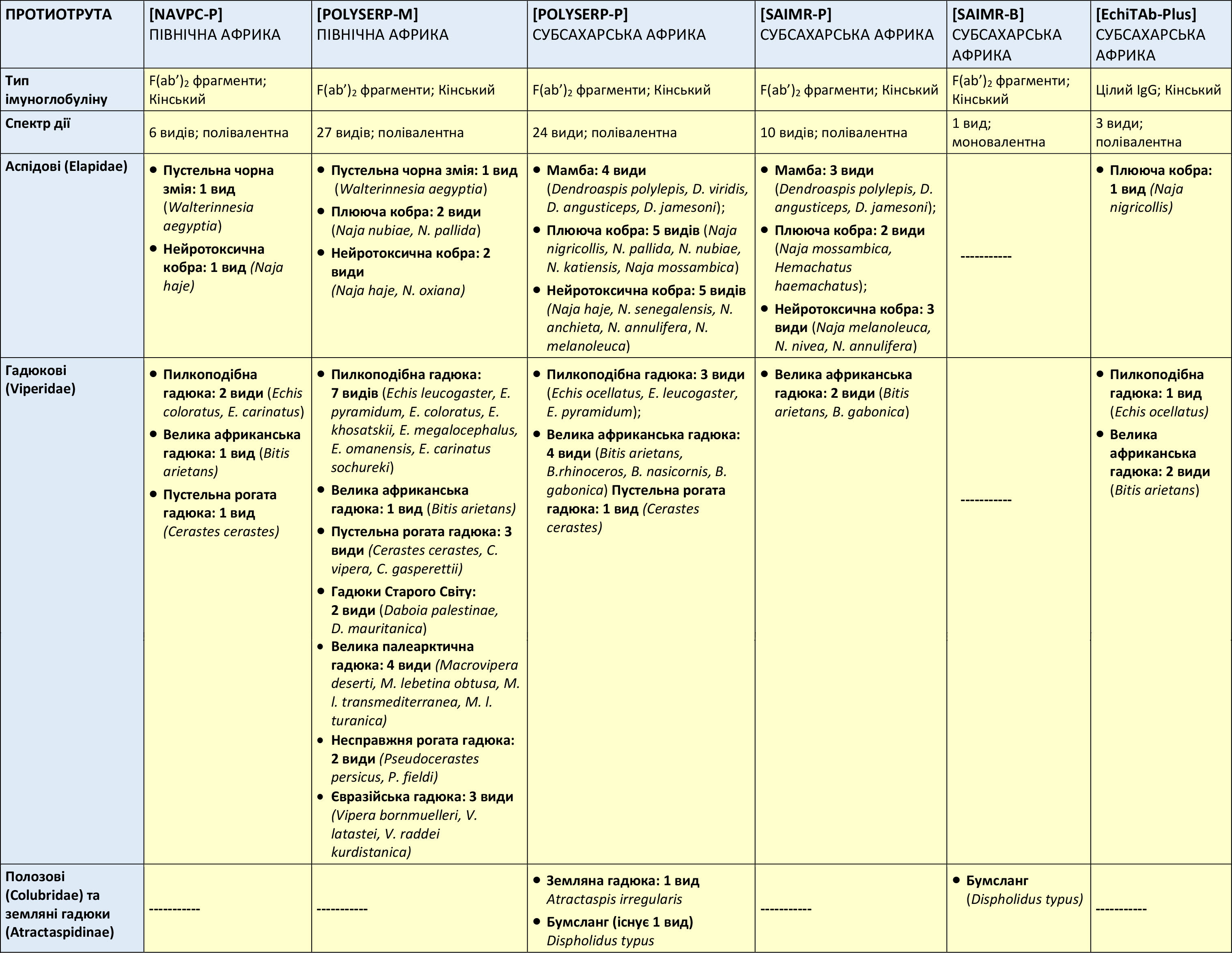
Таблиця 4b. Порівняння складу протиотрут
CENTCOM
Центральне Командування Збройних Сил США
Настанови з лікування
У цій зоні відповідальності (ЗВ) доступні безпечні, стабільні в польових умовах протиотрути широкого спектра дії, ефективні при всіх трьох синдромах отруєння зміїною отрутою; для лікування ідентифікація виду змії не потрібна. Лікування укусів змій для CENTCOM рекомендовано проводити на тому місці, де відбувся укус, через тривалий час евакуації, високу частоту укусів змій і високий ризик смерті чи стійкої інвалідності, який спричиняють багато отруйних змій у цій ЗВ при недоступності раннього лікування протиотрутою.
Лікування побічних реакцій
- У разі виникнення реакції легкого чи помірного ступеня зменшіть швидкість інфузії та проведіть симптоматичне лікування антигістамінними препаратами, стероїдами та/або протиблювотними препаратами за необхідності.
- У разі виникнення тяжкої реакції, наприклад, анафілаксії, припиніть інфузію та проведіть лікування згідно з протоколом лікування анафілаксії, наведеним у даних настановах. Повторно оцініть стан пацієнта після зникнення проявів реакції та відновіть інфузію з нижчою швидкістю, якщо не усунутий повністю будь-який зі специфічних симптомів-критеріїв для застосування протиотрути, наведених в інших розділах настанов.
Протокол лікування гострої судинної недостатності (колапсу)
У пацієнта протягом 30 хвилин після укусу швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта за допомогою ВМ або ВВ введення адреналіну та розчинів для інфузії відповідно до протоколів лікування анафілаксії.
- Виконайте інтубацію трахеї при набряку дихальних шляхів, якщо відсутня швидка реакція на застосування адреналіну.
- Після введення адреналіну негайно ВВ або ВК болюсно введіть високу дозу відповідної регіональної протиотрути, продовжуючи заходи ресусцитації.
- Підтримуйте артеріальний тиск за допомогою ВВ або ВК введення розчинів та адреналіну, доки гемодинаміка не стабілізується завдяки дії протиотрути.
Для отримання додаткової інформації див. розділ «Гостра судинна недостатність (колапс)».
Контакти
Для екстрених телемедичних консультацій телефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
Таблиця 5. CENTCOM - протиотрути першої лінії
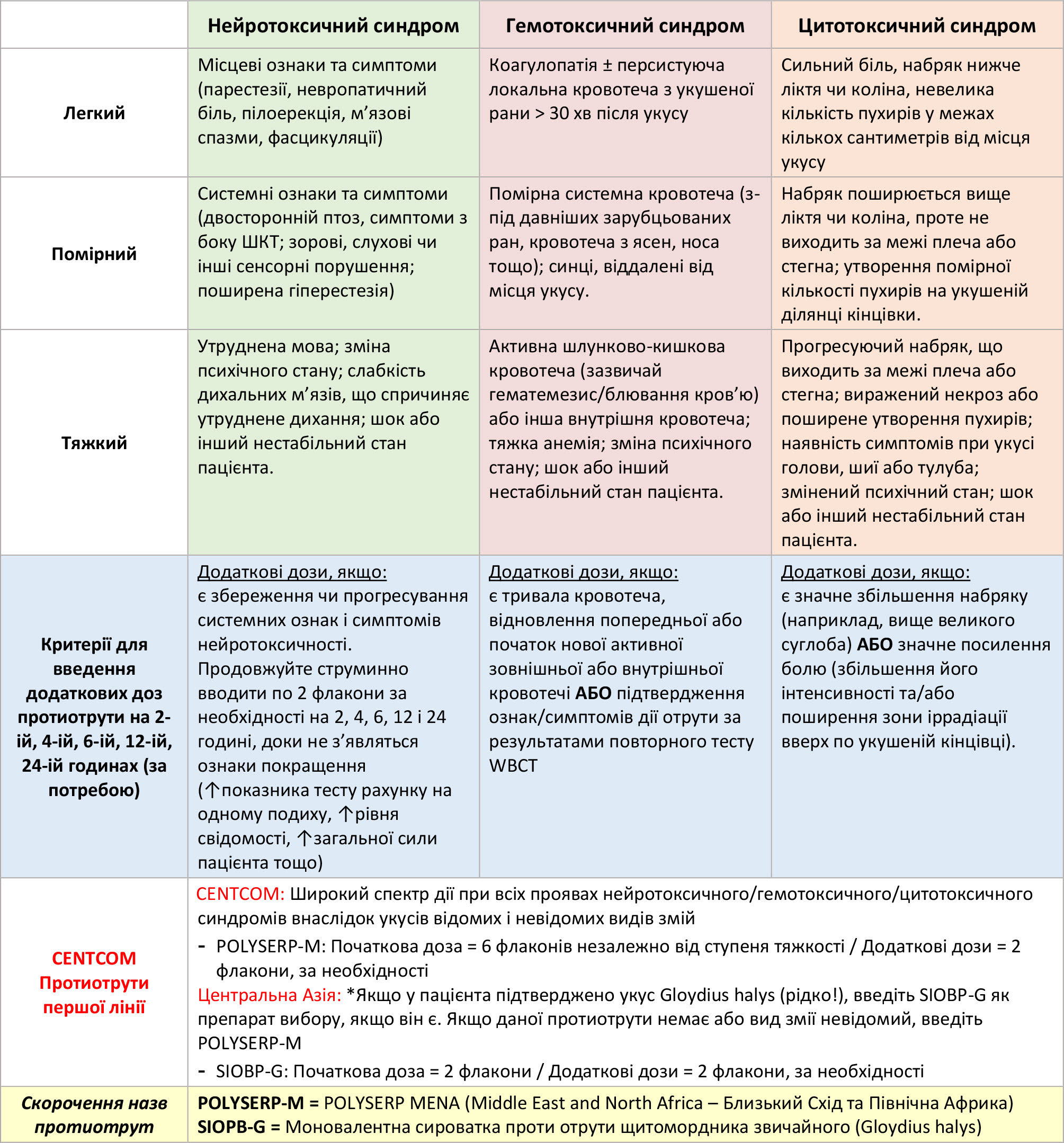
Малюнок 3. Алгоритм введення протиотрути: зона відповідальності CENTCOM
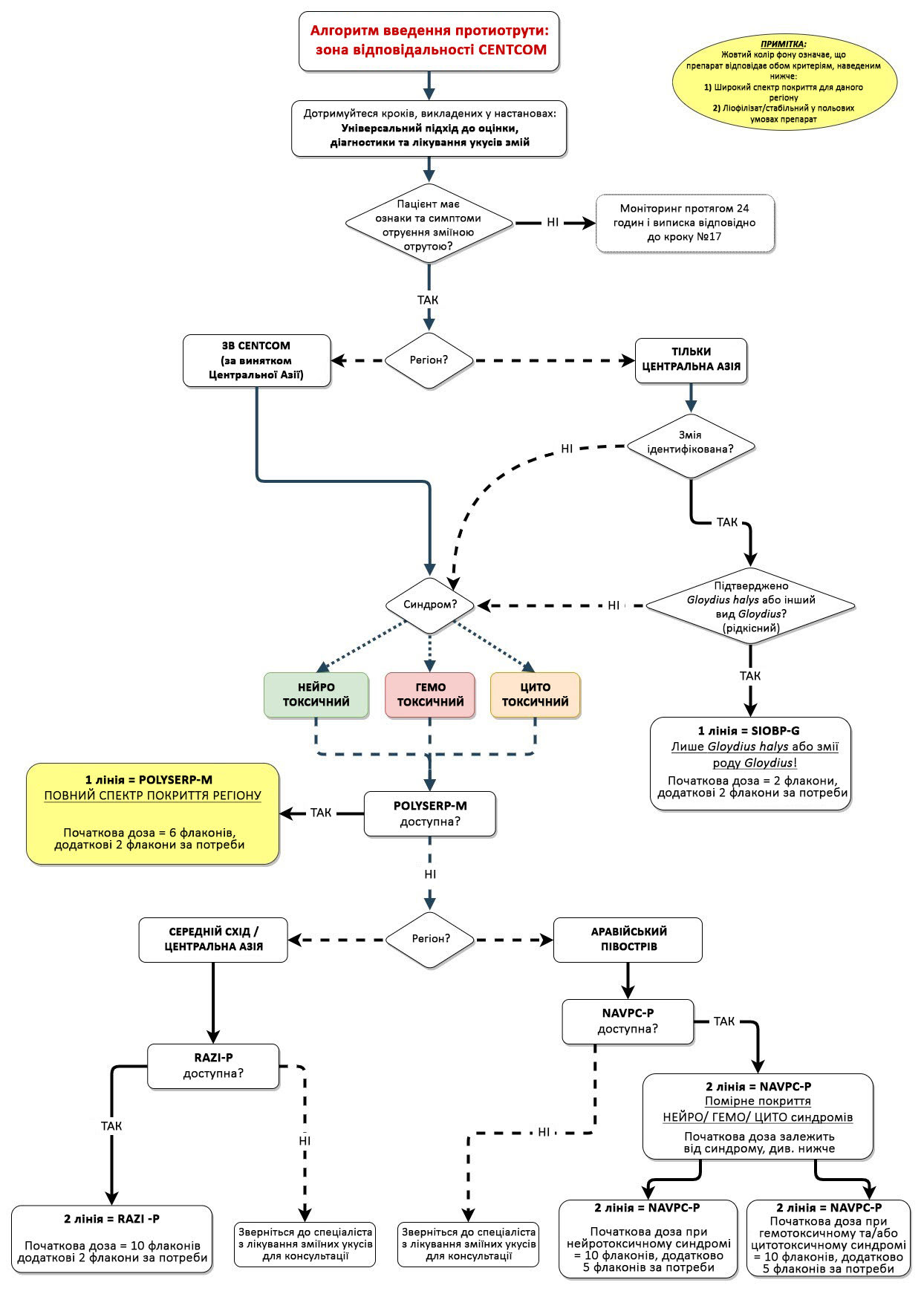
Протиотрута першої лінії (CENTCOM - Аравійський півострів/Близький Схід/Центральна Азія): POLYSERP-M
POLYSERP / Inosan, Іспанія - Полівалентна протиотрута POLYSERP MENA (POLYSERP-M) (Ліофілізат/Не потребує охолодження)162-172
- Стабільна в польових умовах. Широкий спектр дії для 27+ видів змій при цито-/гемо-/нейротоксичному синдромах.
- Варіант лікування одним курсом всіх нейротоксичних, гемотоксичних і цитотоксичних зміїних отруєнь на Аравійському півострові, Близькому Сході та в Центральній Азії, коли вид змії або невідомий, або належить до 27 видів змій, для яких цей препарат безпосередньо показаний. Прямо чи опосередковано охоплює всі види 1 категорії за ВООЗ у регіоні. Прямо чи опосередковано охоплює всіх змій 2 категорії за ВООЗ у цьому регіоні, для яких наразі існує протиотрута, за винятком Gloydius halys, яку нейтралізує Шанхайська протиотрута SIOBP-G або іранська RAZIP. Параспецифічна нейтралізація отрути змій роду Gloydius не досліджувалася, проте очікувати ефекту не слід.
- Початкова доза = 6 флаконів для всіх синдромів, додаткові дози = 2 флакони за потреби.
Можливість застосування в непристосованих умовах: Рекомендована для використання в бойових умовах і спеціально розроблена з урахуванням можливостей наземних медиків, які працюють в зоні бойових дій у цих районах. Оновлена версія протиотрути Inoserp MENA створена спеціально для непристосованих умов і тактичної медицини. Ліофілізована, не потребує охолодження, стабільна при температурі > 37ºС протягом щонайменше 180 днів без втрати ефективності. Широкий спектр покриття та просте дозування дозволяють застосовувати препарат у польових умовах при будь-яких симптомах внаслідок укусу змій невідомого виду в цьому регіоні. Сили спеціальних операцій і звичайні підрозділи, що розгортаються в непристосованих оперативних умовах та в районах із критично небезпечними отруйними видами змій, повинні мати при собі по 8 флаконів на кожного медика. Рекомендовано також мати запас протиотрути у всіх медичних закладах CENTCOM 2-го та 3-го рівня на випадок, якщо після прибуття знадобиться додаткова доза протиотрути, а також для поповнення запасів польових медиків, які використали отриману протиотруту.
Побічні реакції: Висока ефективність проти всіх основних синдромів і низька частота серйозних побічних реакцій - приблизно 1% на основі поточних публікацій.
Показання: Полівалентна протиотрута широкого спектра дії, призначена для лікування нейротоксичного, гемотоксичного і цитотоксичного синдромів отруєння, викликаних 27 різними видами близькосхідних, північноафриканських і центральноазійських змій з родин Elapidae і Viperidae. Перша лінія лікування при отруйних укусах змій у цьому регіоні, коли вид невідомий або серед видів, для яких препарат прямо показаний.
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Naja haje, N. oxiana; Walterinnesia aegyptia
- ЦИТОТОКСИЧНИЙ та/або ГЕМОТОКСИЧНИЙ ЕФЕКТ: Bitis arietans; Cerastes cerastes, C. vipera, C. gasperettii; Daboia palestinae, D. mauritanica, D. deserti; Echis. carinatus sochureki, E. coloratus, E. khosatskii, E. leucogaster, E. megalocephalus, E. omanensis, E. pyramidum; Macrovipera lebetina obtusa, M. l. transmediterranea, M. l. turanica; Montivipera bornmuelleri, M. raddei kurdistanica; Naja nubiae, N. pallida; Pseudocerastes persicus persicus, P. fieldi; Vipera latastei
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром: початкова доза = 6 флаконів
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 6 флаконів
- ЦИТОТОКСИЧНИЙ синдром: початкова доза = 6 флаконів
Додаткове дозування: Можливе додаткове застосування по 2 флакони POLYSERP-М на 2-й, 4-й, 6-й, 12-й та 24-й годинах, якщо це необхідно.
Підготовка та введення: Розчиняйте по 2 флакони POLYSERP-P в одному шприці об’ємом 10 мл. Введіть ізотонічний розчин у перший флакон, змішайте, втягніть назад у шприц та введіть у другий флакон, щоб загалом отримати дозу 2 флаконів у 1 шприці (загальна доза: 6 флаконів = 3 шприци). Один за одним вводьте вміст шприців з отриманим розчином повільно й безперервно ВВ або ВК струминно (болюсно), приблизно по 2 хв на кожен шприц. У разі виникнення побічної реакції припиніть введення, проведіть лікування реакції, повторно оцініть на наявність відповіді згідно з критеріями лікування. Решту дози розчиніть у пакеті зі 100 мл ізотонічного розчину та вводьте повільно ВВ або ВК краплинно протягом 30 хв, якщо необхідно.
Для зручності рекомендоване струминне (болюсне) введення, проте POLYSERP-P також можна вводити ВВ або ВК краплинно. Розчиніть ліофілізат у пакеті з 50 мл або 100 мл ізотонічного розчину, введіть весь вміст пакета за 5-10 хв.
Протиотрута першої лінії та другої лінії (CENTCOM - Близький Схід/Центральна Азія): SIOBP-G
Шанхайський інститут біологічних речовин, Китай - Моновалентна сироватка проти отрути щитомордника звичайного Agkistrodon (Gloydius) halys (SIOBP-G) (Рідка/Потребує охолодження)194-196:
ПРИМІТКА. Цей продукт вказано як протиотруту для змій виду Agkistrodon halys на веб-сайті SIOBP і на упаковці продукту, але таксономія цього виду змінилася. Agkistrodon halys був переміщений до роду Gloydius і має бути зазначений як Gloydius halys, як це вказано в інших джерелах. Продукт скорочено позначається як SIOBP-G у CPG, щоб врахувати це виправлення.
- Нестабільна в польових умовах. Не широкого спектра дії. Охоплює один вид.
- Моновалентна, проти отрути змії виду Gloydius halys (категорія 2 за ВООЗ). Вказується як перша лінія лише для підтвердженого отруєння внаслідок укусу Gloydius halys або спорідненими видами Gloydius. Показана як друга лінія для невідомих цитотоксичних та/або гемотоксичних отруєнь на Близькому Сході чи в Центральній Азії без ознак покращення після введення 10 флаконів POLYSERP-M. Не забезпечує покриття проти інших видів змій категорій 1 або 2 за ВООЗ.
- Початкова доза = 6 флаконів; лише при гемотоксичному/цитотоксичному синдромах; додаткові дози = 2 флакони за потреби.
Протиотрута першої лінії (CENTCOM - БЛИЗЬКИЙ СХІД / ЦЕНТРАЛЬНА АЗІЯ): Моновалентна, проти отрути змії виду Gloydius halys (категорії 2 за ВООЗ). Показана лише для підтвердженого отруєння внаслідок укусу Gloydius halys або споріднених видів Gloydius. Не забезпечує покриття проти інших видів видів змій категорій 1 або 2 за ВООЗ.
Протиотрута другої лінії (CENTCOM - БЛИЗЬКИЙ СХІД / ЦЕНТРАЛЬНА АЗІЯ): Показана для невідомих цитотоксичних і/або гемотоксичних отруєнь на Близькому Сході або в Центральній Азії без ознак покращення після 10 флаконів POLYSERP-M.
Можливість застосування в непристосованих умовах: Не рекомендовано використовувати в польових умовах. Вимагає дотримання “холодового ланцюга”. Рекомендуємо зберігати невеликі кількості на стратегічно розташованих об’єктах другого та третього етапів медичної допомоги у ЗВ CENTCOM.
Частота побічних реакцій: Очікується низька або помірна частота побічних реакцій і сироваткової хвороби, але клінічні дані обмежені.
Показання: Дану моновалентну протиотруту можна використовувати для лікування цитотоксичних і гемотоксичних отруєнь при укусах Gloydius halys, щитомордника звичайного з підродини ямкоголових (гримучникових) гадюк, що мешкає на Близькому Сході та в Центральній Азії. Препарат, швидше за все, нейтралізує отруту споріднених видів роду Gloydius через параспецифічність, але це не було детально перевірено. Є кілька публікацій, які вказують на те, що він також може мати параспецифічність проти деяких зелених ямкоголових гадюк Південно-Східної Азії родів Cryptelytrops і Trimeresurus.196,197 Однак наразі виробник не вказує про дію протиотрути на ці види.
- ГЕМОТОКСИЧНИЙ ТА/АБО ЦИТОТОКСИЧНИЙ ЕФЕКТ: Gloydius halys
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 2 флакони
- ЦИТОТОКСИЧНИЙ синдром: початкова доза = 2 флакони
Додаткове дозування: Можливе додаткове введення по 2 флакони SIOBP-G на 2-й, 4-й, 6-й, 12-й та 24-й годинах, якщо це необхідно.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування.
Підготовка та введення: Розчиніть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії за 10–30 хвилин.
Протиотрута другої лінії (CENTCOM - Близький Схід/Центральна Азія): RAZI-P
Дослідницький інститут сироватки та вакцини Razi, Ісламська Республіка Іран - Полівалентна зміїна протиотрута (RAZI-P) (Рідка/Потребує охолодження)198-205:
- Нестабільна в польових умовах. Широкий спектр дії з нейтралізацією нейротоксичних, гемотоксичних або цитотоксичних синдромів, спричинених укусами 6+ видів змій.
- Нейротоксичне, гемотоксичне або цитотоксичне отруєння внаслідок укусу змії невідомого виду без ознак покращення після введення 10 флаконів POLYSERP-M. Прямо чи опосередковано охоплює всі види 1 категорії за ВООЗ у регіоні. Прямо чи опосередковано охоплює деяких змій категорії 1 і 2 за ВООЗ у цьому регіоні, для яких наразі існує протиотрута.
Можливість застосування в непристосованих умовах: Не рекомендована для використання в умовах ведення бойових дій. Вимагає дотримання “холодового ланцюга”. Рекомендовано зберігати невеликий запас препарату на стратегічно розташованих об’єктах другого та третього етапів медичної допомоги у ЗВ CENTCOM або вибрати альтернативну другу лінію, вказану в даних настановах.
Побічні реакції: Обмежена кількість доказових даних, але, схоже, що частота побічних реакції є низькою на основі поточних публікацій.
Показання: Цей полівалентний засіб можна використовувати для лікування нейротоксичних і цитотоксичних отруєнь 6 різних видів змій Близького Сходу, Північної Африки та Центральної Азії. Він може нейтралізувати отруту інших видів шляхом параспецифічної нейтралізації, але щодо цього дослідження не проводились. Для шести видів змій, перелічених нижче, є офіційні показання щодо лікування, рекомендовані виробником:
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Naja oxiana
- ГЕМОТОКСИЧНИЙ та/або ЦИТОТОКСИЧНИЙ ЕФЕКТ: Pseudocerastes persicus fieldi, Echis carinatus, Vipera albicornuta, Vipera lebetina obtusa, Agkistrodon (Gloydius) halys
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром початкова доза = 10 флаконів
- ГЕМОТОКСИЧНИЙ синдром початкова доза = 5 флаконів
- ЦИТОТОКСИЧНИЙ синдром початкова доза = 5 флаконів
Додаткове дозування: Можливе додаткове застосування 5 флаконів RAZI-P на 2, 4, 6, 12 та 24 годині, якщо це необхідно.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута другої лінії (CENTCOM - Аравійський півострів): NAVPC-C
Національний центр виробництва протиотрут і вакцин, Саудівська Аравія - Полівалентна зміїна протиотрута (NAVPC-P) (Рідка/Потребує охолодження)187-192:
- Нестабільна в польових умовах. Широкий спектр дії з нейтралізацією нейротоксичних, гемотоксичних або цитотоксичних синдромів, спричинених укусами 6+ видів змій.
- Нейротоксичне, гемотоксичне або цитотоксичне отруєння внаслідок укусу змії невідомого виду без ознак покращення після введення 10 флаконів POLYSERP-M. Тільки для Аравійського півострова, дуже обмежена користь далі на схід. Прямо чи опосередковано охоплює деяких змій категорії 1 і 2 за ВООЗ у цьому регіоні, для яких наразі існує протиотрута.
- Початкова доза при нейротоксичному синдромі = 10 флаконів. Початкова доза при гемо/цитотоксичному синдромі = 5 флаконів. Усі додаткові дози = 5 флаконів.
Можливість застосування в непристосованих умовах: Не рекомендована для використання в бойових умовах. Потребує зберігання в холодильнику; ймовірність розвитку побічних реакцій - від середньої до високої. Існують кращі альтернативи. У разі придбання даної протиотрути, її слід зберігати в закладах другого та третього етапів медичної допомоги на Аравійському півострові.
Побічні реакції: На даний момент недостатньо доказових даних для визначення ризику побічних реакцій.
Показання: Цей полівалентний засіб можна використовувати для лікування нейротоксичних і цитотоксичних отруєнь 6 різних видів змій Близького Сходу, Північної Африки та Центральної Азії. Він може нейтралізувати отруту інших видів шляхом параспецифічної нейтралізації, але щодо цього досліджень не проводилось. Для шести видів змій, перелічених нижче, є офіційні показання щодо лікування, рекомендовані виробником:
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: Walterinnesia aegyptia, Naja haje
- ГЕМОТОКСИЧНИЙ та/або ЦИТОТОКСИЧНИЙ ЕФЕКТ: Bitis arietans, Echis coloratus, Echis carinatus, Cerastes cerastes
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром початкова доза = 10 флаконів
- ГЕМОТОКСИЧНИЙ синдром початкова доза = 5 флаконів
- ЦИТОТОКСИЧНИЙ синдром початкова доза = 5 флаконів
Додаткове дозування: Можливе додаткове застосування 5 флаконів NAVPC-C на 2, 4, 6, 12 та 24 годинах, якщо це необхідно.
Претерапія: РЕКОМЕНДОВАНА для цієї протиотрути через недостатню кількість доказів для визначення ризику ранніх побічних реакцій. Введіть 0,25 мг адреналіну ПШ перед початком інфузії протиотрути, щоб зменшити ризик серйозної реакції. Дозування адреналіну для дітей визначається на основі маси тіла (0,01 мг/кг, максимальна доза - 0,25 мг).
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
EUCOM
Європейське Командування Збройних Сил
Настанови з лікування
У цій зоні відповідальності (ЗВ) доступні безпечні охолоджені протиотрути широкого спектра дії, ефективні при всіх трьох синдромах отруєння внаслідок укусу гадюк у цій зоні; для лікування ідентифікація виду змії не потрібна. У зоні EUCOM лікування зміїного укусу на місці травми, зазвичай, не рекомендується. У даному розділі наведено особливості використання протиотрут у цьому регіоні.
Лікування побічних реакцій
- У разі виникнення реакції легкого чи помірного ступеня зменшіть швидкість інфузії та проведіть симптоматичне лікування антигістамінними препаратами, стероїдами та/або протиблювотними препаратами за необхідності.
- У разі виникнення тяжкої реакції, наприклад, анафілаксії, припиніть інфузію та проведіть лікування згідно з протоколом лікування анафілаксії, наведеним у даних настановах. Повторно оцініть стан пацієнта після зникнення проявів реакції та відновіть інфузію з нижчою швидкістю, якщо не усунутий повністю будь-який зі специфічних симптомів-критеріїв для застосування протиотрути, наведених в інших розділах настанов.
Протокол лікування гострої судинної недостатності (колапсу)
У пацієнта протягом 30 хвилин після укусу швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта за допомогою ВМ або ВВ введення адреналіну та розчинів для інфузії відповідно до протоколів лікування анафілаксії.
- Виконайте інтубацію трахеї при набряку дихальних шляхів, якщо відсутня швидка реакція на застосування адреналіну.
- Після введення адреналіну негайно ВВ або ВК болюсно введіть високу дозу відповідної регіональної протиотрути, продовжуючи заходи ресусцитації.
- Підтримуйте артеріальний тиск за допомогою ВВ або ВК введення розчинів та адреналіну, доки гемодинаміка не стабілізується завдяки дії протиотрути.
Для отримання додаткової інформації див. розділ «Гостра судинна недостатність (колапс)».
Контакти
Для екстрених телемедичних консультацій телефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
Таблиця 6. EUCOM - протиотрути першої лінії
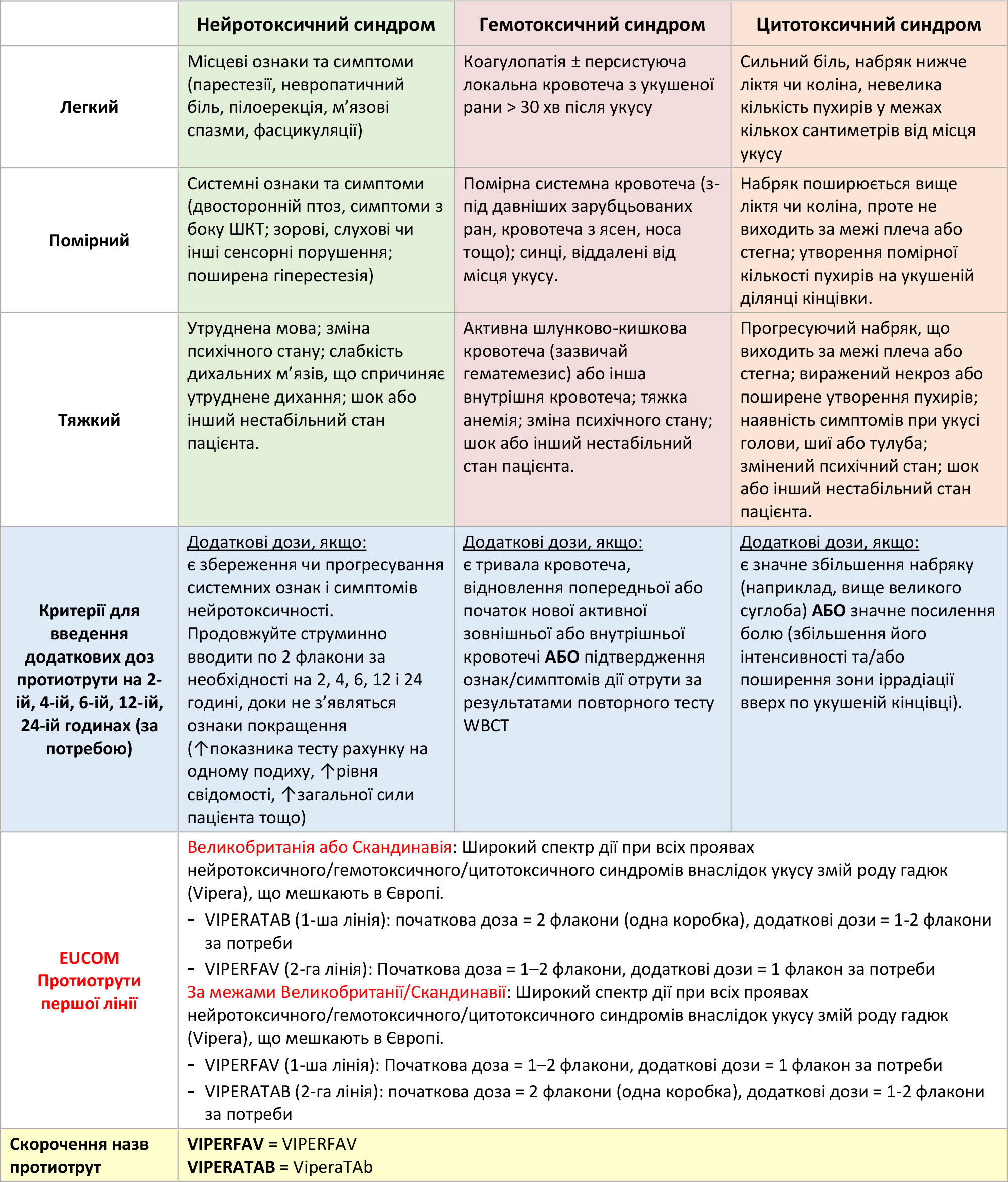
Малюнок 4. Алгоритм введення протиотрути: зона відповідальності EUCOM
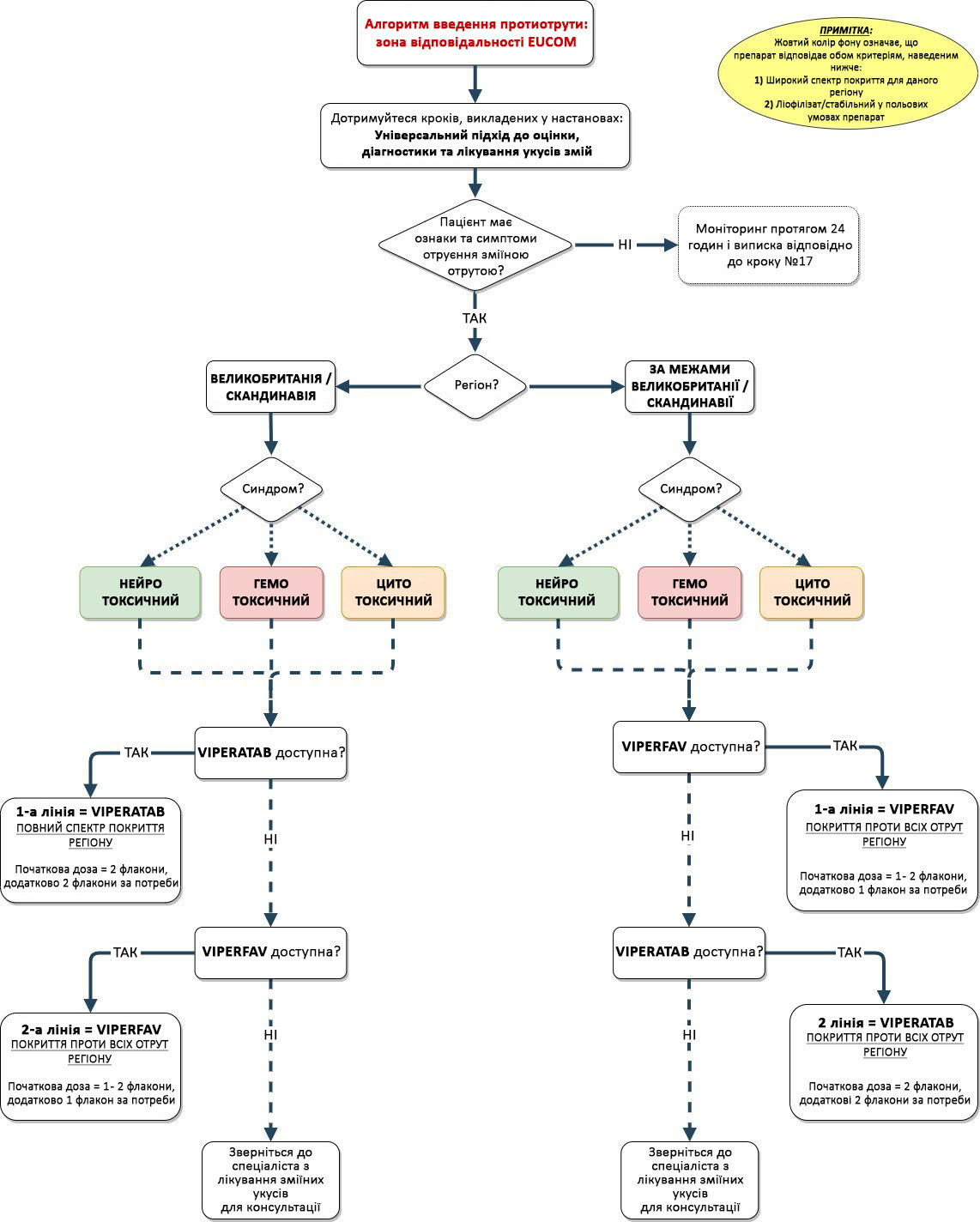
Протиотрута першої лінії (EUCOM - За межами Великобританії/Скандинавії): VIPERFAV
Протиотрута другої лінії (EUCOM - На території Великобританії/Скандинавії): VIPERFAV
Санофі-Пастер, Франція - Viperfav (VIPERFAV) (Ліофілізат/Потребує охолодження)206-212:
- Нестабільна в польових умовах. Широкий спектр дії проти отрути багатьох видів європейських гадюк.
- Варіант лікування першої лінії (EUCOM - поза межами Великобританії/Скандинавії): Варіант лікування одним курсом всіх нейротоксичних, гемотоксичних, цитотоксичних отруєнь внаслідок укусів найбільш медично та епідеміологічно значущих видів гадюк в Європі (Vipera berus, V. aspis, V. ammodytes) з параспецифічним покриттям проти інших європейських видів гадюк (Viperaе). Може використовуватися в зоні відповідальності EUCOM, якщо вид змії невідомий або якщо це вид, для якого цей препарат прямо показаний.
- Варіант лікування другої лінії (EUCOM - Великобританія/Скандинавія) для всіх нейротоксичних, гемотоксичних і цитотоксичних отруєнь внаслідок укусу змій на території Великобританії та Скандинавії, якщо перша лінія (VIPERATAB) недоступна.
- Початкова доза = 1–2 флакони для всіх синдромів, додаткові дози = 1 флакон за потреби.
Можливість застосування в непристосованих умовах: Не рекомендована для використання в бойових умовах. Вимагає дотримання “холодового ланцюга”- зберігання при температурі 2–8 ºC (35,6–46,4 ºF). Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги. Ймовірно, протиотрута збереже ефективність протягом кількох тижнів у польових умовах, але її слід утилізувати після закінчення цього періоду часу (зберігання без охолодження).
Побічні реакції: Висока ефективність проти всіх основних синдромів і низька частота серйозних побічних реакцій на основі поточних публікацій.
Показання: Полівалентна протиотрута, безпосередньо показана для лікування нейротоксичних, гемотоксичних і цитотоксичних синдромів отруєння, спричинених гадюками Vipera berus, V. aspis, V. ammodytes; крім цього, також продемонструвала ефективність проти інших видів європейських гадюк (рід Vipera).
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром: початкова доза = 2 флакони
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 1 - 2 флакони
- ЦИТОТОКСИЧНИЙ синдром: початкова доза = 1 - 2 флакони
Додаткове дозування: Можливе додаткове застосування по 1 флакону VIPERFAV на 2, 4, 6, 12 та 24 годинах, якщо це необхідно.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (EUCOM – На території Великобританії/Скандинавії: VIPERATAB
Протиотрута другої лінії (EUCOM – За межами Великобританії/Скандинавії): VIPERATAB
Micropharm, Великобританія - ViperaTAb (VIPERATAB) (Ліофілізат/Потребує охолодження)206,210,213-215:
- Нестабільна в польових умовах. Широкий спектр дії проти кількох видів європейських гадюк.
- Варіант лікування першої лінії (EUCOM – ВЕЛИКОБРИТАНІЯ / СКАНДИНАВІЯ): Варіант лікування одним курсом всіх нейротоксичних, гемотоксичних, цитотоксичних отруєнь внаслідок укусів найбільш медично та епідеміологічно значущих видів змій на території Великобританії та Скандинавії (Vipera berus) з параспецифічним покриттям проти деяких інших європейських видів гадюк (Viperaе).
- Варіант лікування другої лінії (EUCOM - ЗА МЕЖАМИ ВЕЛИКОБРИТАНІЇ / СКАНДИНАВІЇ) для лікування нейротоксичних, гемотоксичних та цитотоксичних отруєнь внаслідок укусів змій у зоні відповідальності EUCOM за межами Великобританії та Скандинавії, якщо перша лінія (VIPERFAV) недоступна.
- Початкова доза = 2 флакони для всіх синдромів, додаткові дози = 2 флакони за потреби. Кожна коробка = 2 флакони.
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Вимагає дотримання “холодового ланцюга” - зберігання при температурі 2–8 ºC (35,6–46,4 ºF). Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги. Ймовірно, протиотрута збереже ефективність протягом кількох тижнів у польових умовах, але її слід утилізувати після закінчення цього періоду (тобто перебування без охолодження).
Побічні реакції: Висока ефективність проти британської/скандинавської європейської гадюки (Vipera berus) і низька частота серйозних побічних реакцій згідно з поточними публікаціями.
Показання: Полівалентна протиотрута, яка безпосередньо показана для лікування нейротоксичних, гемотоксичних і цитотоксичних синдромів при отруєнні, спричиненому укусом гадюки Vipera berus. Продемонструвала ефективність проти інших видів європейських гадюк (V. aspis, V. ammodytes), але прямо не призначена для цих видів.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром початкова доза = 2 флакони
- ГЕМОТОКСИЧНИЙ синдром початкова доза = 2 флакони
- ЦИТОТОКСИЧНИЙ синдром початкова доза = 2 флакони
Додаткове дозування: Можливе додаткове застосування по 2 флакони VIPERATAB на 2, 4, 6, 12 та 24 годинах, якщо це необхідно.
Підготовка та введення: Кожна упаковка VIPERATAB містить два флакони протиотрути по 4 мл кожний (одна коробка = одна доза). Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 100–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
INDOPACOM
Настанови з лікування
У Південно-Східній Азії та кількох інших регіонах цієї зони доступні безпечні протиотрути широкого спектра дії, стабільні в польових умовах та ефективні при всіх трьох синдромах отруєння внаслідок укусу змій. Лікування зміїних укусів в зоні відповідальності INDOPACOM в цілому є складнішим, ніж в AFRICOM або CENTCOM через відсутність паназійського полівалентного препарату. У багатьох районах лікування не вимагає ідентифікації виду, але препарати є специфічними щодо синдрому, і не існує єдиної протиотрути для всіх 3 синдромів. Лікування зміїного укусу на місці травми рекомендовано для тих територій зони INDOPACOM, де доступні стабільні в польових умовах протиотрути. У даному розділі наведено особливості використання протиотрут у цьому регіоні.
Лікування побічних реакцій
- У разі виникнення реакції легкого чи помірного ступеня зменшіть швидкість інфузії та проведіть симптоматичне лікування антигістамінними препаратами, стероїдами та/або протиблювотними препаратами за необхідності.
- У разі виникнення тяжкої реакції, наприклад, анафілаксії, припиніть інфузію та проведіть лікування згідно з протоколом лікування анафілаксії, наведеним у даних настановах. Повторно оцініть стан пацієнта після зникнення проявів реакції та відновіть інфузію з нижчою швидкістю, якщо не усунутий повністю будь-який зі специфічних симптомів-критеріїв для застосування протиотрути, наведених в інших розділах настанов.
Протокол лікування гострої судинної недостатності (колапсу)
У пацієнта протягом 30 хвилин після укусу швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта за допомогою ВМ або ВВ введення адреналіну та розчинів для інфузії відповідно до протоколів лікування анафілаксії.
- Виконайте інтубацію трахеї при набряку дихальних шляхів, якщо відсутня швидка реакція на застосування адреналіну.
- Після введення адреналіну негайно ВВ або ВК болюсно введіть високу дозу відповідної регіональної протиотрути, продовжуючи заходи ресусцитації.
- Підтримуйте артеріальний тиск за допомогою ВВ або ВК введення розчинів та адреналіну, доки гемодинаміка не стабілізується завдяки дії протиотрути.
Для отримання додаткової інформації див. розділ «Гостра судинна недостатність (колапс)».
Контакти
Для екстрених телемедичних консультацій телефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
Таблиця 7. Індійсько-тихоокеанське Командування – протиотрути першої лінії
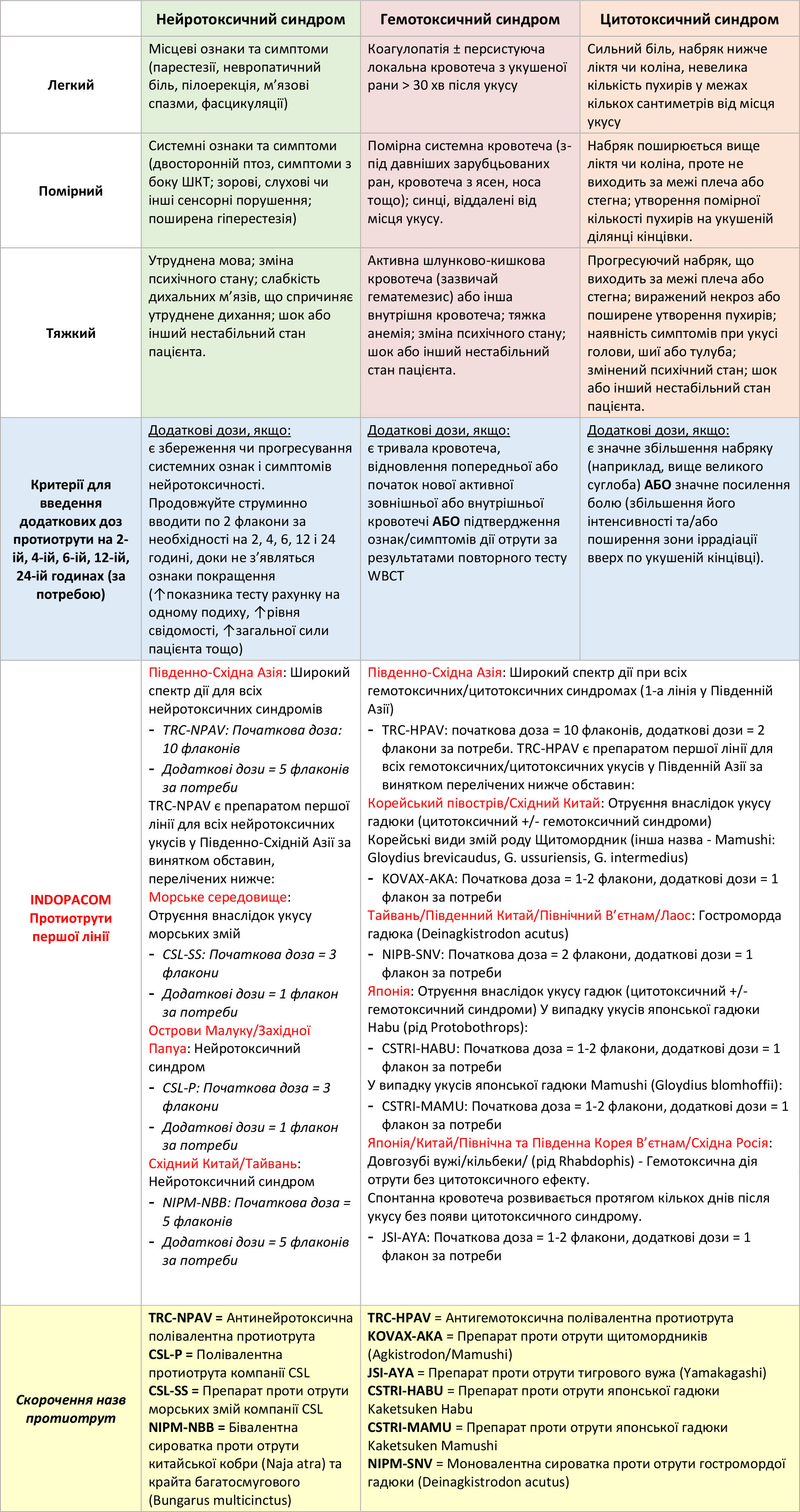
Малюнок 5. Алгоритм введення протиотрути: зона відповідальності INDOPACOM
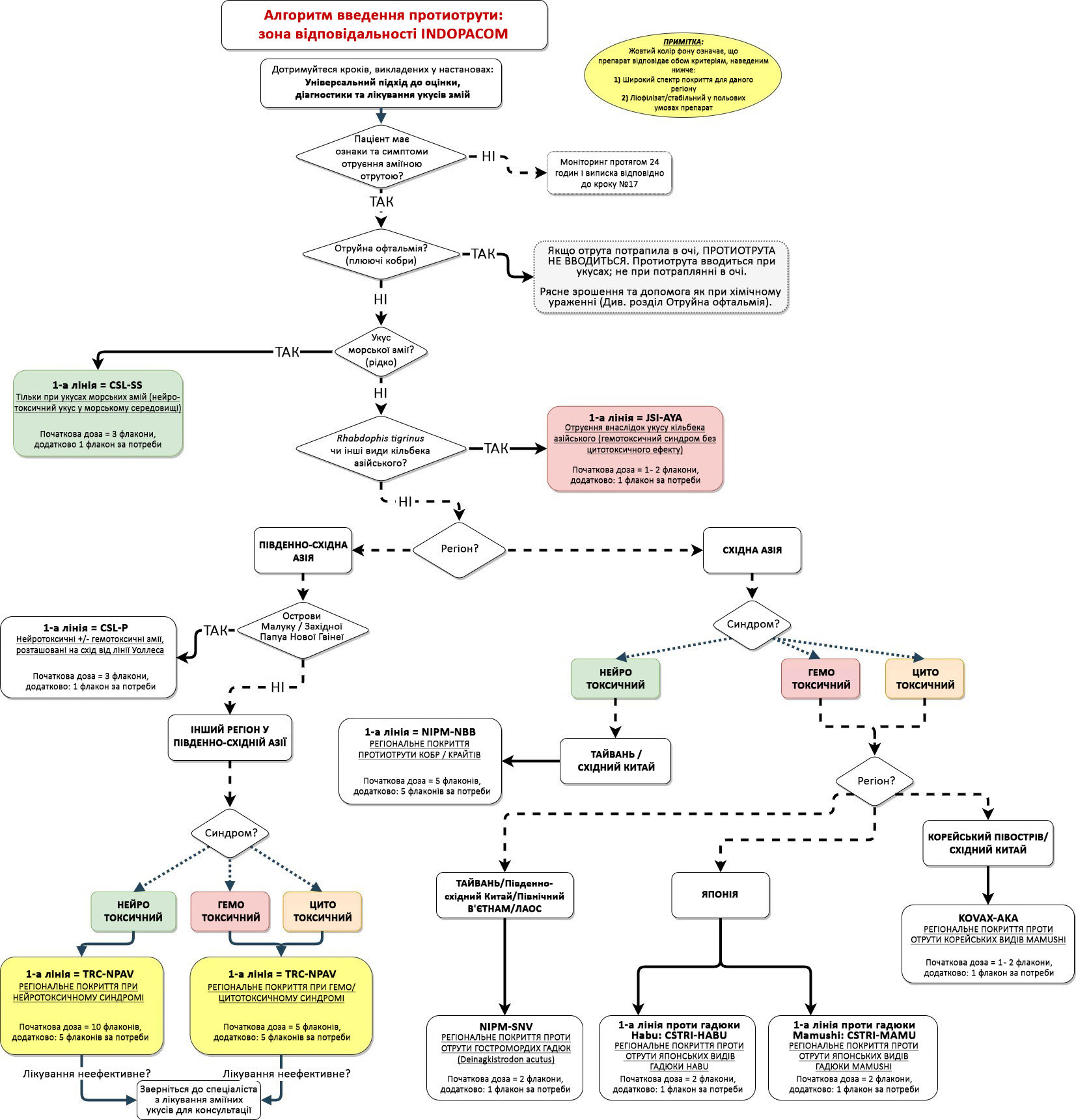
Протиотрута першої лінії (INDOPACOM - Південно-Східна Азія): TRC-HPAV
Тайський Червоний Хрест, Таїланд - Антигемотоксична полівалентна протиотрута (TRC-HPAV) (Ліофілізат/Не потребує охолодження)62,196,197,216-218:
- Стабільна в польових умовах. Широкий спектр дії проти кількох видів гемо/цитотоксичних змій.
- Варіант лікування широкого спектра дії для всіх гемотоксичних і цитотоксичних отруєнь відомими або невідомими видами змій в Південно-Східній Азії. Кращий регіональний полівалентний препарат.
- Початкова доза (лише при гемотоксичному/цитотоксичному синдромі) = 10 флаконів, додаткові дози = 5 флаконів за потреби.
Можливість застосування в непристосованих умовах: Рекомендована для застосування в бойових умовах. Не потребує холодильника, зберігається при температурі навколишнього тропічного середовища ≤ 25º C / 77º F. Це ліофілізований препарат, який, ймовірно, зберігає стабільність при більш високих температурах протягом коротких періодів часу (ймовірно, до кількох місяців). Рекомендовано брати з собою повну дозу при тривалих бойових операціях у непристосованих умовах і зберігати більший запас у стратегічно розташованих закладах другого та третього етапів медичної допомоги зони відповідальності INDOPACOM.
Побічні реакції: Висока ефективність і низька частота серйозних побічних реакцій (на основі поточних публікацій).
Показання: Полівалентна протиотрута, яка безпосередньо показана для лікування гемотоксичного і цитотоксичного синдромів, спричинених зміями Calloselasma rhodostoma, Trimersurus albolabris та Daboia russelli siamensis. Продемонструвала ефективність проти інших споріднених видів азійських гадюк того ж роду (Crytelytrops, Popeia, Daboia тощо); прямо не показана для цих видів, але є найкращим гемотоксичним/цитотоксичним полівалентним препаратом у регіоні, і її слід пробувати застосовувати як препарат першого ряду в більшості випадків.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНА ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 10 флаконів
- ЦИТОТОКСИЧНИЙ синдром: початкова доза = 10 флаконів
Додаткове дозування: Можливе додаткове застосування по 2 флакони TRC-HPAV на 2, 4, 6, 12 та 24 годинах, якщо це необхідно.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Південно-Східна Азія, антинейротоксичний препарат широкого спектра): TRC-NPAV
Тайський Червоний Хрест, Таїланд - Антинейротоксична полівалентна протиотрута (TRC-NPAV) (Ліофілізат/Не потребує охолодження)62,196,217,219-221:
- Стабільна в польових умовах. Широкий спектр охоплення кількох видів з нейротоксичною отрутою.
- Варіант лікування широкого спектра для всіх нейротоксичних отруєнь відомими або невідомими видами змій в Південно-Східній Азії. Кращий регіональний полівалентний препарат.
- Початкова доза = 10 флаконів, лише при нейротоксичному синдромі, додаткові дози = 5 флаконів за потреби.
Можливість застосування в непристосованих умовах: Рекомендована для використання у бойових умовах. Зберігання без охолодження при температурі навколишнього тропічного середовища ≤ 25º C / 77º Це ліофілізований препарат, який, ймовірно, зберігає стабільність при вищих температурах під час польових умов (ймовірно, стабільний протягом кількох місяців при вищих температурах на основі даних для подібних препаратів). Рекомендовано брати з собою повну дозу при тривалих бойових операціях у непристосованих умовах і зберігати більший запас у стратегічно розташованих закладах другого та третього етапів медичної допомоги зони відповідальності INDOPACOM.
Побічні реакції: Висока ефективність і низька частота серйозних побічних реакцій на основі поточних публікацій.
Показання: Полівалентна протиотрута, яка безпосередньо показана для лікування гемотоксичного і цитотоксичного синдромів, спричинених Ophiophagus hannah, Naja kaouthia, Bungarus candidus та B. fasciatus candidus. Продемонструвала ефективність проти інших споріднених видів азійських кобр і крайтів; не показана безпосередньо для цих видів, але є найкращим гемотоксичним/цитотоксичним полівалентним препаратом у регіоні, і його слід пробувати як препарат першого ряду в більшості випадків.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром початкова доза = 10 флаконів
ПРИМІТКА. Укуси королівської кобри (O. hannah) вимагають набагато вищих доз препарату через масивний вихід отрути; у цих випадках нерідко потрібні десятки флаконів. - НЕ ПОКАЗАНИЙ ПРИ ГЕМОТОКСИЧНОМУ синдромі
- НЕ ПОКАЗАНИЙ ПРИ ЦИТОТОКСИЧНОМУ синдромі
Додаткове дозування: Можливе додаткове застосування по 2 флакони TRC-NPAV на 2, 4, 6, 12 та 24 годинах, якщо це необхідно. Для укусів великої королівської кобри може знадобитися кілька десятків або і більше флаконів через величезну кількість отрути.
Підготовка і введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Тайвань/ Південно-Східний Китай/Півн. Лаос/ Півн. В’єтнам): NIPM-NBB
Національний інститут превентивної медицини, Тайвань - Бівалентна сироватка проти отрути китайської кобри (Naja atra) та крайта багатосмугового (Bungarus multicinctus) - NIPM-NBB (Ліофілізат/Потребує охолодження)220-230:
- Рідка, але стабільна в польових умовах (для коротких періодів часу). Широкий спектр охоплення кількох нейротоксичних видів.
- Варіант двовалентного лікування нейротоксичних отруєнь кобри та крайтів у Східній Азії.
- Початкова доза = 5 флаконів, лише при нейротоксичному синдромі, додаткові дози = 5 флаконів за потреби.
Можливість застосування в непристосованих умовах: Рекомендована для використання в умовах бойових дій під час коротких походів. Ліофілізована, але потребує дотримання “холодового ланцюга”- зберігання при температурі нижче 10ºC (50 ºF); однак тестування, проведене тайванським CDC, не показало втрати ефективності після 30 днів інкубації при 35º C / 95º F, а також протягом 4 місяців після повернення в холодильну камеру. Рекомендовано брати з собою повну дозу при тривалих бойових операціях у непристосованих умовах і зберігати більший запас у стратегічно розташованих закладах другого та третього етапів.
Побічні реакції: Висока ефективність і низька частота серйозних побічних реакцій на основі поточних публікацій.
Показання: Полівалентна протиотрута, яка безпосередньо показана для лікування гемотоксичного та цитотоксичного синдромів, спричинених Naja atra та Bungarus multicinctus. Продемонструвала ефективність проти інших споріднених видів азійських кобр і крайтів, але безпосередньо не показана для цих видів.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром початкова доза = 5 флаконів
- НЕ ПОКАЗАНИЙ ПРИ ГЕМОТОКСИЧНОМУ синдромі
- НЕ ПОКАЗАНИЙ ПРИ ЦИТОТОКСИЧНОМУ синдромі
Додаткове дозування: Можливе додаткове застосування по 5 флаконів NIPM-NBB 2, 4, 6, 12 та 24 годинах, якщо це необхідно.
Підготовка та введення: Розвести всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 100–500 мл і ввести шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Японія): CSTRI-HABU
Інститут терапевтичних досліджень Chemo-Sero, Японія - Препарат проти отрути японської гадюки Kaketsuken Habu (CSTRI-HABU) (Ліофілізат/Потребує охолодження)231-235:
- Нестабільна в польових умовах. Не широкого спектра дії. Активна лише проти отрути японської гадюки Kaketsuken Habu.
- Перша лінія лікування отруєння внаслідок укусу японської гадюки Habu (види Protobothrops).
- Початкова доза = 1-2 флакони, додаткові дози = 1 флакон за потреби
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Ліофілізована, але потребує “холодового ланцюга” - зберігання при температурі нижче 10ºC (50 ºF); ймовірно, збереже ефективність для коротких походів, що триватимуть кілька тижнів, але препарат слід утилізувати (та взяти новий) після тривалого перебування поза холодильником. Рекомендуємо зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги.
Побічні реакції: Висока ефективність і низька частота серйозних побічних реакцій на основі поточних публікацій.
Показання: Препарат прямо показаний для лікування гемотоксичного і цитотоксичного синдромів, спричинених укусом японської гадюки Habu (Protobothrops [Trimeresurus] flavoviridis)
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Однак загальна кількість реакцій (~11% загалом; ~25% сироваткова хвороба) вища, ніж для інших регіональних препаратів. Розгляньте доцільність претерапії у кожному конкретному випадку.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром = 1 - 2 флакони
- ЦИТОТОКСИЧНИЙ синдром = 1 - 2 флакони
Додаткове дозування: Можливе додаткове застосування по 1 флакону CSTRI-HABU на 2, 4, 6, 12 та 24 годинах.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Японія): CSTRI-MAMU
Chemo-Sero Therapeutic Research Institute, Японія - Препарат проти отрути японської гадюки Kaketsuken Mamushi (CSTRI-MAMU) (Ліофілізат/Потребує охолодження)231-235:
- Нестабільна в польових умовах. Не широкого спектра дії. Нейтралізує лише отруту японської гадюки Mamushi.
- Варіант лікування першої лінії для гемотоксичного і цитотоксичного синдромів, спричинених укусом японської гадюки Mamushi (Gloydius blomhoffii).
- Початкова доза = 1-2 флакони, додаткові дози = 1 флакон за потреби
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Ліофілізована, проте потребує дотримання “холодового ланцюга” - зберігання при температурі нижче 10ºC (50 ºF); ймовірно, збереже ефективність для коротких польових походів, що триватимуть кілька тижнів, але препарат слід утилізувати (та замінити на новий) після тривалого його перебування поза холодильником. Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги.
Побічні реакції: Висока ефективність і низька частота серйозних побічних реакцій на основі поточних публікацій.
Показання: Препарат безпосередньо показаний для лікування гемотоксичного та цитотоксичного синдромів, спричинених укусами японської гадюки Mamushi (Gloydius blomhoffii).
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром = 1 - 2 флакони
- ЦИТОТОКСИЧНИЙ синдром = 1 - 2 флакони
Додаткове дозування: Можливе додаткове застосування по 1 флакону CSTRI-MAMU на 2, 4, 6, 12 та 24 годинах.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Японія/ Китай/Північна Корея/В’єтнам/Східна Росія): JSI-AYA
Японський інститут змій, Японія - Препарат проти отрути тигрового вужа/кільбека/ (Yamakagashi) (JSI-AYA) (Ліофілізат/Потребує охолодження)231-233:
- Нестабільна в польових умовах. Не широкого спектра дії. Нейтралізує лише отруту кільбека азійського.
- Варіант лікування першої лінії для гемотоксичного та цитотоксичного синдромів, спричинених тигровим кільбеком (Rhabdophis tigrinus) та іншими видами східноазійського кільбека.
- Початкова доза = 1-2 флакони, додаткові дози = 1 флакон за потреби
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Ліофілізована, але потребує дотримання “холодового ланцюга” - зберігання при температурі нижче 10ºC (50 ºF); ймовірно, збереже ефективність для коротких польових походів, що триватимуть кілька тижнів, але препарат слід утилізувати (та замінити на новий) після тривалого перебування поза холодильником. Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги.
Побічні реакції: Висока ефективність і низька частота серйозних побічних реакцій на основі поточних публікацій.
Показання: Препарат безпосередньо показаний для лікування гемотоксичного та цитотоксичного синдромів, спричинених тигровим кільбеком (Rhabdophis tigrinus) та іншими східноазійськими кільбеками.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром = 1 - 2 флакони
- ЦИТОТОКСИЧНИЙ синдром = 1 - 2 флакони
Додаткове дозування: Можливе додаткове застосування по 1 флакону JSI-AYA на 2, 4, 6, 12 та 24 годинах, якщо це необхідно.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Північна Корея/Південна Корея/Східний Китай): KOVAX-AKA
Korea Vaccine, Корея - Препарат проти отрути щитомордників (Agkistrodon/Mamushi) (KOVAX-AKA) (Ліофілізат/Потребує охолодження)234–240:
- Нестабільна в польових умовах. Не має широкого спектра дії. Охоплює лише корейський вид змії Mamushi.
- Варіант першої лінії для лікування гемотоксичного та цитотоксичного синдромів отруєння, спричинених основними видами змій Mamushi на Корейському півострові (Gloydius brevicaudus, G. ussuriensis, G. intermedius). Може нейтралізувати отруту інших споріднених видів.
- Початкова доза = 1 – 2 флакони, додаткові дози = 1 флакон за потреби.
Можливість застосування в непристосованих умовах: Не рекомендована для використання в польових умовах. Ліофілізована, але вимагає дотримання “холодового ланцюга” - зберігання при температурі нижче 10ºC (50 ºF); ймовірно, збереже ефективність при коротких польових походах (кілька тижнів), але препарат слід утилізувати (та замінити на новий) після тривалого перебування його поза холодильником. Рекомендовано зберігати невеликий запас на стратегічно розташованих об’єктах другого та третього етапів медичної допомоги.
Побічні реакції: Висока ефективність і низька частота тяжких побічних реакцій на основі поточних публікацій.
Показання: Безпосередньо показаний для лікування гемотоксичного та цитотоксичного синдромів отруєння, спричинених основними видами змій Mamushi на Корейському півострові (Gloydius brevicaudus, G. ussuriensis, G. intermedius). Може нейтралізувати інші споріднені види.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром = 1 - 2 флакони
- ЦИТОТОКСИЧНИЙ синдром = 1 - 2 флакони
Додаткове дозування: Можливе додаткове застосування по 1 флакону KOVAX-AKA на 2, 4, 6, 12 та 24 годині, якщо це необхідно.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Тайвань/ Південно-Східний Китай/Лаос/ Півн. В’єтнам): NIPM-SNV
Національний інститут превентивної медицини, Тайвань - Моновалентна сироватка проти отрути гостромордої гадюки Deinagkistrodon acutus (NIPM-SNV) (Ліофілізат/Потребує охолодження)223,235–240:
- Ліофілізований препарат, який потребує дотримання “холодового ланцюга”, але, ймовірно, буде стабільним під час короткого періоду перебування в польових умовах. Не має широкого спектра дії. Нейтралізує лише отруту гостромордої гадюки.
- Моновалентна протиотрута першої лінії, яка безпосередньо показана для лікування гемотоксичного та цитотоксичного синдромів отруєння, спричинених гостромордою гадюкою (Deinagkistrodon acutus).
- Початкова доза = 2 флакони, додаткові дози = 1 флакон за потреби.
Можливість застосування в непристосованих умовах: Умовно рекомендована для використання під час коротких польових походів. Ліофілізована, але вимагає дотримання “холодового ланцюга” при температурі нижче 10ºC (50 ºF); однак тестування, проведене тайванським CDC, не показало втрати ефективності після 30 днів інкубації при 35º C / 95º F, а також протягом 4 місяців після повернення в холодильну камеру. Рекомендовано брати з собою повну дозу при тривалих бойових операціях у непристосованих умовах і зберігати більший запас у стратегічно розташованих закладах другого та третього етапів.
Побічні реакції: Висока ефективність і низька частота важких побічних реакцій на основі поточних публікацій.
Показання: Моновалентна протиотрута, яка безпосередньо показана для лікування гемотоксичного та цитотоксичного синдромів отруєння, спричиненого Deinagkistrodon acutus.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ДЛЯ НЕЙРОТОКСИЧНОГО синдрому
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 2 флакони
- ЦИТОТОКСИЧНИЙ синдром: початкова доза = 2 флакони
Додаткове дозування: Можливе додаткове застосування по 1 флакону NIPM-SNV на 2, 4, 6, 12 та 24 годині, якщо це необхідно.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Лише для морських середовищ): CSL-SS
Commonwealth Serum Laboratories, Австралія - Препарат проти отрути морських змій (CSL-SS) (Рідка/Потребує охолодження)231-245:
- Нестабільна у польових умовах. Широкий спектр дії лише проти індо-тихоокеанських морських змій.
- Використовується в INDOPACOM при нейротоксичному синдромі отруєння внаслідок укусу морських змій або невідомих видів, що зустрічаються виключно в морському середовищі.
- Початкова доза = 3 флакони, додаткові дози = 1 флакон за потреби.
Можливість застосування в непристосованих умовах: Не рекомендована для використання в бойових умовах. Вимагає дотримання “холодового ланцюга” - зберігання при температурі 2–8 ºC (35,6–46,4 ºF). Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги. Ймовірно, протиотрута збереже ефективність протягом кількох тижнів у польових умовах, але її слід утилізувати після закінчення цього періоду часу поза холодильником.
Побічні реакції: Високоякісний продукт з низьким рівнем очікуваних реакцій.
Показання: Цей полівалентний препарат можна використовувати для лікування нейротоксичних отруєнь при укусах більшості основних видів морських змій в Австралії.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром: початкова доза = 3 флакони
- НЕ ПОКАЗАНИЙ при гемотоксичних отруєннях
- НЕ ПОКАЗАНИЙ при цитотоксичних отруєннях
Додаткове дозування: Можливе додаткове застосування по 1 флакону CSL-SS на 2, 4, 6, 12 і 24 годинах, якщо необхідно.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (INDOPACOM - Лише для островів Малуку/ Західної Папуа Нової Гвінеї): CSL-P
Commonwealth Serum Laboratories, Австралія - Полівалентна протиотрута (CSL-P) (Рідка/Потребує охолодження)61, 241, 245-248:
- Нестабільна в польових умовах. Широкий спектр охоплення.
- Протиотрута першої лінії в INDOPACOM при нейротоксичному/гемотоксичному отруєнні внаслідок укусів австралійських вужів або невідомих видів, що зустрічаються на схід від лінії Уоллеса.
- Початкова доза = 3 флакони, додаткові дози = 1 флакон за потреби
Можливість застосування в непристосованих умовах: Не рекомендована для використання в бойових умовах. Вимагає дотримання “ холодового ланцюга” - зберігання при температурі 2–8 ºC (35,6–46,4 ºF). Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги. Ймовірно, протиотрута збереже ефективність протягом кількох тижнів у польових умовах, але її слід утилізувати (та замінити на нову) після закінчення цього періоду часу поза холодильником.
Побічні реакції: Високоякісний продукт з низьким рівнем очікуваних реакцій.
Показання: Цей полівалентний засіб можна використовувати для лікування нейротоксичних отруєнь при укусах найбільш значущих з медичної точки зору видів австралійських вужів, які мешкають на схід від лінії Уоллеса.
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром: початкова доза = 3 флакони
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 3 флакони
- НЕ ПОКАЗАНИЙ ПРИ ЦИТОТОКСИЧНИХ ОТРУЄННЯХ
Додаткове дозування: Можливе додаткове застосування по 1 флакону CSL-P на 2, 4, 6, 12 і 24 годинах, якщо це необхідно.
Попереднє лікування: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
NORTHCOM
Північне Командування Збройних сил США
Настанови з лікування
У цій зоні відповідальності доступні безпечні протиотрути, ефективні при всіх нейро/гемо/цитотоксичних отруєннях внаслідок укусу ямкоголових/гримучникових гадюк та при нейротоксичних отруєннях внаслідок укусу коралових аспідів. Лікування не вимагає ідентифікації виду. У зоні NORTHCOM лікування зміїного укусу на місці події зазвичай не рекомендоване.
Для всіх протиотрут ЗВ NORTHCOM: читайте листок-вкладку (інструкцію до препарату), щоб отримати конкретні вказівки щодо використання згідно з правилами FDA для схвалених у США продуктів. Також див. Уніфікований алгоритм лікування укусу гримучникової змії в Сполучених Штатах Америки (Unified treatment algorithm for the management of crotaline snakebite in the United States, Lavonas et al. 2011), щоб отримати рекомендації щодо дозування та лікування отруєння внаслідок укусу гримучникової гадюки.101 У даному розділі наведено особливості використання протиотрут у цьому регіоні.
Лікування побічних реакцій
- У разі виникнення реакції легкого чи помірного ступеня зменшіть швидкість інфузії та проведіть симптоматичне лікування антигістамінними препаратами, стероїдами та/або протиблювотними препаратами за необхідності.
- У разі виникнення тяжкої реакції, наприклад, анафілаксії, припиніть інфузію та проведіть лікування згідно з протоколом лікування анафілаксії, наведеним у даних настановах. Повторно оцініть стан пацієнта після зникнення проявів реакції та відновіть інфузію з нижчою швидкістю, якщо не усунутий повністю будь-який зі специфічних симптомів-критеріїв для застосування протиотрути, наведених в інших розділах настанов.
Протокол лікування гострої судинної недостатності (колапсу)
У пацієнта протягом 30 хвилин після укусу швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта за допомогою ВМ або ВВ введення адреналіну та розчинів для інфузії відповідно до протоколів лікування анафілаксії.
- Виконайте інтубацію трахеї при набряку дихальних шляхів, якщо відсутня швидка реакція на застосування адреналіну.
- Після введення адреналіну негайно ВВ або ВК болюсно введіть високу дозу відповідної регіональної протиотрути, продовжуючи заходи ресусцитації.
- Підтримуйте артеріальний тиск за допомогою ВВ або ВК введення розчинів та адреналіну, доки гемодинаміка не стабілізується завдяки дії протиотрути.
Для отримання додаткової інформації див. розділ «Гостра судинна недостатність (колапс)».
Контакти
Для екстрених телемедичних консультацій телефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
Таблиця 8. NORTHCOM - протиотрути першої лінії
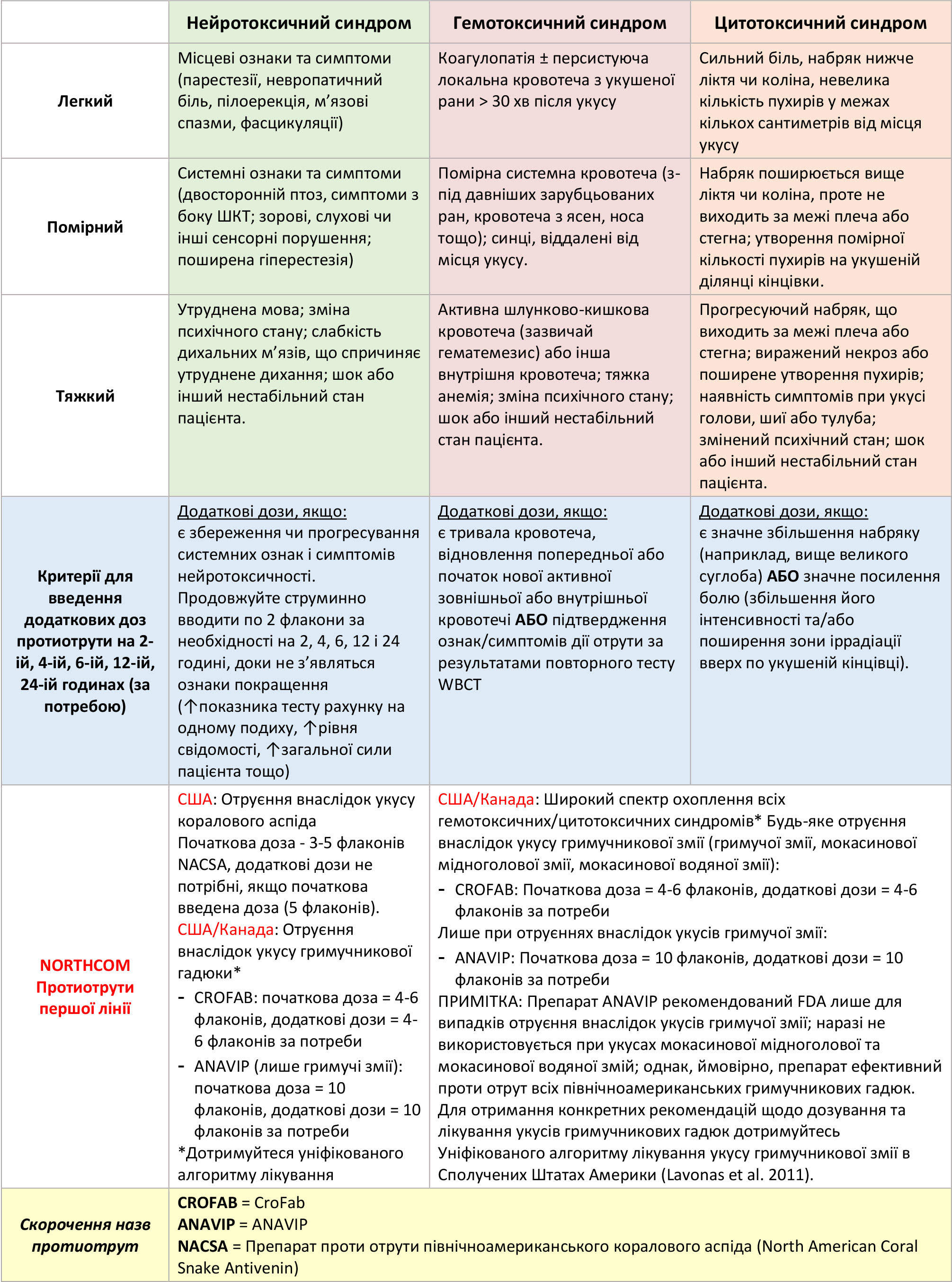
Малюнок 6. Алгоритм введення протиотрути: зона відповідальності NORTHCOM
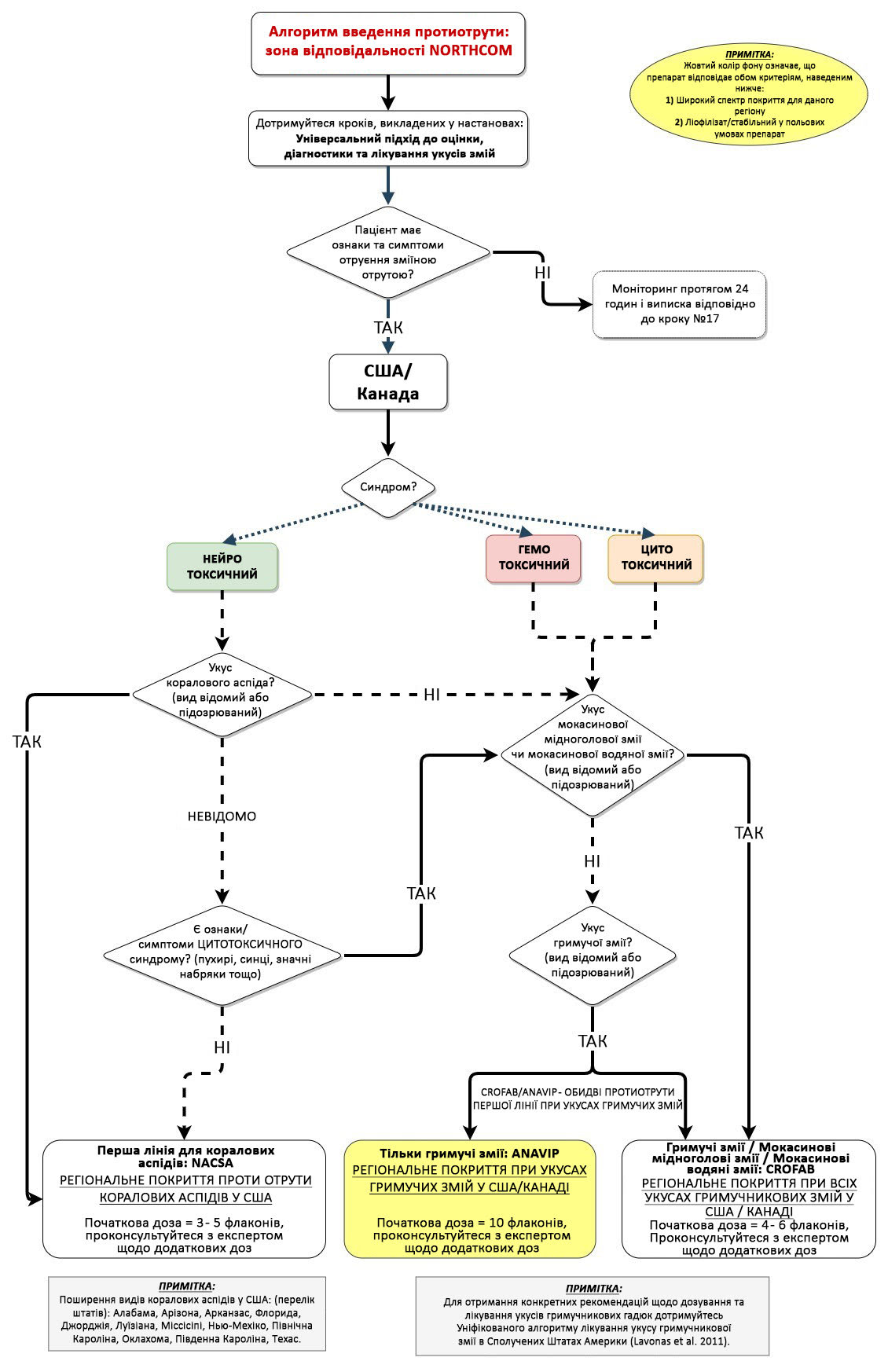
BTG Therapeutics, США – CroFab
(Ліофілізат/Потребує охолодження) 94,95,101,249-250:
- Показання: Отруєння внаслідок укусу всіх видів гримучникових змій (гримучої змії, мокасинової мідноголової змії, мокасинової водяної змії) у Північній Америці. Ліофілізована; потребує зберігання в холоді; одне дослідження показало, що вона зберігає ефективність у польових умовах протягом ≥ 90 днів, якщо це необхідно.
- Початкове дозування: 4 – 6 флаконів
RDT/Instituto Bioclon, США/Мексика – ANAVIP
(Ліофілізат/Не потребує охолодження)92:
- Показання: На даний момент FDA рекомендує препарат лише при отруєнні внаслідок укусу гримучої змії.
- Наразі не показана при отруєнні внаслідок укусів мокасинової мідноголової та мокасинової водяної змій, хоча це може змінитися найближчим часом залежно від результатів досліджень. Ліофілізована і стабільна у польових умовах при температурі 25º C / 77º F.
- Початкове дозування: 10 флаконів
Pfizer, США – Препарат проти отрути північноамериканського коралового аспіда (North American Coral Snake Antivenin) (NACSA)
(Ліофілізат/Потребує охолодження)251:
- Показання: При нейротоксичному синдромі внаслідок укусу північноамериканських коралових аспідів (NACSA) на території Сполучених Штатів, включаючи східного коралового (арлекінового) аспіда (Micrurus fulvius) і техаського коралового аспіда (Micrurus tener). Зберігати при температурі від 2 до 8 ºC / 35,6 - 46,4 ºF; однак, ймовірно, препарат зберігає стабільність під час коротких періодів перебування у польових умовах.
- Початкове дозування: 5 флаконів
SOUTHCOM
Південне Командування Збройних сил США
Настанови з лікування
У цій зоні відповідальності доступні безпечні протиотрути, ефективні при всіх гемо/ цитотоксичних отруєннях внаслідок укусу ямкоголових/гримучникових гадюк та нейротоксичних отруєнь внаслідок укусу коралових аспідів. Лікування не вимагає ідентифікації виду, що спричинив отруєння, але вимагає виявлення синдрому. Для SOUTHCOM рекомендовано проводити лікування укусу змії одразу на місці його отримання. У цьому розділі надана детальна інформація про використання протиотрут у цьому регіоні.
Лікування побічних реакцій
- У разі виникнення реакції легкого чи помірного ступеня зменшіть швидкість інфузії та проведіть симптоматичне лікування антигістамінними препаратами, стероїдами та/або протиблювотними препаратами за необхідності.
- У разі виникнення тяжкої реакції, наприклад, анафілаксії, припиніть інфузію та проведіть лікування згідно з протоколом лікування анафілаксії, наведеним у даних настановах. Повторно оцініть стан пацієнта після зникнення проявів реакції та відновіть інфузію з нижчою швидкістю, якщо не усунутий повністю будь-який зі специфічних симптомів-критеріїв для застосування протиотрути, наведених в інших розділах настанов.
Протокол лікування гострої судинної недостатності (колапсу)
У пацієнта протягом 30 хвилин після укусу швидко розвивається шок ± ангіоневротичний набряк, зміна психічного стану, системна кровотеча та діарея.1
- Стабілізуйте стан пацієнта за допомогою ВМ або ВВ введення адреналіну та розчинів для інфузії відповідно до протоколів лікування анафілаксії.
- Виконайте інтубацію трахеї при набряку дихальних шляхів, якщо відсутня швидка реакція на застосування адреналіну.
- Після введення адреналіну негайно ВВ або ВК болюсно введіть високу дозу відповідної регіональної протиотрути, продовжуючи заходи ресусцитації.
- Підтримуйте артеріальний тиск за допомогою ВВ або ВК введення розчинів та адреналіну, доки гемодинаміка не стабілізується завдяки дії протиотрути.
Для отримання додаткової інформації див. розділ «Гостра судинна недостатність (колапс)».
Контакти
Для екстрених телемедичних консультацій телефонуйте на гарячу лінію ADVISOR (866-972-9966) і виберіть у меню телефону пункт «Токсикологія».
Для отримання додаткової інформації про лікування укусів змій або про ці Настанови з клінічної практики пишіть на електронну пошту jordan@snakebitefoundation.org або телефонуйте за номером 415-218-2211.
Таблиця 9. SOUTHCOM - протиотрути першої лінії
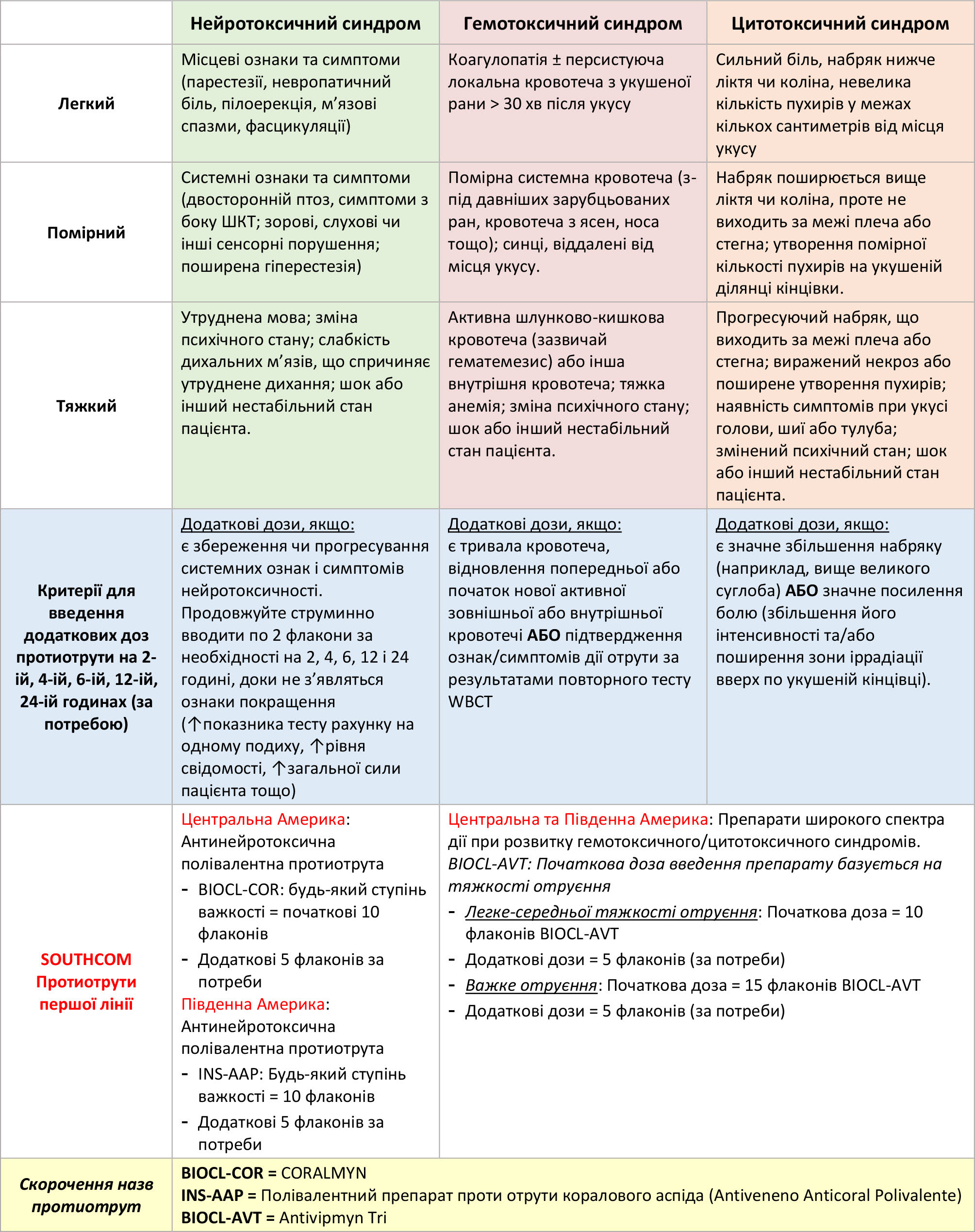
Малюнок 7. Алгоритм введення протиотрути: зона відповідальності SOUTHCOM
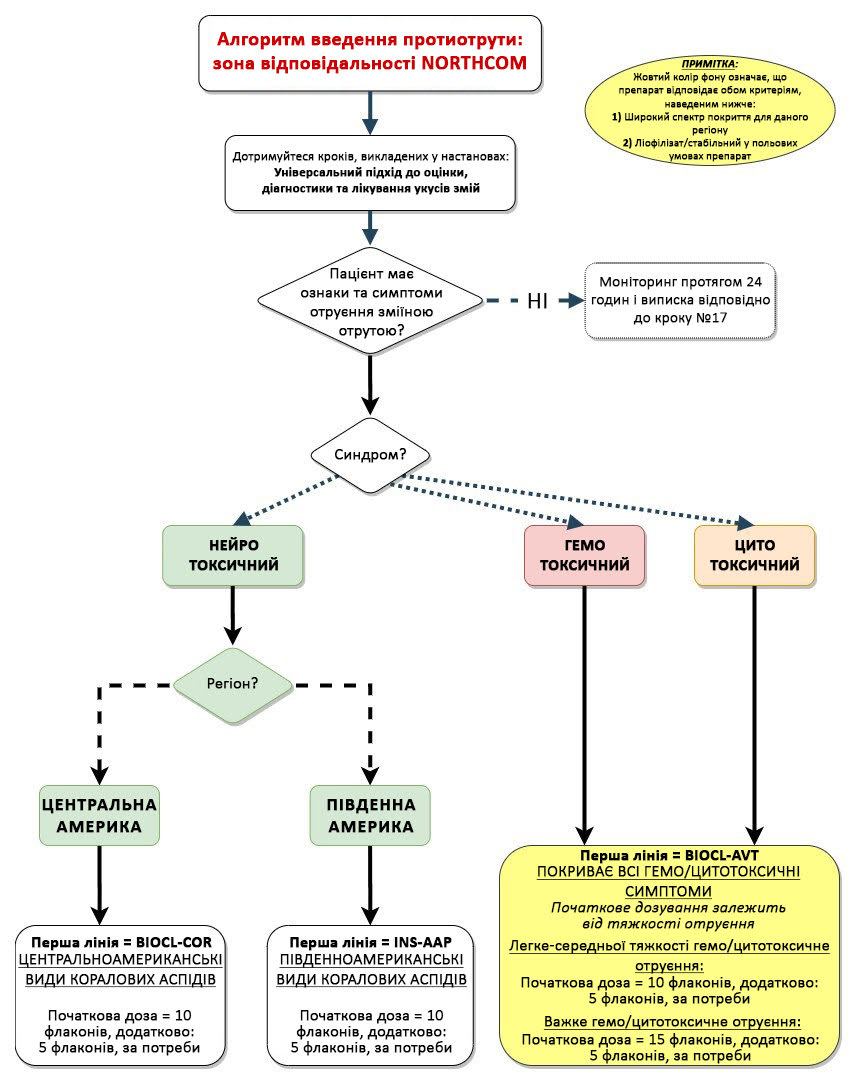
Протиотрута першої лінії (Уся зона відповідальності SOUTHCOM): BIOCL-AVT
Instituto Bioclon, Мексика - ANTIVIPMYN-TRI (BIOCL-AVT) (Ліофілізат/Не потребує охолодження) 251-255:
- Стабільна в польових умовах. Широкий спектр дії, охоплює 14 видів гемо/цитотоксичних змій.
- Варіант лікування першої лінії при всіх гемотоксичних і цитотоксичних отруєннях внаслідок укусів змій у будь-якій точці ЗВ SOUTHCOM, коли вид або невідомий, або входить в число ≥ 14 змій, для яких безпосередньо показаний цей препарат. Прямо чи опосередковано поширюється на більшість змій категорії 1 та 2 за ВООЗ у цьому регіоні.
- Початкова доза = 10 флаконів, лише при гемотоксичному/цитотоксичному синдромах, додаткові дози = 5 флаконів за необхідності.
Можливість застосування в непристосованих умовах: Рекомендована для використання у бойових умовах. Не потребує охолодження, зберігати при температурі менше 37 С. Ліофілізований препарат, який, найбільш ймовірно, зберігає стабільність і при вищих температурах (для коротких походів). Рекомендовано брати з собою на поле бою повну або навантажувальну дозу (≥ 5 флаконів) на час тривалих бойових операцій у непристосованих умовах і зберігати більшу кількість у стратегічно розташованих закладах другого та третього етапів медичної допомоги ЗВ SOUTHCOM.
Побічні реакції: Високоякісний продукт з очікуваною низькою частотою побічних реакцій.
Показання: Цей полівалентний засіб широкого спектра дії може бути використаний для лікування гемотоксичних та цитотоксичних отруєнь внаслідок укусів більш ніж 14 різних видів центрально- та південноамериканських змій. Може нейтралізувати отруту інших видів шляхом параспецифічної нейтралізації, але це офіційно не визначено. Для видів змій, перелічених нижче, є офіційні показання щодо лікування, рекомендовані виробником:
- ГЕМОТОКСИЧНИЙ та / або ЦИТОТОКСИЧНИЙ ефект: Crotalus durissis terrificus; Bothrops asper, B. atrox, B. neuwiedii, B. alternatus, B. jararacussu, B. venezulensis, B. pictus, B. brazili; Lachesis muta muta, L. m. stenophyrs; Sistrurus spp.; Agkistrodon spp.
Претерапія: Зазвичай не проводиться, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування.
Початкове дозування відповідно до синдрому:
- НЕ ПОКАЗАНИЙ ПРИ НЕЙРОТОКСИЧНОМУ синдромі
- ГЕМОТОКСИЧНИЙ синдром: початкова доза = 10 флаконів
- ЦИТОТОКСИЧНИЙ синдром: початкова доза = 10 флаконів
Додаткове дозування: Можливе додаткове застосування по 5 флаконів BIOCL-AVT на 2, 4, 6, 12 і 24 годинах, якщо це необхідно.
Претерапія: Зазвичай не проводиться, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Підготовка та введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (SOUTHCOM - Центральна/Південна Америка): BIOCL-COR
Протиотрута другої лінії (SOUTHCOM - Південна Америка): BIOCL-COR
Instituto Bioclon, Мексика - CORALMYN (BIOCL-COR) (Рідка / Потребує охолодження) 256-262:
- Нестабільна в польових умовах. Широкого спектра дії при нейротоксичному отруєнні внаслідок укусу змій в Центральній Америці.
- Варіант лікування першої лінії при нейротоксичному отруєнні внаслідок укусу коралових аспідів або невідомих видів змій у Центральній Америці (коралові аспіди є єдиними зміями в ЗВ SOUTHCOM, отрута яких є винятково нейротоксичною). Варіант лікування другої лінії при отруєнні внаслідок укусу коралового аспіда або нейротоксичного отруєння внаслідок невідомого виду змії в Південній Америці, якщо перша лінія (INS-AAP) недоступна.
- Початкова доза = 10 флаконів, тільки при нейротоксичному синдромі; додаткові дози = 5 флаконів, за потреби.
Перша лінія (SOUTHCOM – Центральна Америка): Нейротоксичне отруєння внаслідок укусу коралових аспідів або невідомих видів змій у Центральній Америці (коралові аспіди є єдиними зміями в ЗВ SOUTHCOM, отрута яких є винятково нейротоксичною).
Друга лінія (SOUTHCOM-Південна Америка): Може нейтралізувати отруту деяких коралових аспідів у Південній Америці, але має значні прогалини в охопленні цього регіону, в порівнянні з першою лінією для Південної Америки (INS-AAP).
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Потребує дотримання “холодового ланцюга” - зберігання при температурі 2–8 ºC (35,6–46,4 ºF). Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги в Південній Америці. Ймовірно, збереже ефективність для коротких (кілька тижнів) польових операцій, але препарат слід утилізувати після тривалого зберігання поза холодильником.
Побічні реакції: Високоякісний продукт з очікуваною низькою частотою побічних реакцій.
Показання: Цей полівалентний засіб може бути використаний для лікування нейротоксичних отруєнь, спричинених укусами більшості видів центральноамериканських коралових аспідів роду Micrurus.
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: центральноамериканські коралові аспіди (рід Micrurus)
Початкове дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром: початкова доза = 10 флаконів
- НЕ ПОКАЗАНИЙ при ГЕМОТОКСИЧНОМУ синдромі
- НЕ ПОКАЗАНИЙ при ЦИТОТОКСИЧНОМУ синдромі
Додаткове дозування: Можливе додаткове застосування по 5 флаконів BIOCL-COR на 2, 4, 6, 12 і 24 годинах.
Претерапія: Зазвичай не призначається, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Підготовка і введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Протиотрута першої лінії (SOUTHCOM - Південна Америка): INS-AAP
Протиотрута другої лінії (SOUTHCOM - Центральна Америка): INS-AAP
Національний інститут охорони здоров'я, Колумбія – Полівалентний препарат проти отрути коралового аспіда / Antiveneno Anticoral Polivalente (INS-AAP) (Рідка / Потребує охолодження) 260-2:
- Нестабільна в польових умовах. Широкого спектра дії при нейротоксичному отруєнні на території Південної Америки.
- Варіант лікування першої лінії при нейротоксичному отруєнні внаслідок укусу коралових аспідів або невідомих видів змій у Південній Америці (коралові аспіди є єдиними зміями в ЗВ SOUTHCOM, отрута яких є винятково нейротоксичною). Варіант лікування другої лінії при отруєнні внаслідок укусу коралового аспіда або нейротоксичного отруєння внаслідок невідомого виду змії в Центральній Америці, якщо перша лінія (INS-AAP) недоступна.
- Початкова доза = 10 флаконів, тільки при нейротоксичному синдромі; додаткові дози = 5 флаконів за потреби.
Перша лінія (SOUTHCOM - Південна Америка): Найбільша ефективність проти нейротоксичних укусів коралових аспідів або невідомих видів змій у Південній Америці. Коралові аспіди - єдиний виключно нейротоксичний вид у ЗВ SOUTHCOM.
Друга лінія (SOUTHCOM - Центральна Америка): Очікується охоплення більшості видів коралових аспідів у Центральній Америці, але існують прогалини в порівнянні з першою лінією для Центральної Америки (BIOCL-COR).
Можливість застосування в непристосованих умовах: Не рекомендована для використання у бойових умовах. Рідка, потребує дотримання “холодового ланцюга” - зберігання при температурі 4–8 ºC (39.2 - 46.4 ºF). Рекомендовано зберігати невеликий запас (кілька флаконів) у стратегічно розташованих закладах другого та третього етапів медичної допомоги в Південній Америці. Ймовірно, збереже ефективність для коротких (кілька тижнів) польових операцій, але препарат слід утилізувати після тривалого зберігання поза холодильником.
Побічні реакції: Високоякісний продукт з очікуваною низькою частотою реакцій.
Показання: Цей полівалентний засіб може бути використаний для лікування нейротоксичних отруєнь внаслідок укусів більшості видів південноамериканських коралових аспідів роду Micrurus, а також деяких центральноамериканських видів змій.
- НЕЙРОТОКСИЧНИЙ ЕФЕКТ: південноамериканські коралові аспіди (Micrurus spp.), включно з Micrurus dumerilii, M. mipartitus, M. surinamensis, M. isozonus, M. lemniscatus, M. spixi, M. Medemi.
Початкова дозування відповідно до синдрому:
- НЕЙРОТОКСИЧНИЙ синдром: початкова доза = 10 флаконів
- НЕ ПОКАЗАНИЙ при ГЕМОТОКСИЧНОМУ синдромі
- НЕ ПОКАЗАНИЙ при ЦИТОТОКСИЧНОМУ синдромі
Додаткове дозування: Можливе додаткове застосування по 5 флаконів INS-AAP на, 4, 6, 12 і 24 годинах, за потреби.
Претерапія: Зазвичай не проводиться, крім випадків нестабільного стану пацієнта, наявності астми/атопічних захворювань, відомої гіперчутливості чи інших критеріїв для попереднього лікування. Низький ризик розвитку тяжких алергічних реакцій та інших ранніх побічних реакцій.
Підготовка і введення: Розведіть всю дозу протиотрути в одному пакеті ізотонічного розчину об’ємом 250–500 мл і введіть шляхом внутрішньовенної інфузії протягом 10–30 хвилин.
Моніторинг покращення ефективності (ПЕ)
Досліджувана група
Усі пацієнти, що постраждали від укусу змій.
Мета (очікувані результати)
- Лікування всіх пацієнтів з укусами змій повинно здійснюватися відповідно до кроків, викладених у розділі "Універсальний підхід до оцінки, діагностики та лікування укусів змій".
- Оцінка, діагностика та лікування пацієнтів із укусами змій повинні базуватися на клінічному синдромі отруєння, а не на ідентифікації виду змій, що спричинили укус.
- Якщо для лікування даного синдрому в даній місцевості не існує протиотрути широкого спектра дії, виконайте кроки, описані в регіональних алгоритмах, щоб визначити найбільш відповідну протиотруту для пацієнта.
- Отруєння внаслідок укусу змії - це динамічний процес; пацієнтів слід часто повторно оглядати протягом усього курсу лікування щодо наявності ознак нейротоксичного, гемотоксичного і цитотоксичного синдромів, оскільки деякі синдроми будуть розвиватися швидше, ніж інші.
- Абсолютних протипоказань до застосування протиотрути у пацієнта з симптоматичним отруєнням внаслідок укусу змії немає.
- Введення протиотрути повинно виконуватися медичними працівниками, здатними забезпечити розширену підтримку життєдіяльності, і які пройшли підготовку на мінімальному рівні парамедика (або еквівалентний рівень у Міністерстві оборони) і вище (тобто SOCM, 18D, PJ, IDC, IDMT, RN, PA, MD чи DO, тощо).
- Раннє введення протиотрути є стандартом лікування отруєнь внаслідок укусу змій у всьому світі. Якщо можливо, відповідну протиотруту слід вводити на місці отримання укусу до проведення медичної евакуації, щоб нейтралізувати циркулюючу отруту до того, як відбудеться значна та потенційно незворотна шкода.
- У ці настанови з клінічної практики включені стійкі в польових умовах протиотрути широкого спектра дії для всіх бойових командувань, за винятком EUCOM.
- Відповідні регіональні препарати, перелічені в настановах, повинні зберігатися в медичних установах другого та третього етапів медичної допомоги. Передові підрозділи, в яких працюють парамедики, повинні бути оснащені стійкими в польових умовах протиотрутами широкого спектра дії, які можна зберігати в пункті надання медичної допомоги, а також носити з собою на полі бою протягом тривалого часу при високих температурах без втрати ефективності.
- Якщо протиотрута недоступна, пацієнта слід перевести в лікувальний заклад, де є запас відповідного препарату. Перед транспортуванням пацієнта переконайтеся, що лікарня, яка його приймає, має потрібну протиотруту. Якщо потрібного препарату там немає, то слід перевести пацієнта в той лікувальний заклад, де протиотрута є.
- Дозування, підготовка та введення протиотрути проводиться відповідно до вказівок для кожного конкретного препарату.
- При необхідності перед випискою слід провести профілактику проти правця.
- При укусі змії фасціотомія протипоказана; у всіх випадках підозри на компартмент-синдром його слід лікувати додатковими дозами протиотрути і підвищеним положенням (вище 60 градусів) укушеної кінцівки для зниження онкотичного тиску.
- Зверніться за телемедичною консультацією до кваліфікованого експерта з укусів змій щодо будь-яких питань, занепокоєнь або незвичайних проявів.
- Не намагайтеся вбити або зловити змію для ідентифікації, оскільки лікування базується на клінічних проявах. Якщо є фотографія змії, її можна відправити експерту для ідентифікації, але це не повинно затримувати введення протиотрути пацієнту з симптомами будь-якого синдрому отруєння.
Показники результативності/Дотримання рекомендацій
- Введення протиотрути усім пацієнтам з клінічними ознаками та симптомами нейротоксичного, гемотоксичного або цитотоксичного синдромів.
- Раннє введення відповідних протиотрут симптоматичним пацієнтам в польових умовах.
- Швидке транспортування пацієнтів до закладу, забезпеченого відповідною протиотрутою, якщо її немає на місці.
- Введення протиотрути повинно виконуватися кваліфікованим фахівцем з навичками ALS (Advanced Life Support - Розширена підтримка життя), який має підготовку на рівні парамедика (чи еквівалентного рівня в Міністерстві оборони США) або вище.
- Профілактика правця за потреби.
- Зниження підвищеного тиску при компартмент-синдромі за допомогою протиотрути, не виконуючи фасціотомію.
Джерела даних
- Медична картка пацієнта
- Реєстр травм Міністерства оборони (DoDTR)
Системна звітність та її частота
Згідно з даними настановами, вказане вище становить мінімальні критерії моніторингу ПЕ. Системна звітність проводитиметься щороку; додатковий моніторинг ПЕ та системну звітність можна проводити залежно від потреб.
Системний огляд та аналіз даних виконуватиме керівник JTS та відділ ПЕ JTS
Обов’язки
Керівник команди з надання допомоги при травмах відповідає за ознайомлення з даними Настановами з клінічної практики, належне дотримання вказаних у ній вимог та моніторинг ПЕ на місцевому рівні.
-
- Benjamin JM, Abo BN, Brandehoff N. Review Article: Snake Envenomation in Africa. Current Tropical Medicine Reports. January 2020. doi:10.1007/s40475-020-00198-y
- Chippaux J-P. Snakebite envenomation turns again into a neglected tropical disease! J Venom Anim Toxins Incl Trop Dis. 2017;23:38. doi:10.1186/s40409-017-0127-6
- Chippaux J-P. Incidence and mortality due to snakebite in the Americas. PLoS Negl Trop Dis. 2017;11(6):e0005662. doi:10.1371/journal.pntd.0005662
- Chippaux J-P. Estimate of the burden of snakebites in sub-Saharan Africa: a meta-analytic approach. Toxicon. 2011;57(4):586-599. doi:10.1016/j.toxicon.2010.12.022
- Kasturiratne A, Wickremasinghe AR, de Silva N, et al. The global burden of snakebite: a literature analysis and modelling based on regional estimates of envenoming and deaths. PLoS Med. 2008;5(11):e218. doi:10.1371/journal.pmed.0050218
- Mohapatra B, Warrell DA, Suraweera W, et al. Snakebite mortality in India: a nationally representative mortality survey. PLoS Negl Trop Dis. 2011;5(4):e1018. doi:10.1371/journal.pntd.0001018
- Gutiérrez JM, Calvete JJ, Habib AG, Harrison RA, Williams DJ, Warrell DA. Snakebite envenoming. Nat Rev Dis Primers. 2017;3:17063. doi:10.1038/nrdp.2017.63
- Habib AG, Kuznik A, Hamza M, et al. Snakebite is Under Appreciated: Appraisal of Burden from West Africa. PLoS Negl Trop Dis. 2015;9(9):e0004088. doi:10.1371/journal.pntd.0004088
- Longbottom J, Shearer FM, Devine M, et al. Vulnerability to snakebite envenoming: a global mapping of hotspots. Lancet. 2018;392(10148):673-684. doi:10.1016/S0140-6736(18)31224-8
- Williams DJ, Faiz MA, Abela-Ridder B, et al. Strategy for a globally coordinated response to a priority neglected tropical disease: Snakebite envenoming. PLoS Negl Trop Dis. 2019;13(2):e0007059. doi:10.1371/journal.pntd.0007059
- Lial JP. [Health assessments of a military company stationed on the Maroni River in French Guiana]. Med Trop . 1999;59(1):95-98. https://www.ncbi.nlm.nih.gov/pubmed/10472589.
- Lynch JH, Verlo AR, Givens ML, Munoz CE. Bites, stings, and rigors: clinical considerations in African operations. J Spec Oper Med. 2014;14(4):113-121. https://www.ncbi.nlm.nih.gov/pubmed/25399379.
- Kairi JK, Lal V, Ghate JV, Nayak BB, Kotabagi RB. Poisoning and envenomation registry: analysis of 200 case reports. Armed Forces Med J India. 2011;67(2):131-137. doi:10.1016/S0377-1237(11)60011-7
- Maddry JK, Sessions D, Heard K, Lappan C, McManus J, Bebarta VS. Wartime toxicology: evaluation of a military medical toxicology telemedicine consults service to assist physicians serving overseas and in combat (2005-2012). J Med Toxicol. 2014;10(3):261-265. doi:10.1007/s13181-014-0398-z
- Ellis BC, Brown SGA. Management of anaphylaxis in an austere or operational environment. J Spec Oper Med. 2014;14(4):1-5. https://www.ncbi.nlm.nih.gov/pubmed/25399361.
- Pearn JH. Bee stings in operational theatres. Mil Med. 1972;137(6):241-242. https://www.ncbi.nlm.nih.gov/pubmed/4625675.
- Heiner JD, Bebarta VS, Varney SM, Bothwell JD, Cronin AJ. Clinical effects and antivenom use for snake bite victims treated at three U.S. hospitals in Afghanistan. Wilderness Environ Med. 2013;24(4):412-416. doi:10.1016/j.wem.2013.05.001
- Haviv J, Huerta M, Shpilberg O, Klement E, Ash N, Grotto I. Poisonous animal bites in the Israel Defense Forces. Public Health Rev. 1998;26(3):237-245. https://www.ncbi.nlm.nih.gov/pubmed/10444961.
- Shiau DT, Sanders JW, Putnam SD, et al. Self-reported incidence of snake, spider, and scorpion encounters among deployed U.S. military in Iraq and Afghanistan. Mil Med. 2007;172(10):1099-1102. doi:10.7205/milmed.172.10.1099
- Wilkins D, Burns DS, Wilson D, et al. Snakebites in Africa and Europe: a military perspective and update for contemporary operations. J R Army Med Corps. 2018;164(5):370-379. doi:10.1136/jramc-2017-000883
- Cline CR, Goodnight ME. Pit viper envenomation in a military working dog. U.S. Army Med Dep J. January 2013:28-33. https://www.ncbi.nlm.nih.gov/pubmed/23277442.
- Murdock RT, White GL Jr, Pedersen DM, DeFaller JM, Snyder CC. Prevention and emergency field management of venomous snakebites during military exercises. Mil Med. 1990;155(12):587-590. https://www.ncbi.nlm.nih.gov/pubmed/2134840.
- Haviv J, Huerta M, Shpilberg O, et al. Field treatment of snakebites in the Israel Defense Forces. Public Health Rev. 1998;26(3):247-256.
- Pierson JF. Journal of Special Operations Medicine Volume. 2007;7:50-60. https://www.jsomonline.org/articles/0704/2007450Pierson.pdf.
- Hansen EA, Stein EA, Mader TH, Mazzoli RA. Spitting cobra ophthalmia in United Nations Forces in Somalia. Am J Ophthalmol. 1994;117(5):671. doi:10.1016/s0002-9394(14)70078-9
- Mehta SR, Sashindran VK. Clinical features and management of snake bite. Armed Forces Med J India. 2002;58(3):247-249. doi:10.1016/S0377-1237(02)80140-X
- Sagar A, Joshi DC. First reported case of African Viper bite treated with Indian Polyvalent Anti Snake Venom. Armed Forces Med J India. 2010;66(2):199-200. doi:10.1016/S0377-1237(10)80154-6
- Chauhan K, Nayar KR. An epidemiological study of snake bites in an area in the foothills of the north western Himalayas. Armed Forces Med J India. 1995;51(4):270-272. doi:10.1016/S0377-1237(17)30990-5
- Virmani SK. Cardiac involvement in snake bite. Armed Forces Med J India. 2002;58(2):156-157. doi:10.1016/S0377-1237(02)80054-5
- Chen C, Gui L, Kan T, Li S, Qiu C. A survey of snakebite knowledge among field forces in China. Int J Environ Res Public Health. 2016;14(1). doi:10.3390/ijerph14010015
- Flowers HH, Berlinger FG. The psychological importance of snakes to the combat soldier. Mil Med. 1973;138(3):144-145. https://www.ncbi.nlm.nih.gov/pubmed/4631483.
- Berlinger FG, Flowers HH. Some observations on the treatment of snakebites in Vietnam. Mil Med. 1973;138(3):139-143. doi:10.1093/milmed/138.3.139
- Heap BJ, Cowan GO. The epidemiology of snake bite presenting to British Military Hospital Dharan during 1989. J R Army Med Corps. 1991;137(3):123-125. doi:10.1136/jramc-137-03-03
- Roszko PJD, Kavanaugh MJ, Boese ML, Longwell JJ, Earley AS. Rotational thromboelastometry (ROTEM) guided treatment of an Afghanistan viper envenomation at a NATO military hospital. Clin Toxicol . 2017;55(3):229-230. doi:10.1080/15563650.2016.1263857
- Handford C. Case of venom ophthalmia following contact with Naja pallida: the red spitting cobra. J R Army Med Corps. 2018;164(2):124-126. doi:10.1136/jramc-2017-000891
- Lavon O, Bentur Y. Poison exposures in young Israeli military personnel: a National Poison Center Data analysis. Clin Toxicol . 2017;55(5):322-325. doi:10.1080/15563650.2016.1278225
- Ari AB. Patient with purely extraocular manifestations from a pit viper snakebite (Agkistrodon halys brevicaudus). Mil Med. 2001;166(7):667-669. https://www.ncbi.nlm.nih.gov/pubmed/11469043.
- Deshwal R, Gupta V. Krait envenomation disguised as heat exhaustion in a wilderness setting. Wilderness Environ Med. 2015;26(1):102-104. doi:10.1016/j.wem.2014.08.005
- Donat N, Masson Y, Villevieille T, et al. A case of combat-related scorpion envenomation in Afghanistan. Mil Med. 2011;176(4):472-474. doi:10.7205/milmed-d-10-00387
- Radonić V, Budimir D, Bradarić N, et al. Envenomation by the horned viper (Vipera ammodytes L.). Mil Med. 1997;162(3):179-182. https://www.ncbi.nlm.nih.gov/pubmed/9121663.
- Schäfer CN, Nissen LR, Kofoed LT, Hansen FØ. A suspected case of systemic envenomation syndrome in a soldier returning from Iraq: implications for Special Forces Operations. Mil Med. 2010;175(5):375-378. https://www.ncbi.nlm.nih.gov/pubmed/20486513.
- Poyrazoglu Y, Toygar M, Turk Y, Yildirim A, Ozenc S. Pit Viper Envenomation in Military Personnel. TAF Preventive Medicine Bulletin. 2012;11(2):127. doi:10.5455/pmb.1-1328962738
- Groshong TD. Scorpion envenomation in eastern Saudi Arabia. Ann Emerg Med. 1993;22(9):1431-1437. doi:10.1016/s0196-0644(05)81992-4
- Johnson C, Rimmer J, Mount G, Gurney I, Nicol ED. Challenges of managing snakebite envenomation in a deployed setting. J R Army Med Corps. 2013;159(4):307-311. doi:10.1136/jramc-2013-000047
- Dewar C, Meusnier J-G, Larréché S. Envenimation scorpionique chez des militaires français en poste isolé au Nord Mali : à propos de cinq cas. Annales françaises de médecine d’urgence. 2016;6(6):431-434. doi:10.1007/s13341-016-0690-4
- Larréché S, Aigle L, Puidupin M, et al. Animaux venimeux terrestres en opérations extérieures: présentation des principaux risques et du Comité technique des envenimations. Médecine et Armées. 2018;46(1):63-72.
- Gutiérrez JM, Rucavado A, Escalante T, et al. Unresolved issues in the understanding of the pathogenesis of local tissue damage induced by snake venoms. Toxicon. 2018;148:123-131. doi:10.1016/j.toxicon.2018.04.016
- Abubakar SB, Habib AG, Mathew J. Amputation and disability following snakebite in Nigeria. Trop Doct. 2010;40(2):114-116. doi:10.1258/td.2009.090266
- Baldé MC, Chippaux J-P, Boiro MY, Stock RP, Massougbodji A. Use of antivenoms for the treatment of envenomation by Elapidae snakes in Guinea, Sub-Saharan Africa. J Venom Anim Toxins Incl Trop Dis. 2013;19(1):6. doi:10.1186/1678-9199-19-6
- Erulu VE, Okumu MO, Ochola FO, Gikunju JK. Revered but poorly understood: a case report of Dendroaspis Polylepis (Black Mamba) Envenomation in Watamu, Malindi Kenya, and a Review of the Literature. Trop Med Infect Dis. 2018;3(3). doi:10.3390/tropicalmed3030104
- Ranawaka UK, Lalloo DG, de Silva HJ. Neurotoxicity in snakebite--the limits of our knowledge. PLoS Negl Trop Dis. 2013;7(10):e2302. doi:10.1371/journal.pntd.0002302
- Halilu S, Iliyasu G, Hamza M, et al. Snakebite burden in Sub-Saharan Africa: estimates from 41 countries. Toxicon. 2019;159:1-4. doi:10.1016/j.toxicon.2018.12.002
- Habib AG, Brown NI. The snakebite problem and antivenom crisis from a health-economic perspective. Toxicon. 2018;150:115-123. doi:10.1016/j.toxicon.2018.05.009
- WHO/Regional Office for Africa. Guidelines for the prevention and clinical management of snakebite in Africa. (Tempowski DJH, ed.). World Health Organization; 2010. https://apps.who.int/iris/bitstream/handle/10665/204458/9789290231684.pdf.
- Langley RL. Snakebite during pregnancy: a literature review. Wilderness Environ Med. 2010;21(1):54-60. doi:10.1016/j.wem.2009.12.025
- Adewole AA, Ugiagbe OA, Onile TG, et al. Snake bite in third trimester of pregnancy with systemic envenomation and delivery of a live baby in a low resource setting: A case report. Case Rep Womens Health. 2017;16:14-17. doi:10.1016/j.crwh.2017.10.001
- Muhammed A, Dalhat MM, Joseph BO, et al. Predictors of depression among patients receiving treatment for snakebite in General Hospital, Kaltungo, Gombe State, Nigeria: August 2015. Int J Ment Health Syst. 2017;11:26. doi:10.1186/s13033-017-0132-8
- Williams SS, Wijesinghe CA, Jayamanne SF, et al. Delayed psychological morbidity associated with snakebite envenoming. PLoS Negl Trop Dis. 2011;5(8):e1255. doi:10.1371/journal.pntd.0001255
- Hiller K, Jarrod MM, Franke HA, Degan J, Boyer LV, Fox FM. Scorpion antivenom administered by alternative infusions. Ann Emerg Med. 2010;56(3):309-310. doi:10.1016/j.annemergmed.2010.04.007
- Williams DJ, Jensen SD, Nimorakiotakis B, Müller R, Winkel KD. Antivenom use, premedication and early adverse reactions in the management of snake bites in rural Papua New Guinea. Toxicon. 2007;49(6):780-792. doi:10.1016/j.toxicon.2006.11.026
- Thiansookon A, Rojnuckarin P. Low incidence of early reactions to horse-derived F(ab’)(2) antivenom for snakebites in Thailand. Acta Trop. 2008;105(2):203-205. doi:10.1016/j.actatropica.2007.09.007
- de Menezes JB Hering SE. . CPA-MM. Immediate hypersensitivity reactions following intravenous use of antivenom sera: predictive value of hypersensitivity skin test. Rev Inst Med Trop Sao Paulo. 1991;33(2):115-122. doi:10.1590/s0036-46651991000200005.
- Klaewsongkram J. A role of snake antivenom skin test from the allergist’s point of view. Acta Trop. 2009;109(1):84-85; author reply 86. doi:10.1016/j.actatropica.2008.09.007
- Norris RL, Ngo J, Nolan K, Hooker G. Physicians and lay people are unable to apply pressure immobilization properly in a simulated snakebite scenario. Wilderness Environ Med. 2005;16(1):16-21. doi:10.1580/PR12-04.1
- O’Connor AD, Ruha A-M, Levine M. Pressure immobilization bandages not indicated in the prehospital management of North American snakebites. J Med Toxicol. 2011;7(3):251. doi:10.1007/s13181-011-0163-5
- American College of Medical Toxicology, American Academy of Clinical Toxicology, American Association of Poison Control Centers, European Association of Poison Control Centres, International Society of Toxinology, Asia Pacific Association of Medical Toxicology. Pressure immobilization after North American Crotalinae snake envenomation. J Med Toxicol. 2011;7(4):322-323. doi:10.1007/s13181-011-0174-2
- Benjamin JM, Chippaux J-P, Jackson K, et al. Differential Diagnosis of an Unusual Snakebite Presentation in Benin: Dry Bite or Envenomation? J Spec Oper Med. 2019;19(2):18-22. https://www.ncbi.nlm.nih.gov/pubmed/31201747.
- Watt G, Theakston RDG, Padre L, Laughlin LW, Tuazon ML. Tourniquet Application after Cobra Bite: Delay in the Onset of Neurotoxicity and the Dangers of Sudden Release. Am J Trop Med Hyg. 1988;38(3):618-622. doi:10.4269/ajtmh.1988.38.618
- Warrell DA, Davidson NMcD, Greenwood BM, et al. Poisoning by bites of the saw-scaled or carpet viper (Echis carinatus) in Nigeria. Q J Med. 1977;46(181):33-62. doi:10.1093/oxfordjournals.qjmed.a067493
- Benjamin JM, Chippaux J-P, Tamou-Sambo B, Akpakpa OC, Massougbodji A. successful management of two patients with intracranial hemorrhage due to carpet viper (Echis ocellatus) Envenomation in a Limited-Resource Environment. Wilderness Environ Med. June 2019. doi:10.1016/j.wem.2019.04.003
- Dart RC, Hurlbut KM, Garcia R, Boren J. Validation of a severity score for the assessment of crotalid snakebite. Ann Emerg Med. 1996;27(3):321-326. doi:10.1016/s0196-0644(96)70267-6
- Rega PP, Bork CE, Burkholder-Allen K, Bisesi MS, Gold JP. Single-Breath-Count Test: An Important Adjunct in the Triaging of Patients in a Mass-Casualty Incident Due to Botulism. Prehosp Disaster Med. 2010;25(3):219-222. doi:10.1017/S1049023X00008062
- Alirol E, Sharma SK, Bawaskar HS, Kuch U, Chappuis F. Snake bite in South Asia: a review. PLoS Negl Trop Dis. 2010;4(1):e603. doi:10.1371/journal.pntd.0000603
- Gold BS. Neostigmine for the treatment of neurotoxicity following envenomation by the Asiatic cobra. Ann Emerg Med. 1996;28(1):87-89. doi:10.1016/s0196-0644(96)70142-7
- Winkel KD, Mc Gain F, Nimorakiotakis B, Williams D. The use of anticholinesterase therapy. Clinical management of snakebite in Papua New Guinea, Independent Publishing, Independent Group, 1 ed. 2004, pp. 12.1-12.4.
- Bawaskar HS, Bawaskar PH. Envenoming by the common krait (Bungarus caeruleus) and Asian cobra (Naja naja): clinical manifestations and their management in a rural setting. Wilderness Environ Med. 2004;15(4):257-266. doi:10.1580/1080-6032(2004)015[0257:EBTCKB]2.0.CO;2
- WHO/Regional Office for South-East Asia. Guidelines for the Management of Snakebites, 2nd Edition. (Warrell DA, ed.). World Health Organization; 2016.
- Benjamin JM, Chippaux J-P, Sambo BT, Massougbodji A. Delayed double reading of whole blood clotting test (WBCT) results at 20 and 30 minutes enhances diagnosis and treatment of viper envenomation. J Venom Anim Toxins Incl Trop Dis. 2018;24:14. doi:10.1186/s40409-018-0151-1
- Ogunfowokan O, Jacob DA, Livinus OL. Relationship between bite-to-hospital time and morbidity in victims of carpet viper bite in North-Central Nigeria. West Afr J Med. 2011;30(5):348-353. https://www.ncbi.nlm.nih.gov/pubmed/22752823.
- Lavonas EJ, Tomaszewski CA, Ford MD, Rouse AM, Kerns WP 2nd. Severe puff adder (Bitis arietans) envenomation with coagulopathy. J Toxicol Clin Toxicol. 2002;40(7):911-918. https://www.ncbi.nlm.nih.gov/pubmed/12507061.
- Hatten BW, Bueso A, French LK, Hendrickson RG, Horowitz BZ. Envenomation by the Great Lakes Bush Viper (Atheris nitschei). Clin Toxicol . 2013;51(2):114-116. doi:10.3109/15563650.2012.763134
- Jeon YJ, Kim JW, Park S, Shin DW. Risk factor, monitoring, and treatment for snakebite induced coagulopathy: a multicenter retrospective study. Acute Crit Care. 2019;34(4):269-275. doi:10.4266/acc.2019.00591
- Cumpston KL. Is there a role for fasciotomy in Crotalinae envenomations in North America? Clin Toxicol . 2011;49(5):351-365. doi:10.3109/15563650.2011.597032
- Hawkins SC. Wilderness EMS. Lippincott Williams & Wilkins; 2017. https://play.google.com/store/books/details?id=2yQ6DwAAQBAJ.
- Tanen DA, Danish DC, Grice GA, Riffenburgh RH, Clark RF. Fasciotomy worsens the amount of myonecrosis in a porcine model of crotaline envenomation. Ann Emerg Med. 2004;44(2):99-104. doi:10.1016/S0196064404000575
- Mazer-Amirshahi M, Boutsikaris A, Clancy C. Elevated compartment pressures from copperhead envenomation successfully treated with antivenin. J Emerg Med. 2014;46(1):34-37. doi:10.1016/j.jemermed.2013.05.025
- Moore EC, Porter LM, Ruha A-M. Rattlesnake venom-induced recurrent coagulopathy in first trimester pregnant women – Two Cases. Toxicon. 2019;163:8-11. doi:10.1016/j.toxicon.2019.03.006
- Diallo B, Keita M, Dicko H, et al. [Recurrent retroperitoneal hematoma due to viperine envenomation: case study]. Pan Afr Med J. 2019;32:70. doi:10.11604/pamj.2019.32.70.17951
- Boyer LV, Seifert SA, Clark RF, et al. Recurrent and persistent coagulopathy following pit viper envenomation. Arch Intern Med. 1999;159(7):706-710. doi:10.1001/archinte.159.7.706
- Lavonas EJ, Schaeffer TH, Kokko J, Mlynarchek SL, Bogdan GM. Crotaline Fab antivenom appears to be effective in cases of severe North American pit viper envenomation: an integrative review. BMC Emerg Med. 2009;9:13. doi:10.1186/1471-227X-9-13
- Boyer LV, Ruha A-M. Pitviper Envenomation Guidelines Should Address Choice Between FDA-approved Treatments for Cases at Risk of Late Coagulopathy. Wilderness Environ Med. 2016;27(2):341-342. doi:10.1016/j.wem.2015.10.013
- Bush SP, Ruha A-M, Seifert SA, et al. Comparison of F(ab’)2 versus Fab antivenom for pit viper envenomation: a prospective, blinded, multicenter, randomized clinical trial. Clin Toxicol . 2015;53(1):37-45. doi:10.3109/15563650.2014.974263
- Gutiérrez JM, León G, Lomonte B. Pharmacokinetic-pharmacodynamic relationships of immunoglobulin therapy for envenomation. Clin Pharmacokinet. 2003;42(8):721-741. doi:10.2165/00003088-200342080-00002
- Clark RF, McKinney PE, Chase PB, Walter FG. Immediate and delayed allergic reactions to Crotalidae polyvalent immune Fab (ovine) antivenom. Ann Emerg Med. 2002;39(6):671-676. doi:10.1067/mem.2002.123134
- Dart RC, McNally J. Efficacy, safety, and use of snake antivenoms in the United States. Ann Emerg Med. 2001;37(2):181-188. doi:10.1067/mem.2001.113372
- Lavonas EJ, Kokko J, Schaeffer TH, et al. Short-term outcomes after Fab antivenom therapy for severe crotaline snakebite. Ann Emerg Med. 2011;57(2):128-137.e3. doi:10.1016/j.annemergmed.2010.06.550
- Boyer L, Degan J, Ruha A-M, et al. Safety of intravenous equine F(ab’)2: insights following clinical trials involving 1534 recipients of scorpion antivenom. Toxicon. 2013;76:386-393. doi:10.1016/j.toxicon.2013.07.017
- de Silva HA, Ryan NM, de Silva HJ. Adverse reactions to snake antivenom, and their prevention and treatment. Br J Clin Pharmacol. 2016;81(3):446-452. doi:10.1111/bcp.12739
- Chippaux JP, Lang J, Eddine SA, et al. Clinical safety of a polyvalent F(ab’)2 equine antivenom in 223 African snake envenomations: a field trial in Cameroon. (Venin Afrique de l'Ouest) Investigators. Trans R Soc Trop Med Hyg. 1998;92(6):657-662. doi:10.1016/s0035-9203(98)90802-1
- Warrell DA, Ormerod LD, Davidson NM. Bites by puff-adder (Bitis arietans) in Nigeria, and value of antivenom. Br Med J. 1975;4(5998):697-700. doi:10.1136/bmj.4.5998.697
- Lavonas EJ, Ruha A-M, Banner W, et al. Unified treatment algorithm for the management of crotaline snakebite in the United States: results of an evidence-informed consensus workshop. BMC Emerg Med. 2011;11:2. doi:10.1186/1471-227X-11-2
- Gerardo CJ, Quackenbush E, Lewis B, et al. The efficacy of Crotalidae polyvalent immune Fab (Ovine) antivenom versus placebo plus optional rescue therapy on recovery from copperhead snake envenomation: a randomized, double-blind, placebo-controlled, clinical trial. Ann Emerg Med. 2017;70(2):233-244. https://www.sciencedirect.com/science/article/pii/S0196064417305103.
- Gerardo CJ, Vissoci JRN, Evans CS, Simel DL, Lavonas EJ. Does this patient have a severe snake envenomation?: the rational clinical examination systematic review. JAMA Surg. 2019;154(4):346-354. doi:10.1001/jamasurg.2018.5069
- Habib AG, Abubakar SB. Factors affecting snakebite mortality in north-eastern Nigeria. Int Health. 2011;3(1):50-55. doi:10.1016/j.inhe.2010.08.001
- Iliyasu G, Tiamiyu AB, Daiyab FM, Tambuwal SH, Habib ZG, Habib AG. Effect of distance and delay in access to care on outcome of snakebite in rural north-eastern Nigeria. Rural Remote Health. 2015;15(4):3496. https://www.ncbi.nlm.nih.gov/pubmed/26590373.
- Chippaux J-P, Baldé MC, Sessinou É, et al. Evaluation of a new polyvalent antivenom against snakebite envenomation (Inoserp® Panafricain) in two different epidemiological settings: Northern Benin and Maritime Guinea]. Med Sante Trop. 2015;25(1):56-64. doi:10.1684/mst.2014.0413
- Agarwal R, Aggarwal AN, Gupta D, Behera D, Jindal SK. Low dose of snake antivenom is as effective as high dose in patients with severe neurotoxic snake envenoming. Emerg Med J. 2005;22(6):397-399. doi:10.1136/emj.2004.020727
- Alirol E, Sharma SK, Ghimire A, et al. Dose of antivenom for the treatment of snakebite with neurotoxic envenoming: Evidence from a randomised controlled trial in Nepal. PLoS Negl Trop Dis. 2017;11(5):e0005612. doi:10.1371/journal.pntd.0005612
- Chippaux J-P, Massougbodji A, Stock RP, Alagon A, Investigators of African Antivipmyn in Benin. Clinical trial of an F(ab’)2 polyvalent equine antivenom for African snake bites in Benin. Am J Trop Med Hyg. 2007;77(3):538-546. https://www.ncbi.nlm.nih.gov/pubmed/17827375.
- Chippaux J-P, Lang J, Eddine SA, et al. Clinical safety of a polyvalent F(ab′)2 equine antivenom in 223 African snake envenomations: a field trial in Cameroon. Trans R Soc Trop Med Hyg. 1998;92(6):657-662. doi:10.1016/S0035-9203(98)90802-1
- Abubakar IS, Abubakar SB, Habib AG, et al. Randomised controlled double-blind non-inferiority trial of two antivenoms for saw-scaled or carpet viper (Echis ocellatus) envenoming in Nigeria. PLoS Negl Trop Dis. 2010;4(7):e767. doi:10.1371/journal.pntd.0000767
- Sano-Martins IS, Fan HW, Castro SCB, et al. Reliability of the simple 20 minute whole blood clotting test (WBCT20) as an indicator of low plasma fibrinogen concentration in patients envenomed by Bothrops snakes. Toxicon. 1994;32(9):1045-1050. doi:10.1016/0041-0101(94)90388-3
- Gaus DP, Herrera DF, Troya CJ, Guevara AH. Management of snakebite and systemic envenomation in rural Ecuador using the 20-minute whole blood clotting test. Wilderness Environ Med. 2013;24(4):345-350. doi:10.1016/j.wem.2013.08.001
- Chippaux JP, Amadi-Eddine S, Fagot P. [Diagnosis and monitoring of hemorrhage due to viper envenomation in the African savanna]. Bull Soc Pathol Exot. 1999;92(2):109-113. https://www.ncbi.nlm.nih.gov/pubmed/10399601.
- Madaki JKA, Obilom R, Mandong BM. Clinical Presentation And Outcome Of Snake-Bite Patients At Zamko Comprehensive Health Centre, Langtang, Plateau State. Highland Medical Research Journal. 2004;2(2):61-68. https://www.ajol.info/index.php/hmrj/article/view/33855. Accessed Dec 2019.
- Dsilva AA, Basheer A, Thomas K. Snake envenomation: is the 20 min whole blood clotting test (WBCT20) the optimum test for management? QJM. 2019;112(8):575-579. doi:10.1093/qjmed/hcz077
- Ratnayake I, Shihana F, Dissanayake DM, Buckley NA, Maduwage K, Isbister GK. Performance of the 20-minute whole blood clotting test in detecting venom induced consumption coagulopathy from Russell’s viper (Daboia russelii) bites. Thromb Haemost. 2017;117(3):500-507. doi:10.1160/TH16-10-0769
- Isbister GK, Maduwage K, Shahmy S, et al. Diagnostic 20-min whole blood clotting test in Russell’s viper envenoming delays antivenom administration. QJM. 2013;106(10):925-932. doi:10.1093/qjmed/hct102
- Punguyire D, Iserson KV, Stolz U, Apanga S. Bedside Whole-Blood Clotting Times: Validity after Snakebites. J Emerg Med. 2013;44(3):663-667. doi:10.1016/j.jemermed.2012.07.073
- Bawaskar HS, Bawaskar PH. Profile of snakebite envenoming in western Maharashtra, India. Trans R Soc Trop Med Hyg. 2002;96(1):79-84. doi:10.1016/s0035-9203(02)90250-6
- Baldé MC, Chippaux J-P, Boiro MY, Stock R, Massougbodji A. [Clinical study of tolerance and effectiveness of a F(ab’)(2) polyvalent antienom for African snake bites in Kindia, Guinea]. Bull Soc Pathol Exot. 2012;105(3):157-161. doi:10.1007/s13149-012-0223-3
- Curry S. Rapid collapse and anaphylactoid reactions from rattlesnake bites. The tox and the hound (EMCrit). April 5, 2019 https://emcrit.org/toxhound/ff-rapid-collapse-rattlesnake
- Chaisakul J, Isbister GK, Kuruppu S, et al. An examination of cardiovascular collapse induced by eastern brown snake (Pseudonaja textilis) venom. Toxicol Lett. 2013;221(3):205-211. doi:10.1016/j.toxlet.2013.06.235
- Kakumanu R, Kemp-Harper BK, Silva A, et al. An in vivo examination of the differences between rapid cardiovascular collapse and prolonged hypotension induced by snake venom. Sci Rep. 2019;9(1):20231. doi:10.1038/s41598-019-56643-0
- Norris RL, Wilkerson JA, Feldman J. Syncope, massive aspiration, and sudden death following rattlesnake bite. Wilderness Environ Med. 2007;18(3):206-208. doi:10.1580/06-WEME-CR-012R.1
- Tilbury CR, Verster J. A fatal bite from the burrowing asp Atractaspis corpulenta (Hallowell 1854). Toxicon. 2016;118:21-26. doi:10.1016/j.toxicon.2016.04.035
- Brooks DE, Graeme KA. Airway compromise after first rattlesnake envenomation. Wilderness Environ Med. 2004;15(3):188-193. doi:10.1580/1080-6032(2004)15[188:ACAFRE]2.0.CO;2
- Ryan KC, Martin Caravati E. Life-threatening anaphylaxis following envenomation by two different species of Crotalidae. J Wilderness Med. 1994;5(3):263-268. doi:10.1580/0953-9859-5.3.263
- Hinze JD, Barker JA, Jones TR, Winn RE. Life-threatening upper airway edema caused by a distal rattlesnake bite. Ann Emerg Med. 2001;38(1):79-82. doi:10.1067/mem.2001.114321
- Kerns W 2nd, Tomaszewski C. Airway obstruction following canebrake rattlesnake envenomation. J Emerg Med. 2001;20(4):377-380. https://www.ncbi.nlm.nih.gov/pubmed/11348818.
- Johnston MA, Fatovich DM, Haig AD, Daly FFS. Successful resuscitation after cardiac arrest following massive brown snake envenomation. Med J Aust. 2002;177(11-12):646-649. https://www.ncbi.nlm.nih.gov/pubmed/12463988.
- Boyd JJ, Agazzi G, Svajda D, Morgan AJ, Ferrandis S, Norris RL. Venomous snakebite in mountainous terrain: prevention and management. Wilderness Environ Med. 2007;18(3):190-202. doi:10.1580/06-WEME-RA-087R.1
- Morais V. Antivenom therapy: efficacy of premedication for the prevention of adverse reactions. J Venom Anim Toxins Incl Trop Dis. 2018;24:7. doi:10.1186/s40409-018-0144-0
- de Silva HA, Pathmeswaran A, Ranasinha CD, et al. Low-dose adrenaline, promethazine, and hydrocortisone in the prevention of acute adverse reactions to antivenom following snakebite: a randomised, double-blind, placebo-controlled trial. PLoS Med. 2011;8(5):e1000435. doi:10.1371/journal.pmed.1000435
- Premawardhena AP, de Silva CE, Fonseka MMD, Gunatilake SB, de Silva HJ. Low dose subcutaneous adrenaline to prevent acute adverse reactions to antivenom serum in people bitten by snakes: randomised, placebo controlled trial. BMJ. 1999;318(7190):1041-1043. doi:10.1136/bmj.318.7190.1041
- Habib AG. Effect of pre-medication on early adverse reactions following antivenom use in snakebite: a systematic review and meta-analysis. Drug Saf. 2011;34(10):869-880. doi:10.2165/11592050-000000000-00000
- Dassanayake AS, Karunanayake P, Kasturiratne K, et al. Safety of subcutaneous adrenaline as prophylaxis against acute adverse reactions to anti-venom serum in snakebite. Ceylon Med J. 2011;47(2). https://www.researchgate.net/profile/Anuradha_Dassanayake/publication/11240909_Safety_of_subcutaneous_adrenaline_as_prophylaxis_against_acute_adverse_reactions_to_anti-venom_serum_in_snakebite/links/02e7e52f860d6e1296000000/Safety-of-subcutaneous-adrenaline-as-prophylaxis-against-acute-adverse-reactions-to-anti-venom-serum-in-snakebite.pdf.
- Herrera M, Sánchez M, Machado A, et al. Effect of premedication with subcutaneous adrenaline on the pharmacokinetics and immunogenicity of equine whole IgG antivenom in a rabbit model. Biomed Pharmacother. 2017;90:740-743. doi:10.1016/j.biopha.2017.04.039
- Choo KJL, Simons E, Sheikh A. Glucocorticoids for the treatment of anaphylaxis: Cochrane systematic review. Allergy. 2010;65(10):1205-1211. doi:10.1111/j.1398-9995.2010.02424.x
- Stokes S, Hudson S. Managing anaphylaxis in a jungle environment. Wilderness Environ Med. 2012;23(1):51-55. doi:10.1016/j.wem.2011.12.002
- Simons FE, Gu X, Simons KJ. Epinephrine absorption in adults: intramuscular versus subcutaneous injection. J Allergy Clin Immunol. 2001;108(5):871-873. doi:10.1067/mai.2001.119409
- Duvauchelle T, Robert P, Donazzolo Y, et al. Bioavailability and Cardiovascular Effects of Adrenaline Administered by Anapen Autoinjector in Healthy Volunteers. J Allergy Clin Immunol Pract. 2018;6(4):1257-1263. doi:10.1016/j.jaip.2017.09.021
- Campbell RL, Bellolio MF, Knutson BD, et al. Epinephrine in anaphylaxis: higher risk of cardiovascular complications and overdose after administration of intravenous bolus epinephrine compared with intramuscular epinephrine. J Allergy Clin Immunol Pract. 2015;3(1):76-80. doi:10.1016/j.jaip.2014.06.007
- Simons FE, Roberts JR, Gu X, Simons KJ. Epinephrine absorption in children with a history of anaphylaxis. J Allergy Clin Immunol. 1998;101(1 Pt 1):33-37. doi:10.1016/S0091-6749(98)70190-3
- Coralic Z. The dirty epi drip: IV Epinephrine when you need it. ALiEM. https://www.aliem.com/2013/06/dirtyepi/. Published June 27, 2013.
- Einterz EM, Bates ME. Snakebite in northern Cameroon: 134 victims of bites by the saw-scaled or carpet viper, Echis ocellatus. Trans R Soc Trop Med Hyg. 2003;97(6):693-696. doi:10.1016/s0035-9203(03)80105-0
- Chippaux J-P. Snake venoms and envenomations. Krieger Publishing Company; 2006.
- Bush SP. Snakebite suction devices Do not remove venom: they just suck. Ann Emerg Med. 2004;43(2):187-188. doi:10.1016/j.annemergmed.2003.10.031
- Parker-Cote J, Meggs WJ. First Aid and Pre-Hospital Management of Venomous Snakebites. Trop Med Infect Dis. 2018;3(2). doi:10.3390/tropicalmed3020045
- Alberts MB, Shalit M, LoGalbo F. Suction for venomous snakebite: A study of “mock venom” extraction in a human model. Ann Emerg Med. 2004;43(2):181-186. doi:10.1016/S0196-0644(03)00813-8
- Leopold RS, Huber GS. Ineffectiveness of suction in removing snake venom from open wounds. U S Armed Forces Med J. 1960;11:682-685. https://www.ncbi.nlm.nih.gov/pubmed/14415856.
- Bush SP, Hegewald KG, Green SM, Cardwell MD, Hayes WK. Effects of a negative pressure venom extraction device (Extractor) on local tissue injury after artificial rattlesnake envenomation in a porcine model. Wilderness Environ Med. 2000;11(3):180-188. doi:10.1580/1080-6032(2000)011[0180:eoanpv]2.3.co;2
- Panagides N, Jackson TNW, Ikonomopoulou MP, et al. How the Cobra Got Its Flesh-Eating Venom: Cytotoxicity as a Defensive Innovation and Its Co-Evolution with Hooding, Aposematic Marking, and Spitting. Toxins . 2017;9(3). doi:10.3390/toxins9030103
- Bittenbinder MA, Zdenek CN, Op den Brouw B, et al. Coagulotoxic Cobras: clinical implications of strong anticoagulant actions of African spitting Naja venoms that are not neutralised by antivenom but are by LY315920 (Varespladib). Toxins . 2018;10(12). doi:10.3390/toxins10120516
- Spawls S, Branch B. The Dangerous Snakes of Africa. Ralph Curtis Pub; 1995.
- Chu ER, Weinstein SA, White J, Warrell DA. Venom ophthalmia caused by venoms of spitting elapid and other snakes: Report of ten cases with review of epidemiology, clinical features, pathophysiology and management. Toxicon. 2010;56(3):259-272. doi:10.1016/j.toxicon.2010.02.023
- Warrell DA, Ormerod LD. Snake venom ophthalmia and blindness caused by the spitting cobra (Naja nigricollis) in Nigeria. Am J Trop Med Hyg. 1976;25(3):525-529. doi:10.4269/ajtmh.1976.25.525
- Hoffman J. Venom ophthalmia from Naja mossambica in KwaZulu Natal, South Africa: a reminder to all that for ocular chemical injury, dilution is the solution. Trop Doct. 2015;45(4):250-251. doi:10.1177/0049475514564695
- Chu ERL, White J, Weinstein S. Is there any role for intravenous antivenom for snake venom ophthalmia? J Emerg Med. 2010;39(5):659-660; author reply 660-661. doi:10.1016/j.jemermed.2009.06.128
- WHO Expert Committee on Biological Standardization. WHO Guidelines for the Production, Control and Regulation of Snake Antivenom Immunoglobulins. World Health Organization; 2010.
- Lam A, Cabral M, Touré A, et al. Évaluation de l’efficacité et la tolérance de Inoserp® Panafricain au Sénégal. Toxicologie Analytique et Clinique. 2019;31(1):18-29. doi:10.1016/j.toxac.2018.12.008
- Coulibaly SK, Diallo T, Diara A, Soulaymani A, Maiga AI. Sérothérapie antivenimeuse au Mali : expérience du centre de santé de référence de Kati région de Koulikoro. Toxicologie Analytique et Clinique. 2018;30(3):165. doi:10.1016/j.toxac.2018.07.094
- Baldé MC. Defis et perspectives de la prise en charge des envenimations par elapids en Guinee. A` propos d’une patiente traitee par Inoserp Pan-Africa. In: One Health, Vers Une Seule Santé. Med Sante Trop; :446. doi:10.1684/mst.2019.0908
- Lam A, Cabral M, Touré A, Fall M, Diouf A, Chippaux JP. Evaluation de la prise en charge des envenimations au Sénégal : étude clinique de l’Inoserp® Panafricain. Toxicologie Analytique et Clinique. 2018;30(3):165-166. doi:10.1016/j.toxac.2018.07.095
- Chafiq F, Rhalem N, Hmimou R, et al. Snakebite and use of three antivenoms in Morocco: FAV-Afrique (R), Favirept (R) and Inoserp (R) MENA. In: Clinical Toxicology. Vol 54. TAYLOR & FRANCIS LTD 2016:513-513.
- Chafiq F, Elkarimi ME, Rhalem N, et al. Assessment of Use of Inoserp MENA in the management of snake envenomation in Morocco. In: Toxinology in the 21st Century: Public Health Impact from Basic, Translational and Clinical Sciences.
- Chafiq F. Centre Antipoison du Maroc: Rapports de toxicovigilance sur les morsures de serpent au Maroc en 2015. Toxicologie Maroc. 12-2015;27(4):15.
- Chafiq F. Centre Antipoison du Maroc: Rapports de toxicovigilance sur les morsures de serpent au Maroc en 2016. Toxicologie Maroc. 12-2015;27(4):13.
- Chafiq F. Centre Antipoison du Maroc: Rapports de toxicovigilance sur les morsures de serpent au Maroc en 2017. Toxicologie Maroc. 12-2017;35(4):15.
- Chafiq F. Centre Antipoison du Maroc: Rapports de toxicovigilance sur les morsures de serpent au Maroc en 2018. Toxicologie Maroc. 6-2015;41(2):15.
- Chafiq F, Hmimou R, Rhalem N, Soulaymani A, Mokhtari A, Soulaymani Bencheikh R. Caractéristiques épidémiologiques des morsures de serpent notifiées au centre antipoison et de pharmacovigilance du Maroc. Année 2016. Toxicologie Analytique et Clinique. 2018;30(3):175-176. doi:10.1016/j.toxac.2018.07.042
- Badr A, Abderrahman E, Hassan A, Mina AE, Rachid E, Yassir B. Epidemiological profile of snakebites cases recorded at the 3rd military hospital laayoune morocco between 2011 and 2017. Research Journal of Pharmacy and Technology. 2018;11(5):1752-1756. http://search.proquest.com/openview/73f63493507471f15363286e5da163f2/1?pq-origsite=gscholar&cbl=1096441.
- Krüger HJ, Lemke FG. Fatal Boomslang bite in th Safety profile e Northern Cape. Afr J Emerg Med. 2019;9(1):53-55. doi:10.1016/j.afjem.2018.12.006
- Moran NF, Newman WJ, Theakston RD, Warrell DA, Wilkinson D. High incidence of early anaphylactoid reaction to SAIMR polyvalent snake antivenom. Trans R Soc Trop Med Hyg. 1998;92(1):69-70. doi:10.1016/s0035-9203(98)90959-2
- du Toit DM. Boomslang (Dispholidus typus) bite: A case report and a review of diagnosis and management. S Afr Med J. 1980;57(13):507-510. https://www.ncbi.nlm.nih.gov/pubmed/7368013.
- Lakier JB, Fritz VU. Consumptive coagulopathy caused by a boomslang bite. S Afr Med J. 1969;43(34):1052-1055. https://www.ncbi.nlm.nih.gov/pubmed/5822937.
- Geddes J, Thomas JE. Boomslang bite--a case report. Cent Afr J Med. 1985;31(6):109-112. https://www.ncbi.nlm.nih.gov/pubmed/4042146.
- Aitchison JM. Boomslang bite--diagnosis and management. A report of 2 cases. S Afr Med J. 1990;78(1):39-42. https://www.ncbi.nlm.nih.gov/pubmed/2363083.
- Tilston SIG, Young M. Severe cutaneous blistering following a bite by a boomslang snake and subsequent clinical response to boomslang antivenom. Br J Dermatol. 2004;151:42-43.
- Gomperts ED, Demetriou D. Laboratory studies and clinical features in a case of boomslang envenomation. S Afr Med J. 1977;51(6):173-175. https://www.ncbi.nlm.nih.gov/pubmed/841447.
- Matell G, Nyman D, Werner B, Wilhelmsson S. Consumption coagulopathy caused by a boomslang bite: A case report. Thrombosis Research. 1973;3(2):173-182. doi:10.1016/0049-3848(73)90067-4.
- Al-Durihim H, Al-Hussaini M, Bin Salih S, Hassan I, Harakati M, Al Hajjaj A. Snake bite envenomation: experience at King Abdulaziz Medical City, Riyadh. East Mediterr Health J. 2010;16(4):438-441. https://www.ncbi.nlm.nih.gov/pubmed/20795431.
- Al-Lawati A, Al-Abri SS, Lalloo DG. Epidemiology and outcome of snake bite cases evaluated at a Tertiary Care Hospital in Oman. J Infect Public Health. 2009;2(4):167-170. doi:10.1016/j.jiph.2009.09.001.
- Haidar NA, Deitch E. Snake bites in the Arabian Peninsula, a review article. J Arid Environ. 2015;112:159-164. doi:10.1016/j.jaridenv.2014.04.010.
- Haidar NA, Emran MY, Al Muslemani EA. Snakebites in Hajjah, Yemen Republic: Epidemiology, management and the relation of the degree of acuity at presentation with outcome. Journal of Emergency Medicine, Trauma and Acute Care. 2012;2012(1):2. doi:10.5339/jemtac.2012.2.
- Khan YMT, Fatema N, Shekeili NAA. Snake Bite Envenomation: Experience in a Regional Hospital, Oman: A Retrospective Observational Study. SM Trop Med J. 2017;2(1):1015. https://www.researchgate.net/profile/Nishat_Fatema/publication/320685439_Snake_Bite_Envenomation_Experience_in_a_Regional_Hospital_Oman_A_Retrospective_Observational_Study/links/59f40a0d0f7e9b553eba83c7/Snake-Bite-Envenomation-Experience-in-a-Regional-Hospital-Oman-A-Retrospective-Observational-Study.pdf.
- Mahaba HM. Snakebite: epidemiology, prevention, clinical presentation and management. Ann Saudi Med. 2000;20(1):66-68. doi:10.5144/0256-4947.2000.66
- Al-Sadoon MK. Snake bite envenomation in Riyadh province of Saudi Arabia over the period (2005-2010). Saudi J Biol Sci. 2015;22(2):198-203. doi:10.1016/j.sjbs.2014.09.008
- Kingston Michael E. Management of Snake Bite in Saudi Arabia. Ann Saudi Med. 1981;1(2):87-94. doi:10.5144/0256-4947.1981.87
- AlTamimi A, Malhis NK, Khojah NM, Manea SA, AlTamimi A, AlShammary SA. Antidote Availability in Saudi Arabia Hospitals in the Riyadh Province. Basic Clin Pharmacol Toxicol. 2018;122(2):288-292. doi:10.1111/bcpt.12897
- al Harbi N. Epidemiological and clinical differences of snake bites among children and adults in south western Saudi Arabia. J Accid Emerg Med. 1999;16(6):428-430. doi:10.1136/emj.16.6.428
- Malik GM. Snake bites in adults from the Asir region of southern Saudi Arabia. Am J Trop Med Hyg. 1995;52(4):314-317. doi:10.4269/ajtmh.1995.52.314
- Fung HT, Lam KK, Kam CW. Efficacy and safety of snake antivenom therapy: experience of a regional hospital. Hong Kong Journal of Emergency Medicine. 2006;13(2):70-78. doi:10.1177/102490790601300209
- Mong R, Ng VCH, Tse ML. Safety profile of snake antivenom (use) in Hong Kong--a review of 191 cases from 2008 to 2015. Clin Toxicol. 2017;55(10):1066-1071. https://www.tandfonline.com/doi/abs/10.1080/15563650.2017.1334916.
- Manufacture and application of Agkistrodon halys antivenin. She Zhi. February 1991.
- Fung HT, Yung WH, Crow P, et al. Green pit viper antivenom from Thailand and Agkistrodon halys antivenom from China compared in treating Cryptelytrops albolabris envenomation of mice. Hong Kong Med J. 2012;18(1):40-45. https://www.ncbi.nlm.nih.gov/pubmed/22302910.
- Lam SK, Yip SF, Crow P, et al. Comparison of green pit viper and Agkistrodon halys antivenom in inhibition of coagulopathy due to Trimeresurus albolabris venom: an in-vitro study using human plasma. Hong Kong Med J. 2017;23(1):13-18. doi:10.12809/hkmj154617
- Monzavi SM, Salarian AA, Khoshdel AR, Dadpour B, Afshari R. Effectiveness of A Clinical Protocol Implemented To Standardize Snakebite Management In Iran: Initial Evaluation. Wilderness Environ Med. 2015;26(2):115-123. doi:10.1016/j.wem.2014.09.011
- Dadpour B, Shafahi A, Monzavi SM, et al. Snakebite prognostic factors: Leading factors of weak therapeutic response following snakebite envenomation. Asia pacific journal of medical toxicology. 2012;1(1):27-33.
- Dehghani R, Dadpour B, Mehrpour O. Epidemiological profile of snakebite in Iran, 2009-2010 based on information of Ministry of Health and Medical Education. International journal of medical toxicology and forensic medicine. 2014;4(2):33-41. https://www.researchgate.net/profile/Rouhullah_Dehghani/publication/287253083_Epidemiological_profile_of_snake_bite_in_Iran_2009-2010_based_on_information_of_Ministry_of_Health_and_Medical_Education/links/56af14be08ae43a3980f69e5.pdf.
- Rahmani AH, Jalali A, Alemzadeh-Ansari MH, Tafazoli M, Rahim F. Dosage comparison of snake anti-venomon coagulopathy. Iran J Pharm Res. 2014;13(1):283-289. https://www.ncbi.nlm.nih.gov/pubmed/24734082.
- Eslamian L, Mobaiyen H, Bayat-Makoo Z. Snake bite in Northwest Iran: A retrospective study. J Anal Res Clin. 2016.
- Dehghani R, Fathi B, Shahi MP, Jazayeri M. Ten years of snakebites in Iran. Toxicon. 2014;90:291-298. doi:10.1016/j.toxicon.2014.08.063
- Monzavi SM, Dadpour B, Afshari R. Snakebite management in Iran: Devising a protocol. J Res Med Sci. 2014;19(2):153-163. https://www.ncbi.nlm.nih.gov/pubmed/24778670.
- Dehghani R, Mehrpour O, Shahi MP, et al. Epidemiology of venomous and semi-venomous snakebites (Ophidia: Viperidae, Colubridae) in the Kashan city of the Isfahan province in Central Iran. J Res Med Sci. 2014;19(1):33-40. https://www.ncbi.nlm.nih.gov/pubmed/24672563.
- Lamb T, de Haro L, Lonati D, Brvar M, Eddleston M. Antivenom for European Vipera species envenoming. Clin Toxicol . 2017;55(6):557-568. doi:10.1080/15563650.2017.1300261
- Haro L de, de Haro L, Lang J, et al. Envenimations par vipères européennes. Étude multicentrique de tolérance du ViperfavTM, nouvel antivenin par voie intraveineuse. Annales Françaises d’Anesthésie et de Réanimation. 1998;17(7):681-687. doi:10.1016/s0750-7658(98)80105-6
- De Haro L, Lang J, Bedry R, et al. Snake bite by European vipers. A multicenter study of tolerance to Viperfav, a new intravenous antivenom. In: Annales Francaises D’anesthesie et de Reanimation. Vol 17. ; 1998:681-687. https://europepmc.org/article/med/9750806.
- Kurtović T, Brvar M, Grenc D, Lang Balija M, Križaj I, Halassy B. A Single Dose of Viperfav(TM) May Be Inadequate for Vipera Ammodytes snake bite: a case report and pharmacokinetic evaluation. Toxins . 2016;8(8). doi:10.3390/toxins8080244
- Boels D, Hamel JF, Le Roux G, et al. Snake bites by European vipers in Mainland France in 2017-2018: comparison of two antivenoms Viperfav® and Viperatab®. Clin Toxicol . March 2020:1-8. doi:10.1080/15563650.2020.1726377
- de Haro L, Choumet V, Robbe-Vincent A, et al. Vipers with neurotoxic venom in southeastern France: effectiveness of the polyvalent antivenom Viperfav* for the treatment of envenomed patients. Journal of Toxicology-Clinical Toxicology. 1999;37(3):389-390.
- Boels D, Hamel JF, Bretaudeau Deguigne M, Harry P. European viper envenomings: Assessment of ViperfavTM and other symptomatic treatments. Clin Toxicol . 2012;50(3):189-196. doi:10.3109/15563650.2012.660695
- Brvar M, Kurtović T, Grenc D, et al. Vipera ammodytes bites treated with antivenom ViperaTAb: a case series with pharmacokinetic evaluation. Clin Toxicol . 2017;55(4):241-248. doi:10.1080/15563650.2016.1277235
- Casewell NR, Al-Abdulla I, Smith D, Coxon R, Landon J. Immunological cross-reactivity and neutralisation of European viper venoms with the monospecific Vipera berus antivenom ViperaTAb. Toxins . 2014;6(8):2471-2482. doi:10.3390/toxins6082471
- Kurtović T, Brvar M, Grenc D, et al. Vipera ammodites bites treated with antivenom ViperaTAb®: a case series and pharmacokinetic evaluation. In: 2016 Annual Meeting of the Croatian Immunological Society. ; 2016. https://pdfs.semanticscholar.org/0170/0069102950f36c1c575a00191c46977dd091.pdf.
- Debono J, Bos MHA, Frank N, Fry B. Clinical implications of differential antivenom efficacy in neutralising coagulotoxicity produced by venoms from species within the arboreal viperid snake genus Trimeresurus. Toxicol Lett. September 2019. doi:10.1016/j.toxlet.2019.09.003
- Leong PK, Tan CH, Sim SM, et al. Cross neutralization of common Southeast Asian viperid venoms by a Thai polyvalent snake antivenom (Hemato Polyvalent Snake Antivenom). Acta Trop. 2014;132:7-14. doi:10.1016/j.actatropica.2013.12.015
- Tan CH, Liew JL, Tan NH, et al. Cross reactivity and lethality neutralization of venoms of Indonesian Trimeresurus complex species by Thai Green Pit Viper Antivenom. Toxicon. 2017;140:32-37. doi:10.1016/j.toxicon.2017.10.014
- Leong PK, Sim SM, Fung SY, Sumana K, Sitprija V, Tan NH. Cross neutralization of Afro-Asian cobra and Asian krait venoms by a Thai polyvalent snake antivenom (Neuro Polyvalent Snake Antivenom). PLoS Negl Trop Dis. 2012;6(6):e1672. doi:10.1371/journal.pntd.0001672
- Silva A, Hodgson WC, Isbister GK. Cross-neutralisation of in vitro neurotoxicity of Asian and Australian snake neurotoxins and venoms by different antivenoms. Toxins . 2016;8(10). doi:10.3390/toxins8100302
- Leong PK, Fung SY, Tan CH, Sim SM, Tan NH. Immunological cross-reactivity and neutralization of the principal toxins of Naja sumatrana and related cobra venoms by a Thai polyvalent antivenom (Neuro Polyvalent Snake Antivenom). Acta Trop. 2015;149:86-93. doi:10.1016/j.actatropica.2015.05.020
- Chen JC, Bullard MJ, Chiu TF, Ng CJ, Liaw SJ. Risk of immediate effects from F(ab)2 bivalent antivenin in Taiwan. Wilderness Environ Med. 2000;11(3):163-167. doi:10.1580/1080-6032(2000)011[0163:roieff]2.3.co;2
- Mao Y-C, Hung D-Z. Management of Snake Envenomation in Taiwan. Clinical Toxinology in Asia Pacific and Africa. 2015:23-52. doi:10.1007/978-94-007-6386-9_43
- Chen JC, Liaw SJ, Bullard MJ, Chiu TF. Treatment of poisonous snakebites in northern Taiwan. J Formos Med Assoc. 2000;99(2):135-139. https://www.ncbi.nlm.nih.gov/pubmed/10770028.
- Liu C-C, You C-H, Wang P-J, et al. Analysis of the efficacy of Taiwanese freeze-dried neurotoxic antivenom against Naja kaouthia, Naja siamensis and Ophiophagus hannah through proteomics and animal model approaches. PLoS Negl Trop Dis. 2017;11(12):e0006138. doi:10.1371/journal.pntd.0006138
- Lin C-C, Chaou C-H, Tseng C-Y. An investigation of snakebite antivenom usage in Taiwan. J Formos Med Assoc. 2016;115(8):672-677. doi:10.1016/j.jfma.2015.07.006
- Chang K-P, Lai C-S, Lin S-D. Management of poisonous snake bites in southern Taiwan. Kaohsiung J Med Sci. 2007;23(10):511-518. doi:10.1016/S1607-551X(08)70009-3
- Ho C-H, Mao Y-C, Tsai Y-D, et al. Descriptive study of snakebite patients in Northern Taiwan: 2009 to 2016. J Med Sci . 2019;39(3):114. doi:10.4103/jmedsci.jmedsci_68_18
- Mao Y-C, Hung D-Z. Epidemiology of snake envenomation in Taiwan. In: Toxinology. Springer, Dordrecht; 2014:1-17.
- Hsieh Y-H, Hsueh J-H, Liu W-C, et al. Contributing factors for complications and outcomes in patients with snakebite: experience in a medical center in Southern Taiwan. Ann Plast Surg. 2017;78(3 Suppl 2):S32-S36. doi:10.1097/SAP.0000000000001002
- Tomari T. An epidemiological study of the occurrence of Habu snake bite on the Amami Islands, Japan. Int J Epidemiol. 1987;16(3):451-461. doi:10.1093/ije/16.3.451
- Yasunaga H, Horiguchi H, Kuwabara K, Hashimoto H, Matsuda S. Short report: Venomous snake bites in Japan. Am J Trop Med Hyg. 2011;84(1):135-136. doi:10.4269/ajtmh.2011.10-0403
- Hifumi T, Sakai A, Kondo Y, et al. Venomous snake bites: clinical diagnosis and treatment. J Intensive Care Med. 2015;3(1):16. doi:10.1186/s40560-015-0081-8
- Chiba T, Koga H, Kimura N, et al. Clinical Condition and Management of 114 Mamushi (Gloydius blomhoffii) Bites in a General Hospital in Japan. Intern Med. 2018;57(8):1075-1080. doi:10.2169/internalmedicine.9409-17
- Fukuda T, Iwaki M, Hong SH, et al. Standardization of regional reference for mamushi (Gloydius blomhoffii) antivenom in Japan, Korea, and China. Jpn J Infect Dis. 2006;59(1):20-24. https://www.ncbi.nlm.nih.gov/pubmed/16495629.
- Min YG, Ham SH, Jung YS, Choi S. Gaboon viper envenomation: An unexpected injury by non-indigenous snake in South Korea. Turk J Emerg Med. 2018;18(2):75-77. doi:10.1016/j.tjem.2018.04.003
- Senek MZF, Kong SY, Shin SD, Sun KM, Kim J, Ro YS. Epidemiological profile and outcomes of snakebite injuries treated in emergency departments in South Korea, 2011-2016: a descriptive study. Trans R Soc Trop Med Hyg. 2019;113(10):590-598. doi:10.1093/trstmh/trz050
- Kim ES, Choi WJ. Clinical review of venomous snake bite. J Korean Surg Soc. 2000;59(4):433-440. https://www.komci.org/GSResult.php?RID=0037JKSS%2F2000.59.4.433&DT=6.
- Lim H, Kang HG, Kim KH. Antivenom for snake bite in Korea. Journal of the Korean Medical Association/Taehan Uisa Hyophoe Chi. 2013;56(12). http://search.ebscohost.com/login.aspx?direct=true&profile=ehost&scope=site&authtype=crawler&jrnl=19758456&AN=97769554&h=aCL3DOIU4Hd42wlqYcgdgZj%2FBGL85TNYqaRzpVEugU8VMNFsJPUh89ow7KIxuquHIM1uSTGZjlV9DyrrRuZQxw%3D%3D&crl=c.
- Rha JH, Kwon SM, Oh JR, Han BK, Lee KH, Kim JH. Snakebite in Korea: A Guideline to Primary Surgical Management. Yonsei Med J. 2015;56(5):1443-1448. doi:10.3349/ymj.2015.56.5.1443
- Baxter EH, Gallichio HA. Cross-neutralization by tiger snake (Notechis scutatus) antivenene and sea snake (Enhydrina schistosa) antivenene against several sea snake venoms. Toxicon. 1974;12(3):273-278. doi:10.1016/0041-0101(74)90069-5.
- Auerbach PS, Cushing TA, Stuart Harris N. Auerbach’s Wilderness Medicine E-Book. Elsevier Health Sciences; 2016.
- Tan CH, Tan KY, Tan NH. Revisiting Notechis scutatus venom: on shotgun proteomics and neutralization by the “bivalent” Sea Snake Antivenom. J Proteomics. 2016;144:33-38. doi:10.1016/j.jprot.2016.06.004.
- Tan CH, Tan NH, Tan KY, Kwong KO. Antivenom cross-neutralization of the venoms of Hydrophis schistosus and Hydrophis curtus, two common sea snakes in Malaysian waters. Toxins . 2015;7(2):572-581. doi:10.3390/toxins7020572.
- White J. A Clinician’s Guide to Australian Venomous Bites and Stings: Incorporating the Updated CSL Antivenom Handbook. Australia: bioCSL Pty Ltd; 2013.
- Jensen S. Treatment Overview. In: Clinical Management of Snakebite in Papua New Guinea.
- Trevett AJ, Lalloo DG, Nwokolo NC, et al. The efficacy of antivenom in the treatment of bites by the Papuan taipan (Oxyuranus scutellatus canni). Trans R Soc Trop Med Hyg. 1995;89(3):322-325. doi:10.1016/0035-9203(95)90562-6
- Winkel KD, Mc Gain F, Nimorakiotakis B, Williams D. The role and use of antivenom in Papua New Guinea.
- Kanaan NC, Ray J, Stewart M, et al. Wilderness Medical Society Practice Guidelines for the Treatment of Pitviper Envenomations in the United States and Canada. Wilderness Environ Med. 2015;26(4):472-487. doi:10.1016/j.wem.2015.05.007
- Bush SP, Green SM, Moynihan JA, Hayes WK, Cardwell MD. Crotalidae polyvalent immune Fab (ovine) antivenom is efficacious for envenomations by Southern Pacific rattlesnakes (Crotalus helleri). Ann Emerg Med. 2002;40(6):619-624. doi:10.1067/mem.2002.129939
- Curran-Sills G, Kroeker J. Venomous snakebites in Canada: a national review of patient epidemiology and antivenom usage. Wilderness Environ Med. 2018;29(4):437-445. doi:10.1016/j.wem.2018.06.005
- Wood A, Schauben J, Thundiyil J, et al. Review of Eastern coral snake (Micrurus fulvius fulvius) exposures managed by the Florida Poison Information Center Network: 1998-2010. Clin Toxicol . 2013;51(8):783-788. doi:10.3109/15563650.2013.828841
- Otero-Patiño R, Silva-Haad JJ, Acevedo MJB, et al. Accidente bothrópico en Colombia: estudio multicéntrico de la eficacia seguridad de Antivipmyn-Tri®, un antiveneno polivalente producido en México. Iatreia. 2007;20(3):244-262. https://www.redalyc.org/articulo.oa?id=180513858002.
- Resiere D, Villalta M, Arias AS, et al. Snakebite envenoming in French Guiana: Assessment of the preclinical efficacy against the venom of Bothrops atrox of two polyspecific antivenoms. Toxicon. 2020;173:1-4. doi:10.1016/j.toxicon.2019.11.001
- Baum RA, Bronner J, Akpunonu PDS, Plott J, Bailey AM, Keyler DE. Crotalus durissus terrificus (viperidae; crotalinae) envenomation: Respiratory failure and treatment with antivipmyn TRI® antivenom. Toxicon. 2019;163:32-35. doi:10.1016/j.toxicon.2019.03.009
- Williams KL, Woslager M, Garland SL, Barton RP, Banner W. Use of polyvalent equine anti-viper serum to treat delayed coagulopathy due to suspected Sistrurus miliarius streckeri envenomation in two children. Clin Toxicol . 2017;55(5):326-331. doi:10.1080/15563650.2017.1284334
- Baum RA, Bronner J, Akpunonu PDS, Keyler DE. Crotalus durissus terrificus (Viperidae; Crotalinae) envenomation and treatment with Antivipmyn TRI® antivenom. Toxicon. 2018;150:328.
- Yang DC, Dobson J, Cochran C, et al. The bold and the beautiful: a neurotoxicity comparison of New World Coral Snakes in the Micruroides and Micrurus Genera and relative neutralization by antivenom. Neurotoxicity Research. 2017;32(3):487-495. doi:10.1007/s12640-017-9771-4
- de Roodt AR, Paniagua-Solis JF, Dolab JA, et al. Effectiveness of two common antivenoms for North, Central, and South American Micrurus envenomations. J Toxicol Clin Toxicol. 2004;42(2):171-178. doi:10.1081/clt-120030943
- Pérez ML, Fox K, Schaer M. A retrospective evaluation of coral snake envenomation in dogs and cats: 20 cases (1996--2011). J Vet Emerg Crit Care . 2012;22(6):682-689. https://onlinelibrary.wiley.com/doi/abs/10.1111/j.1476-4431.2012.00806.x.
- Sánchez EE, Lopez-Johnston JC, Rodríguez-Acosta A, Pérez JC. Neutralization of two North American coral snake venoms with United States and Mexican antivenoms. Toxicon. 2008;51(2):297-303. doi:10.1016/j.toxicon.2007.10.004
- Castillo-Beltrán MC, Hurtado-Gómez JP, Corredor-Espinel V, Ruiz-Gómez FJ. A polyvalent coral snake antivenom with broad neutralization capacity. PLoS Negl Trop Dis. 2019;13(3):e0007250. doi:10.1371/journal.pntd.0007250
Додаток А: Тест на згортання цільної крові (Whole Blood Clotting Test, WBCT)
Тест на згортання цільної крові при коагулопатіях споживання, індукованих отрутою
Тест на згортання цільної крові (WBCT) - це просте, але важливе, обстеження, яке можна виконати біля ліжка хворого. Тест використовується для загальної оцінки, діагностики та терапевтичного моніторингу пацієнтів із укусами змій у країнах, що розвиваються, та віддалених районах.1-10 Інструкції з проведення тесту наведені нижче. На 20-й і 30-й хвилинах пробірку обережно піднімають і нахиляють на 90 градусів; стійкий щільний згусток, що утримується на місці всередині пробірки, оцінюється як "0-й ступінь" і вказує на нормальну коагуляцію. Патологічні результати оцінюються як "1-й ступінь" - для не повністю сформованого, напівщільного згустка, який розпадається на частини і відокремлюється від стінок скляної пробірки незабаром після її перевертання, або "2-й ступінь" - для рідкої крові, яка не згорнулась і одразу витікає з пробірки після її перевертання. Спроба оцінити тест раніше, ніж через 20 хвилин, не дасть точних результатів через патофізіологічний механізм коагулопатії споживання. Використання здорового донора в якості контролю ідеально підходить для підтвердження сумнівних результатів.
Проводьте WBCT впродовж усього курсу лікування, щоб контролювати вторинне виникнення коагулопатії споживання, індукованої отрутою.11-13 Після досягнення контролю над отруєнням, проводьте WBCT кожні 24 години протягом всього курсу госпіталізації. Важливо пам'ятати, що WBCT слід інтерпретувати в контексті клінічної картини. Якщо у пацієнта покращилися всі параметри, за винятком стійкого патологічного WBCT, це може відображати сповільнене поповнення використаних факторів згортання крові після важкого гемотоксичного синдрому.1 Якщо отрута активна, то гематокрит буде і надалі знижуватися, або будуть ознаки триваючого гемолізу або кровотечі.
Тест на згортання цільної крові (WBCT)

Література
- Benjamin JM, Chippaux J-P, Sambo BT, Massougbodji A. Delayed double reading of whole blood clotting test (WBCT) results at 20 and 30 minutes enhances diagnosis and treatment of viper envenomation. J Venom Anim Toxins Incl Trop Dis. 2018;24:14. doi:10.1186/s40409-018-0151-1
- Sano-Martins IS, Fan HW, Castro SCB, et al. Reliability of the simple 20 minute whole blood clotting test (WBCT20) as an indicator of low plasma fibrinogen concentration in patients envenomed by Bothrops snakes. Toxicon. 1994;32(9):1045-1050. doi:10.1016/0041-0101(94)90388-3
- Gaus DP, Herrera DF, Troya CJ, Guevara AH. Management of snakebite and systemic envenomation in rural Ecuador using the 20-minute whole blood clotting test. Wilderness Environ Med. 2013;24(4):345-350. doi:10.1016/j.wem.2013.08.001
- Chippaux JP, Amadi-Eddine S, Fagot P. Diagnosis and monitoring of hemorrhage due to viper envenomation in the African savanna. Bull Soc Pathol Exot. 1999;92(2):109-113. https://www.ncbi.nlm.nih.gov/pubmed/10399601.
- Madaki JKA, Obilom R, Mandong BM. Clinical presentation and outcome of snake-bite patients at Zamko Comprehensive Health Centre, Langtang, Plateau State. Highland Medical Research Journal. 2004;2(2):61-68. https://www.ajol.info/index.php/hmrj/article/view/33855. Accessed December 29, 2019.
- Dsilva AA, Basheer A, Thomas K. Snake envenomation: is the 20 min whole blood clotting test (WBCT20) the optimum test for management? QJM. 2019;112(8):575-579. doi:10.1093/qjmed/hcz077
- Ratnayake I, Shihana F, Dissanayake DM, Buckley NA, Maduwage K, Isbister GK. Performance of the 20-minute whole blood clotting test in detecting venom induced consumption coagulopathy from Russell’s viper (Daboia russelii) bites. Thromb Haemost. 2017;117(3):500-507. doi:10.1160/TH16-10-0769
- Isbister GK, Maduwage K, Shahmy S, et al. Diagnostic 20-min whole blood clotting test in Russell’s viper envenoming delays antivenom administration. QJM. 2013;106(10):925-932. doi:10.1093/qjmed/hct102
- Punguyire D, Iserson KV, Stolz U, Apanga S. Bedside whole-blood clotting times: validity after snakebites. J Emerg Med. 2013;44(3):663-667. doi:10.1016/j.jemermed.2012.07.073
- Bawaskar HS, Bawaskar PH. Profile of snakebite envenoming in western Maharashtra, India. Trans R Soc Trop Med Hyg. 2002;96(1):79-84. doi:10.1016/s0035-9203(02)90250-6
- Benjamin JM, Abo BN, Brandehoff N. Review Article: Snake Envenomation in Africa. Current Tropical Medicine Reports. January 2020. doi:10.1007/s40475-020-00198-y
- Benjamin JM, Chippaux J-P, Tamou-Sambo B, Akpakpa OC, Massougbodji A. successful management of two patients with intracranial hemorrhage due to carpet viper (Echis ocellatus) envenomation in a limited-resource environment. Wilderness Environ Med. June 2019. doi:10.1016/j.wem.2019.04.003
- Lial JP. Health assessments of a military company stationed on the Maroni River in French Guiana. Med Trop . 1999;59(1):95-98. https://www.ncbi.nlm.nih.gov/pubmed/10472589.
Додаток В: Додаткова інформація щодо не передбаченого інструкцією застосування лікарських засобів у Настановах з клінічної практики
Мета
Мета цього Додатка — надати роз'яснення політики та практики Міністерства оборони США щодо включення в Настанови з клінічної практики «незатверджених» показів для продуктів, які були схвалені Управлінням з контролю якості продуктів харчування і лікарських засобів США (FDA). Це стосується використання препаратів не за призначенням для пацієнтів, які належать до Збройних сил США.
Вихідна інформація
Незатверджене (тобто «не за призначенням» - "off-label") використання продуктів, схвалених FDA, надзвичайно поширене в медицині США і зазвичай не регулюється окремими нормативними актами. Проте, згідно з Федеральним законодавством, за деяких обставин застосування схвалених лікарських засобів за незатвердженими показами регулюється положеннями FDA про «досліджувані нові ліки». До цих обставин належить використання в рамках клінічних досліджень, а також, у військовому контексті, використання за незатвердженими показами згідно з вимогами командування. Деякі види використання за незатвердженими показами також можуть підлягати окремим нормативним актам.
Додаткова інформація щодо застосування за незатвердженими показами у Настановах з клінічної практики
Включення до Настанов з клінічної практики використання медикаментів за незатвердженими показами не належить до клінічних випробувань і не є вимогою командування. Більше того, таке включення не передбачає, що Військова система охорони здоров'я вимагає від медичних працівників, які працюють в структурах Міноборони США, застосовувати відповідні продукти за незатвердженими показами або вважає це «стандартом медичної допомоги». Швидше, включення до CPGs використання засобів «не за призначенням» має поглиблювати клінічне судження відповідального медичного працівника шляхом надання інформації щодо потенційних ризиків та переваг альтернативного лікування. Рішення приймається на основі клінічного судження відповідальним медичним працівником у контексті відносин між лікарем і пацієнтом.
Додаткові процедури
Виважений розгляд
Відповідно до цієї мети, в обговореннях використання медикаментів «не за призначенням» в CPG конкретно зазначено, що це використання, яке не схвалено FDA. Крім того, такі обговорення є збалансованими у представленні даних клінічних досліджень, включаючи будь-які дані, які свідчать про обережність у використанні продукту, і, зокрема, включаючи усі попередження, видані FDA.
Моніторинг забезпечення якості
Що стосується використання «не за призначенням», діяльність Міністерства оборони США полягає у підтримці регулярної системи моніторингу забезпечення якості результатів і відомих потенційних побічних ефектів. З цієї причини підкреслюється важливість ведення точних клінічних записів.
Інформація для пацієнтів
Належна клінічна практика передбачає надання відповідної інформації пацієнтам. У кожних Настановах з клінічної практики, де йдеться про використання засобу «не за призначенням», розглядається питання інформування пацієнтів. За умови практичної доцільності, слід розглянути можливість включення додатка з інформаційним листком для пацієнтів, що видаватиметься до або після застосування продукту. Інформаційний листок має в доступній для пацієнтів формі повідомляти наступне: a) що дане застосування не схвалене FDA; b) причини, чому медичний працівник Міністерства оборони США може прийняти рішення використати продукт з цією метою; c) потенційні ризики, пов'язані з таким застосуванням.







































