Вступ
Відомо, що пацієнти з травмами мають високий ризик розвитку венозної тромбоемболії (ВТЕ), включаючи тромбоз глибоких вен (ТГВ) і тромбоемболію легеневої артерії (ТЕЛА). Частота ТГВ у пацієнтів зі значними травмами може сягати до 58%.1 Севітт і Галлахер (Sevitt and Gallagher) повідомили про навіть вищу частоту (65%) серед пацієнтів з травмами та опіками, а також про 16,5% випадків ТЕЛА, виявлених на розтині у цій когорті пацієнтів.2,3
На додаток до гіперкоагуляції, спричиненої важким травматичним ушкодженням, поранені бійці мають додаткові фактори ризику розвитку ТГВ, включаючи:1,4-8
- Раннє переливання препаратів крові (≤24 годин);
- Переливання «старої» крові (заготовленої ≥28 днів);
- Множинні ампутації та/або ампутації вище коліна
Використання свіжозамороженої плазми (СЗП) поза переливанням великого об’єму препаратів крові (менше 4 ОД еритроцитарної маси) підвищує ризик ВТЕ.9 За умови досягнення якісного гемостазу рекомендується проведення ранньої профілактики у цій групі пацієнтів.
Особливості нинішнього театру бойових дій забезпечили нашим військовим медикам широкі можливості з надання допомоги пораненим внаслідок військових конфліктів дітям. Розвиток у них ТГВ після травми є значно нижчим (6,2%), ніж зареєстрований серед дорослих, описаних у цивільній літературі.10 Хоча, присутність множинних факторів ризику в педіатричних пацієнтів із травмами, включаючи знерухомлення та наявність центрального венозного катетера, асоціювалася з підвищеним ризиком розвитку ТГВ.
Зростає настороженість щодо ймовірності розвитку ТГВ в осіб, які здійснюють тривалі подорожі літаком. Одне з досліджень відзначило 10%-у поширеність безсимптомного ТГВ серед осіб, які перебували у польотах тривалістю 8 годин або більше.11 Поранені бійці мають високий ризик розвитку ВТЕ під час періоду одужання та евакуації; він може бути пов’язаний з тривалими польотами та знерухомленням, тому важливо розпочати профілактику ВТЕ за першої ж клінічної можливості.12
Регіональний медичний центр міста Ландштуль має унікальне розташування, приймаючи пацієнтів, які зазнали тривалих переміщень до моменту госпіталізації.
Різні медичні товариства та робочі групи публікували різноманітні рекомендації щодо профілактики ТГВ.13,14 Дані клінічні настанови представляють або рекомендації з вищим рівнем доказовості на їх підтвердження, або більш консервативні рекомендації. Профілактику розвитку ТГВ рекомендується починати одразу після успішної корекції коагулопатії у пацієнтів, що не мають підвищеного ризику кровотечі.
Рекомендації щодо профілактики тромбозу глибоких вен
За відсутності протипоказань, пов'язаних із пошкодженням нижньої кінцівки, усі пацієнти з травмами повинні отримати:
- Терапію за допомогою пристрою переміжної пневматичної компресії (ППК, англ. Sequential Compression Device (SCD)) як первинну профілактику ТГВ на додаток до;
- Низької дози нефракціонованого гепарину (НФГ)13-15; або
- Низькомолекулярного гепарину (НМГ) - напр., еноксапарин 30 мг підшкірно двічі на день.
- Як альтернативу, щодня можна призначати низьку дозу НМГ, напр., дальтепарин 5000 ОД підшкірно або еноксапарин 40 мг підшкірно 1 раз на день. В одному з досліджень було виявлено нижчу частоту появи ТГВ серед пацієнтів у післяопераційному періоді з таким дозуванням, порівняно з дозою 30 мг 2 рази на добу.14,17,18
- Було продемонстровано, що НФГ (5000 ОД), який вводиться підшкірно 3 рази на день, є таким же ефективним, або, принаймні, нічим не поступається еноксапарину у профілактиці ТГВ серед пацієнтів із травмами.19,20
Слід обдумати можливість застосування НМГ у пацієнтів із порушенням функції нирок (кліренс креатиніну [КК] =30 мл/хв або менше), оскільки існує занепокоєння щодо накопичення НМГ та підвищення ризику кровотечі.
- Незважаючи на це занепокоєння, немає чітких доказів щодо модифікації дози або протипоказань до використання НМГ для профілактики ТГВ у пацієнтів із порушенням функції нирок.21
- Однак Годат та співавт. (Godat et al.) повідомили, що пацієнти з травмами, які вважаються групою найвищого ризику розвитку ВТЕ (особливо у випадку травми спинного мозку з або без перелому таза), протягом перших трьох місяців після поранення мають найбільший ризик, а також те, що цей ризик зменшується через шість місяців після отримання травми.23
Дуплексне ультразвукове сканування як метод діагностики ТГВ слід залишити для симптоматичних пацієнтів. Проведення серійного дуплексного УЗД для діагностики ТГВ не рекомендується.14
Фармакологічна профілактика тромбозу глибоких вен
За умови зупинки кровотечі та корекції коагулопатії фармакологічна профілактика ТГВ після отримання тупих травм паренхіматозних органів (<48 годин після травми) при дослідженнях виявилася безпечною.
Проведення фармакологічної профілактики ТГВ (<48-72 годин) у випадку черепно-мозкової травми (ЧМТ) з внутрішньочерепним крововиливом не посилює внутрішньочерепну кровотечу.26,27 Перед початком фармакологічної профілактики ТГВ вам слід:
- Отримати консультацію нейрохірурга.
- Отримати стабільні* зображення КТ голови через 24 години після травми.
[*Тобто зображення, на яких відсутні зміни, порівняно з попереднім скануванням; усі патологічні процеси (напр., кровотеча) зупинились і більше не прогресують. - Ред.]
Слід припинити профілактику за умови прогресування внутрішньочерепної кровотечі або за наявності встановленого монітора внутрішньочерепного тиску.
Заміна дози еноксапарину на 40 мг на добу в поранених, які потребують знеболення за допомогою епідурального катетера, не збільшує частоту венозної тромбоемболії.28
Встановлення кава-фільтра (IVCF) у зоні бойових дій може бути використане для:
- Первинної профілактики (немає ознак ВТЕ на момент встановлення).
- Вторинної профілактики (задокументований ТГВ) ТЕЛА у пацієнта з політравмою.
Пацієнти, які вважаються групою особливо високого ризику розвитку ВТЕ, проте мають клінічні протипоказання до профілактичного використання антикоагулянтів, є найімовірнішими кандидатами на встановлення кава-фільтра.
Більшість серійних досліджень, які вивчали використання кава-фільтрів для первинної профілактики ТЕЛА у пацієнтів із травмою, підтверджують низьку частоту подальших епізодів ТЕЛА (1,6%), хоча дослідження мають різний дизайн, а також неможливо досягти стійкого консенсусу на підтримку цієї клінічної практики на основі доступних даних.29
Немає жодних доказів того, що профілактичне застосування кава-фільтра пов’язане зі зниженням частоти ТЕЛА або зниженням показника летальності внаслідок даного стану. Слід зазначити, що кава-фільтр встановлюється для запобігання розвитку СМЕРТЕЛЬНОЇ легеневої емболії, оскільки виникнення ТГВ і ТЕЛА повністю не виключається.30-34
Кава-фільтр не має переваг у профілактиці ТГВ і може бути пов’язаний із розвитком тромбозу нижньої порожнистої вени та глибоких вен нижніх кінцівок.14,35
Знімний кава-фільтр ( RIVCF)
Переважна більшість кава-фільтрів, які встановлюються у зоні бойових дій, є знімними (Retrievable Inferior Vena Cava Filter, RIVCF)
Знімному кава-фільтру надають перевагу, щоб уникнути деяких віддалених ускладнень, які пов’язані зі встановленням кава-фільтра. Крім того, багато пацієнтів потребують такої форми профілактики ВТЕ лише протягом визначеного часу одразу після отримання травми.
Незважаючи на успішне видалення кава-фільтра після 180 днів від його встановлення, а також високий успіх і низький рівень ускладнень при його видаленні, частота остаточного видалення фільтра, зазначена у багатьох дослідженнях пацієнтів із травмами в Сполучених Штатах, складала лише від 14% до 22%.36,37,38,39,40
Загальний показник видалення знімних кава-фільтрів, встановлених пораненим бійцям під час операції «Свобода Іраку» (Operation Iraqi Freedom, OIF) та операції «Нескорена свобода» в Афганістані (Operation Enduring Freedom, OEF), складав 18%.41
Однак, слід зазначити, що більшість пацієнтів була втрачена з-під спостереження, або ж їм не було видалено фільтри через тривалі показання до застосування (82%). Таким чином, технічно, загальний показник успішних видалень може бути набагато вищим. Більшість серійних досліджень підтримує видалення найбільш поширених знімних кава-фільтрів, щойно зникає потреба у їх використанні, але не пізніше, ніж приблизно за три місяці.42 Хоча існує можливість усунення будь-якого з них пізніше даного періоду, технічний успіх процедури значно знижується через зростання появи потенційних ускладнень, пов’язаних із видаленням. Для покращення показників успішного видалення кава-фільтрів та мінімізації втрат осіб з-під спостереження, у військово-медичних закладах континентальних штатів США, де бійцям надається остаточна допомога, повинна існувати чітка електронна документація та спеціальна система відстеження.43
Навчання та лікування
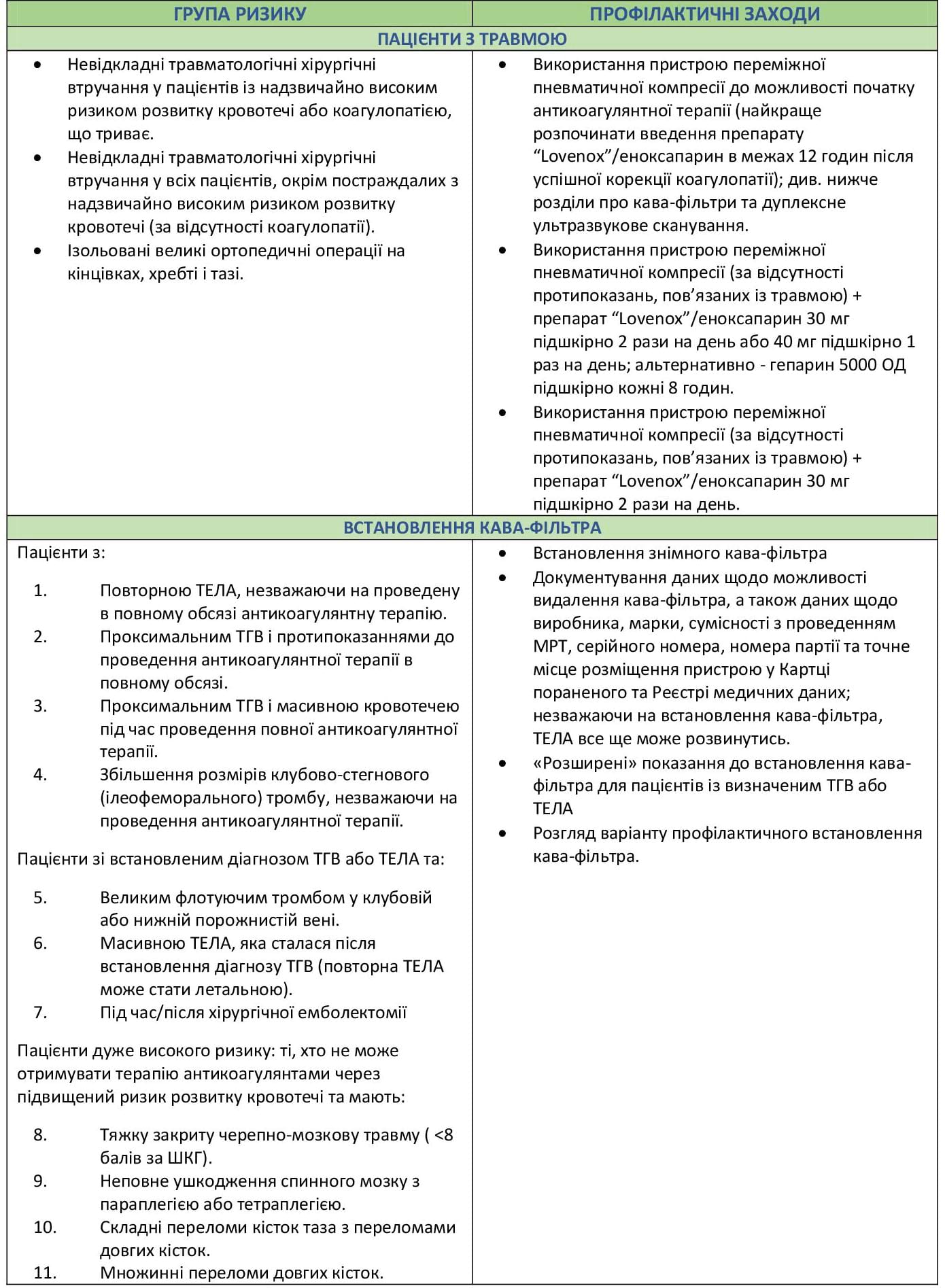
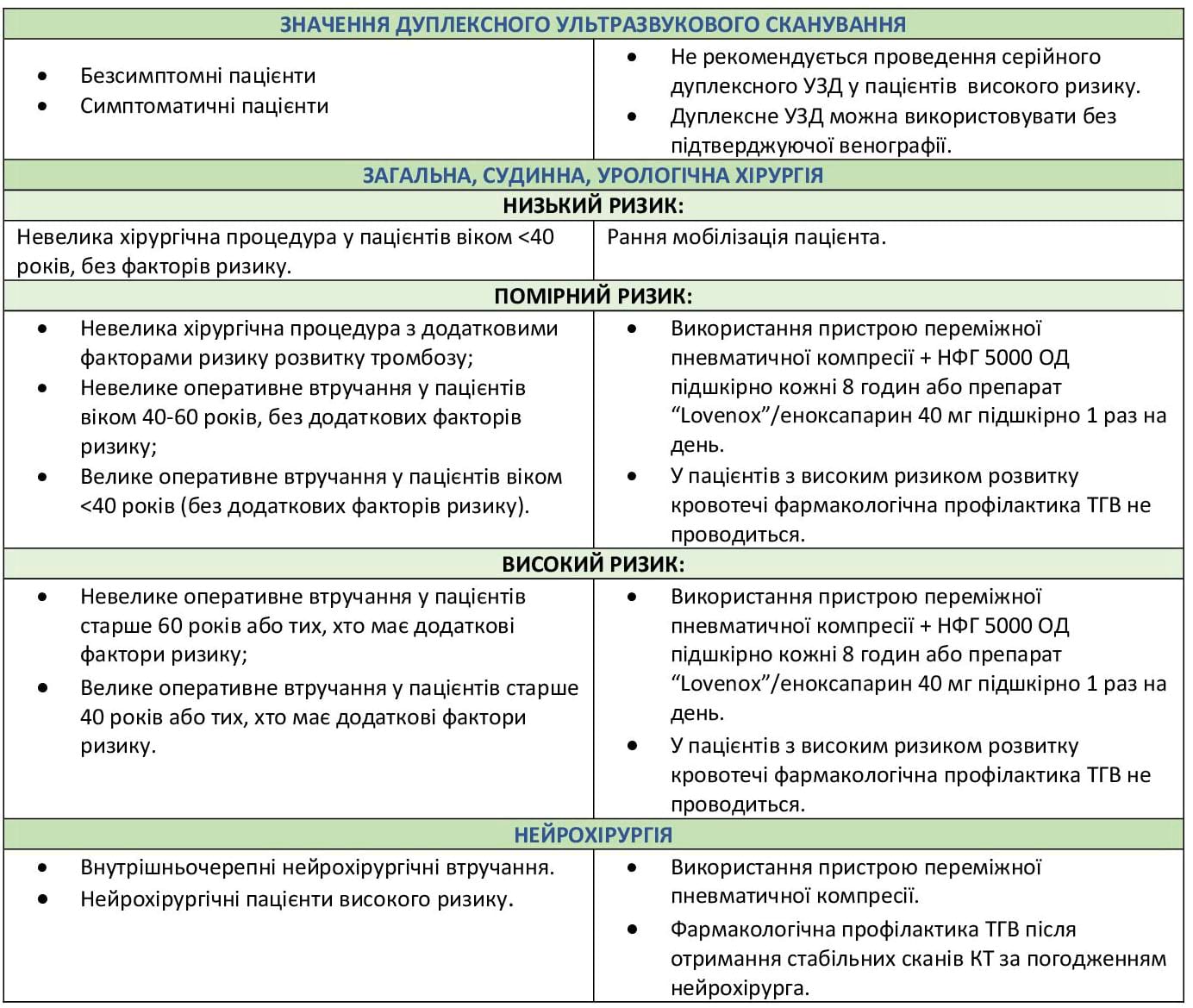
Дивіться Додаток A щодо конкретних настанов для роботи з групами пацієнтів після різних хірургічних втручань.
Дивіться Додаток B для додаткових рекомендацій щодо використання кава-фільтрів.
Особливості аеромедичної евакуації
- Аеромедична евакуація (AE) з будь-якої Зони відповідальності Збройних сил США до континентальної частини Сполучених Штатів може вимагати кількох рейсів протягом кількох днів до моменту прибуття пацієнта в кінцевий пункт призначення.
- Існує чіткий зв’язок між далекими подорожами та підвищеним ризиком розвитку ВТЕ, навіть у «здорових мандрівників».
- Навантаження під час польоту, такі як тривале знерухомлення та знижена вологість, можуть сприяти розвитку ВТЕ, особливо в групах осіб, які вже належать до високого ризику (особи, які мають травми, нещодавно перенесені операції, переломи довгих кісток, курці, вагітні або жінки у післяпологовому періоді, хворі, які нещодавно перенесли інфаркт міокарда, хворі з активним раком, особи з накладеною шиною або гіпсом тощо).
- Профілактика має важливе значення для зниження ризику захворюваності та смертності, пов’язаної з ВТЕ, у всіх пацієнтів, що підлягають аеромедичній евакуації (АЕ).
- Команда АЕ кожні 2 години повинна заохочувати пацієнтів до руху/ходьби, якщо дозволяє їх стан.
- За відсутності протипоказань, пов'язаних із характером травми, використання пристрою переміжної пневматичної компресії має бути універсальним для стаціонарних пацієнтів. Для використання у військових літаках затверджена система компресії Kendal SCD Express.
- Як зазначено вище, для всіх госпіталізованих пацієнтів з травмою або пацієнтів терапевтичного профілю також рекомендована фармакологічна профілактика ВТЕ, за виключенням наявних протипоказань, пов'язаних з медичним станом, таким як незупинена кровотеча або коагулопатія.
- Пацієнти з ВІДОМОЮ гострою ВТЕ, що підлягають АЕ, повинні пройти лікування до початку польоту (якщо для лікування немає чітких протипоказань).
- Лікування залежить від клінічної ситуації, але може включати низькомолекулярний гепарин, фондапаринукс, пероральні інгібітори фактора Xa або нефракціонований гепарин.
- За потреби в підтримувальних заходах під час АЕ пацієнтам з відомою ВТЕ повинні бути доступні кисень та безперервний моніторинг оксигенації за допомогою пульсоксиметра.
- У разі відомої або підозрюваної ТЕЛА слід розглянути можливість обмеження висоти польоту літака, щоб зменшити негативний вплив висоти на оксигенацію та дихання.
- Також у випадках ТЕЛА зі значними респіраторними або гемодинамічними порушеннями слід розглянути залучення аеромедичної бригади інтенсивної терапії (ССАТ).
Моніторинг покращення ефективності (ПЕ)
Досліджувана група
Усі пацієнти з травмами, госпіталізовані на 2 етапі медичної допомоги або вище.
Мета (очікувані результати)
- Усі пацієнти в досліджуваній групі отримують профілактику ТГВ за допомогою пристрою переміжної пневматичної компресії протягом 24 годин після отримання травми.
- Усім пацієнтам у досліджуваній групі, розпочинають хіміопрофілактику (гепарин, препарат «Lovenox») в межах 48 годин після отримання травми, або документують протипоказання до даної процедури.
- При встановленні кава-фільтра, у медичній карті повинна бути інформація щодо показань до процедури, можливість видалення кава-фільтра, дані про виробника, марку, серійний номер, номер партії та точне місце розміщення пристрою.
- Знімні кава-фільтри видаляються в межах 6 місяців.
Показники результативності/ дотримання рекомендацій
- Кількість та відсоток пацієнтів у досліджуваній групі, які розпочали профілактику ТГВ із застосуванням пристрою переміжної пневматичної компресії в межах 24 годин після отримання травми.
- Кількість та відсоток пацієнтів у досліджуваній групі, які отримали хіміопрофілактику ТГВ в межах 48 годин (гепарин, препарат «Lovenox»/еноксапарин) або мають задокументовані протипоказання до її проведення.
- Кількість та відсоток пацієнтів, яким було встановлено кава-фільтр, та які мають задокументовану інформацію щодо показань до проведення процедури, можливості усунення кава-фільтра, даних про виробника, марку, серійний номер, номер партії та точне місце розміщення пристрою.
- Кількість та відсоток встановлених знімних кава-фільтрів, видалених протягом 6 місяців.
Джерела даних
- Медична картка пацієнта
- Реєстр травм Міністерства оборони США (DoDTR)
Системна звітність та її частота
- Згідно з даними настановами, вказане вище становить мінімальні критерії моніторингу ПЕ. Системна звітність проводитиметься щороку; додатковий моніторинг ПЕ та системну звітність можна проводити залежно від потреб.
- Системний огляд та аналіз даних виконуватиме керівник JTS та відділ ПЕ JTS.
Обов'язки
Керівник команди з надання допомоги при травмах відповідає за ознайомлення з даними Настановами з клінічної практики, належне дотримання вказаних у ній вимог та моніторинг ПЕ на місцевому рівні.
Усі медичні працівники повинні:
- Ознайомитися з настановами щодо профілактики ТГВ (див. Додаток А).
- Належним чином надати допомогу пацієнтам, які можуть підлягати ризику розвитку ТГВ.
- Надати зворотний зв’язок щодо цих настанов та пропозиції щодо змін документа керівнику Об'єднаної системи лікування травм.
Старший хірург та/або лікар інтенсивної терапії кожного закладу 3 етапу медичної допомоги має:
- Переглянути всі випадки тромбоемболії в установі 3 рівня, щоб оцінити шляхи зниження ризику її розвитку для пацієнта.
- Разом із керівником відділу покращення ефективності Об'єднаної системи лікування травм аналізувати відповідність настанов, які використовуються, і, за потреби, надавати інформацію для їх оновлення.
-
- Geerts WH, Code KJ, Jay RM, et al: A prospective study of venous thromboembolism after major trauma. N Engl J Med 1994;331(24):1601-1606.
- Sevitt S, Gallagher N. Venous thrombosis and pulmonary embolism. A clinico-pathological study in injured and burned patients. Br J Surg 1961;48:475-489.
- Godat LN Kobayashi L, Chang DC et al. Can we ever stop worrying about venous thromboembolism after trauma? J Trauma 2015;78(3):475-480.
- Differding JA, Underwood SJ, Van PY, et al. Trauma induces a hypercoagulable state that is resistant to hypothermia as measured by thromboelastogram. Am J Surg 2011;201(5):587-591.
- Gearhart MM, Luchette FA, Proctor MC, et al. The risk assessment profile score identifies trauma patients at risk for deep venous thrombosis. Surgery 2000;128(4):631-637.
- Spinella PC, Carroll CL, Staff I, et al. Duration of red blood cell storage is associated increased incidence of deep venous thrombosis and in hospital mortality in patients with traumatic injuries. Critical Care 2009;13(5):R151.
- Hutchinson TN, Krueger CA, Berry, JS, et al. Venous thromboembolism during combat operations: a 10-y review. J Surg Res 2014;187(2):625-630.
- Knudson MM: Thromboembolism after trauma: an analysis of 1602 episodes from the American College of Surgeons National Trauma Data Bank. Ann Surg 2004: 490-496.
- Zander AL, Olson EJ, Van Gent JM, et al. Does resuscitation with plasma increase the risk of venous thromboembolism? J Trauma 2015;78(1):39-43.
- Hanson SJ, Punzalan RC, Greenup RA, et al. Incidence and risk factors for venous thromboembolism in critically ill children after trauma. J Trauma 2010;68(1):52-56.
- Scurr JH; Machin SJ; Bailey-King S; Mackie IJ; McDonald S; Smith PD, “Frequency and Prevention of Symptom-less Deep Venous Thrombosis in Long Haul Flights: A Randomized Trial, Lancet 2001; 357:1485-1489.
- Holley AB, Petteys S, Mitchell JD, et al. Thromboprophylaxis and VTE rates in soldiers wounded in Operation Enduring Freedom and Operation Iraqi Freedom. Chest 2013;144(3):966-973.
- Rogers FB, Cipolle MD, Velmahos G, et al. Practice management guidelines for the prevention of venous thromboembolism in trauma patients: the EAST practice management guidelines work group. J Trauma 2002;53(1):142-164.
- Guyatt GH, Akl EA, Crowther M, et al. Antithrombotic therapy and prevention of thrombosis, 9th edition: American College of Chest Physicians evidence based clinical practice guidelines. Chest 2012;141;(2)7S-47S.
- Kakkos SK, Caprini JA, Geroulakos G, et al. Combined intermittent leg compression and pharmacological prophylaxis for the prevention of venous thromboembolism in high risk patients. Cochrane Database Syst Rev 2008, Issue 4. Art No. CD005258.
- Geerts WH, Jay RM, Code KJ, et al: A comparison of low-dose heparin with low-molecular weight heparin as prophylaxis against venous thromboembolism after major trauma. N Engl J Med 335:701-7, 1996.
- Cothren CC, Smith WR, Moore EE, et al. Utility of once-daily dose of low-molecular weight heparin to prevent venous thromboembolism in multisystem trauma patients. World J Surg 2007;31(1):98-104.
- Riha GM, Van PY, Differding JA, et al. Incidence of deep venous thrombosis is increased with 30 mg twice daily dosing of enoxaparin compared with 40 mg daily. AM J Surg 2012;203(5):598-602.
- Arnold JD, Dart BW, Barker DE, et al. Unfractionated heparin three times a day versus enoxaparin in the prevention of deep venous thrombosis in trauma patients. Am Surg 2010;76(6):563-570.
- Olson EJ, Bandle J, Calvo RY, et al. Heparin versus enoxaparin for prevention of thromboembolism after trauma: A randomized noninferiority trial. J Trauma. 2015;79(6):961-969.
- Nagge J, Crowther M, Hirsh J. Is impaired renal function a contraindication to the use of low molecular-weight heparin? Arch Int Med 2002;162(22):2605-2609.
- Lim W, Dentali F, Eikelboom JW, et al. Meta-analysis: low-molecular weight heparin and bleeding in patients with severe renal insufficiency. Ann Int Med 2006;144(9):673-684.
- Godat LN, Kobayashi L, Chang DC, et al. Can we ever stop worrying about venous thromboembolism after trauma? J Trauma. 2015;78(3):475-481.
- Rostas JW, Manley J, Gonzalez RP, et al. The safety of low molecular weight heparin after blunt liver and spleen injuries. Am J Surg 2015 Jul;210(1):31-34.
- Joseph B, Pandit V, Harrison C, et al. Early thromboembolic prophylaxis in patients with blunt solid abdominal organ injuries undergoing nonoperative management: is it safe? Am J Surg 2015;209(1):194-198.
- Norwood SH, McAuley CE, Berne JD, et al. Prospective evaluation of the safety of enoxaparin prophylaxis for venous thromboembolism in patients with intracranial hemorrhagic injuries. Arch Surg 2002;137(6):696-701.
- Koehler DM, Shipman J, Davidson MA, et al. Is early venous thromboembolism practice safe in trauma patients with intracranial hemorrhage? J Trauma 2011;70(2):324-329.
- Caruso JD, Elster EA, Rodriguez CJ. Epidural placement does not result in an increased incidence of venous thromboembolism in combat-wounded patients. J Trauma 2014;77(1):61-66.
- Cherry RA, Nichols PA, Snavely TM, et al. Prophylactic inferior vena cava filters: do they make a difference in trauma patients? J Trauma 2008;65(3):544-548.
- Kalva SP, Athanasoulis CA, Chieh-Min F, et al. Recovery vena cava filter: experience in 96 patients. Cardiovasc Intervent Radiol 2006;29:559-564.
- Miyahara T, Miyata T, Shigematsu K, et al. Clinical outcome and complications of temporary inferior vena cava filter placement. J Vasc Surg 2006;44:620-624.
- Arsch MR. Initial experience in humans with a new retrievable inferior vena cava filter. Radiology 2002;225(3):835-844.
- White RH, Zhou H, Kim J, et al. A population-based study of the effectiveness of inferior vena cava filter use among patients with venous thromboembolism. Arch Int Med 2000;160(13):2033-2041.
- PREPIC Study Group. Eight-year follow-up of patients with permanent vena cava filters in the prevention of pulmonary embolism: the PREPIC (Prevention du Risque d’Embolie Pulmonaire par Interruption Cave) randomized study. Circulation 2005;112(3):416–422.
- Baglin TP, Brush J, Streiff M. Guidelines on use of vena cava filters. Br J Haematol 2006;134(6):590-595.
- Binkert CA, Sasadeusz K, Stavropoulos SW. Retrievability of the Recovery vena cava filter after dwell times longer than 180 days. J Vasc Interv Radiol 2006;17:299-302.
- Kim HS, Young MJ, Narayan AK, et al. A comparison of clinical outcomes with retrievable and permanent inferior vena cava filters. J Vasc Interv Radiol 2007;19(3):393-399.
- Grande WJ, Trerotola SO, Reilly PM, et al. Experience with the Recovery Filter as a retrievable inferior vena cava filter. J Vasc Interv Radiol 2005;16(9):1189-1193.
- Hoff WS, Hoey BA, Wainwright GA, et al. Early experience with retrievable inferior vena cava filters in high risk trauma patients. J Am Coll Cardiol 2004;199(6):869-874.
- Karmy-Jones R, Jurkovich GJ, Velmahos GC, et al. Practice patterns and outcomes of retrievable vena cava filters in trauma patients: an AAST multicenter study. J Trauma 2007;62(1):17-24.
- Johnson ON, Gillespie DL, Aidinian G, et al. The use of retrievable inferior vena cava filters in severely injured military trauma patients. J Vasc Surg 2009;49:410-416.
- Morris CS, Rogers FB, Najarian KE, et al. Current trends in vena caval filtration with the introduction of a retrievable filter at a level I trauma center. J Trauma 2004;57(1)32-36.
- Lucas DJ, Dunne JR, Rodriguez CJ, et al. Dedicated tracking of patients with retrievable inferior vena cava filters improves retrieval rates. Am Surg 2012;78(8):870-874.
Додаток А: Настанови щодо профілактики венозної тромбоемболії
Додаток В: Рекомендації щодо використання кава-фільтрів
- Усі кава-фільтри, встановлені у зоні бойових дій, мають бути знімними.
- Детальна інформація щодо опису марки кава-фільтра, моделі, сумісності з проведенням МРТ і точного місця розміщення пристрою повинна бути задокументована в системі електронних медичних записів AHLTA T або TC2.
- Усі знімні кава-фільтри, встановлені під час перебування у зоні бойових дій, мають бути видалені, як тільки більше не буде протипоказань до проведення фармакологічної профілактики ВТЕ, або зникне потреба у профілактиці взагалі. Винятки становлять кава-фільтри, які були встановлені для вторинної профілактики у пацієнтів з нововиявленою ВТЕ під час проведення антикоагулянтної терапії, або у пацієнтів, які все ще відносяться до групи високого ризику.
- За відсутності показань до тривалого застосування знімних кава-фільтрів, усі вони повинні бути видалені в межах трьох місяців.
- Рішення про видалення знімного кава-фільтра, встановленого пацієнту в зоні бойових дій (або рішення залишити його), має бути прийняте у першому військово-медичному закладі п'ятого рівня на території континентальних штатів США, через який пацієнт проходить під час повернення з зони бойових дій. За можливості, видалення кава-фільтра має відбуватися в тому ж закладі до переведення пацієнта на наступний рівень надання допомоги. Такий підхід зменшує ймовірність того, що рішення відкладатиметься до моменту, коли видалення пристрою вже стане технічно неможливим.
- Про наявність знімного кава-фільтра у пацієнта, який отримує допомогу у військово-медичному закладі четвертого рівня, слід повідомити приймаючий військово-медичний заклад п'ятого рівня. Як правило, видалення знімного кава-фільтра виконується у закладі п’ятого рівня.
- Усі пацієнти з відомим ТГВ без поточних протипоказань до проведення антикоагулянтної терапії, які мають встановлений кава-фільтр, повинні отримати повноцінну антикоагулянтну терапію. Це переважно досягається за допомогою варфарину (“Coumadin”) до отримання показника міжнародного нормалізованого відношення (МНВ) 2,0-3,0. Якщо планується виконання подальших хірургічних процедур, можна також розглянути застосування НМГ у дозі 1 мг/кг 2 рази на добу або краплинне введення НФГ до тих пір, поки не стане можливим перехід на варфарин.
- При поверненні пацієнта до Сполучених Штатів, наявність кава-фільтра, його марка, модель, сумісність з проведенням МРТ, можливість вилучення пристрою, його точне місце розташування та дата встановлення повинні бути чітко зазначені в Реєстрі медичних даних та продубльовані в системі електронних медичних записів AHLTA.
- У майбутньому слід докласти зусиль для стандартизації типу знімного кава-фільтра, що використовується у всіх зонах бойових дій.
Додаток C: Додаткова інформація щодо не передбаченого інструкцією застосування лікарських засобів у настановах з клінічної практики
Мета
Мета цього Додатка — надати роз’яснення політики та практики Міністерства оборони США щодо включення в Настанови з клінічної практики «незатвердженого» застосування для продуктів, які були схвалені Управлінням з контролю якості продуктів харчування і лікарських засобів США (FDA). Це стосується використання препаратів не за призначенням для пацієнтів, які належать до Збройних сил США.
Вихідна інформація
Незатверджене (тобто «не за призначенням» - “off-label”) використання продуктів, схвалених FDA, надзвичайно поширене в медицині США і зазвичай не регулюється окремими нормативними актами. Проте, згідно з Федеральним законодавством, за деяких обставин застосування схвалених лікарських засобів за незатвердженими показаннями регулюється положеннями FDA про «досліджувані нові ліки». До цих обставин належить використання в рамках клінічних досліджень, а також, у військовому контексті, використання за незатвердженими показаннями згідно з вимогами командування. Деякі види використання за незатвердженими показаннями також можуть підлягати окремим нормативним актам.
Додаткова інформація щодо застосування за незатвердженими показами у настановах з клінічної практики
Включення до Настанов з клінічної практики використання медикаментів за незатвердженими показаннями не належить до клінічних випробувань і не є вимогою командування. Більше того, таке включення не передбачає, що Військова система охорони здоров’я вимагає від медичних працівників, які працюють в структурах Міноборони США, застосовувати відповідні продукти за незатвердженими показаннями або вважає це «стандартом медичної допомоги». Швидше, включення до CPGs використання засобів «не за призначенням» має поглиблювати клінічне судження відповідального медичного працівника шляхом надання інформації щодо потенційних ризиків та переваг альтернативного лікування. Рішення приймається на основі клінічного судження відповідальним медичним працівником у контексті відносин між лікарем і пацієнтом.
Додаткові процедури
Виважений розгляд
Відповідно до цієї мети, в обговореннях використання медикаментів «не за призначенням» в CPG конкретно зазначено, що це використання, яке не схвалено FDA. Крім того, такі обговорення є збалансованими у представленні даних клінічних досліджень, включаючи будь-які дані, які свідчать про обережність у використанні продукту, і, зокрема, включаючи усі попередження, видані FDA.
Моніторинг забезпечення якості
Що стосується використання «не за призначенням», діяльність Міністерства оборони США полягає у підтримці регулярної системи моніторингу забезпечення якості результатів і відомих потенційних побічних ефектів. З цієї причини підкреслюється важливість ведення точних клінічних записів.
Інформація для пацієнтів
Належна клінічна практика передбачає надання відповідної інформації пацієнтам. У кожних Настановах з клінічної практики, де йдеться про використання засобу «не за призначенням», розглядається питання інформування пацієнтів. За умови практичної доцільності, слід розглянути можливість включення додатка з інформаційним листком для пацієнтів, що видаватиметься до або після застосування продукту. Інформаційний листок має в доступній для пацієнтів формі повідомляти наступне: a) що дане застосування не схвалене FDA; b) причини, чому медичний працівник Міністерства оборони США може прийняти рішення використати продукт з цією метою; c) потенційні ризики, пов’язані з таким застосуванням.























